清胰Ⅱ號對急性胰腺炎的保護作用研究*
蔡治方,彭慈軍,傲宇,兌丹華,蘭天罡
(遵義醫學院附屬醫院 肝膽胰外科,貴州 遵義 563000)
急性胰腺炎(acute pancreatitis, AP)是臨床中常見的急腹癥之一,其病理特征為胰腺間質出現水腫、出血,腺泡細胞發生空泡變性、壞死或炎癥細胞大量浸潤[1]。AP因其臨床結局難以預料,嚴重威脅患者健康。清胰Ⅱ號是遵義醫學院附屬醫院經典中藥方劑,盡管許多研究表明其對AP療效顯著,但是作用機制仍不完全明確[2]。為進一步探討清胰Ⅱ號對AP的治療機制,本研究利用3%牛磺膽酸鈉經膽胰管逆行注射復制AP大鼠模型,觀察清胰Ⅱ號灌胃對AP大鼠的胰腺保護作用及其機制。
1 材料與方法
1.1 實驗動物
36只清潔級SD大鼠購自第三軍醫大學實驗動物中心,許可證號:SCXK-(軍)201802154,雌雄不限制,體重210~265 g,平均(238±28)g。
1.2 實驗藥物
清胰Ⅱ號(遵義醫學院附屬醫院藥劑科自制),濃度250 mg/ml。
1.3 試劑與儀器
牛磺膽酸鈉(美國Sigma公司),大鼠腫瘤壞死因子 -α(tumor necrosis factor-α, TNF-α)ELISA 試劑盒(上海齊一生物科技有限公司,QY-H10038),大鼠白細胞介素6(Interleukin 6, IL-6)ELISA 試劑盒(上海易匯生物科技有限公司,ab87933),大鼠白細胞介素1β(Interleukin 1β, IL-1β)ELISA試劑盒(上海江萊生物科技有限公司,AZ-003),iMARK 680通用酶標儀(美國Bio-Rad公司),RIPA裂解液、BCA蛋白濃度測定、組織線粒體分離試劑盒購自上海碧云天生物公司,總RNA抽提試劑Trizol、dNTP、Oligo(dT)15、Taq DNA聚合酶、一抗、二抗購自上海科華生物工程股份有限公司,組織活性氧(DHE-ROS)檢測試劑盒(上海貝博生物科技有限公司),引物設計由上海生工生物工程有限公司完成,TNF-α正向引物:5'-TTCTGTCTACTGAACTTC GGGGTGATCGGTCC-3',反向引物:5'-GTATGAGA TAGCAAATCGGCTGACGGTGTGGG-3';IL-6正向引物:5'-TCCAGTTGCCTTCTTGGGAC-3',反向引物:5'-GTGTAATTAAGCCTCCGACTTG-3';IL-1β 正向引物:5'-GAAAGACGGCACACCCACCCT-3',反向引物:5'-GCTCTGCTTGTGAGGTGCTGATGTA-3';GAPDH正向引物:5'-CATGACCACAGTCCATGCCATCAC-3',反向引物:5'-TGAGGTCCACCACCCTGTTGCTGT-3'。
1.4 實驗分組與模型的復制
根據隨機數字表法,將36只大鼠隨機分為假手術組、模型組和干預組,每組12只。所有大鼠術前禁食12 h,10%水合氯醛(0.33 ml/100 g)麻醉后,取上腹部正中切口進入腹腔,假手術組大鼠開腹后僅翻動腸管,隨后關腹;模型組和干預組大鼠在顯露膽胰管后,采用小動脈夾暫時阻閉膽管,由十二指腸前壁斜行進針經乳頭部插入膽胰管后,勻速逆行向膽胰管內注入3%牛磺膽酸鈉(0.1 ml/100 g),夾閉膽胰管進入十二指腸的開口2 min,隨后松開小動脈夾,關腹。放入代謝籠自由飲水、禁食。
1.5 方法
1.5.1 處理方法 模型復制后,干預組大鼠給予清胰Ⅱ號灌胃(1 ml/100 g),模型組和假手術組大鼠給予生理鹽水(1 ml/100 g)灌胃,各組灌胃6 h/次,連續4次。
1.5.2 TNF-α、IL-6、IL-1β蛋白水平檢測 采用ELISA雙抗體夾心法檢測TNF-α、IL-6、IL-1β蛋白水平。所有大鼠處理24 h后,沿原切口進入腹腔,于下腔靜脈取血3~5 ml,迅速冰上3 000 r/min離心15 min,仔細收集上清液。采用TNF-α、IL-6、IL-1β ELISA試劑盒進行檢測。方法如下:設置標準孔10孔,加樣量均為50μl(根據不同試劑盒要求進行稀釋濃度),同時設置不加樣品和酶標試劑的空白對照孔,待測樣品孔中加入最終稀釋5倍的樣品,混勻后于37℃溫育30 min,隨后小心棄去液體,向每孔中加入洗滌液,靜置30 s后棄去液體,重復5次后,加入辣根過氧化物酶試劑50μl/孔,混勻后于37℃溫育30 min后洗滌,按順序加入顯色劑A、B各50μl/孔,震蕩混勻后避光顯色15 min,加入50μl終止液,于450 nm波長處測定光密度(OD)值,通過標準曲線計算TNF-α、IL-6、IL-1β蛋白水平。
1.5.3 胰腺病理評分檢測 取胰腺組織約3 mm×3 mm×3 mm,10%甲醛固定3 h后脫水,透明、浸蠟、包埋,冷凍30 min后切片、攤烤片、脫蠟、蘇木精染色10 min,分化、復染、脫水、透明后封固,做病理學檢查,按改良的Schmidt標準法聯合Rongione法做胰腺病理評分,取3張非連續切片中3個隨機視野進行病理評分,以各評分平均值作為最終胰腺病理評分。
1.5.4 TNF-α、IL-6、IL-1β mRNA水 平 檢 測采用RT-PCR檢測TNF-α、IL-6、IL-1β mRNA水平。取胰腺組織剪碎后冰上勻漿,在EP管中加入氯仿200μl于勻漿液中,震蕩混勻,4℃、12 000 r/min離心,取上層液加入等量異丙醇,混勻后繼續4℃、12 000 r/min離心,提取沉淀物。紫外分光光度計檢測純度。將上述引物各0.25μl加入5×buffer液5μl、Ex Taq 0.125μl、逆轉錄反應液5μl,用滅菌三蒸水調至25.5μl。PCR擴增條件:94℃變性1 min,65℃退火30 s,72℃延伸1 min,共35個循環,72℃繼續延伸5 min。取產物5μl電泳,以GAPDH為參照,分析灰度值。
1.5.5 核因子κB(nuclear factor κB, NF-κB)核轉位水平檢測 采用SABC免疫組織化學法檢測NF-κB核轉位水平,取胰腺組織石蠟標本進行脫蠟、水化,以3%雙氧水去過氧化物酶封閉,加入抗NF-κB多克隆抗體(1∶100)、生物素化羊抗鼠IgG、SABC復合物,孵育后DAB染色、復染、封片。陰性對照以PBS代替一抗。每只大鼠選取5張切片,每張切片隨機選取2個高倍鏡視野觀察,以出現棕黃色顆粒為NF-κB陽性細胞。
1.5.6 胰腺組織活性氧自由基(reactive oxygen species, ROS)水平檢測 采用流式細胞術檢測胰腺組織ROS水平,剪取胰腺組織50 mg左右,PBS清洗后于冰上加入線粒體分離試劑A(100μl/10 mg)勻漿8~12次,4℃、3 000 r/min離心5 min,收集上清液后繼續4℃、3 000 r/min離心5 min,沉淀物即為線粒體,按1∶20加入勻漿介質,低溫勻漿10 min,收集上清液,加入DCFH-DA工作液1 mmol,混勻后37℃溫育30 min,流式細胞儀測定ROS水平。
1.5.7 Western blotting檢測 采用Western blotting檢測磷酸化c-Jun氨基末端激酶(phosphorylated c-Jun N-terminal kinase, p-JNK, p-JNK)和總c-Jun氨基端激酶(c-Jun N-terminal kinase, JNK)水平。取胰腺組織剪碎后勻漿,加入裂解液裂解約30 min后低溫離心,測定蛋白質濃度,配置12%分離膠,取10μl樣品上樣,在80~120 V電壓下進行電泳。轉膜后加入一抗,4℃過夜。加入二抗后,37℃搖床中孵育1.5 h,進行發光顯影。
1.6 統計學方法
數據分析采用SPSS 22.0統計軟件,計量資料以均數±標準差(±s)表示,多組比較用方差分析,進一步兩兩比較用SNK-q檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 各組大鼠胰腺病理評分比較
假手術組、模型組、干預組胰腺病理評分比較,經方差分析,差異有統計學意義(P<0.05);干預組胰腺病理評分低于模型組(P<0.05),模型組胰腺病理評分高于假手術組(P<0.05),說明模型復制成功,清胰Ⅱ號干預效果明顯,可以用于后續研究。見表1和圖1。
2.2 各組大鼠NF-κB核轉位水平比較
假手術組、模型組、干預組胞漿NF-κB水平比較,經方差分析,差異有統計學意義(P<0.05);干預組胞漿NF-κB水平低于假手術組(P<0.05),但高于模型組(P<0.05)。假手術組、模型組、干預組胞核NF-κB水平比較,經方差分析,差異有統計學意義(P<0.05);干預組胞核NF-κB水平高于假手術組(P<0.05),但低于模型組(P<0.05)。假手術組、模型組、干預組NF-κB核轉位率比較,經方差分析,差異有統計學意義(P<0.05);干預組NF-κB核轉位率低于假手術組和模型組(P<0.05)。見表1。
2.3 各組大鼠TNF-α、IL-6、IL-1β水平比較
假手術組、模型組、干預組TNF-α蛋白和mRNA水平比較,經方差分析,差異有統計學意義(P<0.05);干預組TNF-α蛋白和mRNA水平低于模型組(P<0.05),但高于假手術組(P<0.05)。假手術組、模型組、干預組IL-6蛋白和mRNA水平比較,經方差分析,差異有統計學意義(P<0.05);干預組IL-6蛋白和mRNA水平低于模型組(P<0.05),但高于假手術組(P<0.05)。假手術組、模型組、干預組IL-1β蛋白和mRNA水平比較,經方差分析,差異有統計學意義(P<0.05),干預組IL-6蛋白和mRNA水平低于模型組(P<0.05),但高于假手術組(P<0.05)。見表2。
表1 各組大鼠胰腺病理評分、NF-κB核轉位水平比較 (n =12,±s)
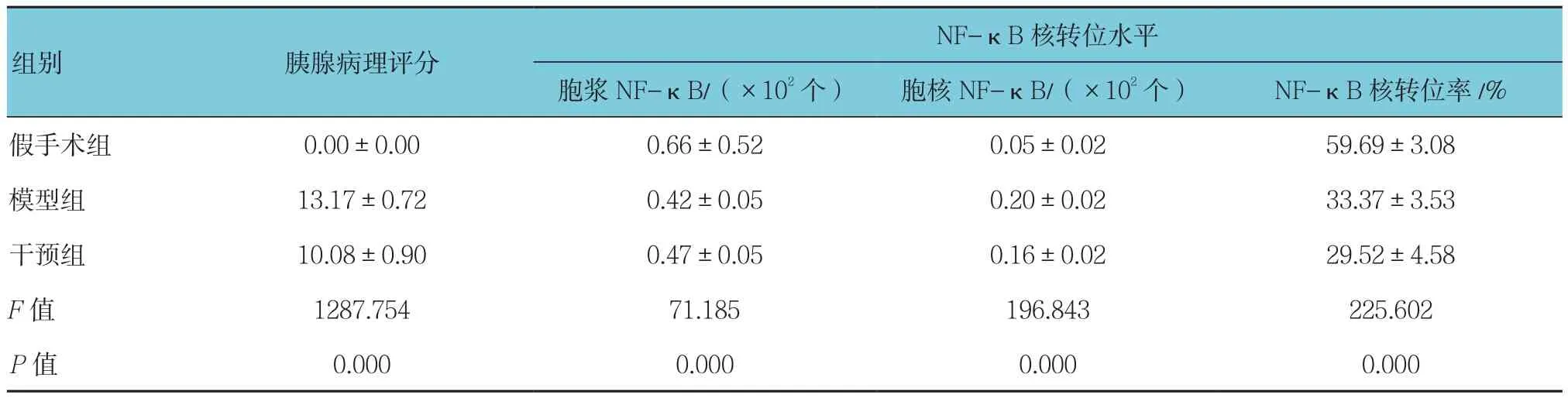
表1 各組大鼠胰腺病理評分、NF-κB核轉位水平比較 (n =12,±s)
組別 胰腺病理評分NF-κB核轉位水平胞漿NF-κB/(×102個) 胞核NF-κB/(×102個) NF-κB核轉位率/%假手術組 0.00±0.00 0.66±0.52 0.05±0.02 59.69±3.08模型組 13.17±0.72 0.42±0.05 0.20±0.02 33.37±3.53干預組 10.08±0.90 0.47±0.05 0.16±0.02 29.52±4.58 F值 1287.754 71.185 196.843 225.602 P值 0.000 0.000 0.000 0.000
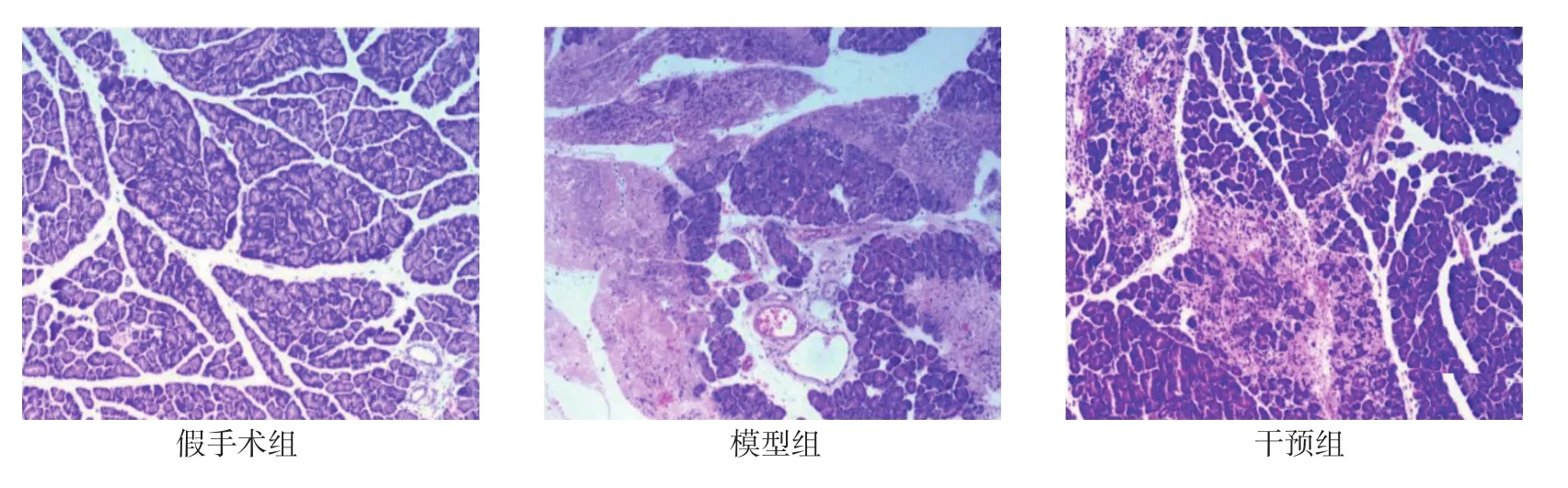
圖1 各組大鼠胰腺組織病理切片圖 (HE×100)
表2 各組大鼠TNF-α、IL-6、IL-1β水平比較 (n =12,±s)

表2 各組大鼠TNF-α、IL-6、IL-1β水平比較 (n =12,±s)
組別TNF-α IL-6 IL-1β蛋白 mRNA 蛋白 mRNA 蛋白 mRNA假手術組 6.43±1.01 2.30±0.41 1.20±0.25 3.61±1.86 23.65±7.05 44.55±10.85模型組 25.57±8.43 38.06±14.66 5.81±1.74 27.85±10.22 59.16±14.90 67.44±10.59干預組 18.51±8.53 22.36±10.65 2.28±1.33 11.13±4.27 34.60±14.07 57.73±9.64 F值 23.275 35.223 43.163 43.932 25.349 14.711 P值 0.000 0.000 0.000 0.000 0.000 0.000
2.4 各組大鼠ROS、p-JNK、JNK水平比較
假手術組、模型組、干預組ROS、p-JNK、JNK蛋白水平比較,經方差分析,差異有統計學意義(P<0.05);干預組ROS、p-JNK、JNK蛋白水平低于模型組(P<0.05),但高于假手術組(P<0.05)。見表3。
表3 各組大鼠ROS、p-JNK、JNK水平比較(n =12,±s)

表3 各組大鼠ROS、p-JNK、JNK水平比較(n =12,±s)
組別 ROS p-JNK JNK假手術組 11.64±6.42 6.41±2.85 7.04±3.39模型組 85.99±13.53 34.82±6.64 44.40±9.40干預組 41.85±11.38 13.89±4.23 18.04±9.31 F值 142.299 111.236 41.180 P值 0.000 0.000 0.000
3 討論
目前,越來越多的研究表明,ROS導致的JNK信號通路激活在AP的炎癥反應中扮演重要角色[3-4],而一系列炎癥因子如TNF-α、IL-6、IL-1β等是導致AP惡化的主要因素[5]。同時,課題組前期研究結果表明,清胰Ⅱ號對AP動物模型的療效較好[6-8],然而其是否通過抑制ROS/JNK通路導致的炎癥反應仍不清楚。因此,筆者在以往研究基礎上,進一步觀察清胰Ⅱ號對AP大鼠的治療作用,并且對其可能的機制進行探討。
研究結果顯示,假手術組胰腺病理評分低于干預組,干預組胰腺病理評分低于模型組,提示清胰Ⅱ號對AP大鼠胰腺具有一定的保護作用,與以往研究結果一致[2,6-8]。同時,本研究也發現,模型組NF-κB核轉位率高于假手術組;干預組NF-κB核轉位率高于假手術組,但低于模型組。NF-κB在正常細胞中以無活性狀態存在于細胞漿,當細胞受到特定刺激時,NF-κB迅速從細胞漿易位到細胞核,進而調控炎癥級聯瀑布反應相關酶等基因的表達,在炎癥反應中具有重要作用。由此可見,NF-κB必須發生核轉位才可以啟動下游炎癥細胞因子的表達,因此本研究以NF-κB核轉位率評價其在AP大鼠中的活化。本研究結果顯示,當大鼠發生AP時,NF-κB核轉位率增加,應用清胰Ⅱ號干預后,NF-κB核轉位率得到明顯抑制。為探討其下游炎癥因子是否受到抑制,本實驗繼續觀察TNF-α、IL-6、IL-1β水平,結果顯示,模型組TNF-α、IL-6、IL-1β水平高于假手術組,干預組上述指標高于假手術組,但低于模型組。這一結果與NF-κB核轉位率的變化互相印證,說明清胰Ⅱ號能夠通過抑制AP大鼠NF-κB核轉位率,進而抑制其下游炎癥因子的表達,最終起到保護胰腺的作用。
目前研究表明,ROS與JNK相互作用可導致細胞炎癥的發生、發展[3,9]。因此,本研究選取ROS/JNK作為機制研究的觀察目標。結果顯示,模型組ROS、p-JNK、JNK水平高于假手術組,干預組上述指標高于假手術組,但低于模型組。這提示清胰Ⅱ號可能通過抑制ROS、JNK,進而減少細胞炎癥的發生。但由于ROS與JNK的作用關系較為復雜,在多數情況下,JNK接受上游ROS調控,ROS促進LNK的激活[10]。但也有學者報道,ROS產生生物活性的前提是JNK的存在,或者需要JNK的活化[11-12]。目前關于兩者間的作用關系尚未達成一致,因此清胰Ⅱ號抑制AP大鼠ROS、JNK表達的具體機制還需要進一步探索。
綜上所述,清胰Ⅱ號對AP大鼠的胰腺保護作用機制可能是通過下調NF-κB及ROS/JNK通路,降低TNF-α、IL-6、IL-1β的表達水平從而發揮作用,但由于NF-κB、ROS及JNK間存在復雜關系,對于清胰Ⅱ號治療AP的機制研究仍任重道遠。

