喹諾酮金屬配合物的研究進展
胡 健
(南京洵安文化傳媒有限公司,江蘇 南京 210009)
喹諾酮類也被稱作吡酮酸類或吡啶酮酸類,是一大類人工合成的具有抗菌活性的化合物,具有效果好,口服吸收好,生物利用度高等特點[1-2]。按研發時間的先后順序及抗菌譜及適應癥的不同,喹諾酮類分為一到四代,各代都是以前代或同代其它化合物為基礎,對母核及側鏈進行不同程度的修飾,在抗菌譜和適應癥方面逐漸擴大。此類藥物近三十年來發展極為迅速,不但品種層出不窮,新一代產品的治療效果已不遜于同期常用的頭孢類抗生素,由于頭孢類抗生素開發成本持續提高,因而開發抗菌活性更強、抗菌譜更廣、不易產生耐藥、對常見耐藥菌有效、半衰期更長、不良反應更少的喹諾酮類抗生素成為相關研發機構關注的熱點。
配位聚合物由于其結構特點往往具有獨特的功能,在醫療等領域有著廣泛而重要的應用。某些可形成配合物的藥物的價值有待進一步開發,喹諾酮類化合物的結構中存在多個配位點,可與某些金屬離子反應生成金屬配合物,為此喹諾酮類藥用價值的深入挖掘提供了重要思路。
1 喹諾酮類藥物的發展過程
美國 Sterling-Winthrop研究所Lesher等人于1962年發現首個喹諾酮類藥物萘啶酸(圖1)[3]:
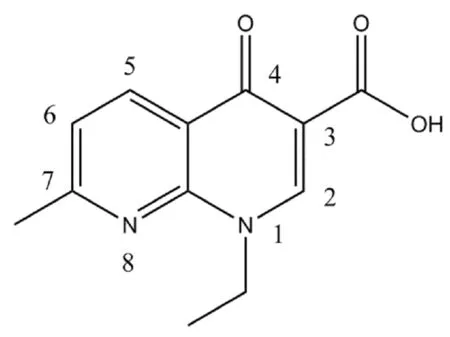
圖1 萘啶酸的結構式
但是僅對大多數革蘭氏陰性菌有作用,藥代動力學特性較差,安全性不理想,現已完全淘汰。萘啶酸自身狹窄的抗菌譜限制了臨床應用范圍,為了擴大抗菌譜和改善藥代動力學特性,科研人員在萘啶酸母核結構基礎上做了幾項修飾,其中兩項被認為是主要的修飾:在7號位置引入哌嗪環或另外的N-雜環及在6號(個別化合物同時在8號)位置引入氟原子(圖2)。
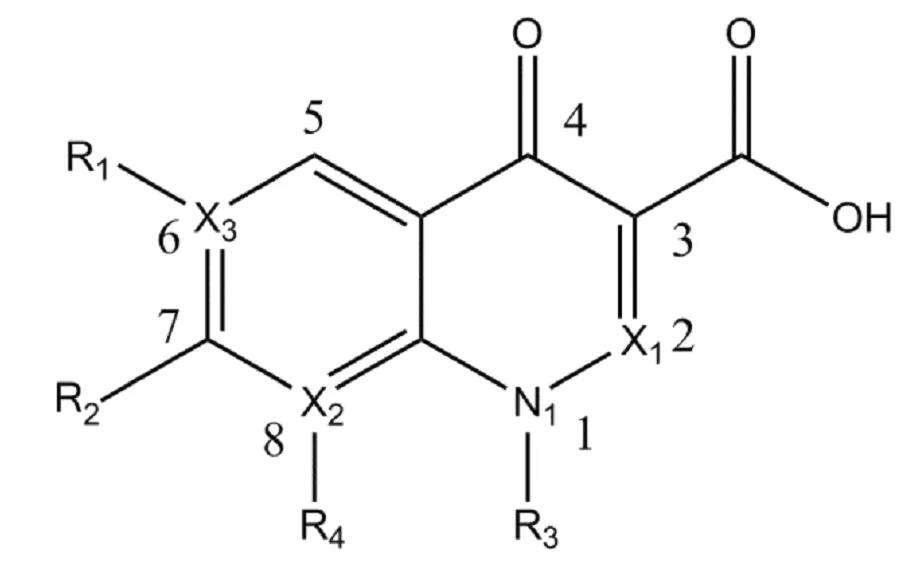
圖2 4-喹諾酮的一般結構
由此導致了20世紀80年代發現了新的4-喹諾酮類化合物——氟喹諾酮類,使得此類藥物步入了快速發展的軌道。早期發明的諾氟沙星、氧氟沙星等目前依然廣泛應用于臨床。步入90年代以后,喹諾酮類抗生素在前期產品藥代動力學及抗菌活性得到全面優化的基礎上擴大了抗菌譜,已經可以普遍應用于革蘭氏陽性菌、衣原體、支原體及細胞內致病菌感染。90年代中后期陸續上市的莫西沙星等喹諾酮類結構中引入的8位甲氧基加強了抗厭氧菌活性,而7位上的引入比早期產品吡哌酸結構中哌嗪環更復雜的含一氮或二氮單/雙環結構則使得此類化合物具有了較強的抗革蘭氏陽性菌活性,并保持了原來抗革蘭氏陰性菌的活性,同時毒副作用更小,安全性更高,同時藥物動力學也有很大改善,普遍具有大大低于50%的蛋白質結合率,較長的半衰期和更高的血清、組織濃度。基于抗菌譜和藥代動力學特點的不同,喹諾酮類藥物可以分為四代[4-8]。
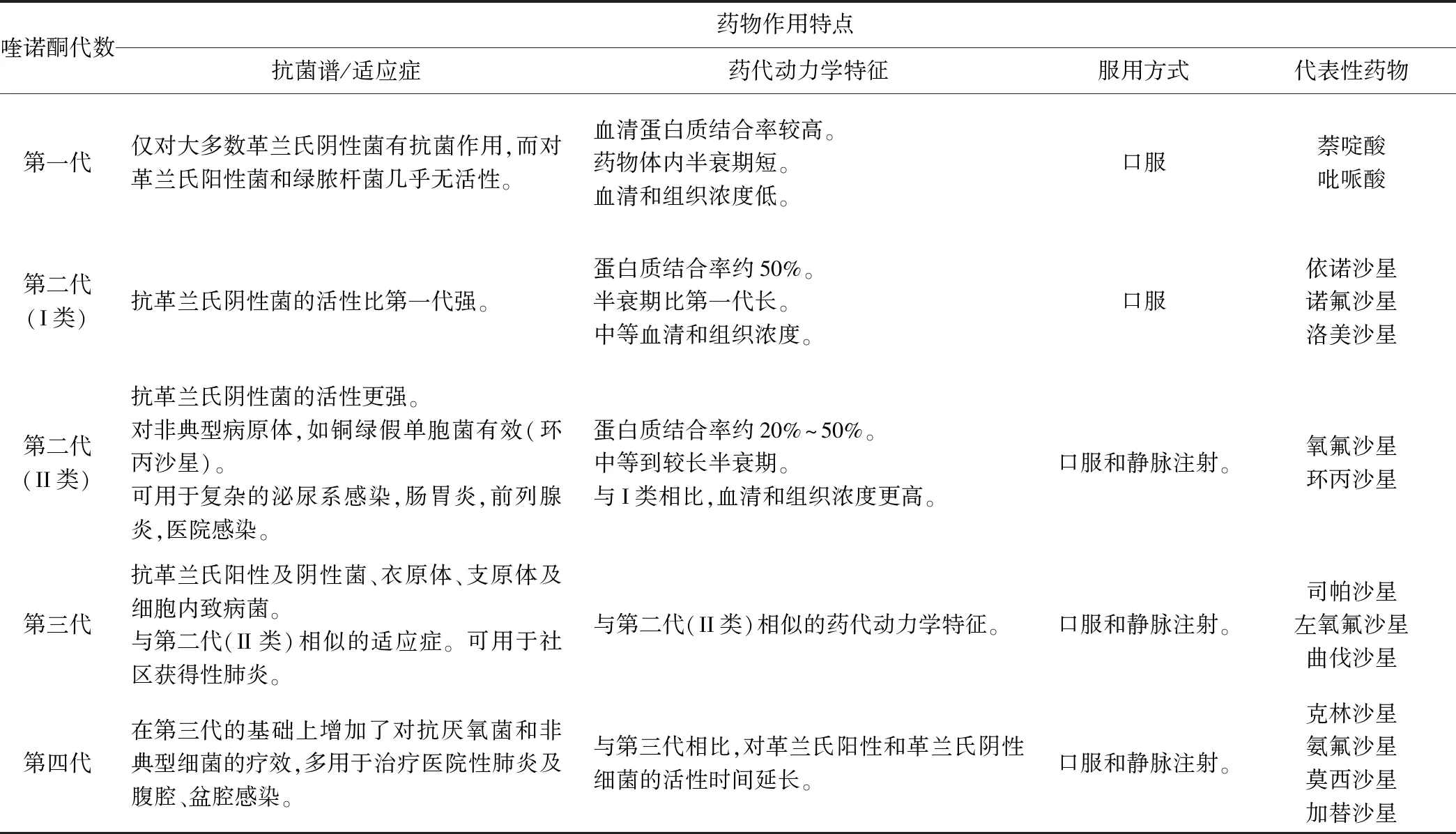
表1 根據喹諾酮類藥物抗菌譜和藥代動力學特性的分代/分類列表
喹諾酮類以細菌DNA為靶,妨礙DNA回旋酶正常發揮功能,抑制細菌DNA的復制和轉錄,進一步造成細菌DNA的不可逆損害,從而導致細菌迅速死亡,由此實現抗菌效果[9-10]。
喹諾酮類抑制DNA回旋酶(DNA拓撲異構酶II)和DNA拓撲異構酶IV,DNA回旋酶由編碼為GyrA和GyrB的兩個亞基組成,其作用是將負超螺旋引入DNA,從而催化子代染色體的分離。 DNA拓撲異構酶IV由四個亞基:兩個ParC和兩個ParE亞基組成,它負責DNA的解鏈,從而允許兩段DNA分離到兩個子細胞內[11-12]。喹諾酮與酶-DNA復合物相互作用,形成藥物- 酶-DNA復合物,阻止復制和轉錄過程[13-14]。
對革蘭氏陰性菌和陽性菌都有效的喹諾酮類中早期發現的化合物對革蘭氏陰性細菌DNA回旋酶的活性大于對拓撲異構酶IV的活性,對革蘭氏陽性細菌的拓撲異構酶IV有更強活性。后期發現的喹諾酮類對兩種酶具有幾乎同等的強抑制作用[15-17]。
2 喹諾酮類藥物金屬配合物的研究進展
喹諾酮類經過半個多世紀的發展已經在臨床藥物應用中占據重要地位,早期喹諾酮藥物被替代及淘汰,此類藥物同樣也面臨耐藥菌不斷出現以及后續研發成本持續攀升等問題,隨著生物無機化學領域的發展,氟喹諾酮出現并壟斷喹諾酮類藥品市場以后,氟喹諾酮類金屬配合物的研究也陸續展開。
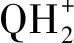
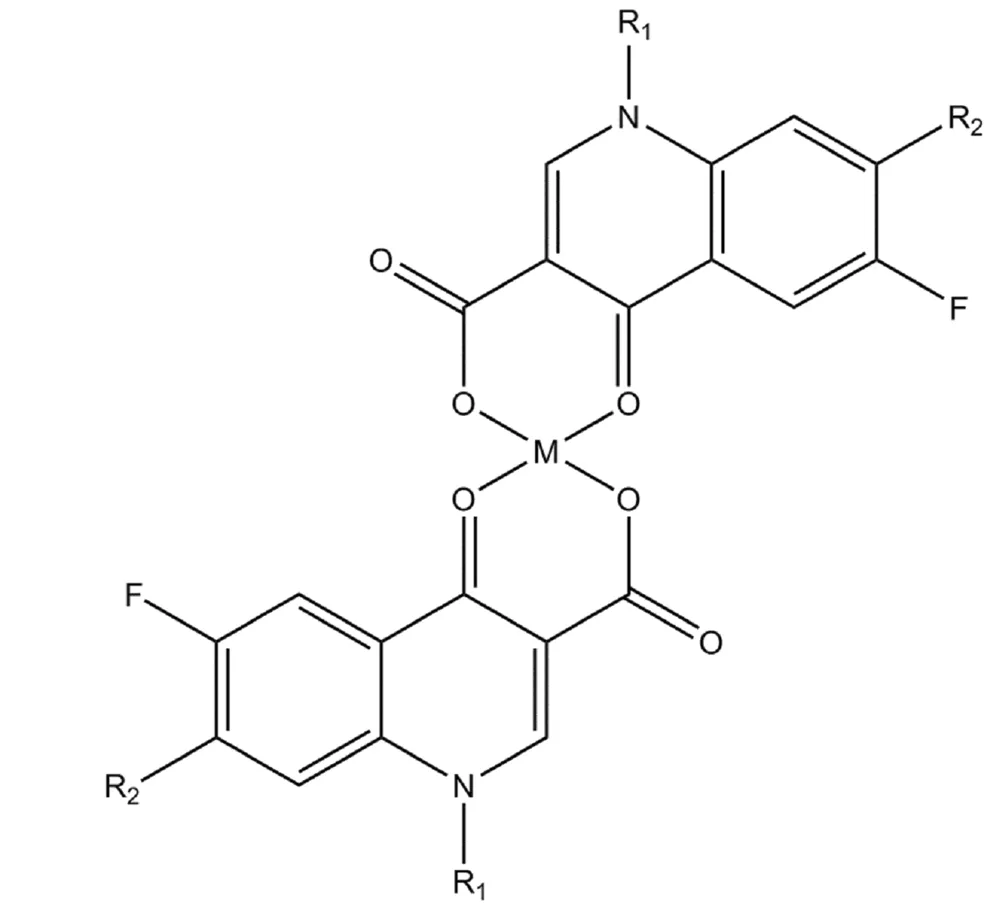
圖3 2價金屬陽離子與喹諾酮類以1∶2形成配合物的一般結構
進入21世紀以來,研究者對喹諾酮類金屬配合物進行了廣泛的研究,配體涵蓋了已經發現的一到四代喹諾酮類化合物,金屬離子則由最初的Mg2+、Al3+、Ca2+、Fe2+、Fe3+、Zn2+、Cu2+、Mn2+、Co2+、Ni2+、VO2+等原子量較小的離子逐步擴展至Ba2+、Bi3+、Ce3+、Y3+、Pd2+、La3+、Pt2+、Ru3+、Au3+、Eu3+等原子量較大的離子[22],其中稀土金屬配合物是目前研究的一個重要領域。

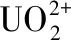

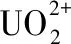
3 展望
金屬離子-喹諾酮配合物是近年來發展迅速的一個研究領域,作為目前抗感染化療領域最前沿和最容易產生新成果的領域,日益受到醫藥界的重視。一方面臨床上應該規范此類藥物的使用,盡量避免產生耐藥菌株,另一方面母核修飾及金屬配合物開發方面是兩個重要的研究方向。喹諾酮類藥物通過與某些金屬離子的絡合獲得溶解度增強的配合物來改善其藥物特性,許多金屬離子-喹諾酮類配合物表現出不同的生物學特性:抗菌活性(有時與母體喹諾酮類藥物相當或更好),抗癌活性,個別喹諾酮金屬配合物也具有一定的抗真菌和抗寄生蟲活性以及抗氧化性,更多的用途正在持續被發現。
喹諾酮金屬配合物的研究廣泛采用了分光光度法、熒光分光光度法和原子吸收光譜法的最新成果,同時與喹諾酮類可以形成穩定配合物的金屬離子可以利用喹諾酮作為絡合劑來測定。
喹諾酮類金屬配合物及其應用領域的進展與具有更大生物活性的新型喹諾酮類的開發是同步的。結合近年來喹諾酮類金屬配合物的研究成果,尋找具有明確分子結構及晶型并在臨床上有更強效用及更廣應用范圍的新型喹諾酮金屬配合物是未來重要的研究方向。

