高熱伴兩肺多發病變AFOP 1例
葉瑞海 楊珺超 徐峻 呂昕 毛玉萍 江立斌 王真
急性纖維素性機化性肺炎(acute fibrinous and organizing pneumonia,AFOP)臨床表現與急性肺損傷類似,可急性或亞急性起病,主要病理表現為肺泡內纖維素沉著伴機化性肺炎改變,其病變為片狀分布,且不能歸入已知間質性肺炎的病理類型[1]。其為一種罕見彌漫肺部病變,可能為間質性肺疾病的獨特類型。現報道1例我院確診的AFOP病例。
患者女性,59歲。16年前曾行膽囊切除術,術后恢復可;6年前因甲狀腺癌行甲狀腺切除術,術后口服優甲樂50μg、1次/d治療。有“青霉素及莫西沙星”過敏史。因“發熱伴咳嗽5d”于2017年4月3日收住入院。患者5d前受涼后出現發熱,最高40.5℃,有畏寒無寒戰,伴咳嗽,無明顯咳痰,無胸悶、氣急等不適,遂至當地醫院查血常規:WBC 16.49×109/L,中性粒細胞百分比84.4%,C反應蛋白(CRP)25mg/L;胸部 CT 示:兩肺多發病灶,炎癥首先考慮(圖1)。予左氧氟沙星、克林霉素等抗感染治療,消炎痛栓退熱,未見明顯好轉。遂至我院急診就診,復查血常規+CRP:WBC 20.2×109/L,中性粒細胞百分比 84.8%,CRP:133.09mg/L。先后予頭孢唑肟、美羅培南等抗感染治療,現為進一步治療收住入院。入院體檢:神志清,口唇無發紺,氣管居中,淺表淋巴結未及,兩肺呼吸音略粗,左下肺聞及濕啰音,心律齊,未聞及雜音,腹平軟,無壓痛,肝脾肋下未及,兩下肢無浮腫,舌紅,苔黃,脈弦。入院后先后予美羅培南針、可樂必妥針、頭孢他啶針、斯沃針抗感染治療,退熱、補液、化痰對癥處理。入院后進行輔助檢查,血氣分析:pH7.484,PaO280.9mmHg,二氧化碳分壓30.7mmHg,鉀3.10mmol/L,鈉132.0mmol/L。血常規+CRP:WBC 20.2×109/L,中性粒細胞百分比84.8%,淋巴細胞百分比10.1%,嗜酸粒細胞百分比0.1%。纖維蛋白原4.58g/L,D-二聚體6.41mg/L。肌鈣蛋白+生化急診:葡萄糖 6.96mmol/L,鉀 3.35mmol/L,白蛋白 39.46g/L,TBil 23.4μmol/L,谷丙轉氨酶48U/L,谷氨酰轉肽酶82U/L,肌酸激酶155U/L。降鈣素原:0.11。尿常規:蛋白質(+),尿膽原(+),黏液絲 14/μl。甲狀腺功能類:總 T3<0.25ng/ml,總 T4 4.51μg/dl,游離 T3<1.00pg/ml,抗甲狀腺球蛋白抗體14.2U/ml。甲狀腺球蛋白<0.04。痰真菌涂片檢查:找到真菌孢子。血ANA譜(16項):ANA(歐蒙法)陽性1∶100。血ANCA譜:抗內皮細胞抗體陽性,余無殊。血過敏原IgE 170.50U/ml。血G試驗+內毒素檢測:革蘭陰性菌脂多糖 (內毒素)0.072EU/ml,G實驗陰性。T 淋巴細胞亞群:T 抑制 (CD3+、CD8+)14.28%,CD19+32.96%,NK 細胞(CD3-/CD16+56+)4.28%。血病毒類:巨細胞病毒抗體IgG陽性,單純皰疹病毒抗體1型IgG陽性,單純皰疹病毒抗體2型IgG陽性,EB病毒IgG陽性,腺病毒抗體IgG陽性。血白細胞形態手工分類:中性分葉核78.0%,淋巴細胞19.0%,單核細胞3.0%。血免疫五項、GM試驗、抗結核抗體、肺炎支原體抗體、肺炎支原體DNA檢測、甲型乙型流感病毒抗原均陰性。產毒素難辨梭菌檢測陰性。多次血培養陰性。血管緊張素轉化酶(ACE)正常范圍。于2017年4月10日行支氣管鏡檢查:右肺中葉黏膜略充血,鏡下基本正常。患者反復高熱,最高體溫達40.2℃,4月17日在CT定位下經皮肺穿刺術,肺部穿刺液:培養藥敏陰性,涂片找抗酸菌陰性。肺穿刺病理:左下肺穿刺病理檢查示纖維素滲出伴機化性肺炎(圖2)。偏光鏡檢(-);免疫組化:CK7(上皮+)、SMA(肌纖維+);特殊染色:Masson(-)網染(+),彈力纖維(-),未找到抗酸桿菌,PAS(-),PAS-M(-)。診斷:AFOP。4月 18日加用甲強龍針 40mg靜脈滴注,1次/d,患者體溫逐漸恢復正常,1個月后復查胸部CT提示兩肺病灶明顯吸收好轉(圖3),改美卓樂片(甲潑尼龍片,輝瑞制藥,批號W10023)16mg,口服,2次/d序貫治療,每周減少4mg,門診隨訪3個月,病情穩定,未見復發。
討論 AFOP于2002年由Beasley首次提出[1],其在開胸肺活檢及尸檢標本發現一種臨床表現與急性肺損傷類似,可急性或亞急性起病,主要病理表現為肺泡內纖維素沉著伴機化性肺炎改變,其病變為片狀分布,且不能歸入已知間質性肺炎的病理類型。2013年美國胸科協會發布了特發性間質性肺炎的最新分類,其中AFOP被認為是特發性間質性肺炎的罕見類型[2]。我們通過Pubmed檢索英文文獻,以“acute fibrinous and organizing pneumonia”為關鍵詞,檢索時間為2002年1月至2017年8月,共檢索出英文文獻69篇,其中AFOP病例報道83例,回顧性文獻16篇[1-16]。國內核心期刊萬方數據庫檢索見19篇22例報道。本例為以反復高熱伴兩肺多發病變為特點的AFOP,患者中年女性,既往有膽囊切除術、甲狀腺癌切除術病史,有“青霉素及莫西沙星”過敏史,急性起病,臨床表現高熱、咳嗽癥狀,胸部影像學初為炎性滲出改變,之后形成實變及多發不規則結節影伴長毛刺改變,經強有力抗感染治療病灶無明顯吸收,確診主要依靠組織病理學診斷。
AFOP臨床表現與急性肺損傷類似,但缺乏特異性,其臨床表現以發熱、咳嗽、胸悶多見,影像學可表現為單發或多發斑片狀浸潤影,可為磨玻璃樣、實變等多種形態,其分布以下葉及靠近胸膜為主。其病程進展較成人型呼吸窘迫綜合征(ARDS)慢,需呼吸機機械通氣者約占1/3。AFOP臨床及影像學表現易誤診為感染性病變,常應用各種抗生素治療,但其對抗生素治療效果差,病情進展迅速。本例患者反復高熱,血常規各項指標及CRP持續升高,應用各種抗生素均未見明顯好轉,但患者肺部體征相對隱匿,且多次血培養及降鈣素原檢測未見明顯異常改變,提示為非感染性病變可能。病理活檢是其確診依據,本例患者最終行CT定位下經皮肺穿刺術獲得確診。Beasley認為AFOP診斷需依賴大塊肺組織活檢標本,鏡下見大面積分布典型纖維球,且不伴透明膜、Masson小體、嗜酸細胞浸潤改變[1],需排除彌漫性肺泡損傷、機化性肺炎、嗜酸粒細胞性肺炎。因臨床取得常為穿刺活檢小標本,故臨床診治仍應結合病史、影像學及臨床療效進行判斷。
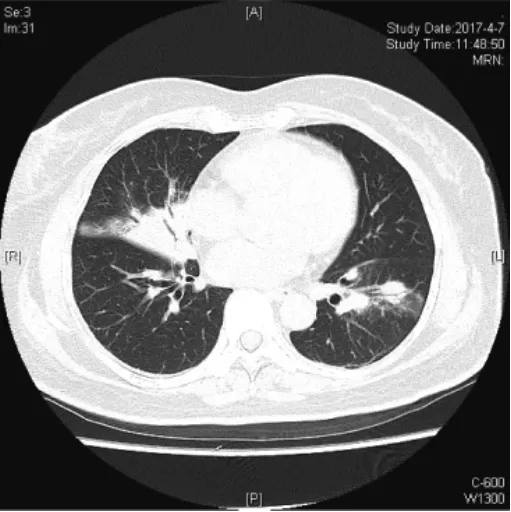
圖1 患者治療前胸部CT檢查所見(右肺中葉實變伴左下肺多發結節改變)

圖2 左下肺穿刺病理檢查所見(肺泡腔內見大量泡沫細胞和纖維素樣滲出,淋巴細胞聚集,HE 染色,×400)
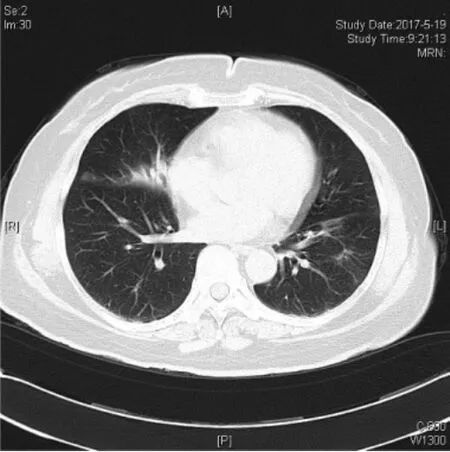
圖3 患者治療1個月后的胸部CT檢查所見(兩肺病變較前明顯吸收好轉)
AFOP的治療方案主要為激素,因其為罕見病,激素劑量及療程目前仍沒有定論。臨床上主要采用靜脈激素加口服激素序貫治療,部分頑固患者需加用免疫抑制劑治療[17-20]。此例患者靜脈起始激素劑量為0.75mg/(kg·d),1周后改口服序貫治療,治療3個月,療效好,未見激素相關不良反應,期間患者病情穩定,無復發。
AFOP具有獨特病理類型,是否為獨立疾病目前仍有爭議。因其臨床表現不典型,易漏診、誤診,故臨床醫生應加強對該病的認識,在疑診社區獲得性肺炎抗感染治療效果欠佳時,需鑒別診斷該疾病,及時病理活檢有助于該疾病診治。

