HPLC測定千里光提取物及千柏鼻炎膠囊中金絲桃苷在大鼠體內的血藥濃度及藥動學研究
朱雪飛
(江蘇省揚州市食品藥品檢驗檢測中心,江蘇 揚州 225000)
千柏鼻炎膠囊收載于《中國藥典》2015版一部,由千里光、卷柏、羌活、決明子、麻黃、川芎、白芷7味制成,具有清熱解毒,活血祛風,宣肺通竅之功效,臨床主要用于風熱犯肺、內郁化火、凝滯氣血所致的鼻塞、鼻癢氣熱、流涕黃稠,或持續鼻塞、嗅覺遲鈍;急慢性鼻炎、急慢性鼻竇炎見上述證候者[1]。千里光為菊科植物千里光SenecioscandensBuch.-Ham.的干燥地方部分,具有清熱解毒,明目,利濕的功效[2]。金絲桃苷是千里光中的指標性成分[3],也是千柏鼻炎膠囊中的主要藥效成分之一[4]。金絲桃苷具有抗肝腎損傷、抗抑郁、抗炎癥、抗癌、抗氧化應激與抗細胞凋亡等藥理作用[5-9]。關于千里光提取物及其復方制劑中金絲桃苷的藥動學差異的比較尚未見報道,本研究為了考察復方中金絲桃苷的體內過程是否受中藥配伍的影響,考察了大鼠灌胃千里光提取物和千柏鼻炎膠囊后的藥動學特征,初步評價復方中其他中藥配伍對金絲桃苷藥動學特征的影響,以揭示中藥復方配伍的合理性。
1 材料
日本島津LC-20AT高效液相色譜儀(包括SPD-20A紫外檢測器);N2000雙通道色譜工作站(浙江大學智能信息工程研究所);高速冷凍離心機(美國Sigma公司);快速混勻器(江蘇金壇儀器廠);島津AUW220D分析天平(島津);微量移液器(美國Thermo公司);BuchiR旋轉蒸發儀(瑞士Buchi公司);HH系列數顯恒溫水浴鍋(江蘇金壇儀器廠);冷凍干燥機(德國Marin Christ公司)。金絲桃苷對照品(中國食品藥品檢定研究院,批號:111521-201205);千里光提取物(自制,HPLC法測得金絲桃苷含量為0.8312 mg·g-1);千柏鼻炎膠囊(廣州白云山奇星藥業有限公司,國藥準字Z44022415,批號:160707,HPLC法測定金絲桃苷含量為0.7135 mg·g-1);乙腈(色譜純,美國TEDIA);純凈水(自制)。清潔級SD雄性大鼠(揚州大學動物實驗中心提供),體重250 g左右,適應性飼養1周。
2 方法
2.1 色譜條件
色譜柱:Kromasil C18(250×4.6mm,5μm);流動相:乙腈-0.2%醋酸水溶液(14∶86);檢測波長:360 nm;流速:1mL·min-1;柱溫30℃;進樣量20μL。
2.2 千里光提取物的制備(同千柏鼻炎膠囊的制備工藝)
稱取千里光藥材適量,加10倍量水煎煮2次,第一次3h,第二次1.5h,合并煎液,濾過,濾液減壓濃縮至適量,真空干燥后即得。經HPLC法測得金絲桃苷的含量為0.8312 mg·g-1。
2.3 對照品溶液的配制
精密稱取金絲桃苷對照品適量,加乙腈醇制成每1mL含0.1364 mg的溶液,即得。
2.4 血漿樣品的預處理
精密吸取血漿0.1mL,加0.2mL乙腈沉淀蛋白,渦流振蕩1min,12000r·min-1高速離心5min,取上清0.45μm微孔濾膜濾過,20μL進樣。
2.5 藥動學研究
將SD雄性大鼠12只隨機分成2組,每組6只,給藥前禁食18h,自由飲水,將千里光提取物和千柏鼻炎膠囊(內容物)分別用1%CMC-Na分散,分別灌胃給藥,給藥劑量按金絲桃苷折算均為10 mg·kg-1,并于給藥后給藥前和給藥后0.083,0.25,0.5,0.75,1,1.5,2,3,4,6,8,12,24 h眼眶后靜脈叢取血,置肝素化的EP管中,分離血漿待預處理后測定。
2.6 統計學處理
采用DAS2.0藥動學軟件進行數據處理,血漿中金絲桃苷的峰濃度Cmax及達峰時間Tmax由實測數據直接得出。
3 結果
3.1 方法的專屬性
空白血漿、空白血漿中加入金絲桃苷對照品、灌胃千里光提取物及灌胃千柏鼻炎膠囊的血漿樣品色譜圖見圖1。由圖可見,金絲桃苷與其他內源性成分分離效果良好,無干擾。
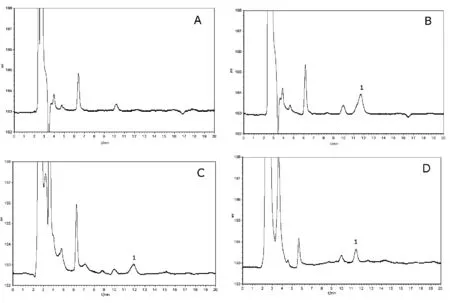
A.空白血漿;B.血漿中加入金絲桃苷對照品;C.灌胃千里光提取物后的血漿樣品;D.灌胃千柏鼻炎膠囊后的血漿樣品;1為金絲桃苷
圖1 大鼠血漿樣品中金絲桃苷的HPLC色譜圖
3.2 線性范圍及檢測限
精密吸取金絲桃苷對照品溶液適量,置于1mL離心管中,加入大鼠空白血漿100μL,配制成金絲桃苷濃度分別為0.341,0.682,1.364,3.410,6.820,13.640 μg·mL-1的血漿樣品,按2.4項下方法操作,進樣分析,以峰面積(Y)對血藥濃度(X)進行線性回歸得Y=81.013X+1257(r=0.9998)(n=6),血漿中金絲桃苷在0.341~13.64 μg·mL-1之間線性關系良好,血漿中金絲桃苷檢測限為0.079 μg·mL-1。
3.3 準確度實驗
精密吸取100μL空白血漿置于1mL離心管中,18份,分3組,精密加入不同量的金絲桃苷對照品,使分別為1.364,3.410,6.820 μg·mL-1的低、中、高濃度樣品,按 2.4項下方法操作,測定金絲桃苷含量,計算回收率,結果見表1。

表1 金絲桃苷回收率實驗(n=6,x±s)
3.4 精密度實驗
分別取金絲桃苷濃度為1.364,3.410,6.820 μg·mL-1的3種質量濃度的血漿樣品在2.5項下的色譜條件下于日內和日間各測定5次,計算日內及日間精密度,結果見表2。
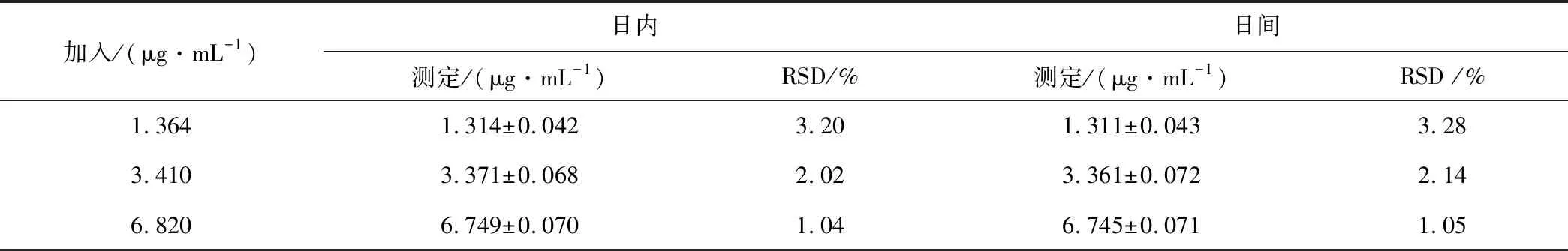
表2 金絲桃苷精密度實驗(n=6,x±s)
3.5 提取回收率
取上述的金絲桃苷濃度為1.364,3.410,6.820 μg·mL-1的血漿樣品(n = 6) ,按2.4項下方法處理,測定得到峰面積平均值A1;另取大鼠空白血漿100 μL,除不加對照品溶液,其他操作同“2.4”,向上清液中加入適量的金絲桃苷對照品溶液,使其濃度也分別為1.364,3.410,6.820 μg·mL-1的樣品,測定得到峰面積平均值A2,計算得低、中、高3個質量濃度的血漿樣品中山奈酚的提取回收率(R=A1/A2×100%)。結果為3個濃度的提取回收率分別為87.2%,89.3%,90.5%,其RSD分別為3.52%,2.79%,2.43%。
3.6 穩定性實驗
分別考察了灌胃給藥后大鼠血漿樣本在室溫、預處理后、反復凍融及長期冷凍條件下金絲桃苷的穩定性。結果表明,樣本室溫放置24h、預處理后樣品室內(4℃)放置3d、反復凍融3次及-20℃冷凍儲藏1月均有良好穩定性。
3.7 藥動學參數
用DAS2.0藥動學軟件對測得的血藥濃度數據擬合計算,結果表明千里光提取物和千柏鼻炎膠囊中的金絲桃苷在大鼠體內的藥動過程均符合2房室模型,主要的藥動學參數見表3,其平均藥-時曲線見圖2。
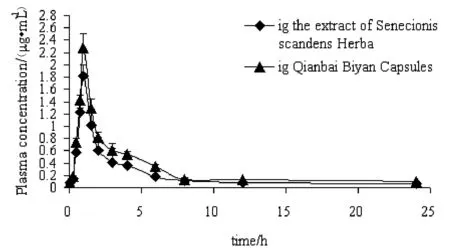
圖2 金絲桃苷在大鼠體內的藥-時曲線(-◆-千柏鼻炎膠囊灌胃;-▲-千里光提取物灌胃)表3 金絲桃苷在大鼠體內的主要藥動學參數
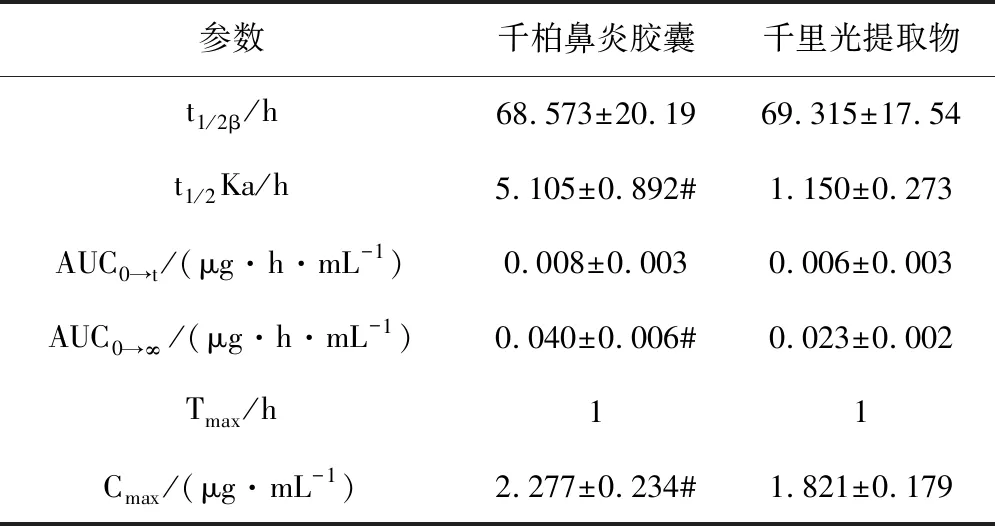
參數千柏鼻炎膠囊千里光提取物t1/2β/h68.573±20.1969.315±17.54t1/2Ka/h5.105±0.892#1.150±0.273AUC0→t/(μg·h·mL-1)0.008±0.0030.006±0.003AUC0→∞/(μg·h·mL-1)0.040±0.006#0.023±0.002Tmax/h11Cmax/(μg·mL-1)2.277±0.234#1.821±0.179
注:與千里光提取物組比,#P<0.05。
4 討論
分別比較了甲醇、乙腈、6 %高氯酸、三氯乙酸等有機溶劑,通過綜合比較雜質干擾及提取回收率因素,發現乙腈沉淀蛋白效果最好。同時考察了不同體積比的血漿-乙腈(1∶2,1∶3,1∶4)對金絲桃苷測定的影響,發現血漿-乙腈(1∶2)時沉淀蛋白效果已經符合要求,如繼續加大乙腈體積,則可能會對樣品的檢測濃度帶來影響。
曾嘗試采用2015版中國藥典一部所載的千柏鼻炎膠囊中金絲桃苷的測定方法,即流動相乙腈-0.2 %醋酸水溶液(15∶85),用于本藥動學研究中血漿樣品的金絲桃苷檢測,但通過前期的摸索研究,金絲桃苷與某內源性成分難以完全分離,故調整流動相為乙腈-0.2 %醋酸水溶液(14∶86)。
在本研究中,兩組大鼠分別灌胃給予千里光提取物和千柏鼻炎膠囊后,金絲桃苷的藥動學研究顯示,其藥-時曲線均符合二房室模型。但灌胃千柏鼻炎膠囊后金絲桃苷的Cmax為千里光提取物的1.25倍,AUC0→∞為1.74倍。上述結果表明,千柏鼻炎膠囊中的其他中藥配伍對金絲桃苷的體內過程有較大的影響,即中藥配伍能提高金絲桃苷口服吸收的生物利用度。此結果也從側面表明中藥在臨床上配伍應用有其內在的合理性,但其具體機制有待進一步的深入研究。

