miR-182抑制HES激活Notch信號協調TGF-β信號途徑促進急性川崎病
呂典一 武付霞 陳鳳儀
川崎病(kawasaki disease,KD)又稱皮膚黏膜淋巴結綜合征(mucocutaneous lymph node syndrome,MCLS),是兒科常見的一種以全身性血管炎為主要病理改變的急性發熱性出疹性疾病。相關研究表明,KD的發生與急性免疫功能失衡有關[1]。Treg細胞屬于T細胞亞群,外周血叉頭樣轉錄因子3(forkhead box protein3,Foxp3)是其主要標志物之一。而Jagged1介導的Notch激活可以抑制人類靜脈內皮的增生。研究表明,轉化生長因子-β(transforming growth factor-β,TGF-β)通過誘導Foxp3表達,促進活化的CD4+T細胞向Treg細胞分化,而TGF-β與白細胞介素6(interleukin-6,IL-6)共同作用可以抑制Treg細胞產生,并誘導初始T細胞分化為Th17細胞[2]。TGF-β信號途徑與Notch信號途徑間存在對話通路,可以在多種細胞中協同作用,共同調節目標基因表達。相關研究表明,Notch信號途徑可以上調Foxp3蛋白的表達[3]。
研究表明miR-23a 、miR-130a和miR-125b在川崎病患者外周血清中均有表達[4-5],通過對川崎病人血液樣本外泌體檢測,發現miR-1246、miR-4436、miR-197、miR-671表達明顯上調。通過高通量篩選發現miR-182在川崎病急性發病期顯著上調,結合目前國際上相關川崎病的miRNA靶標研究,本研究對miR-182在急性川崎病發生及與川崎病患者臨床特征的研究進行探討,旨在為急性川崎病檢測與治療提供新靶點。
對象與方法
一、對象
選取2016年7月至2018年6月本院收治的急性期KD患兒(發熱5~6天)21例為KD急性組,診斷標準參照2015年第七版實用兒科學[11]其中男12例,女9例;平均年齡(23.2±18.4)歲。選取同期于本院治療的治愈期KD患兒14例KD治愈組,平均年齡(20.9±19.1)歲,男8例,女6例;同時選取健康兒童16例為正常對照組,平均年齡(22.3±10.1)歲,男11例,女5例。三組對象的年齡、性別等一般資料比較,差異均無統計學意義(P>0.05),具有可比性。納入標準:(1)無腎病綜合征、先天性免疫缺陷病,過敏性疾病等免疫系統疾病;(2)近6個月未使用影響免疫功能的藥物。本研究經本院倫理委員會批準,且患兒監護人知情同意并簽署知情同意書。
二、方法
1.血樣采集:采用肝素鈉抗凝采血管收集患兒入院時急性期、治愈期及正常對照組兒童清晨空腹靜脈血3ml。KD急性組患兒于靜脈注射丙種球蛋白前l天抽血。
2.流式細胞法檢測外周血Treg細胞比例:取兩個流式細胞檢測管,分別標記為Treg細胞管和陰性對照管。兩管分別加入100 μl血、20 μl CD4-FITC和20 μl CD25-PC5,劇烈蝸旋,室溫下避光孵育15 min。于Treg細胞管中加入100 μl破膜劑I,劇烈蝸旋,室溫下避光孵育15 min;陰性對照管中加入磷酸鹽緩沖液(PBS) 2 ml,20 ℃ 300g離心5 min,棄上清。Treg細胞管中加破膜劑II 100 μl,室溫下孵育5 min,輕輕振蕩1~2 s;兩管分別加試劑20 μl Foxp3-PE、Mouse IgG1-PE,輕輕振蕩,室溫避光孵育15 min,兩管均加PBS 2 ml,20 ℃300g離心5 min,棄上清,加500 μl PBS,4 ℃冰箱保存,24 h內上機檢測。
3.qRT-PCR檢測:取KD急性組、KD治愈組和正常對照組血清標本各0.5 ml,采用TRIzol法提取血清總RNA,采用反轉錄試劑盒將提取到的總RNA進行RNA逆轉錄,合成cDNA。具體實驗步驟嚴格參照Trizol試劑盒說明書。采用qRT-PCR法檢測目的基因mRNA的表達水平,具體實驗步驟嚴格參照試劑盒說明書進行。實驗重復3次。
4.細胞培養:采用含10%胎牛血清的培養基在37 ℃,5%CO2的培養箱中常規培養Treg細胞,待細胞融合度≥80%時,用2.5%的胰蛋白酶每2天進行消化,傳代,并取對數生長期細胞用于實驗。
5.細胞轉染:取對數生長期的Treg細胞,接種于6孔板中,每孔接種1.5×106個,并置于37 ℃、5% CO2培養箱中培養至細胞融合度為60%~70%時進行轉染。將Treg細胞分為2組:Ncontrol的miRNA對照轉染組以及miR-182過表達miRNA轉染組,并將培養基換成每孔1 ml無血清無雙抗的培養基,miRNA及轉染試劑Lipofectamine 2000分別用100 μl OMEM稀釋后,依照公司說明書所需比例混勻后靜置20 min后,逐滴加入并且輕晃混勻,培養6 h后,再換為含完全培養基,待48 h后收集細胞進行下一步分析。
6.熒光素酶報告基因法檢測:通過microRNA靶基因數據庫預測到miR-182與HES1的3’-UTR存在結合位點。為了驗證miR-182與HES1是否存在靶向關系,構建野生型HES1的3’-UTR熒光素酶報告基因質粒pMIR-HES1-wt,并以pMIR-HES1-wt質粒為模板,利用PCR搭橋法(overlapping PCR)構建其潛在結合位點突變型報告基因質粒pMIR-HES1-Mut。將miR-182 mimics,negative control miRNA mimics (miR-NC),內參海腎熒光素酶以及pMIR-HES1-wt和pMIR-HES1-Mut報告基因質粒共轉染進HCAEC細胞中,于37 ℃,5% CO2的細胞培養箱中培養36 h后收取細胞,使用雙熒光素酶報告基因檢測試劑盒測定三組細胞的熒光素酶活性。具體操作步驟嚴格參照試劑盒說明書。實驗共重復3次。
7. Western Blot:采用含50 mmol/L Tris-HCl(pH 7.4),150 mmol/L NaCl,0.5%脫氧膽酸鈉,0.1% SDS和蛋白酶抑制劑及1 mmol/L苯甲基磺酰氟的RIPA裂解液分離蛋白質。通過SDS-PAGE凝膠進行電泳,按說明書進行Western Blot實驗。
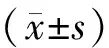
結 果
一、KD患兒的臨床資料及miR-182在KD臨床特征的相關性
我們通過血液常規檢測KD各組的臨床研究數據,結果顯示,除各組研究對象年齡無統計學意義(P>0.05),其他各組數據相比都具有顯著性差異(P<0.05),說明本次實驗對象分組是有可比性的,有研究價值(表1)。我們進一步通過檢測血清miR-182表達水平與KD患兒臨床特征的相關性,結果發現miR-182在血小板計數大于300×109/L的KD急性組血清中的表達水平顯著高于正常對照組(P<0.05),而其他各組數據指標上并無顯著性差異無統計學意義(P>0.05)(表2)。結果提示,急性KD血清中miR-182表達量相對較高,這種異常現象可能是參與KD病理進程,miR-182對急性KD具有調控功能。

表1 血液檢測KD各組的臨床數據

表2 檢測血清miR-182表達水平與KD臨床特征相關性
二、流式細胞法檢測各組外周血中Treg細胞比例
流式細胞儀檢測結果顯示:KD急性組外周血中Treg細胞比例為(4.4±1.4)%,明顯低于KD治愈組和正常對照組的(9.0±2.0)%、(10.2±2.8)%,差異有統計學意義(P<0.05)表3。
三、外周血中目的基因qRT-PCR檢測結果
1.外周血mRNA表達水平的比較:qRT-PCR檢測結果顯示:KD急性組中( Foxp3, Notch1,Notch3,Jagged1,HES1) mRNA 的表達水平低于KD治愈組和正常對照組,差異有統計學意義(P<0.05);而KD急性組中Jagged2 mRNA表達水平與正常對照和KD治愈組比較,差異無統計學意義(P>0.05)表4。



GroupnTreg cell fraction(%)Acute214.4±1.4Cure149.0±2.0Normal control1610.2±2.8

表4 外周血中外周血中mRNA 表達水平的比較
2.TGF-βmRNA表達水平的比較:qRT-PCR檢測結果顯示:KD治愈組與正常對照組外周血中TGF-β mRNA表達水平比較,差異無統計學意義(P>0.05);KD急性組外周血中TGF-β mRNA表達水平明顯低于正常對照組和KD治愈組,差異有統計學意義(P<0.01)(圖1)。
3. TGF-βRI、TGF-βRII、Smad3、Smad4 mRNA表達水平的比較:qRT-PCR檢測結果顯示:KD急性組TGF-βRI、TGF-βRII、Smad3、Smad4 mRNA的表達水平均明顯低于正常對照組與KD治愈組,差異均有統計學意義(P<0.05),見圖2。
四、 miR-182與靶基因HES1的關系
雙熒光素酶檢測結果顯示:miR-182 mimics可以抑制pMIR-HES1-wt質粒熒光素酶活性;而對pMIR-HES1-Mut熒光素酶活性無明顯影響(圖3)。
五、miR-182與靶基因HES1的調控作用
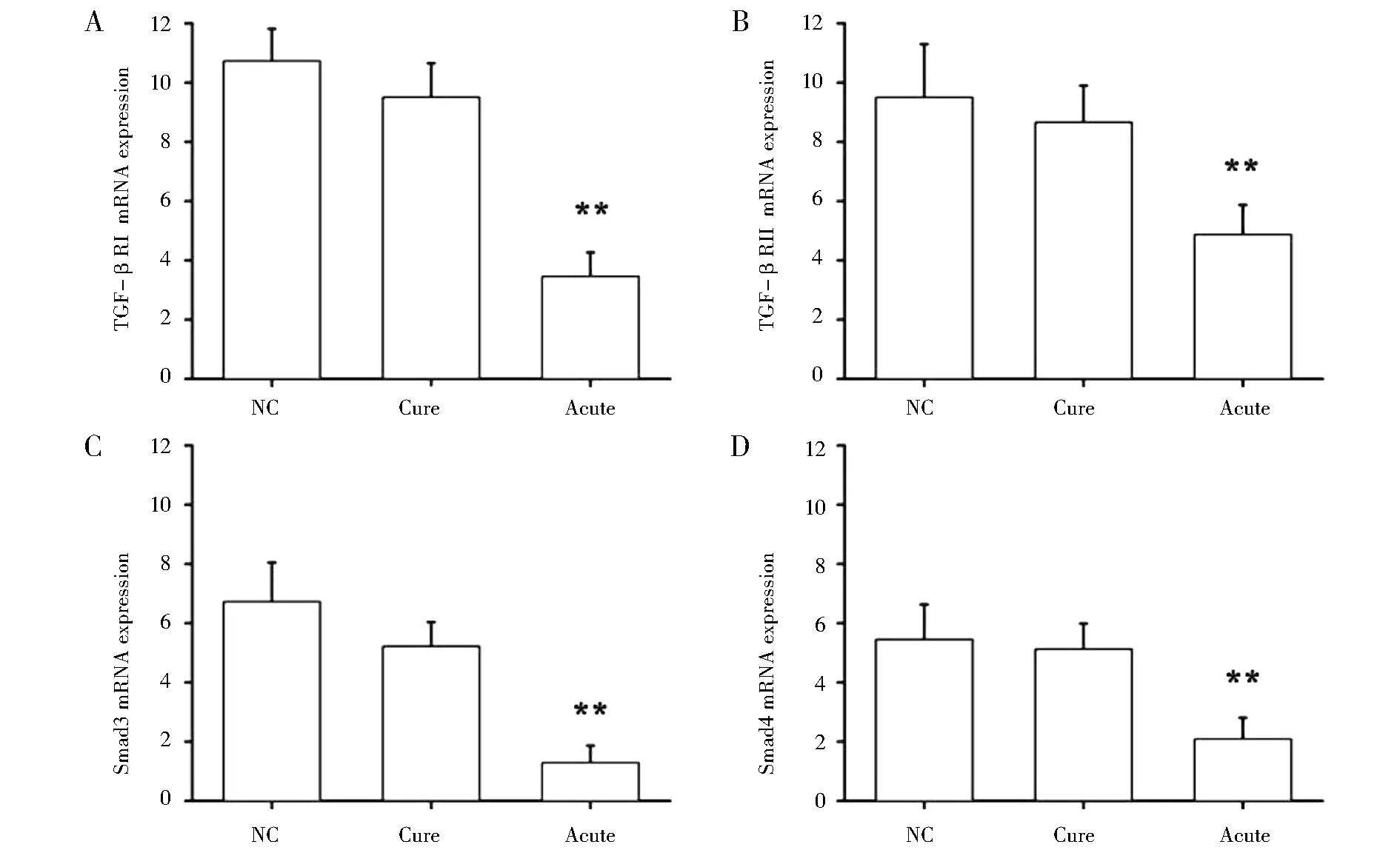
為進一步驗證miR-182對HES1的調控作用,通過qRT-PCR檢測發現,miR-182 mimics轉染組中HES1 mRNA表達水平低于對照組,差異有統計學意義(P<0.05);并且Western blot檢測結果顯示:miR-182 mimics轉染組中HES1蛋白表達水平低于對照組,差異也有統計學意義(P<0.05)。表明miR-182能夠抑制HES1的mRNA翻譯及其蛋白表達(圖4)。

Note: **compared with the normal control group(NC), P<0.01圖1 各組外周血中TGF-β mRNA的表達水平Figure 1 Expression levels of TGF- mRNA in peripheral blood by KD group
Note: **compared with the normal control group(NC), P<0.01圖2 各組外周血中TGF-βRI、TGF-βRII、Smad3、Smad4 mRNA的表達水平Figure 2 Expression levels of TGF- RI mRNA, TGF- RII mRNA, Smad3 mRNA and Smad4 mRNAby groupThe expression levels of A.TGF- RI mRNA, B.TGF-RIImRNA, C.Smad3mRNA,D. Smad4 mRNA were detected by qRT-PCR** compared with the normal control group, P<0.01

Note: B ** compared with the normal control group, P<0.01圖3 miR-182與靶基因HES1的相關性Figure 3 The correlation between miR-182 and the target gene HES11.the binding site of mir-182 to the target gene,B.luciferase activity was detected by luciferase reporter gene assay ** compared with the normal control group, P<0.01
圖4 miR-182與靶基因HES1 mRNA表達水平及蛋白含量的關系Figure 4 Expression and protein content of miR-182 and the target gene HES1 mRNAA.the expression level of HES1 mRNA in miR-182 was detected by qRT-PCR,B.the protein expression level of HES1was detected by Western blot
六、HES1激活Notch及TGF-β信號通路
Western blot檢測結果顯示在HES1處理組中Notch及TGF-β途徑受體Notch1、Notch3、TGF-βRI、TGF-βRII、Smad3、Smad4的磷酸化蛋白表達水平顯著升高,差異有統計學意義(P<0.05),而在加入抑制劑后,在DAPT+HES1處理組中則顯著降低,差異有統計學意義(P<0.05)。結果提示HES1激活了Notch及TGF-β信號通路,誘導了途徑受體表達升高。

圖5 HES1激活Notch及TGF-β信號通路Figure 5 HES1 activated Notch and TGF- signaling pathways
討 論
川崎病是兒童常見的一種自身免疫性血管炎綜合征,其主要累及患兒心臟的冠狀動脈,可導致冠狀動脈擴張、冠狀動脈狹窄及冠狀動脈瘤,嚴重時可導致患兒心肌梗死。目前,KD已成為兒童成年后心臟疾病和冠狀動脈損傷的重要原因之一。
Treg細胞是維持機體自身耐受,負向調節免疫反應的關鍵因素。Foxp3主要表達于Treg細胞,是Treg細胞的主要標志物,也是Treg細胞發育、功能特異性的主要調節因素之一。本研究結果顯示,KD急性組外周血中Treg細胞比例、Foxp3 mRNA表達水平均低于正常對照組和KD治愈組。急性KD患兒外周血中Treg細胞減少,與KD的病理進程有關系,而Foxp3的低表達可能是Treg細胞減少的重要原因,可能在急性川崎病的病理進程中發揮調節作用[6]。
相關研究表明,TGF-β單獨存在時可以上調初始T細胞中Foxp3的表達,促進初始T細胞分化為Treg細胞[7]。本研究結果顯示,KD急性組TGF-β mRNA的表達水平低于正常對照組和KD治愈組。結果提示,TGF-β的低表達可能與Foxp3異常表達有關,是導致Treg細胞減少的重要原因。TGF-β與其受體Ⅱ結合形成雜合四聚體復合物,激活TGF-β信號通路。TGF-β Ⅱ型受體激活時,可使TGF-β Ⅰ型受體富含甘氨酸、絲氨酸的區域磷酸化,進而磷酸化Smad3蛋白。Smad3磷酸化后與受體/SARA復合物脫離,與Smad4形成低聚復合物。低聚復合物可以易位至細胞核,與Foxp3啟動子富含GC序列的區域相互作用,誘導Foxp3表達。本研究結果顯示,KD急性組TGF-βRⅠ、TGF-βRⅡ、Smad3、Smad4 mRNA的表達水平均低于正常對照組與KD治愈組(P<0.05),表明Smad蛋白信號途徑的低表達可能是急性KD Foxp3表達水平下降的直接原因。
相關研究表明,TGF-β和Notch信號途徑間存在對話通路,Notch信號途徑與Treg細胞分化有關,Notch1是TGF-β1介導Treg細胞免疫抑制的關鍵因子[8]。HES1可能是Notch和TGF-β信號途徑的直接靶基因,TGF-β信號途徑中釋放的磷酸化Smad3蛋白與Notch信號途徑中釋放的Notch1受體胞內結合域結合,可以促進磷酸化Smad3蛋白的核易位。當TGF-β信號途徑的表達受影響時,相關下游分子和Notch信號途徑的表達均受到影響,從而導致Foxp3表達下調。Notch的配體Jagged也可以調控Treg細胞,Jagged1過表達可以誘導抑制性CD4+T細胞的分化,Jagged2可以通過Notch途徑推動Treg細胞分化[9]。本研究結果顯示,KD急性組Notch1、Notch3、Jagged1、HES1 mRNA的表達水平低于KD治愈組和正常對照組(P<0.05),而Jagged2 mRNA的表達水平與KD治愈組和正常對照組比較,差異無統計學意義(P>0.05)。然后我們用Western blot檢測結果顯示在HES1處理組中Notch及TGF-β途徑受體Notch1、Notch3、TGF-βRI、TGF-βRII、Smad3、Smad4的磷酸化蛋白表達水平顯著升高,差異有統計學意義(P<0.05),而在DAPT+HES1處理組中顯著降低,差異有統計學意義(P<0.05)。結果說明,靶基因HES1低表達和Notch信號異常有關,Notch信號途徑異常可能與Treg細胞減少也有關,而HES1激活了Notch及TGF-β信號通路,誘導了途徑受體表達升高。
miRNA參與了細胞的代謝、增殖、分化及凋亡等過程,可以廣泛調節機體的生理、病理過程,與腫瘤、心血管疾病、遺傳性疾病等的發生發展有關。miRNA在致病機理的研究、疾病的診斷和治療方面的重要性越來越受到人們的關注[10]。本研究檢測血清miR-182表達水平與KD患兒臨床特征的相關性,結果發現miR-182在血小板計數>300×109/L的急性期KD患兒血清中的表達水平低于血小板計數≤300×109/L的急性期KD患兒(P<0.05),結果提示,急性川崎病(KD)血清中miR-182表達量相對較低,這種異常現象可能是其參與KD病理進程,對KD具有調控功能。通過microRNA靶基因數據庫進行篩選,預測HES1為miR-182的潛在靶基因,構建了HES1野生型3’-UTR熒光素酶報告基因質粒pMIR-HES1-wt及突變型報告基因質粒pMIR-HES1-Mut。將miR-182 mimics,negative control miRNA mimics (miR-NC),內參海腎熒光素酶以及pMIR-HES1-wt和pMIR-HES1-Mut報告基因質粒共轉染進HCAEC細胞中,雙熒光素酶檢測結果顯示,miR-182 mimics可顯著抑制pMIR-HES1-wt質粒熒光素酶活性;而對pMIR-HES1-Mut熒光素酶活性無明顯影響。結果表明miR-182可以通過結合HES1的3’-UTR進而抑制HES1的表達。為進一步驗證miR-182對HES1的調控作用,通過qRT-PCR檢測發現,miR-182 mimics轉染組中HES1的mRNA表達水平顯著低于對照組,并且Western blot檢測結果顯示,相比對照組,miR-182 mimics轉染組中HES1蛋白表達水平顯著降低。上述結果表明miR-182能夠抑制HES1的mRNA翻譯及其蛋白表達。
綜上所述,miR-182可以通過下調HES1的表達抑制Notch與TGF-β信號途徑,可能導致Treg細胞減少,miR-182與HES1的靶向調控可能會成為急性川崎病檢測與治療醫學的新靶點。

