基于PET成像的阿爾茨海默病研究進展
王志強 姚旭峰 黃 鋼
1(上海理工大學醫療器械與食品學院,上海 200082)2(上海健康醫學院醫學影像學院,上海 201308)
引言
進入21世紀以來,全球老齡化的速度在逐步加快,據估計到本世紀中葉世界上患有阿爾茨海默病(Alzheimer′s disease,AD)的人數將會增長至1.15億[1]。作為常見的癡呆病癥,AD的臨床診斷表現為大腦糖代謝能力下降、淀粉樣蛋白積聚以及纖維狀神經糾纏。在眾多檢查AD的成像技術中,正電子發射斷層顯像(positron emission tomography,PET)和磁共振顯像(magnetic resonance imaging,MRI)可以將AD患者的腦部變化以放射性示蹤劑分布和結構萎縮的形式表征出來,因而常被用于診斷AD。18F標記的氟代脫氧葡萄糖正電子發射斷層顯像(18F-fluorodeoxyglucose positron emission tomography,FDG PET)和淀粉樣蛋白正電子發射斷層顯像(beta-amyloid positron emission tomography,Aβ PET)是PET成像中兩種常用的診斷方式,在揭示AD病理過程、診斷AD及辨別其他種類癡呆中有著不可忽視的作用。本文主要闡述FDG PET、Aβ PET以及兩種方式聯合成像的應用現狀,并與MRI成像進行比較,總結存在的問題,并分析AD診斷的發展方向。

表1 FDG PET和Aβ PET診斷效果Tab.1 Diagnostic effect of FDG PET and Aβ PET
注:NC為正常對照組。
Note: Normal controls, NC.
1 PET應用現狀
FDG PET和Aβ PET是臨床上常用的AD診斷技術,前者是依據大腦葡萄糖代謝程度的變化來確認患者是否存在神經變性,進而確診AD;而后者是利用示蹤劑與淀粉樣蛋白特異性結合的特點來顯示神經細胞外部病變,雖起步較晚但發展迅速。尤其近年來,18F類示蹤劑(如18F-Flobetapir[2]、18F-flutemetamol[3]、18F-florbetaben[4]等)的應用增強了人們對AD病理過程的認識。下面將從診斷效果評估和辨別癡呆種類來闡述兩種成像的應用現狀。
1.1 診斷效果評估
如表1所示,Mosconi等[5]采用體素自動比較和疾病特異性FDG模式來表征AD代謝特征;陶霖等[6]采取視覺評估和感興趣區法(reagion of interest,ROI)發現輕、中、重度AD患者腦區代謝差異;周夢溪等[7]采用統計參數圖(statistical parameter map,SPM)討論AD患者腦部代謝與認知功能的相關性,三者采用的都是FDG PET顯像方式。Klunk等[8]通過11C匹茲堡化合物(11C-Pittsburgh compound B PET,PIB PET)顯像發現,受AD病理影響大腦多個腦區都存在PIB滯留;Fu等[9]則探究早期AD患者的大腦默認網絡特征改變;而Sabri等[10]采用半定量分析方法,證實了18F-florbetaben PET(FBB PET)顯像在AD診斷方面的優勢。盡管成像方式不同,但FDG PET和Aβ PET在識別AD患者典型特征和診斷靈敏度方面都具備良好的能力。
1.2 辨別癡呆種類
如表2所示, Pagani等[11]采用協方差和支持向量機(support vector machines,SVM),探究FDG PET預測輕度認知障礙患者(mild cognitive impairment,MCI)發展為AD的能力;Morbelli等[12]借由SPM和Kaplan-Meier曲線法,進行MCI患者轉化為AD的特征腦區和轉化時間的研究;Foster等[13]則采用立體定向表面投影等多種方法鑒別AD與額顳葉癡呆(frontotemporal dementia,FTD),肯定了FDG PET在臨床的輔助診斷作用;Ong等[14]則利用FBB PET探究MCI轉化為AD的預后準確性,發現其有助于精準檢測早期AD患者;Namiki等[15]對48例日本受試者進行18F-florbetapir PET顯像,評估其在臨床上的診斷表現;Jiménez-Bonilla等[16]采用PIB PET顯像,發現其能以較高準確率辨別AD患者及其他種類癡呆;Rabinovici等[17]比較臨床診斷表現時發現,PIB PET在辨別AD和FTD上具備80%以上的診斷準確性,略優于FDG PET。
1.3 聯合成像
FDG PET可以從功能代謝角度來診斷AD,但是對于退行性神經疾病重疊的情況則難以辨別,如非典型額顳葉癡呆和AD的重疊腦區[18]。Aβ PET成像可以從病理變化角度來早期診斷AD,但在病情評估方面不如FDG PET。因而將兩種成像方式結合進行聯合成像,是一種提高AD診斷準確性和辨別癡呆種類的有效方法。
如表3所示,李毅等[19]、Hatashita等[20]、王穎等[21]、Iaccarino等[22]、Brück等[23]采用的是FDG+PIB PET的掃描組合,研究通過辨別癡呆種類和預測MCI轉換方面證實了聯合成像具備優秀的診斷優勢;而Brendel等[24]則采用FDG+FBB PET的掃描組合,研究認為FBB PET可作為可疑病例的最終診斷工具,以及辨別AD和FTD的增值指標。
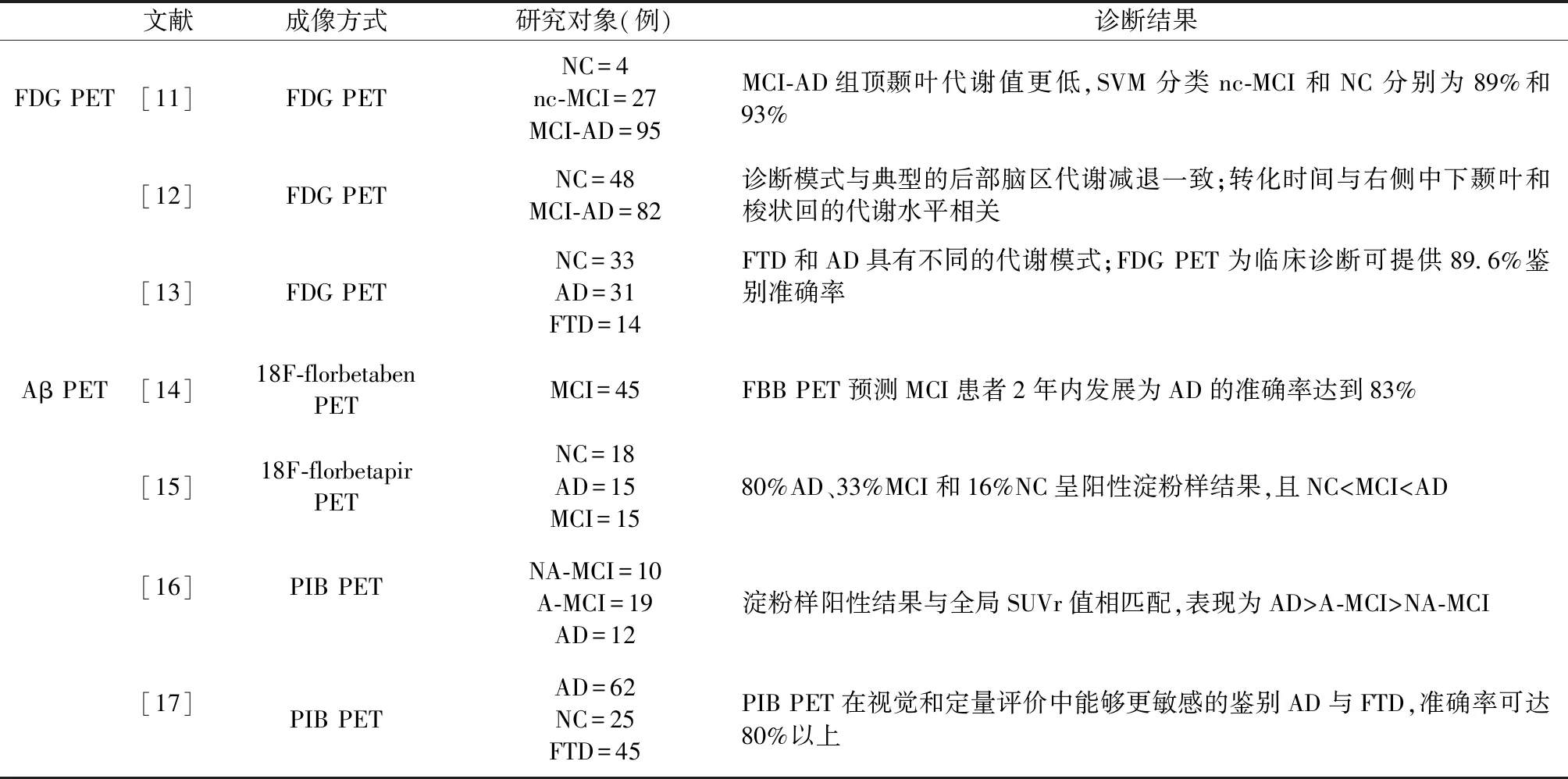
表2 FDG PET和Aβ PET辨別癡呆分類Tab.2 FDG PET and Aβ PET discriminating dementia classification
注:nC-MCI為未轉化為AD的MCI;MCI-AD轉化為AD的MCI;NA-MCI為非遺忘性MCI;A-MCI為遺忘型MCI。
Note: Not convert to AD, nc-MCI; Convert to AD, MCI-AD; Not amnestic MCI, NA-MCI; Amnestic MCI, A-MCI.
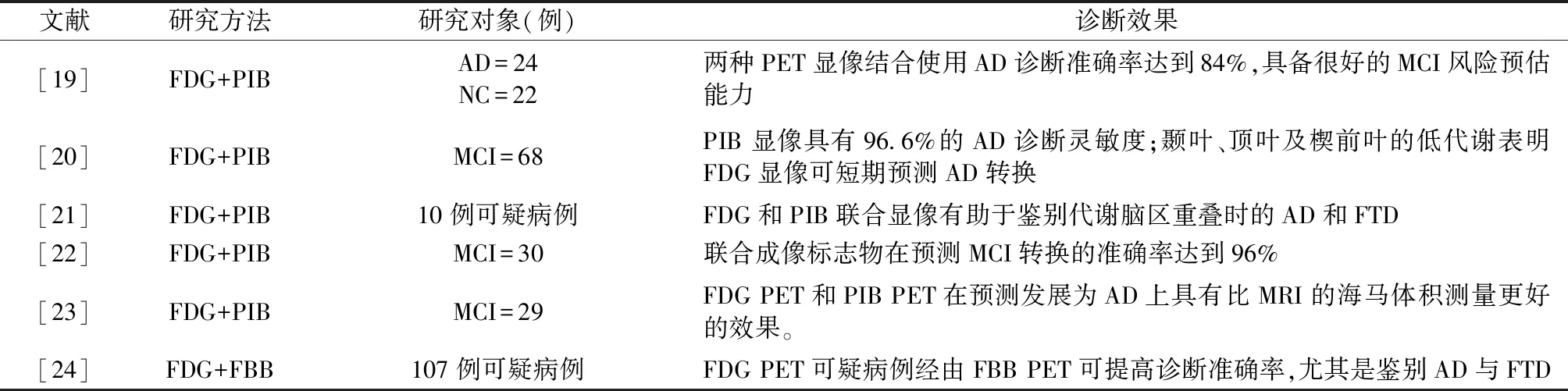
表3 聯合成像診斷效果Tab.3 Joint imaging diagnosis results
2 PET與MRI比較
相比于PET顯像,MRI成像具有以下優勢:高質量的空間分辨率、足夠的對比度,圖像采集期間不需要放射性藥物注射,掃描費用較為廉價。但MRI圖像一般具有高維度,難以進行數據分類和處理,為此出現了多種方法增強了MRI的AD診斷能力,如表4所示。
Faturrahman等[25]提出深度置信網絡(deep belief network,DBN)與結構磁共振(structural magnetic resonance,sMRI)相結合的模型,證實了DBN在處理高維度數據的優勢;Islam等[26]則利用深度卷積網絡 (deep convolutional neural networks,
CNN),為多種分類提供顯著改進,并有助于檢測早期AD;Demirhan等[27]的研究表明,多變量的形態特征和機器學習可成功檢測AD;Steketee等[28]采用動脈自旋標記MRI(ASL-MRI)的方法,證實有助于AD和FTD的診斷和鑒別;徐盼盼等[29]將腦白質圖像和支持張量機(support tensor machine,STM)算法相結合,提高了癡呆診斷的能力;Li等[30]提出卷積自動編碼(convolutional autoencoders,CAEs)和CNN相結合的算法,無需區域分割便可實現較高的AD分類;Yang等[31]證實SVM和耦合特征表示法(coupled feature representation,CFR)在預測MCI轉化為AD方面具備一定的潛力。

表4 MRI診斷效果Tab.4 MRI diagnostic effect table
注:卷積自動編碼表示為CAEs;耦合特征表示為CFR。
Note: Convolutional autoencoders, CAEs; Coupled feature representation, CFR.
3 總結和展望
PET和MRI雖然在臨床AD診斷上得到廣泛應用,但仍存在一些問題,主要包括3個方面:一是圖像質量、受試者數量以及隨訪時間都會影響對AD病理過程的評估和預測;二是臨床和科研中通常采用視覺評估和定量參數相結合的方式解讀醫學圖像,因從醫經驗和評價參數不同,診斷結果帶有主觀性和模糊性;三是正常老齡化個體中也會出現海馬萎縮、代謝降低和淀粉樣陽性結果,故需要結合多模態成像方式聯合診斷AD。
針對這些問題,2011年美國國家老齡化協會頒布了新的AD診斷標準[32],促使科研人員進行多方面的嘗試研究。Lu等[33]、Shi等[34]、Ortiz等[35]和Li[36]等的研究中皆采用阿爾茨海默病神經影像學倡議(Alzheimer′s disease neuroimaging initiative,ADNI)中的數據,并分別將FDG PET、PIB PET、18F-Flobetapir PET與MRI的圖像特征應用于深度神經網絡(deep neural network,DNN)、堆疊深度多項式網絡(stacked deep polynomial networks,SDPN)、稀疏分類器(sparse representation classifiers,SRC)以及圖論方法中,4項研究結果證實,多模態影像數據間的信息互補有助于提高AD診斷率和MCI轉化預測;Youssofzadeh等[37]則利用澳大利亞影像生物標記物數據庫(australian imaging,biomarkers and lifestyle,AIBL)測試出多核學習技術(multi-kernel learning,MKL)和Dartel算法在AD分類效果上的良好表現;另外郝曉勇等[38]還總結出彌散張量成像(diffusion tensor imaging,DTI)、擴散峰度成像(diffusion kurtosis imaging,DKI)等多種MRI技術在AD早期診斷中的應用,預測多模態MRI將在未來AD診斷中發揮重要作用。
除此之外,生物標記物對于理解AD發病機制和變化過程有很大幫助。Oh等[39]針對腦脊液生物標記物Aβ40、42和tau蛋白進行認知功能研究,發現老年人生物標記物與潛在認知功能的聯系會逐漸變弱;Vemuri等[40]使用結構方程模型(structural equation models,SEM)探究血管健康對生物標記物的影響,結果表明其對區域神經變性的影響要高于淀粉樣蛋白,但仍需縱向研究與tau蛋白的關系;Ramana等[41]采用全基因分析(genome-wide analytical strategies,GWAS)對淀粉樣蛋白基因進行研究,證實載脂蛋白基因和丁酰膽堿酯酶會對AD潛在病理學產生影響;另外在Olsson等[42]和Sheikh等[43]的回顧性研究中,肯定了腦脊液和血液標記物在臨床AD診斷的作用。
以上通過對FDG PET和Aβ PET的應用現狀進行總結,并與MRI相比較,對于臨床診斷AD具有一定的參考作用,但要更全面地了解AD仍需要不斷的關注和學習。

