乙型肝炎病毒S區基因突變對乙型肝炎病毒相關性肝細胞癌患者預后的影響研究
吳忱思,趙樂,吳建華,王英南,張風賓,高立明,趙林,張衛國,張瑞星*
原發性肝細胞癌(HCC)是我國常見的惡性腫瘤之一。HCC是目前全球發病率第5位、死亡率第2位的惡性腫瘤,每年約有70萬人死于肝癌[1],慢性乙型肝炎病毒(HBV)感染是導致肝癌發病的主要危險因素之一[2]。HCC患者的臨床特征,包括腫瘤分期、腫瘤大小、病理類型、炎癥程度和門脈瘤栓,是影響其預后的重要因素。HCC復發率高、治療手段有限,因此患者的預后仍然較差[3-4]。
我國HCC的發病率呈逐年上升趨勢,這主要與HBV感染流行有關,據世界衛生組織報道,全球每年約有100萬人死于HBV感染所致的肝衰竭、肝硬化和肝癌[5-6]。我國是乙型肝炎的高發區,根據第三次乙型肝炎流行病學調查統計,我國HBV的平均感染率為7.18%,其中慢性乙型肝炎患者高達3 000萬人[7]。根據HBV全基因序列或S區基因序列差異,HBV可分為A~J 10個基因型,我國HBV基因型主要為B型和C型[8-9]。
HBV是已知真核細胞中最小的病毒,由不完全的環狀雙鏈組成,其中一條較長的為負鏈,由3 200個堿基組成,包含4個開放讀碼框架(ORF),即S、X、C、P基因區,分別編碼外膜蛋白、X蛋白、核殼蛋白和聚合酶蛋白[10]。S基因區可分為3段,從上游開始依次為前S1(pre-S1)區、前S2(pre-S2)區和S區,HBV S區基因編碼的226個氨基酸組成的蛋白質是乙肝表面抗原(HBsAg)的主要組成部分;pre-S2區和S區基因共同編碼中蛋白;pre-S1區、pre-S2區和S區3部分基因共同編碼大蛋白[11]。由于HBV缺乏DNA酶的校正功能,所以HBV特別容易引發基因突變[12]。近年來,多項研究表明HBV基因突變與肝癌患者發病密切相關[13-16],HBV S區基因突變與HCC發病機制的關系已經成為研究熱點,本研究旨在探討HBV S區基因突變與HCC患者預后的關系。
1 材料與方法
1.1 肝癌組織標本采集 本研究于2007—2009年采集在河北醫科大學第四醫院行外科手術治療的46例乙型肝炎病毒相關性肝細胞癌(HBV-HCC)患者的肝癌組織標本,患者均被證實感染HBV,并排除其他肝臟疾病。通過患者的臨床癥狀、體征、肝臟CT和/或MRI、血清甲胎蛋白(AFP)等檢查,診斷為HCC并行HCC根治術,在術前及術后均未接受美國國立綜合癌癥網絡(NCCN)指南所推薦的放化療、靶向治療及局部介入治療。46例患者中女6例、男40例,中位年齡52歲。
本研究價值:
原發性肝細胞癌(HCC)的發病率逐年上升,已經成為威脅我國人民健康的主要疾病,乙型肝炎病毒(HBV)是導致其發病的重要相關因素。我國是乙型肝炎的高發區,有研究表明HBV基因突變與乙型肝炎病毒相關性肝細胞癌(HBVHCC)患者發病密切相關,但是關于基因突變與肝癌患者預后的研究相對較少,因此研究基因突變對HBV-HCC患者預后的影響,對于提高患者生存期具有極其重要的意義,本研究發現門脈瘤栓和HBV S區529位點與HBV-HCC患者術后預后密切相關,這一結果有利于在臨床中識別不良預后的HBV-HCC患者,及早治療,從而延長其生存期。
1.2 一般資料收集 年齡、性別、CHILD分級、基因型、腫瘤數目、門脈瘤栓、TNM分期、腫瘤大小。
1.3 術后隨訪 通過電話對患者或其家屬進行隨訪,隨訪時間截至2012年9月,生存時間從術后第1天開始計算,至死亡之日或隨訪結束日為止。以月為單位計算生存期,隨訪時間為3年,每3個月進行1次隨訪。本研究經過河北醫科大學第四醫院倫理委員會批準。
1.4 基因組DNA提取、PCR擴增及基因測序 采集肝癌組織標本置于-80 ℃冰箱保存,應用Promega公司DNA試劑盒,經過細胞核裂解、RNA降解、蛋白沉淀、離心、純化等步驟提取基因組DNA,并置于-20 ℃冰箱保存。通過美國國立生物技術信息中心(NCBI)數據庫(http://www.ncbi.nlm.nih.gov/genome/5536)查找引物(見表1)。對HBV S區的DNA序列進行PCR擴增,采用美國Promega公司的PCR無色體系預混試劑盒,使用美國基因有限公司PCR儀(AS Applied Biosystems 9902)進行目的基因擴增。其產物應用Life Technologies公司的ABI 7300 TaqMan平臺,通過多重PCR法測出HBV-HCC患者肝癌組織的HBV基因型,并進行循環測序及分析。為確保測序的準確性,對同一個樣本應用雙向重復測序方法,以明確HBV S區基因的突變位點。
1.5 統計學方法 采用SPSS 18.0軟件進行統計分析。采用Log-rank檢驗分析生存率,采用Cox比例風險模型對HBV-HCC患者術后生存影響因素進行分析。以P<0.05為差異有統計學意義。
2 結果
2.1 不同一般資料HBV-HCC患者術后3年生存率比較 46例HBV-HCC患者的基因分型為25例B型、21例C型。不同門脈瘤栓、TNM分期、腫瘤大小的HBVHCC患者3年生存率比較,差異有統計學意義(P<0.05,見表2)。
2.2 不同HBV S區基因突變位點HBV-HCC患者術后3年生存率比較 本研究對HBV S區的DNA序列進行基因測序,共發現13個位點的突變頻率>5%,其中529位點、735位點不同堿基HBV-HCC患者術后3年生存率比較,差異有統計學意義(P<0.05,見表3)。
2.3 HBV-HCC患者術后生存影響因素分析 將臨床指標(年齡、性別、CHILD分級、腫瘤數目、門脈瘤栓、TNM分期、腫瘤大小)和基因突變位點納入Cox比例風險模型進行分析,結果顯示門脈瘤栓、529位點是HBV-HCC患者術后生存的獨立影響因素(P<0.05,見表4)。
3 討論
HBV屬嗜肝DNA病毒科,由于缺乏HBV聚合酶的校對功能,因此特別容易發生基因突變,HBV比其他DNA病毒的突變率高10倍以上[6,11]。由于HBV感染可以引起肝臟的病理及免疫損傷,基因突變的積累會直接影響病毒的活性和免疫應答的強度,因此HBV基因突變所導致的病毒生物學變化在肝臟損傷過程中發揮著重要的作用[17]。研究發現,HBV突變主要集中在基因組的某些特定區域,例如基本核心啟動子(BCP)、pre Core/Core區和pre S/S區[18]。本研究重點探討HBV S區基因的突變與HBV-HCC患者術后3年生存率的關系,并通過生存分析鑒定出與HBV-HCC患者預后相關的突變位點為529位點。

表1 HBV S區基因擴增和測序引物Table 1 Primer pairs used for amplification and sequencing of the S gene region of HBV
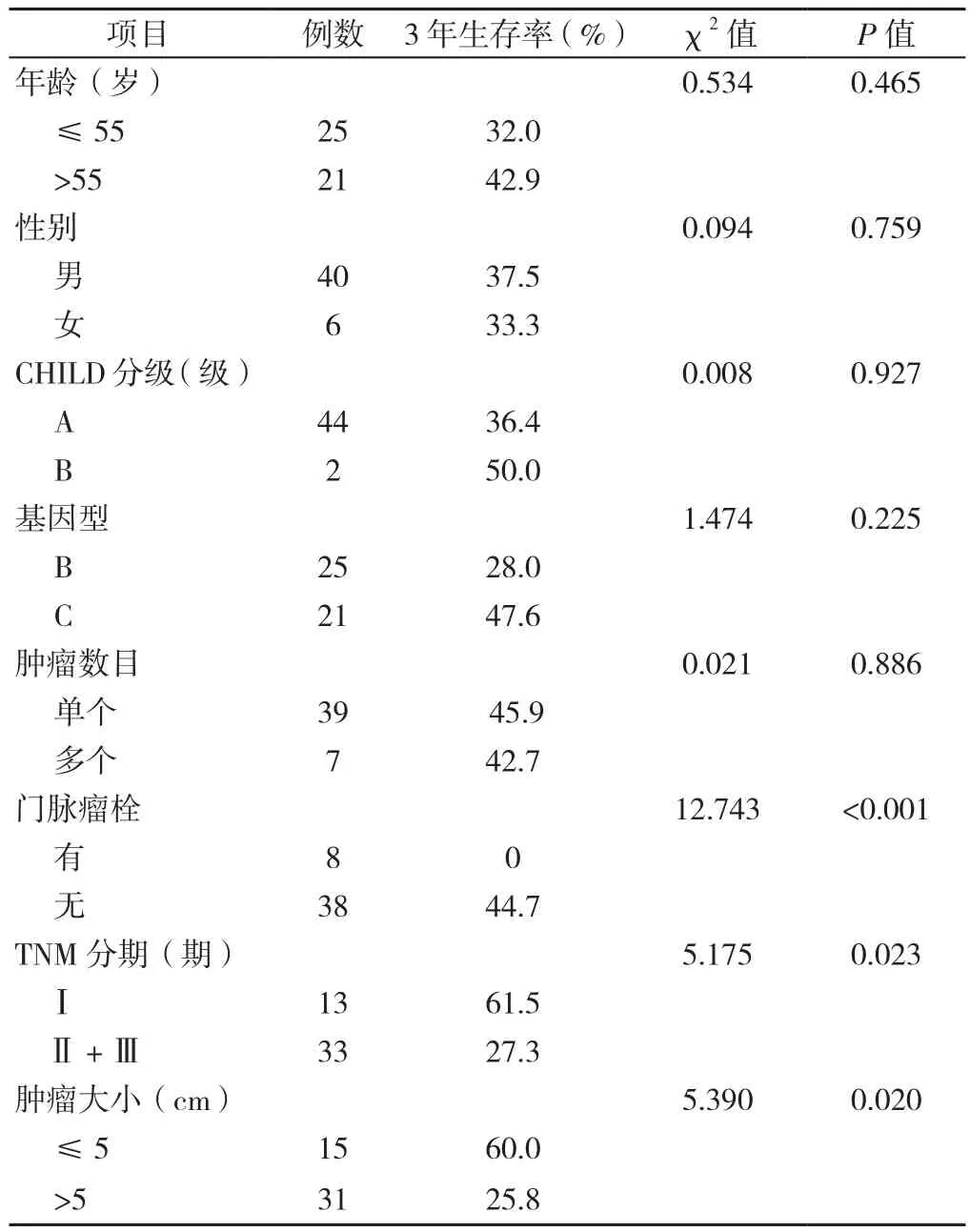
表2 不同一般資料HBV-HCC患者術后3年生存率比較Table 2 Postoperative 3-year survival rate in HBV-associated HCC patients with different data
HBV S區是HBV復制的關鍵區域,其所編碼的蛋白是HBsAg的主要組成部分,由S區基因編碼的HBsAg是HBV主要的抗原域,由226個氨基酸組成,含有一系列的構象性抗原表位,其主要的親水區位于aa99-169,其中最重要的免疫功能區域是位于aa124-147的“a”決定簇[11,19],是HBsAg的主要作用位點。HBsAg可以刺激機體產生抗體從而清除HBV,有研究表明“a”決定簇區域的突變可能誘導HBsAg的抗原性或病毒的適應性發生改變,甚至產生免疫逃逸,該區域的無義突變可以誘導HBsAg抗原性的改變,從而影響特異性抗體的產生[20-21]。如果突變位點位于“a”決定簇區域,該突變不會導致S區基因編碼的氨基酸替代,但是pre S/S區基因位點的突變,可能引起HBV聚合酶中的rtD134N的替代,從而導致HBV聚合酶的功能改變,進而影響病毒復制[22]。本研究發現,HBV S區529、735位點與HBV-HCC患者生存相關,目前尚未見國內外文獻對于這兩個位點的報道。既往研究表明,HBV S區基因突變可以誘導幾個特定的膜蛋白產生,從而激活內質網應激傳導通路,由此所產生的細胞毒性作用可以促進肝臟損傷并誘發疾病,通過內質網應激及大量活性氧的產生,可以引起DNA氧化損傷和基因組不穩定,最終導致HCC的發生[6,23-25]。國內外對于HBV S基因與HCC預后機制的研究尚未見報道,HBV S基因可能通過以上氨基酸替代、氧化損傷等過程,參與了腫瘤細胞的增殖、侵襲和凋亡,導致肝癌的復發與轉移,從而影響了患者的生存期及預后。由于研究的局限性及發病機制的復雜性,對于HBV S基因突變與HCC致病及預后關系的研究有待進一步探討,本研究為單中心研究,如果擴大樣本量,將其推廣到多中心進行聯合研究,并進行長期觀察,將有利于從基因水平深入探討肝癌的發病機制,從而改善患者的預后。
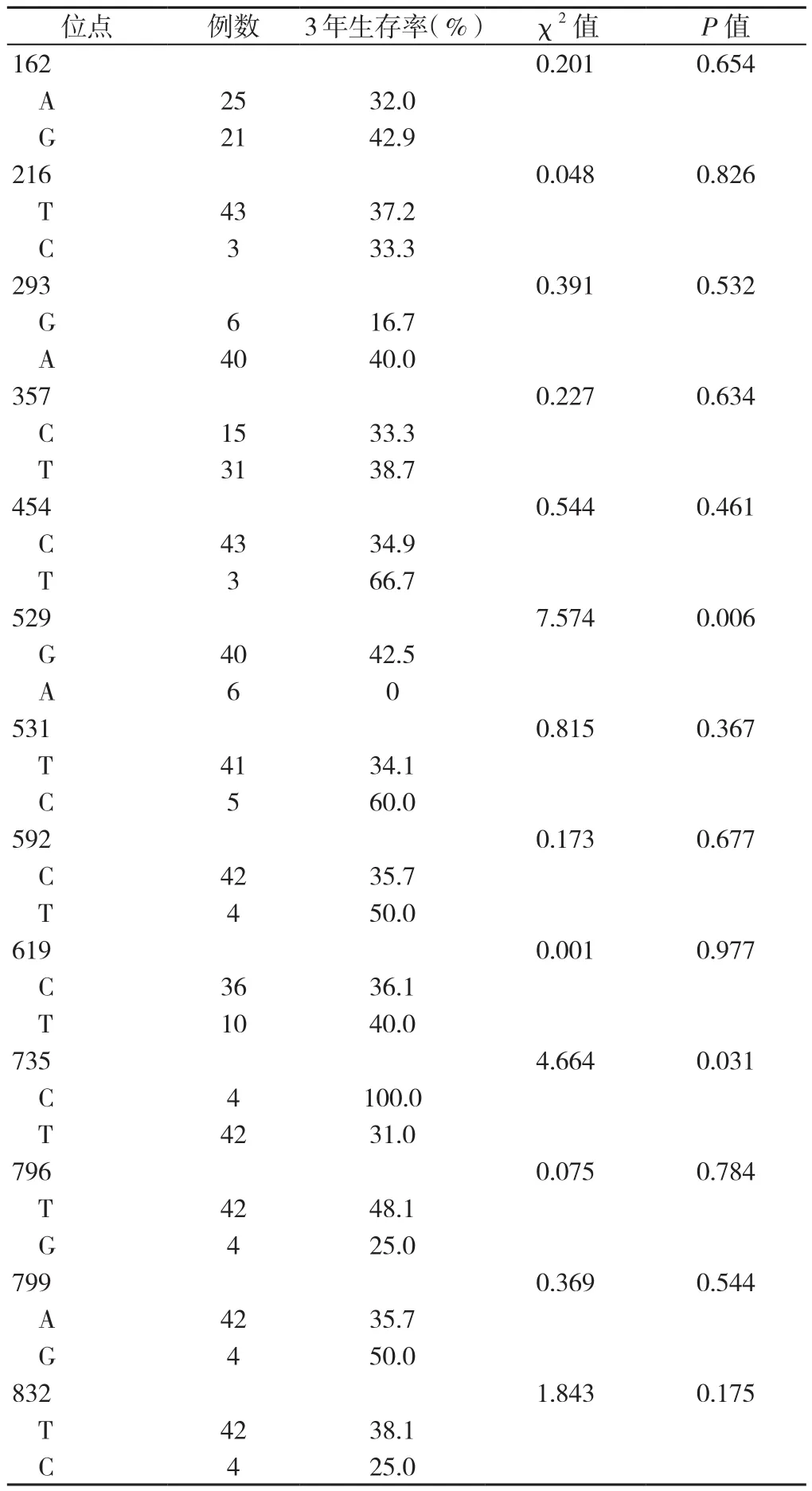
表3 不同HBV S區基因突變位點HBV-HCC患者術后3年生存率比較Table 3 Postoperative 3-year survival rate in HBV-associated HCC patients by mutations in the S gene region of HBV
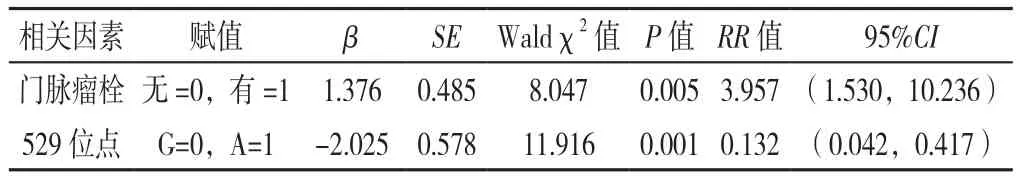
表4 HBV-HCC患者術后生存影響因素的Cox比例風險模型分析Table 4 Analysis of influencing factors for postoperative survival in HBV-associated HCC patients with the Cox proportional hazards model
總之,本研究發現了與HBV-HCC患者術后預后相關的HBV S基因突變位點,在臨床上針對HCC患者進行相關HBV突變位點的基因檢測,有助于鑒定具有不良預后的HBV-HCC患者并對其進行個體化治療。該突變位點的發現對于提高HCC患者生存期、改善其預后具有重要意義。

