基于CuFe2O4載氧體的羊腸煤化學鏈氣化特性
安 梅, 馬晶晶, 吳 唯, 任 天, 胡修德, 郭慶杰
(寧夏大學 省部共建煤炭高效利用與綠色化工國家重點實驗室, 寧夏 銀川 750021)
煤炭是中國目前乃至今后相當長一段時期內的主要能量資源[1]。隨著一帶一路和西部大開發進程的加速,寧東基地作為西部煤炭開發重心[2],其地位日益受到重視。然而,在資源日益短缺和環境日益惡化的雙重壓力下,寧東基地的煤炭轉化利用需要開發節能、環保、高效的煤炭轉化新技術。煤化學鏈氣化技術被認為是一種應用前景廣闊的煤轉化利用新技術[3-5]。因此,針對寧東基地煤炭的化學鏈氣化研究,對寧東煤炭資源開發利用具有重要的理論和現實意義。
煤化學鏈氣化技術的原理與化學鏈燃燒相似[6]。載氧體是煤化學鏈氣化的關鍵[7]。在煤化學鏈氣化反應體系中,除了要求載氧體循環穩定性好、價格低廉、來源廣泛和環境友好外,還需載氧體具有一定的催化功能[8]和適中的氧化能力[9],可以將煤氣化中間產物的碳氫元素盡可能地轉化為CO和H2,減少CO2和H2O的生成。目前已開發的載氧體有銅基[10]、鐵基[11-12]和鈣基[13]等,但銅基載氧體容易燒結、鐵基載氧體反應性能較低,鈣基(CaSO4)載氧體釋放有害含硫氣體。為了克服上述單一金屬載氧體的不足,雙活性組分載氧體被大量開發和測試[14-15],如具有尖晶石結構的CuFe2O4載氧體。Niu等[16-18]考察了CuFe2O4載氧體與不同燃料的化學鏈燃燒反應性能,發現CuFe2O4載氧體在反應過程中既能抑制Cu的燒結,又能增強Fe的還原能力,提高循環穩定性和反應活性。目前,Wang等[19]探究了過氧系數和反應溫度對化學鏈燃燒過程中CuFe2O4載氧體氧傳遞以及其對煤結構演變的影響。但CuFe2O4載氧體在化學鏈氣化和化學鏈燃燒過程中所處環境不同,氧傳遞機理和反應性能也存在差異。對煤化學鏈氣化過程中CuFe2O4載氧體的反應性和氧傳遞機理尚不清楚。因此,探究化學鏈氣化過程中CuFe2O4載氧體的反應性和氧傳遞機理非常必要。
基于此,筆者選擇寧東基地典型礦區羊腸煤為燃料,以CuFe2O4為載氧體,在TG-MS上以模擬煤氣作為燃料探索CuFe2O4載氧體還原過程的氧傳遞機理。在此基礎上,研究羊腸煤與CuFe2O4載氧體反應性能和循環穩定性。旨在為寧東煤炭資源化學鏈氣化新技術的開發利用提供理論基礎。
1 實驗部分
1.1 原料及試劑
三水合硝酸銅(Cu(NO3)2·3H2O)、九水合硝酸鐵(Fe(NO3)3·9H2O)和硼氫化鈉(NaBH4)均為分析純,國藥集團化學試劑有限公司產品。煤粉為次煙煤,產自寧夏寧東基地,粒徑為75~150 μm,使用前于105 ℃干燥12 h,記為YC,其工業分析及元素分析見表1,煤中主要金屬氧化物質量分數見表2。

表1 羊腸煤(YC)工業分析及元素分析結果Table 1 Proximate and ultimate analysis of YC
1) Proximate analysis; 2) Ultimate analysis
Md—Moisture; Ad—Ash; Vd—Volatile; FCd—Fixed carbon; C—Carbon element; H—Hydrogen element; N—Nitrogen element; St—Total sulfur element; O — Oxygen element; LHV — Lower heating value
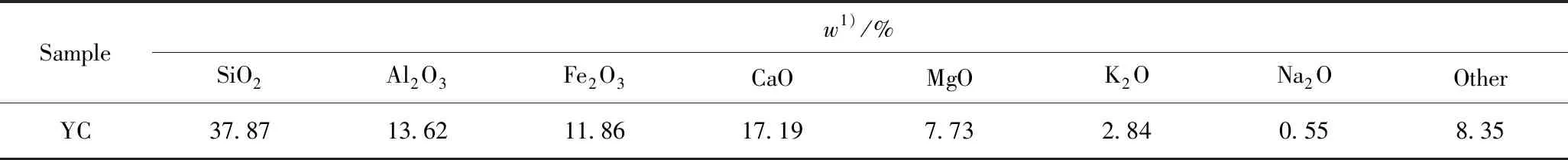
表2 羊腸煤(YC)中金屬氧化物的質量分數Table 2 Inorganic constituents mass fraction in YC
1) Ash composition
1.2 CuFe2O4載氧體的制備
采用氧化還原法[20]一步制備CuFe2O4載氧體。按照n(Cu2+)/n(Fe3+)=0.5,n(NaBH4)/n(Cu2++Fe3+)=2,將9.37 g三水合硝酸銅(Cu(NO3)2·3H2O)和32.32 g九水合硝酸鐵(Fe(NO3)3·9H2O)溶于200 mL 去離子水中,將9.12 g硼氫化鈉(NaBH4)溶解于280 mL去離子水中,然后將上述2種溶液緩慢均勻地加入膠體磨中,以2000 r/min的速率攪拌3 min,得到混合溶液。將上述混合溶液轉移至1000 mL聚四氟乙烯內膽的高壓反應釜中,于150 ℃ 水熱晶化12 h,然后自然冷卻至30 ℃,將得到的黑色沉淀離心分離,用蒸餾水反復洗滌以除去黑色沉淀中可能殘存的雜質離子,最后將黑色沉淀在110 ℃干燥24 h。將干燥后的黑色沉淀再置于950 ℃的馬福爐中恒溫煅燒6 h,破碎,用標準篩篩分得到粒徑為75~150 μm的CuFe2O4載氧體。
1.3 實驗儀器
實驗采用德國耐馳公司的STA449F3熱重-質譜聯用儀。結合脈沖熱分析法,定量檢測煤化學鏈氣化產物,其原理是通過定量環每次向熱重分析儀中打入500 μL的標準氣,通過比較標準氣體峰面積和反應過程中氣體峰面積,實現對反應過程逸出氣體定量。其中,標準氣體是采用稱量法按照n(CO2)∶n(CO)∶n(CH4)∶n(H2)=1∶1∶1∶1配制。
XRD測定采用德國布魯克D8型X射線粉末衍射儀。比表面積(BET) 測定采用美國Quantachrome公司生產的NOVA1000e 型物理吸附儀。SEM-EDS表征采用日本日立公司生產的Hitachi S4800型冷場發射掃描電鏡顯微鏡。
1.4 實驗流程
1.4.1 CuFe2O4載氧體的氧傳遞
稱取300 mg(±0.2 mg) CuFe2O4載氧體,以n(CO2)∶n(CO)∶n(CH4)∶n(H2)=1∶1∶1∶1的混合氣體為還原氣體,在還原氣氛下以10 ℃/min 的升溫速率升至950 ℃,采用質譜分析儀對氣體進行檢測。
1.4.2 YC/CuFe2O4和YC/Al2O3的還原反應性能
由表1中YC的工業分析和元素分析數據,計算YC的化學計量系數為C48H26N0.76S0.13O1.3。按照CuFe2O4與YC載氧體的質量比為10,將CuFe2O4載氧體和YC物理混合,并將混合后的YC/CuFe2O4樣品在水蒸氣氣氛中以10 ℃/min升溫速率從150 ℃加熱至950 ℃,并恒溫20 min。采用質譜分析儀對氣體進行檢測。另外以Al2O3代替CuFe2O4,YC/Al2O3作為對比樣,實驗條件與YC/CuFe2O4的相同。
1.4.3 CuFe2O4載氧體化學鏈氣化循環實驗
YC/CuFe2O4還原反應結束,繼續在950 ℃下切換至空氣氣氛,保持30 min,保證CuFe2O4載氧體完全被氧化。按照上述步驟重復10次。
1.5 數據處理
1.5.1 失氧數(δ)
δ為某溫度段CuFe2O4載氧體在還原氣氛中失去氧原子的個數,也就是失氧數,由式(1)計算:
(1)
式中,Δw為某溫度段CuFe2O4載氧體的質量損失量;M為CuFe2O4載氧體的相對分子質量。
1.5.2 氣體的摩爾累積量
由式(2)計算氣體的摩爾累積量ni:
(2)
式中,ni為氣體i(i為CO2、CO、H2和CH4)的摩爾累積量,mol;Ii為樣品逸出氣體i的離子流強度;Ii0為校正氣體i的離子流強度;ni0為校正氣體i的摩爾累積量,mol。
1.5.3 合成氣的摩爾分數(ηsyn)
合成氣的摩爾分數(ηsyn)為一定時間內煤氣化生成的有效氣(CO、H2和CH4)摩爾累積量與氣體總摩爾累積量的比值,由式(3)計算:
(3)
2 結果與討論
2.1 CuFe2O4載氧體的氧傳遞機理
利用TG-MS探究CuFe2O4載氧體的氧傳遞機理。圖1為CuFe2O4載氧體在模擬煤氣氣氛下的TG、DTG和MS曲線。根據圖1(a)中CuFe2O4載氧體的質量損失率將整個反應過程分為a、b、c、d共4段:4個階段的質量損失率分別為5.66、0.6、6.34和5.16百分點,對應的失氧數δ為0.85、0.09、0.95和0.77。由圖1(a)中TG的a階段(300~500 ℃)表明CuFe2O4載氧體具有較好的低溫反應活性。這個階段CuFe2O4載氧體中Cu2+周圍的O2-容易從晶格中逸出,Cu2+被還原為Cu單質,同時Cu2+的還原加快了Fe3+與Fe2+之間的轉化,形成尖晶石結構Fe3+Fe2+[Fe3+O4][21]。釋氧過程為:3CuFe2O4→3Cu+2Fe3O4+4[O],也就是說CuFe2O4載氧體還原為Cu和Fe3O4。b階段(500~600 ℃)CuFe2O4載氧體的質量損失率穩定,表明Fe3O4是相對穩定的。c和d階段(600~1000 ℃)CuFe2O4載氧體隨著溫度的升高,Fe3O4繼續被還原。當溫度升至1000 ℃時,曲線的質量損失率趨于平穩,表明還原結束。此時,CuFe2O4載氧體的失氧數約為2.66,其釋氧過程為:CuFe2O4→Cu+2Fe+4[O],CuFe2O4載氧體被還原為金屬Cu和金屬Fe。
由圖1(b)可知,在a階段,H2和CO的相對強度呈現負值,CO2和H2O的相對強度呈現正值,表明H2和CO與CuFe2O4載氧體發生反應,生成CO2和H2O。這與圖1(a)中的TG曲線相一致。在b階段,H2和CO與CuFe2O4載氧體繼續反應,H2O的相對強度保持增加的趨勢。但此時CO2相對強度卻呈現降低趨勢。分析造成這一現象的原因是CuFe2O4載氧體在反應過程中形成了氧缺位CuFe2O4-δ,而這種材料可以催化分解CO2,生成CO,所以CO2相對強度呈現降低趨勢。d階段氣體釋放曲線變化較明顯,CH4和CO2相對強度呈現先下降后上升的趨勢,CO和H2的相對強度呈現先上升后下降的趨勢。這主要是由于CuFe2O4載氧體還原程度加劇,生成類似于FeO的低價態氧化物。FeO具有較強的催化CH4和CO2重整的功能[22]。
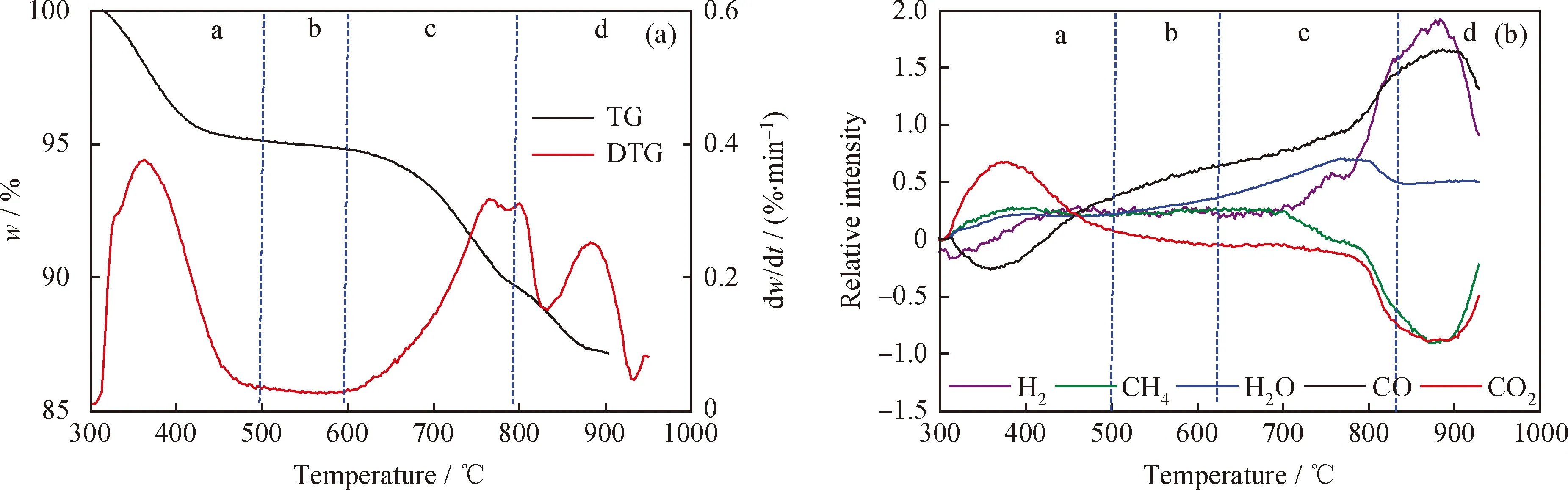
圖1 CuFe2O4載氧體在模擬煤氣氣氛下TG、DTG和MS曲線Fig.1 TG, DTG and MS curves of CuFe2O4 in the syngas atmosphere(a) TG and DTG; (b) MS
綜上所述,CuFe2O4載氧體的氧傳遞過程可以分為以下幾個步驟:首先CuFe2O4載氧體被還原為Cu單質和Fe3O4;然后Fe3O4再繼續還原,生成類似于FeO的低價態氧化物,隨著反應溫度的升高,最終轉化為Fe單質。在這個過程中形成的氧缺位CuFe2O4-δ具有催化分解CO2的作用,尤其是生成類似于FeO的低價態氧化物對CH4和CO2重整作用非常顯著。
2.2 YC和CuFe2O4載氧體的TG特性
圖2為YC/CuFe2O4和YC/Al2O3的質量損失和質量損失率曲線。由圖2(a)可知,CuFe2O4載氧體幾乎沒有質量損失,表明水蒸氣氣氛下CuFe2O4載氧體性能較為穩定。YC/CuFe2O4和YC/Al2O3樣品有明顯的質量損失,而且YC/CuFe2O4比 YC/Al2O3的質量損失更明顯。這一現象的出現主要有以下幾方面原因:1)CuFe2O4載氧體充當了催化劑,在YC熱解過程中促進了YC的熱解,增加了失重率;2)YC熱解產物中的CO、CH4和H2等物質與CuFe2O4載氧體發生還原氧化反應,CuFe2O4氧載體因晶格氧的失去而降低了質量。由圖2(b)可知,YC/Al2O3在826 ℃左右有1個明顯的質量損失峰,這個質量損失峰是由于YC發生了氣化反應所致。YC/CuFe2O4在786 ℃有1個明顯的質量損失峰,比YC/Al2O3的最大質量損失率的溫度提前了50 ℃,表明CuFe2O4載氧體的加入提高了YC氣化的速率。
2.3 YC和CuFe2O4載氧體反應過程的氣體釋放特性
圖3為YC/CuFe2O4和YC/Al2O3氣化過程釋放的H2、CO2、CO和CH4的MS曲線。在熱解階段,YC/Al2O3隨著溫度的升高YC中的脂肪鍵、部分芳香弱鍵以及含氧羧基官能團斷裂,釋放小分子化合物H2、CO、CO2和CH4等[23]。與YC/Al2O3相比,YC/CuFe2O4中由于CuFe2O4載氧體和YC熱解釋放的揮發分發生反應,所以CO2在400 ℃左右出現了1個峰。這個現象與圖2(a)
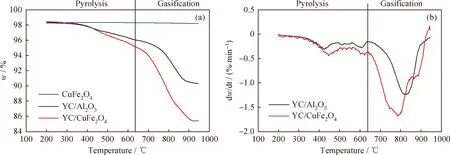
圖2 YC/CuFe2O4和YC/Al2O3的氣化過程中質量損失和質量損失率Fig.2 Comparison of mass loss and mass loss yield for YC coal with CuFe2O4 and YC coal with Al2O3 during the gasification(a) TG; (b) DTG
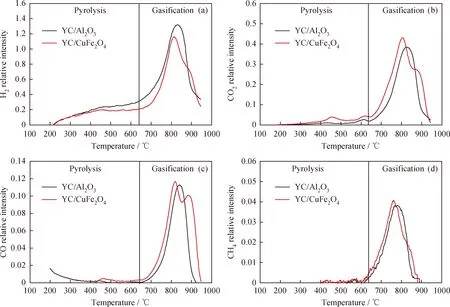
圖3 YC/CuFe2O4和YC/Al2O3氣化過程釋放H2、CO2、CO和CH4的MS曲線Fig.3 Comparison of MS profiles for H2, CO2, CO and CH4 of YC coal with CuFe2O4 and YC coal with Al2O3(a) H2; (b) CO2; (c) CO; (d) CH4
TG曲線相一致。在氣化階段,YC/CuFe2O4中H2的開始釋放時間遲于YC/Al2O3,這主要是由于YC氣化釋放的H2與CuFe2O4載氧體反應。與H2相比,YC/CuFe2O4和YC/Al2O3中CO的開始釋放時間間隔較小,主要是因為H2與CuFe2O4載氧體反應的速率比CO快。
表3為YC/CuFe2O4和YC/Al2O3氣化過程釋放的CO2、CO、H2和CH4的摩爾累積量、合成氣的摩爾分數。與YC/Al2O3氣化相比,YC/CuFe2O4化學鏈氣化過程中H2的摩爾累積量降低,而CO2、CO和CH4的摩爾累積量增加。H2摩爾累積量降低的原因是H2和CuFe2O4載氧體發生了反應。CO2摩爾累積量增加的原因主要有兩個:一是YC的惰質組分含有較多穩定的含氧官能團,在600 ℃之后會釋放含氧氣體CO2[24];二是CO和CH4與CuFe2O4載氧體反應生成的CO2。從還原性氣體與CuFe2O4載氧體發生化學反應的角度出發,CO和CH4摩爾累積量應該呈現降低的趨勢,但由表3可知,CO和CH4的摩爾累積量增加,原因是在CuFe2O4載氧體的還原過程中,形成了具有催化分解CO2功能的氧缺位材料CuFe2O4-δ。并且CuFe2O4載氧體催化分解CO2的速率大于其與CO、CH4發生還原反應的速率。
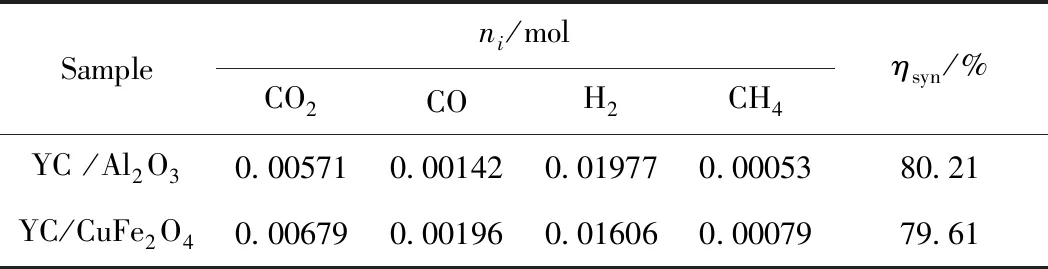
表3 YC/CuFe2O4和YC/Al2O3氣化過程釋放CO2、CO、H2和CH4的摩爾累積量(ni)和合成氣的摩爾分數(ηsyn)Table 3 YC coal with CuFe2O4 and YC coal with Al2O3molar amount of gaseous (ni) and themole fraction of syngas (ηsyn)
2.4 YC和CuFe2O4載氧體的循環實驗
圖4為CO、CO2、CH4和H2氣體摩爾累積量隨循環次數的變化。由圖4可知,6次循環后H2和CO2的摩爾累積量略有升高,CO的摩爾累積量稍有降低,可能是因為CuFe2O4載氧體在循環反應過程中反應活性和催化分解CO2活性略有下降。但從整體分析可知,在10次YC和CuFe2O4載氧體循環過程中,氣體產物各組分的摩爾累積量基本保持穩定,表明10次循環過程CuFe2O4載氧體整體反應性能穩定。

圖4 CO、CO2、CH4和H2氣體摩爾累積量隨循環次數的變化Fig.4 Effect of redox cycles on CO, CO2, CH4 andH2 molar amount of gaseous
2.5 CuFe2O4載氧體反應前后形態結構的分析
圖5為新鮮、還原、1次循環再生和10次循環再生CuFe2O4載氧體的XRD譜。由圖5可知,新鮮CuFe2O4載氧體在30.2°、35.6°、57.0°等處出現CuFe2O4載氧體的特征衍射峰,表明還原氧化法制備的CuFe2O4載氧體具有很好的晶相結構。從還原后的CuFe2O4載氧體的XRD譜可知,Cu2+以Cu單質形式析出,Fe3+以反尖晶石結構Fe3O4存在,而這種結構的載氧體表面具有豐富的氧缺位[25],具有催化分解CO2的作用。1次循環再生的CuFe2O4載氧體的XRD譜上Cu單質衍射峰消失了,說明Cu又重新進入尖晶石結構中恢復了CuFe2O4載氧體晶體結構。10次循環再生CuFe2O4載氧體的XRD譜與新鮮CuFe2O4載氧體相同,其晶體結構依然具有尖晶石結構,說明CuFe2O4載氧體具有良好的循環穩定性。
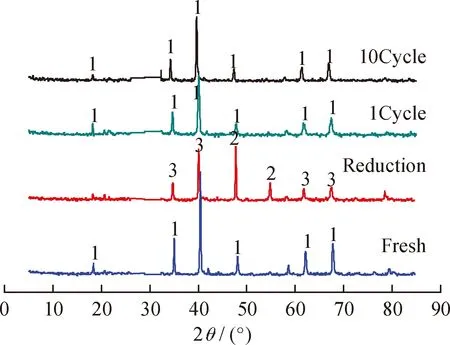
圖5 新鮮-還原-1次循環和10次循環CuFe2O4載氧體的XRD譜Fig.5 XRD profiles of fresh, reduced, 1 cycle and10 cycle CuFe2O4 oxygen carrier1—CuFe2O4; 2—Cu; 3—Fe2O3
圖6為新鮮的CuFe2O4載氧體和10次循環再生的CuFe2O4載氧體的SEM和EDS,表4為新鮮CuFe2O4載氧體和10次循環再生CuFe2O4載氧體的比表面積。由圖6可知,新鮮的CuFe2O4載氧體具有均一的形貌,表面光滑,10次循環后的CuFe2O4載氧體表面變得疏松多孔。這是因為CuFe2O4載氧體在反復的還原和氧化過程中發生了氣-固反應,導致CuFe2O4載氧體孔道受氣體反應物及產物沖擊而變得疏松多孔。由表4還可知,10次循環后CuFe2O4載氧體的比表面積比新鮮CuFe2O4載氧體的比表面積增加了13 m2/g。這與文獻報道的結果一致[26-27]。另外,EDS檢測到10次循環的CuFe2O4載氧體表面含有來自煤灰的元素Si和Al,說明煤灰在CuFe2O4載氧體的表面沉積。結合圖4可知,載氧體表面煤灰的沉積使其反應活性和催化分解CO2活性略微低于新鮮載氧體的,但在10次循環過程中氣體產物各組分的摩爾累積量基本保持穩定。因此,在10次循環再生實驗過程中CuFe2O4載氧體雖然表面沉積了煤灰,但仍呈現良好的循環反應特性。

表4 新鮮CuFe2O4載氧體和10次循環后CuFe2O4載氧體的比表面積Table 4 BET of fresh and 10 cycle CuFe2O4 oxygen carrier

圖6 新鮮的CuFe2O4載氧體和10次循環的CuFe2O4載氧體的SEM照片和EDSFig.6 SEM and EDS of fresh and10 cycle CuFe2O4 oxygen carrier(a),(c) SEM; (b),(d) EDS(a),(b) Fresh CuFe2O4; (c),(d) 10 Cycle CuFe2O4
3 結 論
利用TG-MS研究了CuFe2O4載氧體的氧傳遞機理以及YC和CuFe2O4的化學鏈氣化特性。得出以下幾點結論:
(1)CuFe2O4載氧體具有提供晶格氧和催化分解CO2的雙功能。CuFe2O4載氧體在還原反應過程中形成的氧缺位材料CuFe2O4-δ具有催化分解CO2的功能。
(2)與YC/Al2O3相比,YC/CuFe2O4的化學鏈氣化過程中H2的摩爾累積量含量降低,而CO2、CO和CH4的摩爾累積量增加。
(3)10次循環實驗中,氣體產物各組分的摩爾累積量保持穩定,CuFe2O4載氧體表現良好的反應性能和催化性能。

