RAAS抑制劑在對比劑致維吾爾族患者急性腎損傷中的作用
李文宇,依力哈木江·艾沙,阿達萊提·阿卜力孜,沙德爾丁·斯拉吉,杜紀兵
研究表明,由于危險因素不同,導致對比劑致急性腎損傷(contrast-induced acute kidney injury,CIAKI)發生率存在很大差異(2%~30%)[1],現已成為急性腎損傷的第3 位原因。目前除水化治療、他汀類藥物以外,尚無確切方法能夠降低CI-AKI 發生率[2]。腎素-血管緊張素-醛固酮系統(RAAS)抑制劑可以通過預防和減少蛋白尿、腎纖維化等途徑在腎病的各階段發揮積極保護作用[3]。但是其在CIAKI 中的作用卻存在巨大爭議。近些年來,隨著新疆和田地區維吾爾族患者經皮冠狀動脈介入治療(percutaneous coronary intervention,PCI)量逐年增加,介入并發癥越來越引起重視,但卻鮮見報道。本文旨在探討維吾爾族患者PCI 術后CI-AKI 的發生率和影響因素,尤其是RAAS 抑制劑對CI-AKI 的影響。
1 對象與方法
1.1 研究對象 回顧性分析2015年1月—2017年12月新疆維吾爾自治區和田地區人民醫院心臟診療中心成功行PCI手術,并復查血肌酐患者218例。CI-AKI 診斷標準:采用改善全球腎臟病預后指南(KDIGO)將對比劑誘發的急性腎損傷定義為使用對比劑后24~48 h后血清肌酐值≥44.2μmol/L或較基礎值升高≥25%,并排除其他原因導致的腎損害[4]。排除標準:(1)活動期腎病或需連續腎臟替代治療者。(2)心源性休克。(3)惡性腫瘤、活動性感染、急性腦卒中、嚴重肝功能障礙、甲狀腺功能異常者。(4)PCI 術后未接受標準水化治療者。(5)RAAS藥物應用禁忌證者。(6)新疆維吾爾自治區和田地區漢族患者。將218例患者按照有無CI-AKI分為CI-AKI組(46例,21.10%)和對照組(172例,78.90%)。
1.2 方法 整理患者入院時一般資料(性別、年齡、急性心肌梗死、高血壓史、糖尿病史、RAAS 抑制劑、他汀類藥物、利尿劑應用情況),入院后實驗室檢查指標[血紅蛋白(HB)、腎功能、高敏C 反應蛋白(hs-CRP)、N 末端B 型腦鈉肽前體(NT-proBNP)、同型半胱氨酸(Hcy)、高密度脂蛋白膽固醇(HDLC)及低密度脂蛋白膽固醇(LDL-C)],超聲指標[左室射血分數(LVEF)、左室舒張末容積(LVEDD)、肺動脈收縮壓(PAP)]和臨床指標(手術當日收縮壓、舒張壓、術后第1天入量情況及對比劑用量)。按照Mehran等[5]報道的危險因素進行CI-AKI危險因素評分。
1.3 統計學方法 采用SPSS 18.0軟件進行統計分析。符合正態分布計量資料以±s表示,組間比較采用t檢驗,組內比較采用配對t檢驗;計數資料以例(%)表示,組間比較采用χ2檢驗;將單因素分析有意義指標進行賦值后納入多因素Logistic分析。以P<0.05為差異有統計學意義。
2 結果
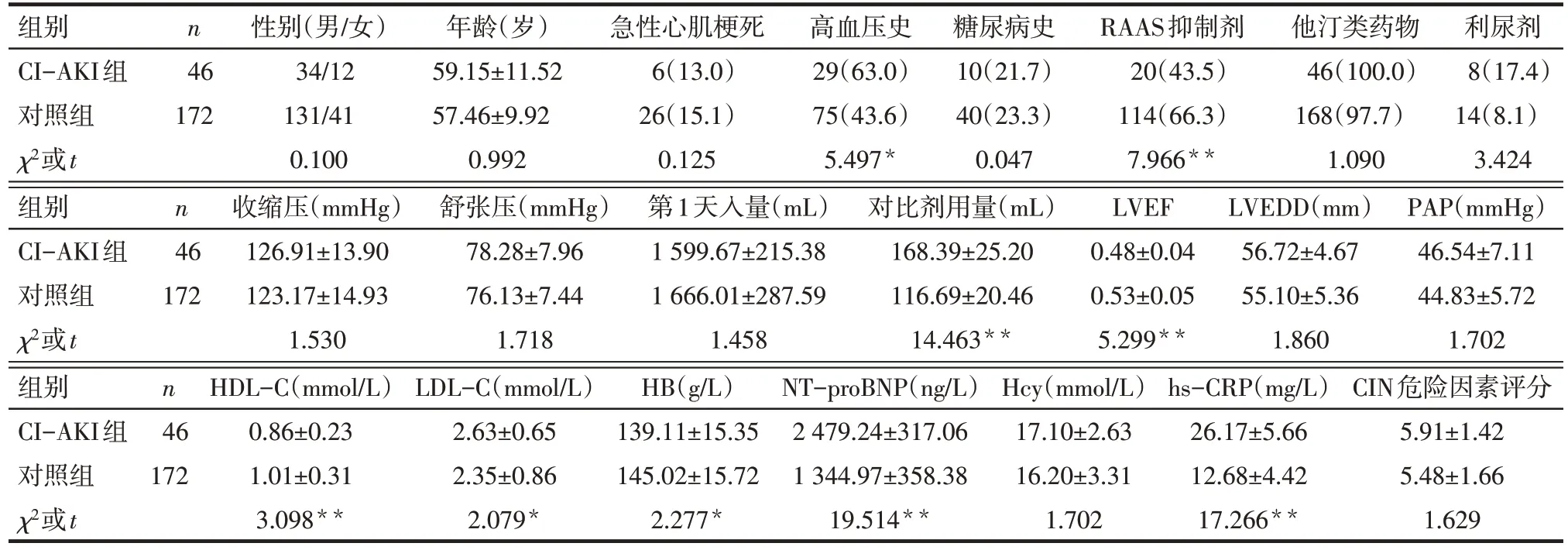
2.1 2組臨床資料比較 雖然CI-AKI組高血壓患者比例高于對照組,但RAAS 抑制劑使用率卻明顯低于對照組。CI-AKI組對比劑用量、LDL-C 水平、NT-proBNP 水平、hs-CRP 水平高于對照組,而LVEF、HDL-C、HB 水平低于對照組,2組間CI-AKI危險因素評分差異無統計學意義,見表1。
2.2 2組治療前后腎功能比較 CI-AKI組及對照組術前肌酐清除率差異無統計學意義[(97.16±11.75)mL/minvs.(95.49±12.65)mL/min,t=0.793,P=0.671]。術前CI-AKI組肌酐水平低于對照組,但術后CI-AKI組肌酐水平較術前明顯增加,且高于對照組(P<0.01)。2組間尿素氮水平術前差異無統計學意義,但術后CI-AKI組尿素氮水平明顯增加(P<0.01)。2組間尿酸水平手術前后及組間比較差異均無統計學意義(P>0.05),見表2。
2.3 CI-AKI 危險因素Logistic 分析結果 以有無CI-AKI 為因變量(無=0,有=1),將單因素分析有意義的因素作為協變量引入Logistic 分析:使用RAAS抑制劑賦值(否=0,是=1)、NT-proBNP 賦值(心力衰竭無=0,有=1)、對比劑用量和hs-CRP 為連續變量,發現使用RAAS抑制劑是維吾爾族患者發生CI-AKI的保護因素;NT-proBNP、對比劑用量和hs-CRP 水平升高均為維吾爾族患者CI-AKI發生的危險因素,見表3。
3 討論
部分研究顯示,維吾爾族與漢族人口某些疾病發生率存在一定差異[6]。和田地區人民醫院作為目前當地唯一一家能夠開展PCI 診療醫院,其維吾爾族患者比例占到98%以上。本文通過觀察發現,維吾爾族患者CI-AKI 的發生率高達21.1%,遠高于國內有關文獻報道[7]。目前研究表明,CI-AKI 與死亡率密切相關[8]。因此如何識別CI-AKI影響因素,采取必要措施降低CI-AKI發生率、改善預后就顯得尤為重要。因此,本文入選了218例成功行PCI 術,并術后給予標準水化治療的維吾爾族患者。既往觀察發現 NT-proBNP[9]、對比劑用量[10]同樣也是維吾爾族患者CI-AKI發生的高危因素,與目前研究相同。
Tab.1 Comparison of general data between two groups of patients表1 2組患者一般資料比較
Tab.2 Comparison of renal function before and after treatment between two groups表2 2組治療前后腎功能比較 (mmol/L,±s)
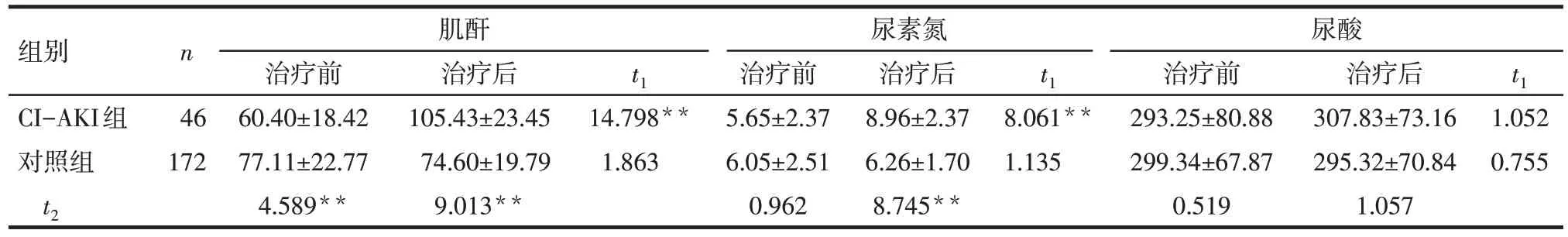
Tab.2 Comparison of renal function before and after treatment between two groups表2 2組治療前后腎功能比較 (mmol/L,±s)
*P<0.05,**P<0.01;t1組內治療前后比較,t2組間比較
組別CI-AKI組對照組t2 n 肌酐 尿素氮 尿酸t1治療后105.43±23.45 74.60±19.79 9.013**治療前60.40±18.42 77.11±22.77 4.589**t1 t1 46 172 14.798**1.863治療前5.65±2.37 6.05±2.51 0.962治療后8.96±2.37 6.26±1.70 8.745**8.061**1.135治療前293.25±80.88 299.34±67.87 0.519治療后307.83±73.16 295.32±70.84 1.057 1.052 0.755
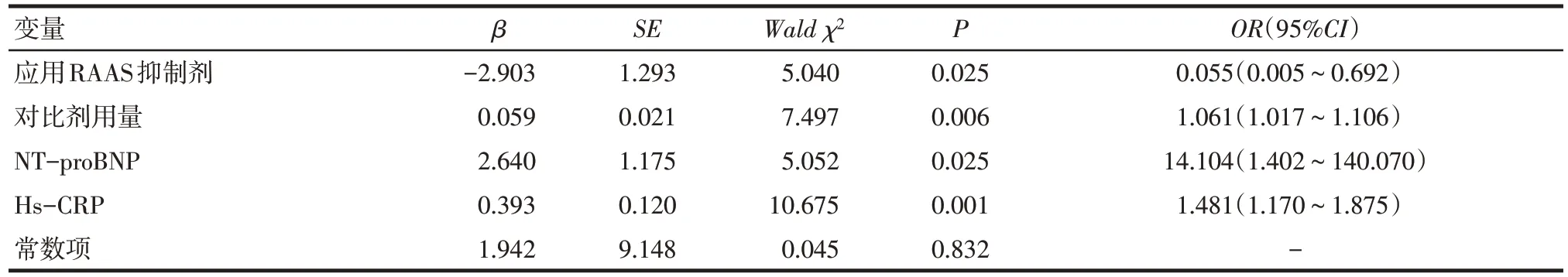
Tab.3 Logistic analysis of risk factors for CI-AKI in Uygur patients表3 維吾爾族患者CI-AKI影響因素Logistic分析
影響因素方面,現已證實標準化水化治療和他汀類藥物[2]能夠降低CI-AKI 發生風險,但本研究2組間比較差異無統計學意義。RAAS 抑制劑作為臨床中常用藥物之一,其在CI-AKI中的作用仍存在爭議。目前2項較大規模人群觀察結果迥異[11-12]。但是本文觀察發現CI-AKI組RAAS 抑制劑應用比例明顯低于對照組,通過Logistic 分析發現RAAS 抑制劑在維吾爾族患者CI-AKI中起到一定保護作用。
目前,CI-AKI 發生機制尚未明確,基礎研究表明多種機制參與其中,包括對比劑致腎小管上皮細胞直接細胞毒性;氧化應激、炎癥反應介導的腎臟組織免疫損傷;局部 RAAS 激活等因素[13]。Toso 等[14]研究顯示,hs-CRP 作為炎癥反應指標之一,其基線水平越高,CI-AKI發生率也越高。可能原因是在全身高hs-CRP水平下,應用對比劑后更容易加劇腎臟局部炎癥過程,從而促發CI-AKI的發生發展有關。
本研究觀察發現,CI-AKI組hs-CRP 水平明顯高于對照組,而CI-AKI組RAAS 抑制劑使用率卻明顯低于對照組。Logistic分析提示RAAS抑制劑是減少維吾爾族CI-AKI發生的保護因素,分析原因可能與RAAS 抑制劑能夠通過抑制全身及局部RAAS 系統激活及炎癥反應、減少腎血管收縮,增加局部NO合成及其生物學活性,導致腎臟的血液灌注量增加等機制有關[15]。
因本文為回顧性研究,所入選指標尚不能完全解釋RAAS 抑制劑能夠在維吾爾族患者CI-AKI 中起到保護作用的具體機制。對于維吾爾族擬行PCI治療患者,如果能夠提高術前RAAS抑制劑使用率,改善術前心功能情況,減少術中對比劑用量,最終或可降低CI-AKI發生率。

