冠狀動脈慢血流患者脂蛋白相關磷脂酶A2及超敏C反應蛋白的變化
邱 敏, 徐少華, 姜 海, 龍明智
(南京醫科大學第二附屬醫院 心內科, 江蘇 南京, 210011)
冠狀動脈慢血流(CSF)是指在冠狀動脈造影檢查過程中冠狀動脈主要分支無明顯狹窄(狹窄程度<40%), 而冠狀動脈遠端血流充盈延遲的現象[1], 由Tambe等[2]在1972年首次報道。慢血流患者多表現為休息時反復發作的胸痛癥狀,與心肌缺血、危及生命的心律失常、心源性猝死、急性冠脈綜合征等臨床表現相關[3-4], 在行常規冠狀動脈造影患者中發生率為1%~7%[5]。最近的研究[5]表明,炎癥反應、早期動脈粥樣硬化、微血管和內皮功能障礙、小血管疾病和血液成分異常可能參與CSF的病理、生理過程。
C反應蛋白是人體最主要的、最敏感的非特異炎癥標志物,而高敏C反應蛋白(hs-CRP)則更為精確和敏感。國內外研究[6]早已表明, hs-CRP水平對冠心病患者心血管不良事件風險具有重要的預測價值。脂蛋白相關磷脂酶A2(Lp-PLA2)是血管特異性炎癥生物標志物,參與動脈粥樣硬化的病理、生理過程。既往臨床研究[7-8]表明, Lp-PLA2水平與心血管疾病的發病及嚴重程度有一定的相關性,但與CSF現象的相關性報道較少。本研究探討CSF患者Lp-PLA2、hs-CRP的水平變化及其與CSF的關系,現報告如下。
1 資料與方法
1.1 一般資料
選取2017年7月—2018年12月因胸痛發作而懷疑冠心病在南京醫科大學第二附屬醫院行冠狀動脈造影患者125例,其中65例患者診斷為冠狀動脈慢血流,設為CSF組。診斷標準: 冠狀動脈造影血管無明顯狹窄(狹窄程度<40%); 校正的心肌梗死溶栓治療(TIMI)幀數大于27幀(回放速度為30幀/s); 3支評價血管中至少有1支存在血流減慢可診斷為CSF。另隨機選取同期冠狀動脈造影血管正常且血流正常的患者60例為對照組。2組患者均排除冠狀動脈明顯異常、既往有心肌梗死、冠脈痙攣、冠脈擴張及溶栓治療后、急性冠狀動脈綜合征、心肌病、中重度心臟瓣膜病、充血性心力衰竭、肝腎功能不全、急慢性感染、未控制的高血壓(收縮壓>160 mmHg或舒張壓>105 mmHg)、慢性阻塞性肺病或肺源性心臟病、免疫性疾病、結締組織病、惡性腫瘤、6個月內有重大創傷或手術史等繼發因素。
1.2 樣本采集及測定
冠狀動脈造影前,患者行全面基線評估,包括性別、年齡、體質量指數(BMI)、吸煙史、既往病史、冠心病家族史以及用藥史,測量患者血壓、心率,行心電圖等檢查。采集清晨空腹靜脈血測量生化指標,應用免疫比濁法檢測血漿Lp-PLA2水平,儀器為南京諾爾曼NORMAN-1生化分析儀,試劑盒為南京諾爾曼生物科技有限公司提供的Lp-PLA2商品試劑盒, Lp-PLA2正常值為<175 ng/mL。
1.3 冠狀動脈血流測定方法
采用標準Judkins技術從橈動脈或股動脈途徑行冠狀動脈造影。采用校正的TIMI血流記幀法判定冠狀動脈血流速度[9]。至少1支冠狀動脈TIMI血流記幀法計數(TFC)>27幀判定為慢血流。平均TFC為通過3個主要冠狀動脈的TFC的總和除以3來計算。
1.4 統計學分析
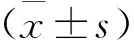
2 結 果
2.1 2組患者基線資料及實驗室指標比較
2組患者年齡、性別、BMI、吸煙狀況、既往史、冠心病家族史、診室血壓和臨床用藥方面比較無顯著差異(P>0.05), 見表1。與對照組相比, CSF組患者的Lp-PLA2、hs-CRP和尿酸水平均顯著升高(P<0.05),其余血液生化指標無顯著差異(P>0.05), 見表2。
2.2 TFC值及CSF中涉及的冠狀動脈分布
與對照組相比,CSF患者的左前降支、左回旋支和右冠狀動脈的校正TFC值和平均TFC值顯著更高(P<0.01),見表3。65例CSF患者中,有48例患者LAD存在慢血流, 25例患者LCX存在慢血流, 31例患者RCA存在慢血流。所有CSF患者中,有24例患者3支血管都存在慢血流, 2支血管慢血流患者有18例,單支血管慢血流患者有23例。
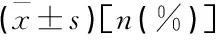
表1 2組患者一般資料比較
CSF: 冠狀動脈慢血流; BMI: 體質量指數;
ACEI: 血管緊張素轉換酶抑制劑; ARB: 血管緊張素Ⅱ受體阻滯劑。
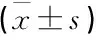
表2 2組患者實驗室結果比較
CSF: 冠狀動脈慢血流; Lp-PLA2: 脂蛋白相關磷脂酶A2。
與對照組比較, *P<0.05。
進一步行Pearson相關性分析顯示, CSF患者血漿Lp-PLA2水平與平均TFC顯著相關(r=0.522,P<0.001), 且隨著CSF中涉及的冠狀動脈數量的增加, Lp-PLA2的水平逐漸增加,其中3支血管、2支血管、單支血管CSF患者以及對照組的Lp-PLA2水平依次為(217.44±46.86)、(194.39±35.35)、(172.93±41.88)、(165.83±49.11) ng/mL, 3支血管、2支血管與對照組比較,差異均有統計學意義(P<0.05或P<0.01)。
2.3 CSF的影響因素
對相關危險因素Lp-PLA2、hs-CRP和尿酸水平行Logistic回歸分析以評估對CSF的影響, Lp-PLA2水平(OR=1.009,P=0.046)、hs-CRP水平(OR=1.071,P=0.048)與CSF獨立相關。Pearson相關性分析表明, Lp-PLA2與hs-CRP顯著正相關(r=0.407,P<0.001)。ROC曲線顯示,血漿Lp-PLA2可能是CSF的特異性預測因子,曲線下面積為0.676(95%可信區間為0.582~0.770,P=0.001)。
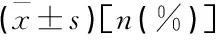
表3 TFC值及慢血流中涉及的冠狀動脈分布
TFC: 心肌梗死溶栓治療血流記幀法計數; CSF: 冠狀動脈慢血流。
與對照組比較, **P<0.01。
3 討 論
目前, CSF的病理生理機制尚未完全明確,動脈粥樣硬化和炎癥可能在CSF的病理生理過程中起重要作用。Pekdemir等[10]研究發現, CSF患者的冠狀動脈血流儲備分數顯著降低,通過血管內超聲觀察到在心外膜動脈中常見有縱向延伸的大量鈣化灶,并且CSF患者的內膜厚度增加。atirolu ?等[11]發現,尾加壓素Ⅱ是參與動脈粥樣硬化血管重塑的重要多肽,在CSF患者中也顯著升高。炎癥在動脈粥樣硬化的所有階段都起著重要作用,炎癥參數的異常可能是內皮功能障礙的指標,二者都有促進冠狀動脈慢血流作用。研究[12-14]證實, CSF現象與血小板/淋巴細胞比例、紅細胞壓積、腫瘤壞死因子-α、hs-CRP和同型半胱氨酸等炎癥相關指標異常有關。
Lp-PLA2是磷脂酶A2超家族成員,也被稱為血小板活化因子乙酰水解酶,主要是由巨噬細胞、T淋巴細胞、單核細胞以及動脈粥樣硬化病變中的肥大細胞等分泌的酶。Lp-PLA2主要與循環中的低密度脂蛋白(LDL)結合,推測與LDL的氧化修飾和動脈內膜炎癥反應的發展有關[15-16]。Lp-PLA2通過水解LDL產生溶血磷脂酰膽堿與游離氧化脂肪酸這兩種重要炎癥因子,這些因子損傷血管內皮,單核細胞聚集在血管內膜并轉化進入巨噬細胞,最終吞噬氧化性LDL形成泡沫細胞,導致動脈粥樣硬化斑塊的形成; 同時, Lp-PLA2可能通過對炎癥因子的激活反饋刺激巨噬細胞產生更多的Lp-PLA2[17], 這種循環加速了動脈粥樣硬化的進展,增加了心血管事件的風險。因此, Lp-PLA2參與動脈粥樣硬化的多個階段,并且可作為預測冠心病(CHD)患者臨床結局的生物標志物。2012年,美國和歐洲指南[18-19]建議將Lp-PLA2測量結果納入患者心血管風險評估方案。
大量臨床研究證實,升高的Lp-PLA2與心血管事件的發生顯著相關,是影響預后的獨立危險因素。Maiolino等[20]研究表明,Lp-PLA2活性可預測高風險白種人冠心病患者的心血管事件和急性冠脈綜合征事件。Yang等[21]研究發現,冠心病患者血漿Lp-PLA2濃度明顯高于對照組,特別是急性冠狀動脈綜合征患者。血漿Lp-PLA2濃度與中國患者的CHD獨立相關。最近的一項薈萃分析[16]包括15項研究共30 857名參與者,結果表明更高的Lp-PLA2活性或濃度與CHD患者的心血管事件獨立相關。然而,關于Lp-PLA2與冠狀動脈慢血流關系的報道很少。本研究中,作者發現CSF組血漿Lp-PLA2水平、hs-CRP水平顯著高于對照組,且Lp-PLA2和hs-CRP水平存在顯著正相關。這些研究結果表明血漿Lp-PLA2引起的炎癥反應、內皮功能障礙和動脈粥樣硬化可能在CSF的發病機制中起作用。此外,回歸分析證實血漿Lp-PLA2水平是CSF的獨立預測因子。隨著CSF中涉及的冠狀動脈數量的增加, Lp-PLA2的血漿水平增加,作者推測多支血管受累可能表現為更嚴重的彌漫性疾病,預后可能更差,未來的隨訪研究需要證實這個假設。
綜上所述,與冠狀動脈解剖和血流正常的患者相比, CSF患者的血漿Lp-PLA2水平更高,并且更高的Lp-PLA2水平與CSF的嚴重程度相關, Lp-PLA2可能成為CSF的另一種新的臨床診斷生物標志物。

