甲狀旁腺激素聯合阿侖膦酸鈉對大鼠骨質疏松性骨折骨痂血管形成的影響
劉穎 孫昌俊 王樂 畢若杰 張恒 王大璐 齊巍
唐山市第二醫院,河北 唐山 063000
骨質疏松癥(osteoporosis,OP)是以骨量減少、骨微結構破壞、骨脆性增加、導致骨折危險性顯著升高的一種全身性骨病。骨折是OP最嚴重的并發癥,20%的OP患者有發生骨質疏松性骨折(osteoporotic fracture,OPF)的可能,是致殘致死的主要原因之一[1],因此,如何降低OPF的發生率已成為治療骨質疏松的防治目的。OP不僅增加了患者發生骨折的風險,嚴重影響骨折愈合進程及效果[2]。隨著我國人口的老齡化的加劇,OP及OPF的發病率逐漸上升,給家庭和社會帶來了沉重的經濟負擔。甲狀旁腺激素(parathyroid hormone,PTH)是目前臨床治療骨質疏松癥的最常用藥物之一,可調節鈣、磷代謝水平。阿侖膦酸鈉是首個以骨質疏松為適應證而獲準上市的第三代二膦酸鹽類藥物,能顯著增加骨量,提高骨質強度,降低骨折發生率。研究表明,甲狀旁腺激素聯合唑來膦酸對去勢大鼠的骨折愈合有累加作用[3]。因此,本研究旨在探討甲狀旁腺激素聯合阿侖膦酸鈉對OPF骨痂血管形成及骨折愈合的作用機制,為臨床應用治療OPF提供理論基礎。
1 材料與方法
1.1 實驗試劑與材料
75只SPF級雌性SD大鼠,12 W齡,體重(320±30)g,購于北京維通利華實驗動物技術有限公司(許可證號:SYXK(京)2017-0033)。重組人甲狀旁腺激素(1-34)(100μg/支,批號:J201708072,美國Sigma公司),阿侖膦酸鈉片(福善美)(70 mg×1 s,生產批號:J20170085,美國默沙東制藥有限公司),柜式X線照片機購置于美國Hologic公司,雙能X線骨密度測定儀購于美國GE公司,MTS-858型生物力學實驗機購于美國MA公司,ELISA檢測試劑盒購于武漢云克隆科技股份有限公司,兔抗鼠血管內皮生長因子(vascular endothelial growth factor,VEGF)多克隆抗體購于武漢博士德生物有限公司。
1.2 方法
1.2.1實驗分組與藥物干預:SD大鼠飼養于華北理工大學醫學動物實驗中心SPF級屏障環境;按隨機數字法分為假手術組、去勢組、甲狀旁腺素組、阿侖膦酸鈉組、聯合用藥組,假手術組僅切除部分脂肪組織,其他4組均行雙側卵巢切除術。于術后第2天分別給予不同藥物干預,假手術組、去勢組:皮下注射0.9% NaCl 5 mL/kg,1次/d;甲狀旁腺素組:皮下注射PTH(1-34)50 μg/kg,1次/d;阿侖膦酸鈉組:灌胃阿侖膦酸鈉片0.5 mg/kg,1次/d;聯合用藥組:皮下注射PTH(1-34)50 μg/kg,1次/d,灌胃阿侖膦酸鈉0.5 mg/kg,1次/d。連續用藥8周。
1.2.2構建去卵巢大鼠骨質疏松骨折模型:10%水合氯醛腹腔麻醉,取腹背部中線第2腰椎做長約2 cm縱行切口,依次分離進入腹腔,沿輸卵管尋找卵巢組織,嚴密結扎輸卵管,切除卵巢,逐層間斷縫合。卵巢切除術后4周行右側股骨干骨折髓內固定術。腹腔麻醉,取左大腿外側縱行切口,暴露股骨中段,使用線鋸橫行鋸斷股骨,用電鉆以直徑1.0 mm克氏針順行插入骨折遠端,骨折達到解剖復位,固定可靠且骨折端對位對線良好,逐層間斷縫合,術后常規青霉素80萬U肌肉注射,預防感染。各組大鼠均分籠飼養,標準飼料,自由飲水,飼養環境條件均相同。
1.2.3組織標本處理:攝片后10%水合氯醛麻醉,采取急性大失血法處死大鼠,打開胸腔,左心室采血5~10 mL,3 000 r/min,離心15 min,收取上層血清0.5~1 mL,-20 ℃保存備用。剝離股骨痂,0.9%NaCl沖洗后于10%甲醛溶液固定,10%硝酸脫鈣,乙醇梯度脫水,二甲苯透明,石蠟包埋,制作5 μm切片,60 ℃烤箱4 h,取出室溫保存備用。
1.2.4放射性(X線)檢查:術后4周選取各組大鼠10%水合氯醛腹腔麻醉后進行X線攝片,觀察各組大鼠骨折愈合情況。放射學評估采用Warden[4]X線評分系統進行評估,依據骨折斷端表現行骨折愈合評分。評分標準:沒有愈合1分;骨痂形成不明顯2分;骨折部分愈合3分;骨折線逐漸消失,骨痂逐漸吸收消失4分;完全愈合5分。
1.2.5骨生物力學檢測:采用電子生物力學測試裝置對骨折骨痂進行三點彎曲實驗,儀器調試正常后固定骨標本位置,測試區域為骨痂中心位置,以支點跨距為20 mm,加載速度2 mm/min給予股骨骨痂施加壓力直至骨頭斷裂,通過計算機記錄加載位移載荷-變形曲線,計算出最大荷載(N)和抗彎強度(N/mm)。
1.2.6骨痂骨密度(bone mineral density,BMD)測定:取出待測骨痂,在LUNAR雙能X線吸收掃描儀測量骨折部位上下區域骨密度,采用分辨率1.0 mm×1.0 mm,掃描速度60 mm/s的掃描模式,以骨折端2.0 mm×2.0 mm為中心區域,測量骨痂BMD(g/cm2),連續測量BMD各5次。
1.2.7血清VEGF和BMP-2濃度測定:采用ELISA試劑盒檢測血清VEGF和BMP-2濃度,按照試劑盒說明書步驟進行操作。
1.2.8HE染色:參照HE染色法實驗步驟進行操作[5],光鏡下觀察染色并采集圖片。隨機選取5個視野,計數新生血管數,取平均值。
1.2.9免疫組織化學染色法:以兔抗鼠VEGF多克隆抗體濃度(1∶1000),參照免疫組織化學染色法實驗步驟進行操作[6]。光學顯微鏡觀察并采集圖片,圖像分析軟件進行分析,免疫組織化學染色結果采用免疫反應評分(IRS)進行測定。
1.3 統計學分析
2 結果
2.1 各組骨折愈合及評分
假手術組骨折線模糊不清或消失,骨痂生長包繞骨折端,連接緊密;去勢組骨折線依然清晰可見,未見明顯骨痂生長,斷端骨痂未連接,骨折愈合欠佳。甲狀旁腺素組和阿侖膦酸鈉組骨折線部分模糊,骨痂少量生長,骨折端骨痂部分連接,連接不緊密;聯合用藥組骨折線模糊,骨折端有連續性骨痂包繞,骨痂體積較大,部分愈合,并開始重建塑形。假手術組、去勢組、甲狀旁腺素組、阿侖膦酸鈉組、聯合用藥組骨折愈合評分分別為:4.86±0.50、2.25±0.24、3.10±0.12、3.27±0.10、4.50±0.42。去勢組較假手術組骨折愈合評分顯著降低(P<0.05),甲狀旁腺素組、阿侖膦酸鈉組、聯合用藥組較去勢組骨折愈合評分均升高,其中以聯合用藥組骨折愈合評分升高最顯著(P<0.05)。詳見圖1。
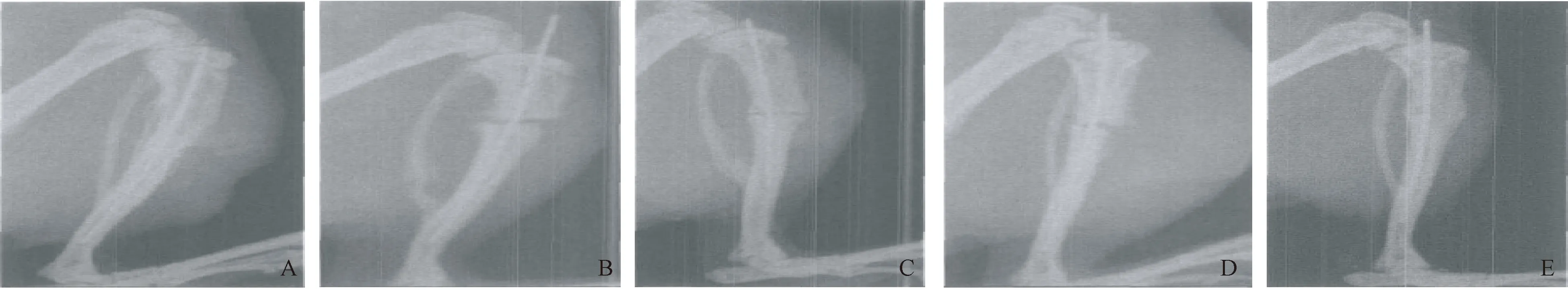
圖1 術后4周X線情況 A:假手術組;B:去勢組;C:甲狀旁腺素組;D:阿侖膦酸鈉組;E:聯合用藥組Fig.1 X-ray situation in 4 w after operation. A: Sham operation group; B: Castration group; C: Parathyroid hormone group; D: Alendronate group; E: Combination group
2.2 各組骨痂生物力學
各組大鼠股骨骨痂生物力學比較見表1。去勢組較假手術組骨痂最大荷載和抗彎強度顯著降低(P<0.05),甲狀旁腺素組、阿侖膦酸鈉組、聯合用藥組較去勢組骨痂最大荷載和抗彎強度均升高,其中以聯合用藥組骨痂最大荷載和抗彎強度升高最顯著(P<0.05)。
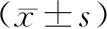
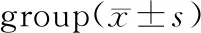

組別例數最大荷載/N抗彎強度/(N/mm)假手術組15230.80±15.30175.64±16.20去勢組15138.64±10.29※105.23±13.50※甲狀旁腺素組15166.28±12.63135.64±14.06阿侖膦酸鈉組15175.60±13.25128.20±11.24聯合用藥組15213.35±12.07#151.28±13.50#
注:與假手術組比較,※P<0.05;與去勢組比較,#P<0.05。
2.3 各組骨痂BMD比較
各組大鼠股骨骨痂BMD比較見表2。去勢組較假手術組骨痂BMD顯著降低(P<0.05),甲狀旁腺素組、阿侖膦酸鈉組、聯合用藥組較去勢組骨痂BMD均增高,尤以聯合用藥組增高最顯著(P<0.05)。
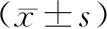
注:與假手術組比較,※P<0.05;與去勢組比較,#P<0.05。
2.4 各組血清VEGF和BMP-2濃度比較
各組大鼠血清VEGF和BMP-2濃度比較見表3。去勢組較假手術組血清VEGF和BMP-2濃度均顯著降低(P<0.05),甲狀旁腺素組、阿侖膦酸鈉組、聯合用藥組較去勢組血清VEGF和BMP-2濃度均升高,其中以聯合用藥組血清VEGF和BMP-2濃度升高最顯著(P<0.05)。
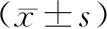
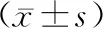

組別例數VEGF/(μg/L)BMP-2/(μg/L)假手術組152.57±0.322.94±0.50去勢組151.40±0.16※1.61±0.10※甲狀旁腺素組151.72±0.252.17±0.37阿侖膦酸鈉組151.80±0.301.97±0.20聯合用藥組152.32±0.35#2.58±0.42#
注:與假手術組比較,※P<0.05;與去勢組比較,#P<0.05。
2.5 各組組織學觀察
假手術組骨痂骨小梁粗細均勻,生長旺盛,排列致密有序,成骨細胞數量較多,大量新生微小血管形成。去勢組骨痂骨小梁明顯減少,生長稀疏,排列紊亂,大量纖維組織及纖維軟骨細胞。甲狀旁腺素組和阿侖膦酸鈉組骨痂骨小梁相對較少,仍較纖細,排列較稀疏,略不規則,成骨細胞數量相對較少,可見新生微小血管。聯合用藥組骨小梁粗大,生長旺盛,排列致密有序,可見較多成熟的骨細胞及成骨細胞,新生微小血管較多。詳見圖2。
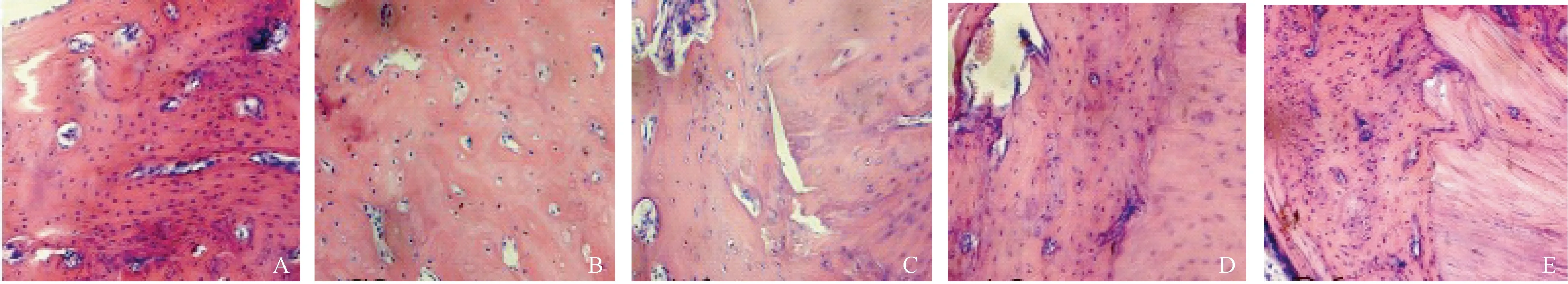
圖2 HE染色觀察骨痂的形態結構變化(×200) A:假手術組;B:去勢組;C:甲狀旁腺素組;D:阿侖膦酸鈉組;E:聯合用藥組Fig.2 Morphological changes of bone callus were observed under HE staining (×200). A: Sham operation group; B: Castration group; C: Parathyroid hormone group; D: Alendronate group; E: Combination group
假手術組、去勢組、甲狀旁腺素組、阿侖膦酸鈉組、聯合用藥組微血管計數(個/100倍視野)分別為:3.74±0.57、1.80±0.36、2.63±0.42、2.54±0.30、3.30±0.44。去勢組微血管數顯著低于假手術組(P<0.05),甲狀旁腺素組、阿侖膦酸鈉組、聯合用藥組較去勢組微血管數均增多,其中以聯合用藥組微血管數增加最顯著(P<0.05)。
2.6 各組VEGF表達
VEGF主要表達于成骨細胞內及少量成熟軟骨細胞,以細胞膜或細胞質呈棕黃色為陽性。依據免疫反應評分得出假手術組、去勢組、甲狀旁腺組、阿侖膦酸鈉組、聯合用藥組的VEGF表達分別為:0.271±0.035、0.143±0.010、0.1885±0.015、0.205±0.020、0.238±0.028。去勢組較假手術組VEGF陽性表達顯著降低(P<0.05),甲狀旁腺素組、阿侖膦酸鈉組、聯合用藥組較去勢組VEGF陽性表達均升高,其中以聯合用藥組VEGF陽性表達升高最顯著(P<0.05)。詳見圖3。

圖3 免疫組化觀察骨痂組織VEGF表達(×200) A:假手術組;B:去勢組;C:甲狀旁腺素組;D:阿侖膦酸鈉組;E:聯合用藥組Fig.3 The VEGF expression in callus was observed with immunohistochemistry (×200). A: Sham operation group; B: Castration group; C: Parathyroid hormone group; D: Alendronate group; E: Combination group
3 討論
骨折愈合是一個復雜但有序的骨組織再生的過程,這一過程不僅由基因表達所致的新骨組織的不斷合成與吸收,而且受到微環境(如細胞因子、生化因子、微血管)的影響[7]。甲狀旁腺激素(parathyroid hormone,PTH)是骨代謝過程中重要的調節因子,在調節機體鈣磷代謝有十分重要的作用。PTH(1-34)不僅可刺激成骨細胞增殖、產生堿性磷酸酶及骨基質蛋白,促進軟骨及骨形成,從而促進纖維性骨痂形成和改善骨痂的生物力學強度;而且也可以激活多種信號通路參與改善骨折愈合的過程[8]。阿侖膦酸鈉(alendronate,ALN)作為首個以骨質疏松為適應證而獲準上市的第三代二膦酸鹽類藥物。其具有抑制骨吸收,降低骨轉換、增加骨量而降低骨折發生率、加速骨折愈合[9]。研究表明,阿侖膦酸鈉通過增加骨痂量及骨密度以增加骨骼強度,通過減少分解代謝抑制破骨細胞的骨吸收作用,從而提高骨折愈合的程度[10]。
骨形態發生蛋白(bone morphogenetic protein,BMP)是骨折愈合的關鍵性細胞因子之一,具有誘導間充質細胞、骨髓基質細胞遷移、增殖、分化成軟骨細胞和成骨細胞,介導軟骨及骨形成[11]。其中尤以BMP-2作用最顯著,BMP-2通過一系列級聯反應激活其下游信號分子促進成骨細胞分化和誘導成骨的能力,參與骨形成過程中的各個階段[12]。研究表明BMP-2干預能夠加速非骨質疏松性骨折愈合速度,縮短愈合時間[13]。本研究表明甲狀旁腺激素聯合阿侖膦酸鈉具有協同上調BMP-2表達,增加骨質疏松性骨折大鼠骨密度,改善生物力學性能及骨組織形態學,加快骨折愈合。
血管形成、恢復骨折斷端血供是骨折修復的前提。VEGF是作用最強的促血管生長因子,VEGF可促進新血管生成,恢復骨折血運,VEGF還可直接作用于骨折部位成骨細胞VEGF受體,促進血管微環境中生長因子的表達。VEGF對原始成骨細胞有遷移趨化及分化作用,對骨的形成和重建有功能性的作用[14]。本研究結果表明甲狀旁腺激素、阿侖膦酸鈉聯合用藥通過介導VEGF,上調BMP-2表達,促進骨質疏松性骨折大鼠骨痂血管形成,增加骨密度,改善生物力學強度及骨組織形態學,加快骨折愈合。同樣,李梅等[15]研究表明,人甲狀旁腺素和阿侖膦酸鈉均對骨質疏松有效,聯合使用可增加骨密度和改善骨力學性能。曾中華等[16]研究表明,在骨折愈合的不同時期,BMP-2和VEGF在成骨細胞中可以互相促進表達,共同調節骨祖細胞的增殖和成骨細胞、軟骨細胞的分化,最終完成骨折修復。
綜上所述,甲狀旁腺激素和阿侖膦酸鈉聯合用藥具有協同促進骨痂血管形成,進而加快骨折愈合。聯合用藥具有潛在的臨床治療價值。但其對骨質疏松性骨折愈合不同階段具體信號調控機制還有待進一步研究。

