促胰液素對去卵巢骨質疏松大鼠血清骨轉換指標和骨密度的影響
張佳鋒 陳文亮 毛一凡 劉鐘 梁博程 史曉林*
1.浙江中醫藥大學,浙江 杭州 310053 2.浙江中醫藥大學附屬第二醫院,浙江 杭州 310005
骨質疏松癥是一種全身性骨科疾病,其特征是骨量減少,骨微觀結構退化,骨質脆性增加,容易發生脆性骨折[1]。人口老齡化的加劇使得骨質疏松發病率居高不下,其中絕經后婦女因雌激素分泌減少等多發因素,致使骨形成與骨吸收之間的動態平衡被打破,呈現高轉換特點,其發病率更是高達30%~60%[2]。而目前治療絕經后骨質疏松癥的藥物主要以雌激素類為主,雖有較好的臨床療效,但也容易引起較多不良反應,如胃腸道不良反應、乳腺癌和子宮內膜癌風險增高等[3]。因此,尋求一種更為安全且具有成本效益的藥物制劑頗有臨床意義。
筆者在醫學實驗與實踐中研究總結發現,促胰液素作為骨質疏松癥差異表達蛋白,其表達水平與骨量水平正相關,進一步研究發現,對去卵巢骨質疏松大鼠給予促胰液素治療,取得顯著療效。
1 材料與方法
1.1 實驗動物
由浙江中醫藥大學實驗動物中心提供60只6月齡健康未孕雌性SD大鼠,體重200~225 g。
1.2 實驗儀器、藥物、試劑
促胰液素:由浙江湃肽生物有限公司提供;乙烯雌酚:產自北京四環制藥二廠;PINP和CTX Elisa試劑盒:由杭州迪安醫學檢驗中心有限公司提供;雙能X線骨密度測量儀:法國Medlink公司生產。
1.3 實驗方法
1.3.1動物造模與分組:將60只SD大鼠隨機分為假手術組、模型對照組、雌激素治療組和促胰液素治療組,每組各15只。采用雙側卵巢去除法制備絕經后骨質疏松大鼠模型[4],給予3%戊巴比妥鈉注射液30 mg/kg腹腔注射麻醉,假手術組只切除卵巢周圍脂肪而不切除卵巢,其余三組均將輸卵管與脂肪結扎后切除雙側卵巢。術后第1天開始注射青霉素G5萬IU以達到抗感染目的,共3 d。
1.3.2藥物干預:卵巢切除術后7 d開始藥物干預,根據黃繼漢等[5]的動物劑量轉換公式計算劑量。假手術組給予生理鹽水1 mL/d灌胃;模型對照組給予生理鹽水1 mL/d灌胃;雌激素治療組給予乙烯雌酚水溶液0.01 mg/(kg·d)灌胃;促胰液素治療組給予促胰液素水溶液0.01 mg/(kg·d)灌胃。每日1次,持續給藥3個月。
1.3.3檢測指標:(1)骨轉換指標檢測。藥物干預3個月后,通過右心室血液取樣處死每只大鼠,并收集每只大鼠的血液標本送至杭州迪安醫學檢驗中心有限公司使用ELISA 試劑盒進行檢測,測定大鼠血清PINP和CTX。(2)骨密度檢測。藥物干預3個月后,使用雙能X線骨密度儀檢測大鼠腰椎骨密度。(3)蛋白相關分析:使用STRING10.0蛋白相互作用網絡分析工具分析骨質疏松相關差異蛋白。
1.4 統計學方法
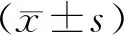
2 結果
2.1 各組大鼠血清PINP、CTX含量
模型對照組、雌激素治療組、促胰液素治療組的PINP含量較假手術組升高,差異有統計學意義(P<0.05);雌激素治療組、促胰液素治療組較模型對照組PINP含量有所降低,差異具有統計學意義(P<0.05);雌激素組與促胰液素組之間PINP含量差異無統計學意義(P>0.05)。
模型對照組的CTX含量高于假手術組,且差異具有統計學意義(P<0.05);假手術組與雌激素治療組、促胰液素治療組之間的CTX含量差異無統計學意義(P>0.05)。雌激素治療組、促胰液素治療組較模型對照組CTX含量有所降低,差異具有統計學意義(P<0.05);雌激素組與促胰液素組之間CTX含量差異無統計學意義(P>0.05)。見表1。
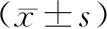
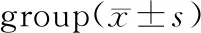
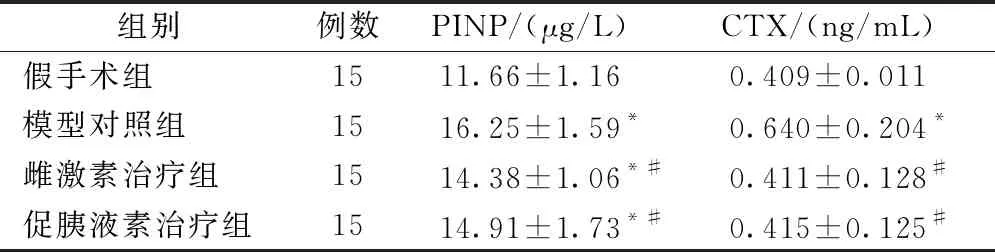
組別例數PINP/(μg/L)CTX/(ng/mL)假手術組1511.66±1.160.409±0.011模型對照組1516.25±1.59*0.640±0.204*雌激素治療組1514.38±1.06*#0.411±0.128#促胰液素治療組1514.91±1.73*#0.415±0.125#
注:與假手術組比較,*P<0.05;與模型對照組比較,#P<0.05。
2.2 各組大鼠腰椎骨密度
各組大鼠腰椎BMD比較,差異具有統計學意義。其中模型對照組BMD明顯低于假手術組,且差異具有統計學意義(P<0.05);假手術組與雌激素治療組、促胰液素治療組之間無顯著差異(P>0.05);雌激素治療組、促胰液素治療組較模型對照組BMD含量升高,差異具有統計學意義(P<0.05);雌激素組與促胰液素組之間無顯著差異(P>0.05)。見表2。
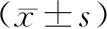
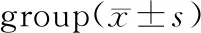

組別例數BMD(g/cm2)假手術組150.170±0.003模型對照組150.103±0.007*雌激素治療組150.168±0.004#促胰液素治療組150.167±0.003#
注:與假手術組比較,*P<0.05;與模型對照組比較,#P<0.05。
2.3 蛋白相互作用網絡分析
通過STRING10.0蛋白相互作用網絡分析工具對23個相關蛋白相互作用網絡建立,發現甲狀旁腺激素(parathyroid hormone,PTH)與促胰液素(secretin,SCT)直接相關。見圖1。

圖1 SCT和PTH以及其他相關蛋白之間的相互作用Fig.1 Interaction between SCT and PTH and other related proteins
3 討論
促胰液素是由Bayliss與Starling等[6]發現的第一種動物激素,屬于secretin/PACAP/VIP超家族,其受體都屬于G蛋白偶聯受體超家族中的B1亞族,是“激素調節”概念的先驅[7],是一種由27個氨基酸殘基組成,含11種不同氨基酸,分子量為305.6的堿性多膚。“S”細胞產生促胰液素,十二指腸粘膜是分布的主要部位,只有少量分布在胃竇、空腸和回腸中[8]。柳力公等[9]發現脂肪消化產物油酸鈉是刺激十二指腸S細胞介成和釋促胰液素的重要物質。促胰液素具有促進胰液分泌,增加胰液總量、能刺激胰腺分泌碳酸氫鹽、促進消化等生理作用。肖小芹等[10]報道烏藥水提液可通過降低大鼠血清促胰液素水平來改善腹瀉型腸易激綜合征大鼠腹痛、腹瀉癥狀。金華等[11]研究發現胃腸激素與高血壓之間存在密切關系,研究結果表明鎮肝熄風湯可通過下調促胰液素表達而降低自發性高血壓大鼠血壓。
促胰液素是人類小腸上部粘膜分泌的極其少量的調節胰液分泌的蛋白質類的激素。因其治療胃潰瘍、十二指腸潰瘍有特效而被人們所注意。促胰液素釋放的因素主要是酸,當十二指腸的pH降到3.0以下時,就會使血中的促胰液素增加,當pH升高到4.5以上時,就抑制促胰液素的繼續釋放[12]。促胰液素能促進胃腸、胰腺、肝膽管的水及電解質分泌,增強縮膽囊素的作用和胰酶的分泌,使胰腺外分泌細胞增生肥大,使細胞內的DNA和蛋白質含量增加,增強營養胰外分泌部的效應,如促進胰液分泌、抑制胃酸分泌等。促胰液素是十二指腸分泌的一種多肽,促進膽管系統和胰腺導管分泌水和碳酸氫鹽,并可阻斷水、NA+、HCO3-的重吸收,其可與CCK協同增加胰酶分泌,可促進胃酸分泌和胃腸運動[13]。黃祝等[8]研究表明,在小鼠胚胎著床過程中促胰液素在子宮內膜基質細胞中表達量增加,促進p-cPLA2、cPLA2和mPGEs-1的表達,并通過PKA信號通路調節cPLA2/p-cPLA2的水平。Secretin及其受體在中樞神經系統內廣泛分布,其中包括海馬、下丘腦垂體軸、基底神經節和小腦,越來越多的研究人員認同Secretin在中樞可能發揮著多種調節作用[14]。
近期,大量研究顯示消化系統疾病與骨質疏松癥關系密切,大部分胃切除、慢性胰腺炎、潰瘍性結腸炎等患者均容易出現骨密度低下[15-21]。這可能是消化系統疾病造成患者體內促胰液素分泌減少,繼而導致維生素D和鈣吸收不良,腸鈣吸收較差,蛋白質攝入減少,從而影響骨量。唐天悅等[22]研究發現半胱胺能夠解除生長抑素對促胰液素和膽囊收縮素的抑制作用,進而促進胰酶的合成與分泌,改善消化道對鈣和總磷等營養物質的表觀消化吸收率。
絕經后婦女由于雌激素缺乏引起骨轉換的增加,破骨細胞再吸收的速度大于成骨細胞的骨形成速度,最終造成比骨累積更多的重吸收并導致骨的凈損失,使得骨重建的正常周期受到損害,骨吸收與骨形成之間的失衡。前期研究發現,促胰液素在低骨量絕經后女性中低表達[23],表明其可能與骨質疏松存在密切聯系,但其參與并影響骨代謝的機制不清楚。而在本實驗中,模型對照組的PINP、CTX含量明顯高于假手術組(P<0.05),而BMD值則明顯低于假手術組(P<0.05),說明卵巢切除術后骨吸收、骨形成指標均有增幅,但骨吸收大于骨形成,動態平衡遭到破壞,這與絕經后骨質疏松癥高轉換特征相一致[24-25],證明本實驗骨質疏松大鼠模型造模成功。而促胰液素治療組與雌激素治療組的 PINP、CTX含量較模型對照組下降,而BMD值升高(P<0.05),且促胰液素治療組與雌激素治療組之間無顯著差異(P>0.05),說明促胰液素與雌激素類似,具有減緩絕經后骨代謝高轉化趨勢,降低骨丟失速度,增加骨密度,具有抗骨質疏松的作用。
另外,本研究使用STRING10.0蛋白質相互作用網絡分析工具來構建23種相關蛋白質的相互作用網絡[26],發現雖然SCT處于網絡邊緣,但與PTH直接相關。所以筆者懷疑SCT可能受PTH調節,調節鈣代謝,干擾Wnt、BMP/Smads、OPG/RANKL/RANK。它影響骨鈣和磷含量,抑制骨質流失,但其具體機制尚需進一步研究。
綜上所述,雖然促胰液素與骨質疏松之間的研究尚處于初始階段,其具體作用機制有待進一步研究揭示,但本研究顯示促胰液素具備一定的抗骨質疏松作用,具備成為新型抗骨質疏松藥物的潛力,為骨質疏松的防治提供了一種新的思路與方法。

