薄荷油納米乳液的制備及其性質分析
綦玉曼,尋崇榮,車佳玲,江連洲,馬文君,張瀟元,李 楊,2,王中江,*
(1.東北農業大學食品學院,黑龍江 哈爾濱 150030;2.哈爾濱食品產業研究院,黑龍江 哈爾濱 150028)
薄荷油是一種具 有濃郁薄荷香味的植物油,因其具有除臭、去腥、抑菌、防腐、增加風味等功效[1],在食品工業中被廣泛用于糖果、清涼飲料、糕點等加工中。但是,薄荷油與大多數精油一樣具有較強的揮發性,在高溫加工以及長時間儲存過程中,將會導致加入產品中的薄荷油揮發殆盡。為改善薄荷油的易揮發性質,文獻[2-4]采用不同壁材制備微膠囊包埋薄荷油提高其穩定性,方便填料和運輸。但是,微膠囊化產品大多是固體香料,不方便作為食品添加劑加入到飲料等液體食品中,且其工業化生產操作繁瑣,產品粒徑較大,生物利用度相對不高,限制其應用[5]。
近年來,納米乳液針對特定功能性物質而構建的營養素包埋與傳遞極大程度上解決了揮發型營養素在水性介質中溶解度差、生物利用率低、易揮發等問題。而且,納米乳液較普通乳液在貯存過程中可以抵抗重力分離、絮凝和聚結,被看成是一種“近熱力學穩定”體系[6]。高壓均質乳化技術作為常用的高能法制備納米乳液技術,具有乳液粒徑小、分布窄、乳液穩定、表面活性劑的需量小、生產成本低、易操作、污染小等優勢[7-8]。本研究以大豆分離蛋白(soy protein isolate,SPI)為表面活性劑、磷脂酰膽堿為助表面活性劑,通過高壓均質乳化技術制備薄荷油納米乳液,使薄荷油能夠稀釋并溶解于水相中,以提高其穩定性及吸收利用率。同時優化SPI質量分數、薄荷油質量分數、均質壓力等影響納米乳液理化性質的主要因素,為制備均一、穩定的薄荷油納米乳液提供一定參考。
1 材料與方法
1.1 材料與試劑
SPI 哈爾濱高科技(集團)股份有限公司;磷脂酰膽堿、薄荷油、胃蛋白酶、胰酶、豬膽鹽 美國Sigma公司;磷酸氫二鈉、磷酸二氫鈉 天津市東麗區天大化學試劑廠。
1.2 儀器與設備
Nano-ZS90粒度分析儀 英國馬爾文公司;ULTRA-TURRAX UTL2000乳化機 德國IKA儀器設備公司;SPCH-10高壓均質機 英國Stansted Fluid Power公司;PHSJ-4A型實驗室pH計 中國上海雷磁公司;電子分析天平(0.000 1 g) 北京賽多利斯儀器系統有限公司;H-7650B型透射電鏡 日本日立公司;7890-5795C型氣相色譜-質譜聯用儀、19091N-136型毛細管色譜柱 美國Agilent公司;Gemini HR Nano流變儀英國Malvern儀器有限公司。
1.3 方法
1.3.1 粗乳液的制備
參考Lee等[9]的方法,將SPI和磷脂酰膽堿溶于緩沖液(0.1 mol/L、pH 7.0磷酸鹽緩沖溶液)中,室溫下連續攪拌120 min,形成水相;在高速分散器的攪拌下把薄荷油作為油相加到水相中,20 000 r/min均質5 min,形成粗乳液。
1.3.2 薄荷油納米乳液的制備
將粗乳液通過高壓均質機進一步均質乳化即得高壓均質薄荷油納米乳液。高壓均質處理方法及條件設定參考Dybowska等[10]并進行一定修改,采用冰水浴保持低溫。
1.3.3 薄荷油納米乳液單因素試驗
以SPI質量分數、薄荷油質量分數、均質壓力為考察因素進行單因素試驗,測定制備的薄荷油納米乳液平均粒徑、多分散性指數(polydispersity index,PDI)、Zeta電位、濁度、乳化產率、乳液穩定性指數(turbiscan stability index,TSI)。
1.3.3.1 SPI質量分數
分別配制質量分數為1.5%、2.0%、2.5%、3.0%、3.5%的SPI和0.2%磷脂酰膽堿混合溶液,室溫下連續攪拌120 min,緩慢加入5%薄荷油,制備粗乳液。高壓均質機均質壓力為80 MPa,均質4 次,測定制備的薄荷油納米乳液平均粒徑、PDI、Zeta電位、濁度、TSI。
1.3.3.2 薄荷油質量分數
配制質量分數為2.5%的SPI和0.2%磷脂酰膽堿混合溶液,室溫下連續攪拌120 min,緩慢加入2%、5%、8%、11%、14%薄荷油,制備粗乳液。高壓均質機采用均質壓力為80 MPa,均質4 次,測定制備的薄荷油納米乳液平均粒徑、PDI、Zeta電位、濁度、TSI。
1.3.3.3 均質壓力
配制質量分數2.5%的SPI和0.2%磷脂酰膽堿混合溶液,緩慢加入5%薄荷油,制備粗乳液。設置均質壓力分別為60、80、100、120、140 MPa,均質4 次,測定制備的薄荷油納米乳液平均粒徑、PDI、Zeta電位、濁度、TSI。
1.3.4 薄荷油納米乳液的平均粒徑、PDI及Zeta電位的測定
用Zetasize r Nano-ZS 90光散射粒度分析儀分別測定上述薄荷油乳液的平均粒徑、粒徑分布規律及Zeta電位變化,薄荷油油滴的折射率為1.45,水相溶液折射率為1.33。為降低多重光散射效應,分析前用pH 7.5磷酸鹽緩沖液(0.05 mol/L)稀釋薄荷油乳液1 000 倍測定粒徑及PDI,稀釋50 倍測定Zeta電位。
1.3.5 薄荷油納米乳液的濁度測定
將薄荷油納米乳液用磷酸鹽緩沖液溶液稀釋40 倍,以磷酸鹽緩沖液為空白對照,用紫外分光光度計 測定600 nm波長處的吸光度,濁度(T)計算見公式(1):

式中:A為稀釋乳液在600 nm波長處的吸光度;V為稀釋倍數;I為光程差0.01 m。
1.3.6 薄荷油納米乳液的乳化產率測定
1.3.6.1 標準曲線的繪制
準確稱取不同質量的薄荷油,分別置于50 mL的容量瓶中,用無水乙醇稀釋定容至刻度,則得到一系列質量濃度梯度的標準溶液,以無水乙醇作為空白組,在最大吸收波長下測定標準溶液的吸光度。以吸光度對質量濃度進行線性回歸,得到標準曲線回歸方程。
1.3.6.2 納米乳液中薄荷油提取
首先稱取一定質量的薄荷油納米乳液,用無水乙醇洗去表面的油。接著把薄荷油納米乳液放入燒瓶中,并加入一定量的無水乙醇進行40 ℃水浴加熱,15 min后將此溶液用超聲波處理1 h,隨后用離心 機除去溶液中的不溶性物質,取上層清液,用50 mL容量瓶定容。
1.3.6.3 乳化產率計算
采用紫外光譜法定量分析薄荷油納米乳液的乳化產率,測定樣品的吸光度,再根據標準曲線回歸方程計算乳化產率,計算見式(2):
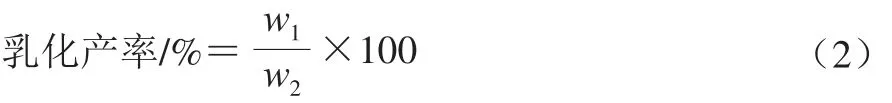
式中:w1為納米乳液中薄荷油質量;w2薄荷油總質量。
1.3.7 TSI的測定
參考劉蕾等[11]方法,取18 mL薄荷油納米乳液于Turbiscan專用圓柱形的玻璃杯(外徑27.5 mm,高度70 mm)中。在55 ℃每30 min掃描1 次,掃描時間6 h。由此可獲得反映薄荷油納米乳液穩定性的差值反射光量隨時間的動態變化,即可作為衡量薄荷油納米乳液穩定性的圖譜。
1.3.8 納米乳液透射電鏡測定
將薄荷油納米乳液樣品用蒸餾水稀釋10 倍后,滴加在覆蓋有碳膜的銅網上,用2%磷鎢酸溶液進行染色處理,放至通風處干燥后,通過透射電鏡觀察納米乳液的形態并拍照。
1.3.9 納米乳液中薄荷油的成分分析
1.3.9.1 樣品準備
將對照組薄荷油純品與從納米乳液中提取的薄荷油直接進行氣相色譜-質譜聯用儀檢測。
1.3.9.2 氣相色譜-質譜聯用儀測定條件
氣相色譜條件:1 9 0 9 1 N-1 3 6型色譜柱(60 m×0.25 mm,0.25 μm),進樣量10 μL,升溫程序:40 ℃持續3 min,然后以4 ℃/min上升至100 ℃,接著以7 ℃/min上升至240 ℃,持續7 min,分流比為10∶1。載氣為氦氣,流速為0.8 mL/min,進樣口溫度為250 ℃。
質譜條件:離子源溫度為200 ℃,檢測器電壓為350 V,電子能量為70 eV,燈絲發射電流為200 μA,接口溫度為250 ℃,質量掃描范圍m/z50~500。
1.3.9.3 化合物鑒定
利用Xcalibur軟件對實驗數據進行分析。通過計算機自動查找化合物,然后與譜庫NIST和Wiley化合物進行匹配度檢測,再手動檢索核對,選擇匹配度大于800的結果,采用歸一化法得到各成分的相對含量。
1.3.10 納米乳液的流變學特性測定
采用AR550型流變儀檢測薄荷油納米乳液的流變學特性,選擇直徑60 mm的錐形板,并控制板間距為50 μm。將1 mL薄荷油納米乳液置于平板上,剪切速率0.01~1 000 s-1,溫度25 ℃。
1.4 數據處理
每組實驗重復測量3 次,采用SPSS Statistics 22軟件對數據進行ANOVA差異顯著性分析,P值小于0.05為顯著性差異,數據均為 ±s,使用Origin Pro9.0軟件繪制曲線圖。
2 結果與分析
2.1 高壓均質制備薄荷油納米乳液工藝優化單因素試驗結果
2.1.1 SPI質量分數對薄荷油納米乳液理化穩定性的影響

表1 SPI質量分數對納米乳液理化穩定性的影響Table 1 Effects of SPI content on physical and chemical stability of nanoemulsion

圖1 SPI質量分數對納米乳液粒徑分布的影響Fig. 1 Effect of SPI content on particle size distribution of nanoemulsion
從表1可以看出,隨著SPI質量分數的增加,薄荷油納米乳液的平均粒徑、PDI、濁度呈現先減小后增加的趨勢。分析認為SPI質量分數在1%~1.5%范圍內,此時乳液中的蛋白質濃度過低,即使全部吸附在油-水界面仍未能達到飽和,溶液中的小液滴因而發生聚合現象,形成粒徑較大的液滴。乳液濁度是粒徑大小和濃度的函數,乳液濁度越大則表明較大粒徑的液滴分布越多,隨著SPI質量分數的增加,蛋白乳液體系在稀釋過程中多余的表面活性 劑膠束發揮作用,吸附破乳過程中釋放出來的油滴,從而使得油滴被包裹,進而使透明度增強。當SPI質量分數為2.5%時,液滴平均粒徑、PDI、濁度同時達到最小值,表明在此條件下蛋白在液滴表面形成緊密的界面膜,同時界面蛋白之間的電荷斥力以及空間位阻作用,使得油滴可以保持粒徑相對較小(約為200 nm)且其分布較為集中(圖1),此時乳液處于相對均一、穩定的狀態[12]。當SPI質量分數大于2.5%時,液滴的平均粒徑具有緩慢上升的趨勢,粒徑分布呈雙峰分布,并逐漸向大粒徑方向移動。說明隨著蛋白分子的不斷吸附,液滴間相對平衡的狀態被破壞,在此條件下,平均粒徑主要受均質條件而非乳化劑性能的影響[13],吸附在不同液滴上的蛋白分子的結合可能造成液滴之間的聚合,從而導致總體系中平均粒徑和濁度的增大。這一現象也可用排斥絮凝理論解釋,即當高分子乳化劑的濃度超過臨界值時,連續相中沒有吸附的蛋白會因為滲透作用引起液滴絮凝,從而引起蛋白質分子鏈從兩液滴表面排斥而出[14]。此趨勢與Mahdi等[15]結果一致,說明過量的乳化劑會影響乳液的均一性,進而影響乳液的穩定性。
從表1可以看出,隨著SPI質量分數的增加,薄荷油納米乳液Zeta電位呈現先逐漸增大后減小的趨勢,當SPI質量分數為2.5%時,納米乳液電位為-30.6 mV,而后,隨著SPI質量分數的增加,納米乳液Zeta電位逐漸降低。這表明,帶負電荷的SPI分子能夠吸附至納米乳液液滴表面,隨著SPI質量分數的增加,SPI在液滴表面吸附逐漸達到飽和,從而使得納米乳液的Zeta電位值達到平衡值,趨于穩定,不再隨著SPI質量分數增加而增加。
從表1可以得出,隨著SPI質量分數的増加,薄荷油納米乳液的乳化產率逐漸提高。當SPI質量分數大于2.5%時,納米乳液乳化產率不再隨著SPI質量分數的增加而顯著提高(P>0.05)。這是因為當SPI質量分數增加時,包裹在水-油界面上的SPI增加,提高了薄荷油納米乳液的乳化產率。根據Bi Lin等[16]的研究可知,乳化劑濃度越大,界面的吸附層越厚,從而提高了薄荷油的乳化產率,當SPI質量分數大于2.5%時,薄荷油納米乳液的乳化產率為95%以上,達到比較高的乳化產率。
從表1可以看出,隨著SPI質量分數的增加,TSI值逐 漸減小,當SPI添加量大于2.5%時,TSI值趨于穩定。以上結果表明,當SPI質量分數較小時,薄荷油納米乳液的TSI變大,表明此時乳液穩定性變差,說明此SPI質量分數并不足以覆蓋乳液液滴表面,可能使得薄荷油液滴發生絮凝,從而降低薄荷油納米乳液的穩定性。當SPI質量分數逐漸增大時,界面上吸附的蛋白分子也增加,膜的強度相應增大,液滴難以聚結,納米乳液能夠保持較好的物理穩定性。同時,隨著SPI質量分數的增大,乳液的黏度增加,根據斯托克斯定理,高黏度體系中,液滴具有較低的沉降速率,從而有利于得到更穩定的乳狀液體系。
本實驗制備以不同添加量的SPI為乳化劑的薄荷油納米乳液,當SPI添加量較少時,界面 蛋白發生構象改變以完全覆蓋水油界面;當SPI添加量較多時,有較多的SPI吸附在界面上,從而使吸附在界面上的SPI不能發生構象改變。界面上SPI較多時,形成較厚的界面膜,對油滴的保護提高;同時因為SPI沒有發生構象改變,其因空間位阻而使液滴相互排斥的作用比較大,進一步防止液滴粒徑增大,提高乳液穩定性[17]。綜合考慮乳化劑濃度對平均粒徑和粒徑分布寬度、乳化產率、濁度、TSI的影響,2.5%的SPI足夠吸附到油滴界面而形成比較穩定的薄荷油納米乳液,此質量分數最適合薄荷油納米乳液的制備。
2.1.2 薄荷油質量分數對薄荷油納米乳液理化穩定性的影響

表2 薄荷油質量分數對納米乳液理化穩定性的影響Table 2 Effect of peppermint oil content on stability of nanoemulsion

圖2 薄荷油質量分數對納米乳液粒徑分布的影響Fig. 2 Effect of peppermint oil content on particle size distribution of nanoemulsion
在乳液的制備過程中,高芯壁比往往是配方 中所追求的,不僅可以提高該運載體系的效率,而且有利于乳液在后續加工和應用中的可操作性。但是,芯材載入量過大時,顆粒間易發生聚集,從而對乳液粒徑和穩定性產生不利影響。由表2可知,乳液的平均粒徑、PDI、濁度、TSI隨薄荷油質量分數的增加先降低后增大。由圖2可知,當薄荷油質量分數為5%時,乳液具有最小粒徑分布寬度。分析原因在于較高的油載荷會使均質化的液滴更多更小,從而使蛋白質有更大的可吸附表面積,這會使圍繞油滴的界面膜更穩定且聚結力更強。因此,制備的納米乳液均比較穩定。薄荷油質量分數為11%、14%的薄荷油納米乳液粒徑分布在1 000 nm處出現了1 個新的峰(圖2),說明過量的油相不能很好地被乳化劑所包埋,極易通過介質的流動而擴散到大油滴中,從而引起乳液粒徑的增加,發生奧氏熟化現象[18],導致粒徑分布變寬,粒徑與濁度變大。
隨著薄荷油質量分數的進一步增加,乳液的Zeta電位絕對值減小。這表明高油負荷降低了乳液的穩定性。在較低的Zeta電位下,分散油滴之間的空間排斥可能不足以克服液滴和能量位壘之間的分子間吸引力(即范德華力和疏水吸引力)[19]。因此,乳液在自然條件下絮凝,并且液滴傾向于聚集,提高了分層率。薄荷油質量分數的增加對乳化后的產率影響不大。因此確定薄荷油的質量分數為5%。
2.1.3 高壓均質壓力對薄荷油納米乳液理化穩定性的影響

表3 均質壓力對納米乳液理化穩定性的影響Table 3 Effect of homogenization pressure on stability of nanoemulsion

圖3 均質壓力對納米乳液粒徑分布的影響Fig. 3 Effect of h omogenization pressure on particle size distribution of nanoemulsion
研究表明,高壓均質采用的壓力參數對粒徑的大小具有顯著影響。由表3和圖3可知,隨著均質壓力的增加,乳液的平均粒徑、PDI、濁度和TSI急劇下降,粒徑分布范圍變窄,集中分布在80~400 nm波長之間,均質壓力高于80 MPa,平均粒徑、PDI、濁度和TSI緩慢上升,粒徑分布峰逐漸向大粒徑方向偏移。影響乳液粒徑主要因素是高壓均質過程中巨大的機械力作用(巨大剪切力、撞擊和空穴效應)[20],兩者間存在一定的函數關系,即均質壓力越高,機械作用越強,粒徑越小,液滴細化程度越高,分布越均勻,但均質壓力過高時,作用在乳液上的沖擊力較大,乳液的液滴過小[21],顆粒之間由于彼此的布朗運動速率加快、相互碰撞的次數增加足以破壞界面膜而發生聚集現象[22],同時高壓可以引起蛋白質變性[23],變性蛋白質分子相互作用形成聚集體,溶解度下降,并從界面上脫落,進而阻礙液滴被均質破壞,降低均質的效果[24],與此同時,由于液滴過小,比表面積增大,乳化劑的數量不足以覆蓋液滴表面,導致液滴聚集。類似結果在Schulz等[25]的研究中也曾被報道。由表3可知,均質壓力對乳液Zeta電位影響不大。當均質壓力小于80 MPa時,隨著均質壓力的增加,乳化產率逐步提高,超過80 MPa時,乳化產率隨均質壓力的增加而快速下降。這是因為均質時的剪切力和空穴效應,導致薄荷油破碎[26]。綜上,均質壓力選擇為80 MPa。
2.2 薄荷油納米乳液的形態及粒徑分布

圖4 薄荷油納米乳液的透射電鏡圖Fig. 4 TEM pictures of peppermint oil nanoemulsion
由圖4可直觀地看出,乳液的平均粒徑小,液滴分布均勻,表明高壓均質過程中產生的巨大剪切、湍流作用、空穴效應的確能起到較好的乳化效果。有研究表明:乳液平均粒徑的減小,不僅有效提高乳液的穩定性,有效抑制沉淀和乳析的發生,也顯著提高功能成分和營養素,尤其是非水溶性物質的生物利用率[14]。
2.3 納米乳液中薄荷油主要成分的檢測結果
對薄荷油納米乳液物理化學穩定性的研究發現,薄荷油納米乳液具有較好的理化穩定性。將單因素試驗優化的最佳工藝條件制備的薄荷油納米乳液和對照組薄荷油進行氣相色譜-質譜檢測,結果如表4所示。結果表明薄荷油經過乳化后其中的部分烯類物質,如2-β-蒎烯、α-蒎烯、檸檬烯、δ-杜松烯、D-大根香葉烯、β-波蒡烯的比例部分降低,分析原因在于一方面可能與上述幾類物質在空氣中極易揮發的性質有關,另一方面可能在高壓均質的作用下造成了這些物質的氧化損失,進而導致總含量稍有下降,此結果與陳碩[27]與梁蓉[28]等研究結果類似。而薄荷油主要的功能性成分薄荷酮、薄荷醇等含量未出現明顯改變,表明薄荷油經高壓均質制備 成納米乳液后,能夠形成一種更穩定的乳液體系,從 而迅速將功能性成分穩 定地乳化在納米體系中,降低薄荷油在生產加工和運輸儲存過程中的損失。

表4 納米乳化包埋前后薄荷油中主要成分相對含量Table 4 Change in relative quantity of main components in peppermint oil before and after incorporation into nanoemulsions
2.4 納米乳液的流變學特性
納米乳液的流變特性在食品領域實際生產中具有一定的指導意義,乳化體系的黏度變化曲線在一定程度上可以表征乳液的聚合程度,進一步反映乳液的動力學穩定性。由圖5可知,隨著納米乳液剪切速率的增大,乳液的黏度逐漸降低。在較小的剪切速率(0.1~400 s-1)時,薄荷油納米乳液的黏度急劇下降,呈現出剪切變稀的特征,主要原因在于流速場中,薄荷油納米乳液的乳滴形成絮體并瓦解[29]。當剪切速率大于400 s-1后,納米乳液的黏度未發生明顯變化,呈現牛頓流體性質,這是因為絮體被裂解成為單個液滴,也可能是乳化體系形成與瓦解絮體的速率相同,絮體具有相對穩定的狀態[30]。薄荷油納米乳液納米級粒徑進一步增大乳液的比表面積,增加乳滴之間的相互作用,導致薄荷油納米乳液的黏度增加,根據Stoke定律,當乳液具有較大的黏度時,有利于減緩液滴的上浮速度,保持更好的穩定性。流變學特性結果補充說明了高壓均質制備的薄荷油乳液具有良好的動力學穩定性。

圖5 薄荷油納米乳液的流變性Fig. 5 Rheological property of peppermint oil nanoemulsion
3 結 論
以SPI-磷脂酰膽堿復合物作為乳化劑,采用高壓均質法制備薄荷油納米乳液,研究SPI質量分數、薄荷油質量分數及均質壓力對薄荷油納米乳液的平均粒徑、PDI、Zeta電位、濁度、乳化產率、TSI的影響機制,并通過動態光散射和透射電鏡驗證,當SPI質量分數2.5%、薄荷油質量分數5%、均質壓力80 MPa時,制備出的薄荷油納米乳液平均粒徑小且分布均勻;通過氣相色譜-質譜檢測發現SPI-磷脂酰膽堿為乳化劑制備的納米乳液可有效保護薄荷油功能成分;流變學特性結果說明薄荷油納米乳液具有良好的動力學穩定性。因此,此方法能夠快速地制備穩定性好的薄荷油納米乳液,是一種較為實用、高效的薄荷油納米乳液制備技術,為今后薄荷油在食品領域中的應用提供依據和參考。

