建蘭花葉病毒RT-LAMP檢測(cè)方法的建立
樊榮輝 黃敏玲 鐘淮欽 羅遠(yuǎn)華

摘? 要? 建蘭花葉病毒(Cymbidium mosaic virus,CyMV)是侵染蘭花的主要病毒,嚴(yán)重影響其觀賞價(jià)值,建立快速、靈敏的檢測(cè)方法顯得尤為重要。根據(jù)CyMV的外殼蛋白基因序列設(shè)計(jì)4對(duì)特異性引物,經(jīng)過(guò)優(yōu)化反應(yīng)條件,建立該病毒的RT-LAMP 檢測(cè)方法,并進(jìn)行LAMP檢測(cè)的特異性、敏感性檢測(cè)。該方法能特異擴(kuò)增CyMV,與其他4種病毒(齒蘭環(huán)斑病毒、菜豆黃花葉病毒、黃瓜花葉病毒和小蒼蘭花葉病毒)不發(fā)生反應(yīng);靈敏度為RT-PCR的10倍。田間檢測(cè)20份樣品中,RT-LAMP和RT-PCR檢測(cè)結(jié)果一致,檢出率為60%。在產(chǎn)物中加入熒光染料SYBR GreenⅠ,直接用肉眼觀察就可判斷樣品是否感染CyMV,可省去電泳分析的時(shí)間。針對(duì)CyMV建立的RT-LAMP方法具有特異性強(qiáng)、靈敏度高、操作簡(jiǎn)單、快速等特點(diǎn),適用于在進(jìn)境檢疫及種苗繁育過(guò)程中的檢測(cè)鑒定。
關(guān)鍵詞? 建蘭花葉病毒;RT-LAMP;檢測(cè)
中圖分類號(hào)? S436.8? ? ? 文獻(xiàn)標(biāo)識(shí)碼? A
建蘭花葉病毒(Cymbidium mosaic virus,CyMV)是蘭花中最嚴(yán)重的病毒之一,洋蘭(蝴蝶蘭、石斛蘭、文心蘭等)主要由CyMV病毒單獨(dú)侵染為主[1]。蘭花受CyMV侵染后出現(xiàn)花葉、畸形、壞死及花瓣變色等癥狀,導(dǎo)致品質(zhì)下降,影響觀賞價(jià)值,制約蘭花產(chǎn)業(yè)發(fā)展[2-3]。目前尚缺乏有效防治建蘭花葉病毒的藥劑,最有效方法是培育無(wú)毒種苗,而這就需要對(duì)種苗進(jìn)行病毒檢測(cè)及鑒定。因此,建立快速、靈敏的檢測(cè)技術(shù)尤為重要。目前,對(duì)CyMV的檢測(cè)主要集中在酶聯(lián)免疫法(ELISA)和RT-PCR技術(shù)。2006年,Lee等[4]建立了CyMV與其他病毒的多重RT-PCR檢測(cè)技術(shù),2008年,Lee等[5]建立了CyMV的抗血清技術(shù)。這些技術(shù)能有效檢測(cè)CyMV,并對(duì)后續(xù)新技術(shù)出現(xiàn)提供借鑒。酶聯(lián)免疫法是目前較常用的一種方法[6],但也存在靈敏度不高、易出現(xiàn)假陽(yáng)性等缺點(diǎn)。PCR技術(shù)已成為常規(guī)檢測(cè)手段[7],但由于實(shí)驗(yàn)設(shè)備要求比較高,不利于向基層檢驗(yàn)部門(mén)推廣。環(huán)介導(dǎo)等溫核酸擴(kuò)增技術(shù)(Loop-me diated isothermal amplification,LAMP)應(yīng)用4條特異性引物,通過(guò)Bst DNA聚合酶,在水浴鍋中對(duì)靶基因進(jìn)行的一種恒溫?cái)U(kuò)增技術(shù)[8],該技術(shù)具有擴(kuò)增特異性強(qiáng)、靈敏度高、操作快速簡(jiǎn)便、檢測(cè)簡(jiǎn)單等特點(diǎn),擺脫了對(duì)PCR儀等昂貴儀器的依賴[9-11],在基層的檢測(cè)更加方便。本研究對(duì)CyMV的保守外殼蛋白(CP)基因設(shè)計(jì)4條特異性引物,并對(duì)其靈敏性和特異性進(jìn)行驗(yàn)證,建立了可特異檢測(cè)該病毒的RT-LAMP檢測(cè)方法,以期為蘭花種苗篩選提供可靠簡(jiǎn)便的檢測(cè)方法,也利于基層檢疫部門(mén)進(jìn)行進(jìn)出口檢測(cè)。
1? 材料與方法
1.1? 材料
感染了建蘭花葉病毒(Cymbidium mosaic virus, CyMV)、黃瓜花葉病毒(Cucumber mosaic virus,CMV)、小蒼蘭花葉病毒(Freesia mosaic virus,F(xiàn)reMV)、齒蘭環(huán)斑病毒(Odontoglossum ringspot virus,ORSV)、菜豆黃花葉病毒(Bean yellow mosaic virus,BYMV)的陽(yáng)性樣品及健康對(duì)照樣品的葉片均由本實(shí)驗(yàn)室保存。
熒光染料SYBR GreenⅠ購(gòu)自北京鼎國(guó)公司;Bst聚合酶、MgSO4購(gòu)自New England Biolabs(美國(guó));EcoR I、PMD18-T載體、JOM109 感受態(tài)細(xì)胞均購(gòu)自TaKaRa;甜菜堿購(gòu)自Sigma(美國(guó))。
1.2? 方法
1.2.1? RT-LAMP 體系的建立? 取感染病毒的葉片,按照多糖多酚植物總RNA提取試劑盒(北京百泰克生物技術(shù)有限公司)方法提取樣品的總RNA。
根據(jù)GenBank公布的CyMV較保守的CP基因序列為靶標(biāo)基因(AY429021、HQ644132、GU295168、AF016914、EU672821和GQ507023),設(shè)計(jì)得到6區(qū)域的4條特異性引物,其中F3和B3為外引物,F(xiàn)IP和BIP為內(nèi)引物(表1)。引物由上海生工生物工程有限公司合成。
反應(yīng)體系(25 μL):10×Bst buffer 2.5 μL、 25 mmol/L MgSO4 4 μL、5 mmol/L Betaine 4 μL、2.5 mmol/L dNTPs 4 μL 、8 U/μL Bst聚合酶1 μL、20 μmol/L FIP 2 μL、20 μmol/L BIP 2 μL、10 μmol/L F3 0.5 μL、10 μmol/L B3 0.5 μL、 ddH2O 2 μL、cDNA 2.5 μL。反應(yīng)條件為:65 ℃、60 min,80 ℃、5 min。進(jìn)行瓊脂糖凝膠電泳分析;同時(shí)產(chǎn)物中加入SYBR GreenⅠ,目視觀察結(jié)果。
1.2.2? RT-LAMP 產(chǎn)物酶切鑒定? 為了進(jìn)一步驗(yàn)證LAMP擴(kuò)增的正確性,在設(shè)計(jì)LAMP引物時(shí)加入了EcoRⅠ酶切位點(diǎn)(gaattc)。將LAMP反應(yīng)產(chǎn)物電泳后,梯形條帶進(jìn)行膠回收,再用EcoR Ⅰ37 ℃酶切過(guò)夜,連接于PMD18-T載體上,用JOM109感受態(tài)細(xì)胞轉(zhuǎn)化,測(cè)序。
1.2.3? 特異性和靈敏度驗(yàn)證? 對(duì)感染ORSV、FreMV、CMV、BYMV、CyMV的陽(yáng)性樣品,分別提取總RNA,應(yīng)用RT-LAMP檢測(cè),瓊脂糖凝膠電泳進(jìn)行分析。
對(duì)感染CyMV陽(yáng)性樣品的總RNA,進(jìn)行10、102、103、104、105倍梯度稀釋,分別進(jìn)行RT-LAMP 和 RT-PCR靈敏度檢測(cè)。
運(yùn)用RT-LAMP和RT-PCR技術(shù),對(duì)田間隨機(jī)采集的10份建蘭和10份文心蘭樣品進(jìn)行特異性檢測(cè)和驗(yàn)證。
2? 結(jié)果與分析
2.1? RT-LAMP
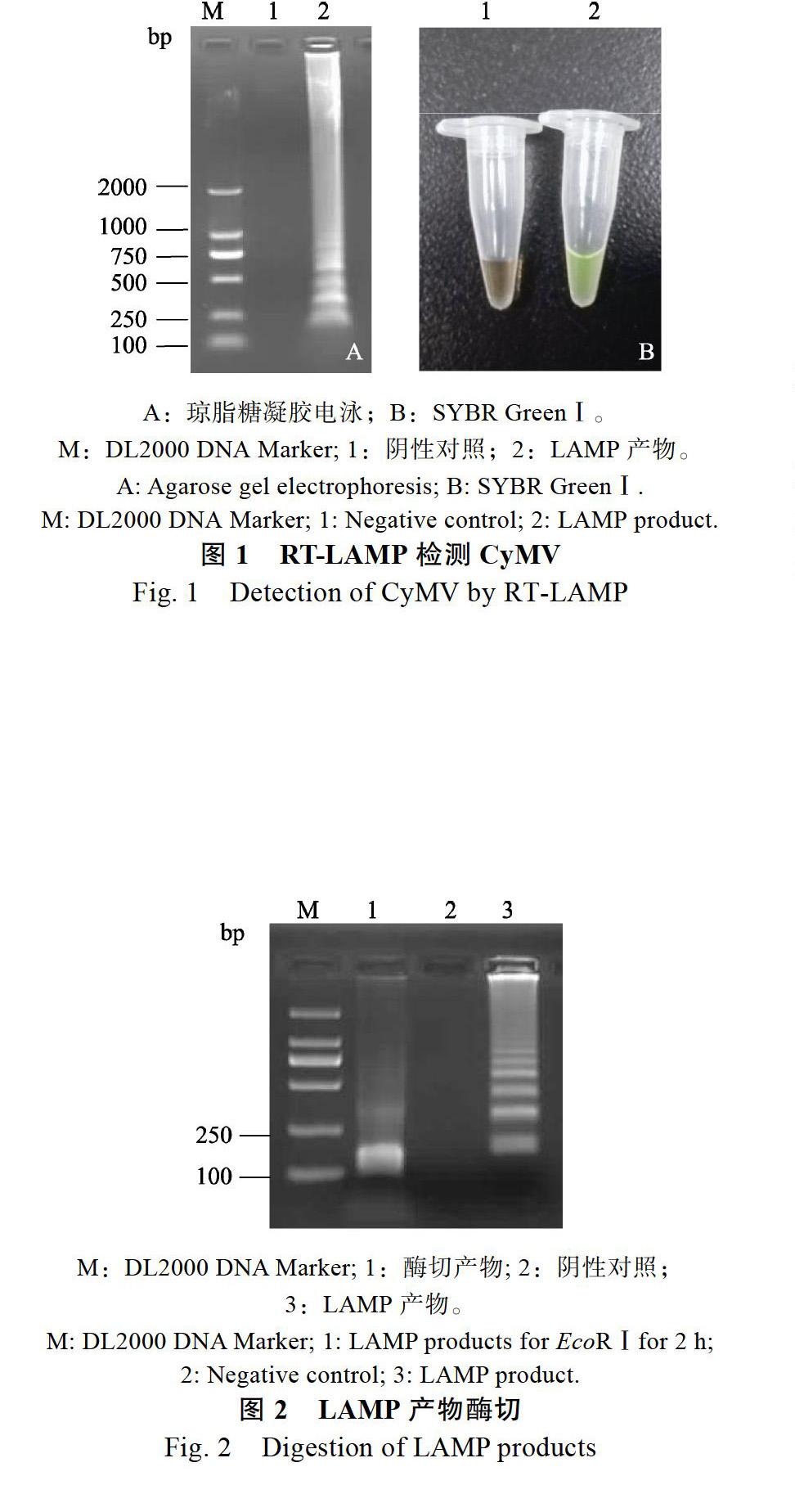
通過(guò)反應(yīng)體系的優(yōu)化,建立了能擴(kuò)增CyMV的RT-LAMP 反應(yīng)體系(圖1),RT-LAMP反應(yīng)產(chǎn)物有階梯狀的條帶,陰性對(duì)照未發(fā)現(xiàn)條帶;加入 SYBR GreenⅠ,混勻,RT-LAMP反應(yīng)產(chǎn)物為黃綠色,陰性對(duì)照為橙色。
2.2? RT-LAMP反應(yīng)產(chǎn)物的酶切驗(yàn)證
將LAMP產(chǎn)物膠回收后,用EcoRⅠ酶切如圖2,并進(jìn)行轉(zhuǎn)化測(cè)序,最終得出,酶切出的片段為目標(biāo)基因的F2-B2的序列,包括酶切堿基在內(nèi)大小為165 bp。證明該體系擴(kuò)增產(chǎn)物為靶基因。
2.3? 特異性驗(yàn)證
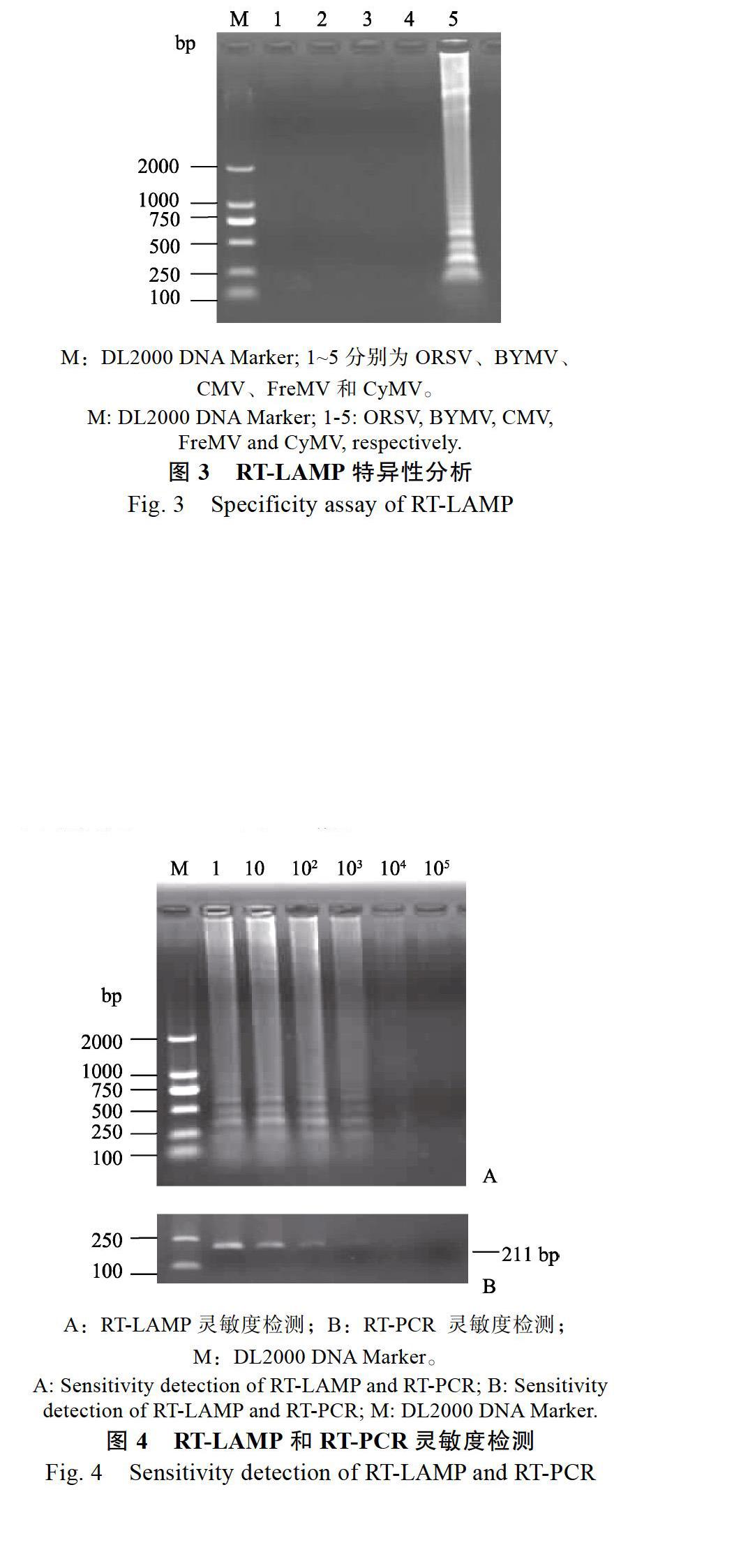
以分別感染ORSV、BYMV、FreMV、CMV和CyMV的樣品總RNA為模板,進(jìn)行RT-LAMP 擴(kuò)增。如圖3所示,只有CyMV有梯狀條帶,檢測(cè)結(jié)果為陽(yáng)性,其他不產(chǎn)生條帶,說(shuō)明建立的檢測(cè)體系對(duì)CyMV檢測(cè)有較好特異性。
2.4? 靈敏度檢測(cè)
對(duì)不同濃度稀釋后的RNA,分別進(jìn)行 RT-LAMP和RT-PCR反應(yīng)。結(jié)果顯示,RT-LAMP在稀釋1000倍時(shí),仍能檢測(cè)出CyMV,而RT-PCR在稀釋100倍還能檢測(cè)出CyMV,稀釋1000倍時(shí),未檢出(圖4),表明RT-LAMP檢測(cè)CyMV的靈敏度是RT-PCR的10倍。
2.5? 田間樣品測(cè)定
隨機(jī)采取建蘭和文心蘭樣品各10份,分別進(jìn)行RT-LAMP和RT-PCR檢測(cè),結(jié)果顯示,兩者檢測(cè)結(jié)果一致,建蘭有4份樣品呈陽(yáng)性,文心蘭有8份樣品呈陽(yáng)性(表2),表明RT-LAMP檢測(cè)技術(shù)能應(yīng)用于田間樣品。
3? 討論
蘭花是中國(guó)四大名花之一,代表高貴、典雅,具有極高的觀賞和收藏價(jià)值。但當(dāng)病毒病侵染時(shí),植株會(huì)出現(xiàn)畸形、壞死,從而造成品質(zhì)下降,這是制約蘭花大規(guī)模生產(chǎn)的重要因子。為滿足消費(fèi)需求,培育無(wú)病毒苗是防止病毒病的重要措施,因此,建立快速、準(zhǔn)確、高效的檢測(cè)方法,對(duì)阻止病毒病的傳播有良好作用;或?qū)γ摱久邕M(jìn)行檢測(cè),從根源上預(yù)防病毒病也具有重要意義。本試驗(yàn)針對(duì)建蘭花葉病毒建立的環(huán)介導(dǎo)等溫?cái)U(kuò)增技術(shù)具有擴(kuò)增快速高效、特異性好、操作簡(jiǎn)便、不需要特殊儀器等優(yōu)點(diǎn),可以針對(duì)性地對(duì)蘭花脫毒種苗進(jìn)行檢測(cè),從種源遏制病毒病的發(fā)生。本研究技術(shù)具有較高的應(yīng)用價(jià)值,在基層和現(xiàn)場(chǎng)檢測(cè)中有很好的應(yīng)用前景。
目前,病毒檢測(cè)的常用方法是PCR和ELISA技術(shù),均且具有較好的檢測(cè)效果,但也存在耗時(shí)長(zhǎng),成本高的特點(diǎn),不太適用于基層檢測(cè)。與常規(guī)PCR方法相比,本研究所建立的LAMP技術(shù),在保持PCR技術(shù)優(yōu)點(diǎn)的基礎(chǔ)上,不需特殊儀器,成本低,且由于不需要熱循環(huán),整個(gè)過(guò)程可以在60 min內(nèi)完成,更加省時(shí),檢測(cè)結(jié)果若采用加入SYBR GreenⅠ目測(cè)的方式,檢測(cè)更快捷方便。因此該方法特別適合在基層中應(yīng)用。
LAMP 技術(shù)使用4~6條引物,會(huì)進(jìn)一步增強(qiáng)反應(yīng)的特異性[12-13]。引物設(shè)計(jì)至關(guān)重要,也較復(fù)雜和困難,除要遵循一般引物設(shè)計(jì)原則外,還有LAMP 引物設(shè)計(jì)自身要注意的事項(xiàng)[14],特別是對(duì)于病毒多個(gè)生理小種間保守的CP基因差異明顯或GC含量較高序列設(shè)計(jì)更加困難[15]。本研究針對(duì)建蘭花葉病毒CP基因設(shè)計(jì)引物,經(jīng)驗(yàn)證該引物的特異性良好。同時(shí),本研究建立的檢測(cè)CyMV的RT-LAMP方法靈敏度較高,比常規(guī)PCR靈敏度高10倍,對(duì)于病毒含量很少的脫毒苗的快速檢測(cè)方面有一定的優(yōu)勢(shì)。LAMP方法靈敏度高,容易出現(xiàn)假陽(yáng)性,因此本研究采用在RT-LAMP 反應(yīng)管蓋上滴加SYBR green I染色劑,待反應(yīng)結(jié)束后在不開(kāi)蓋的情況下直接使染色劑與擴(kuò)增產(chǎn)物混合,以此減少反復(fù)開(kāi)蓋而造成的污染問(wèn)題。
參考文獻(xiàn)
Rubies A C,Autonell C,Ballante M, et al. Viral infections in melon crops of cenral northern Italy[J]. Informatore Fitopatologieo, 1999, 46: 6-10.
Zettler F W, Ko N J, Wisler G C, et al. Viruses of orchids and their control[J]. Plant Disease, 1990, 74(9): 621-626.
Wong S M, Cheng C G, Lee Y H, et al. Incidence of Cymbidium mosaic and Odontoglossum ringspot viruses and their significance in orchid cultivation in Singapore[J]. Crop Protection, 1994, 13: 235-239.
Lee S C, Chang Y C. Multiplex RT-PCR detection of two orchid viruses with an internal control of plant nad5 mRNA[J]. Plant Pathology Bulletin, 2006, 15: 187-196
Lee S C, Chang Y C. Performances and application of antisera produced by recombinant capsid proteins of Cymbidium mosaic virus and Odontoglossum ringspot virus[J]. European Journal of Plant Pathology, 2008, 122: 297-306.
梁敏國(guó), 劉光華. 廣東蘭花病毒病調(diào)查和病原檢測(cè)[J] . 江西植保, 2004, 27(3): 97-100.
柳愛(ài)春, 趙? 蕓, 劉? 超, 等. 雙重一步法RT-PCR檢測(cè)2種主要蘭花病毒[J]. 安徽農(nóng)業(yè)科學(xué), 2009, 37(27): 12960-12961, 13009.
Notomi T, Okayma H, Masubuchi H, et al. Loop-mediated isothermal amplification of DNA[J]. Nucleic Acids Research, 2000, 28(12): e63.
Harper S J, Ward L I, Clover G R. Development of LAMP and real-time PCR methods for the rapid detection of Xylella fastidiosa for quarantine and field applications[J]. Phytopathology, 2010, 100(12): 1282-1288.
Singh P, Mirdha B R, Ahuja V, et al. Loop-mediated isothermal amplification (LAMP) assay for rapid detection of Entamoeba histolytica in amoebic liver abscess[J]. World Microbiol Biotechnol, 2013, 29(1): 27-32.
Ranjan R, Kanjayan M, Subramaniam S, et al. Development and evaluation of a one-step reverse transcription-loop mediated isothemal amplication assay (RT-LAMP) for rapid detection of foot and mouth disease virus in India[J]. Virus Disease, 2014, 25(3): 358-364.
高宏偉,徐? 彪,朱來(lái)華,等. 應(yīng)用LAMP檢測(cè)方法檢測(cè)肉制品中的單增李斯特菌[J]. 食品安全質(zhì)量檢測(cè)技術(shù), 2010, 27(1): 12-17.
Zhang Y Q, Shan X X, Shi L, et al. Development of a fim Y-based loop-mediated isothermal amplification assay for detection of Salmonella in food[J]. Food Research International, 2012, 45(2): 1011-1015.
王? 永, 蘭青闊, 趙? 新, 等. 轉(zhuǎn)基因作物外源轉(zhuǎn)基因成分環(huán)介導(dǎo)等溫?cái)U(kuò)增技術(shù)檢測(cè)方法的建立及應(yīng)用[J]. 中國(guó)農(nóng)業(yè)科學(xué), 2009, 42(4): 1473-1477.
Chen L, Guo J, Wang Q, et al. Development of the visual loop-mediated isothermal amplification assay for seven genecitally modified maize events and their application in practical samples analysis[J]. Journal of Agricultural and Food Chemistry, 2011, 59(11): 5914-5918.