液相色譜-串聯質譜法快速同時測定人血漿中卡培他濱及其活性代謝物
熊璐琪,趙博欣
(1.廣東省惠州市中心人民醫院藥學部,惠州 516001;2.南方醫科大學南方醫院藥學部,廣州 510515)
作為一種影響核酸合成的細胞毒類藥物,氟尿嘧啶(5-fluorouracil,5-FU)至今仍廣泛應用于頭頸部腫瘤、消化道腫瘤、乳腺癌、肺癌等的治療。其主要不良反應包括腹瀉、黏膜炎、口腔炎、惡心、嘔吐以及骨髓抑制等。從藥物代謝角度考慮,多種藥物代謝酶在5-FU的代謝解毒和代謝活化中起重要作用[1],因此其藥動學存在明顯的個體差異。然而,有文獻報道,其血藥濃度與不良反應之間有很強相關性[2-3]。一項隨機Ⅲ期臨床試驗顯示,依據藥動學指標調整5-FU劑量,明顯提高療效并降低不良反應發生率,隨訪結果顯示患者總生存獲益[4]。
卡培他濱作為一種5-FU前體藥物,經胃腸道給藥后,在體內活化為5-FU從而發揮抗腫瘤的作用[5]。由于腫瘤組織中胸腺嘧啶脫氧核苷酸磷酸化酶顯著多于正常組織,使得該藥有一定的靶向性。鑒于卡培他濱在體內代謝過程中的復雜性,加之其與5-FU具有相類似的最終代謝過程,卡培他濱同樣表現出較大的個體差異。然而,筆者尚未見依據卡培他濱藥動學參數來個體化調整給藥劑量從而改善患者臨床收益的相關系統性研究。
為了獲得臨床患者卡培他濱的藥動學參數,高效快速的定量方法是其重要的關鍵技術。國外雖有采用液相色譜-串聯質譜(liquid chromatography-tandem mass spectrometry,LC-MS/MS)法測定卡培他濱及其代謝產物報道,國內卻鮮有相關研究。不僅如此,現有報道的方法由于存在樣本預處理過于繁冗,檢測時間過長,定量限過高,重復性差等不足,難以在臨床實踐中開展。因此,筆者采用親水性液相色譜-串聯質譜(hydrophilic liquid chromatography series mass spectra,HILIC-LC-MS/MS)方法快速定量卡培他濱及其活性代謝產物,旨在為臨床提供更加高效、快速、簡潔的定量方法,以便為臨床針對此類藥物相關的個體化精準治療提供依據。
1 儀器與試藥
1.1儀器 Agilent1260 液相色譜-G6460三重四級桿質譜聯用儀(G1312B型四元輸液泵,G367E型自動進樣器,G1316A型柱溫箱,G1322A型脫氣機)色譜工作站:(B.04.01 SP2),P13110S 電子天平(德國Sartotins公司,感量:0.1 mg);Centrifuge 5810R高速離心機(美國Eppendorf公司)。
1.2試藥 卡培他濱對照品(批號:ZZS17010904)、5-FU對照品(批號:ZZS17010908)均購于上海甄準生物科技有限公司;乙腈、甲酸、乙酸銨為色譜純,其他化學試劑均為化學純。
2 方法與結果
2.1色譜條件 色譜柱為Agilent Poroshell 120 Hilic (2.1 mm×50 mm,2.7 μm); 流動相為乙腈- 25 mmol·L-1乙酸銨溶液(含0.1%甲酸)(95:5);流速:0.3 mL·min-1; 柱溫30 ℃。
2.2質譜條件 離子源為電噴霧離子源(ESI源);Vcap 毛細管電壓4 000 V;干燥器溫度340 ℃;離子源霧化器(N2),流量:9 L·min-1; 霧化氣壓力241.325 kPa。卡培他濱和5-FU的碰撞能分別為-13 eV和-17 eV;裂解電壓均為7 V。
2.3工作液及質量控制樣品的制備 精密稱取卡培他濱及5-FU適量,并溶解于乙腈中,分別制成濃度為400及750 μg·mL-1的儲備液。將儲備液用乙腈連續稀釋制成含兩種成分濃度為390.625,781.25,1562.5,3125,6250,12 500,25 000,50 000及100 000 ng·mL-1的混合工作液。用儲備液以同樣方法單獨稀釋成濃度為781.25,6250,50 000 ng·mL-1的高、中、低濃度質量控制樣品。所有溶液均保存于4 ℃環境中,使用前室溫放置復溫。
2.4血漿樣品的處理 取血漿樣品100 μL加入乙腈400 μL作為提取溶劑,渦旋混合1 min,低溫20 000×g離心15 min,轉移上清液,取2 μL用于 液相色譜-質譜聯用(LC-MS/MS)分析。
2.5質譜分析 應用ESI負離子模式進行檢測。卡培他濱在全掃描的模式下,母離子為358.1(M-H)具有很高的液質響應值,其他雜質不干擾母離子的測定。進行子離子掃描時,當裂解電壓為130 V,碰撞能為13 eV時,卡培他濱主要離子碎片為m/z=154.1。5-FU在全掃描的模式下,母離子的碎片為m/z=129(M-H),在多離子反應監測(multiple reaction monitoring,MRM)模式下,子離子的碎片為m/z=42.1,碰撞能為17 eV,裂解電壓為90 V時,響應值最穩定,卡濱他濱及5-FU的質譜圖見圖1,MRM圖見圖2。
2.6方法專屬性 分別取6份不同來源不含相關檢測藥物的人空白血漿,按“血漿樣品處理”項下操作,進行LC-MS/MS檢測。結果表明,空白血漿中內源性物質不干擾待測物卡培他濱及5-FU的測定。并且在樣品的檢測時無雜峰干擾。見圖3。

A.卡培他濱;B.5-FU
Fig.1Productionspectraofcapecitabineand5-fluorouracil
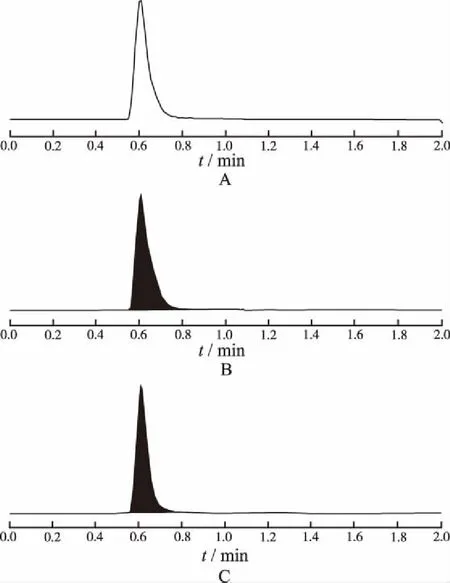
A.空白樣品;B.卡培他濱;C.5-FU
Fig.2MRMchromatogramofcapecitabineand5-fluorouracil
2.7標準曲線的繪制 取工作液10 μL,真空干燥后,加入空白血漿100 μL渦旋混勻,配制成最終濃度為39.062 5~10 000 ng·mL-1的含藥血漿,加入乙腈400 μL,以待測物濃度為橫坐標,待測物的峰面積值為縱坐標,用最小二乘法進行線性回歸,卡培他濱的回歸方程為:Y=5.0645X+60.783,R2=0.999 3 (n=9),5-FU的回歸方程:Y=2.651 3X+37.845,R2=0.999 2 (n=9),方法線性范圍在39.062 5~10 000 ng·mL-1。
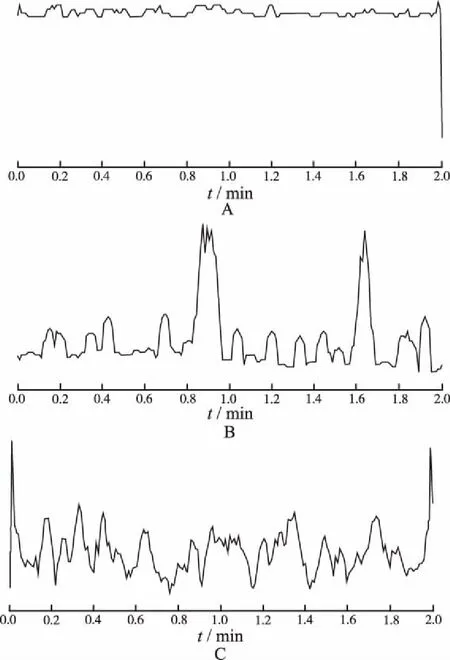
A.TIC;B.卡培他濱;C.5-FU
由于本方法主要適用于臨床檢測,盡管LC-MS/MS法檢測靈敏度高,但由于臨床檢測中卡培他濱及5-FU至31.25 ng·mL-1以下的意義有限,因此,本法中卡培他濱及5-FU的最低定量限均為31.25 ng·mL-1(S/N>10)。
2.8提取回收率 取空白血漿100 μL,按“2.7”項下方法制備低(78.125 ng·mL-1)、中(625 ng·mL-1)、高(5000 ng·mL-1)濃度的質量控制樣品各6份,進樣2 μL,記錄卡培他濱及5-FU峰面積A1;同時檢測(低、中、高)3種質量控制濃度對應檢測藥物標準溶液,進樣2 μL,所得峰面積A2。血漿中提取回收率(%)=A1/A2×100%:卡培他濱低、中、高濃度提取回收率分別為(78.22±3.15)%,(75.37±2.99)%及(81.05±2.78)%,5-FU低、中、高濃度的提取回收率分別為(70.45±2.19)%,(72.56±1.68)%及(72.02±1.72)%。上述結果表明,卡培他濱及5-FU的提取前后一致性良好并且沒有濃度依賴性,提取回收率較高,適用于該方法檢測。
2.9精密度和準確度實驗 取空白血漿100 μL,按“2.7”項方法配制低、中、高濃度的卡濱他濱及5-FU的質量控制樣本,測定日內精密度以及連續測定3 d,并與標準曲線同時進行,計算質量控制樣品的測得濃度,與配制濃度對照,求得本法準確度與精密度。計算得準確度滿足定量分析中90%~110%的范圍,日內以及日間精密度均在±15%(表1)。
2.10穩定性實驗 按“2.7”項下方法配制低、中、高3個濃度含藥血漿,室溫條件下放置1和24 h后,處理樣本,與新鮮配制的儲備液比較;樣本處理后,1 h與24 h后進樣分析,與新鮮配制的儲備液比較;分別于-20 ℃反復凍融3次和樣品預處理后室溫放置24 h,使用相同處理條件,比較放置后所檢測濃度是否穩定。RE(%)=(測量濃度-理論濃度)/理論濃度×100%。考察樣品的穩定性,結果見表2,在上述考察條件下,3個濃度無顯著變化,RE均<10%,上述數據證明卡培他濱及5-FU在室溫、樣品處理、反復凍融的條件下均穩定,實驗結果準確可靠。
2.11基質效應 取6種不同來源空白血漿,分為6組,每組各制備3個空白血漿樣品,按照血漿樣品提取方法進行空白樣品提取。離心后,于每組3管溶液中分別加入低(781.25 ng·mL-1)、中(6250 ng·mL-1)或高(50 000 ng·mL-1)濃度卡培他濱及5-FU標準溶液各10 μL,旋渦10 s,20 000×g離心15 min后取上清液進樣。以此種處理方法測定的卡培他濱與5-FU峰面積與以水為替代基質處理的相應濃度樣品峰面積的比值計算百分比,結果表明,低、中、高濃度的卡培他濱和5-FU的基質效應影響百分比平均值分別為125.45%,131.10%,130.95%及118.34%,126.63%,124.08%,表明兩藥在低、中、高濃度下基質效應對血藥濃度測定影響程度基本一致。
2.12血漿卡培他濱及5-FU濃度檢測的臨床應用 20例患者以卡培他濱說明書規定劑量口服藥物1~2周,隨機抽取服藥前全血并分離血漿,對卡培他濱及5-FU的穩態谷濃度進行檢測。患者卡培他濱的平均血藥濃度為2802.424 ng·mL-1,分布區間為1 661.627~4 438.821 ng·mL-1;5-FU的平均血藥濃度為343.365 ng·mL-1,分布區間為133.735~674.165 ng·mL-1。以卡培他濱血藥濃度為橫坐標,相對應患者5-FU的血藥濃度為縱坐標進行線性回歸分析(圖4),R2=0.1996,表明兩藥間相關性較差。因此,同時檢測卡培他濱與5-FU的血藥濃度具有較好的臨床意義。
表1 3種質量控制濃度的日內及日間精密度
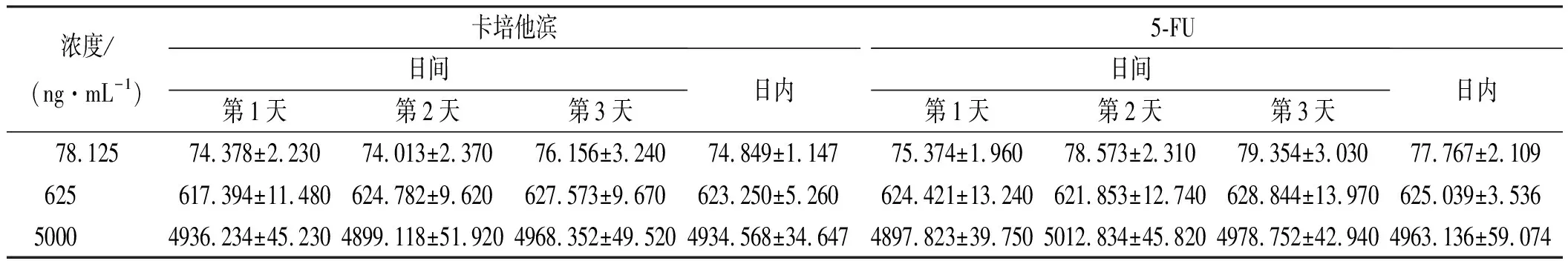
濃度/(ng·mL-1)卡培他濱日間第1天第2天第3天日內5-FU日間第1天第2天第3天日內78.12574.378±2.23074.013±2.37076.156±3.24074.849±1.14775.374±1.96078.573±2.31079.354±3.03077.767±2.109625617.394±11.480624.782±9.620627.573±9.670623.250±5.260624.421±13.240621.853±12.740628.844±13.970625.039±3.53650004936.234±45.2304899.118±51.9204968.352±49.5204934.568±34.6474897.823±39.7505012.834±45.8204978.752±42.9404963.136±59.074
表2 卡培他濱及5-FU在人血漿中的穩定性
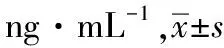
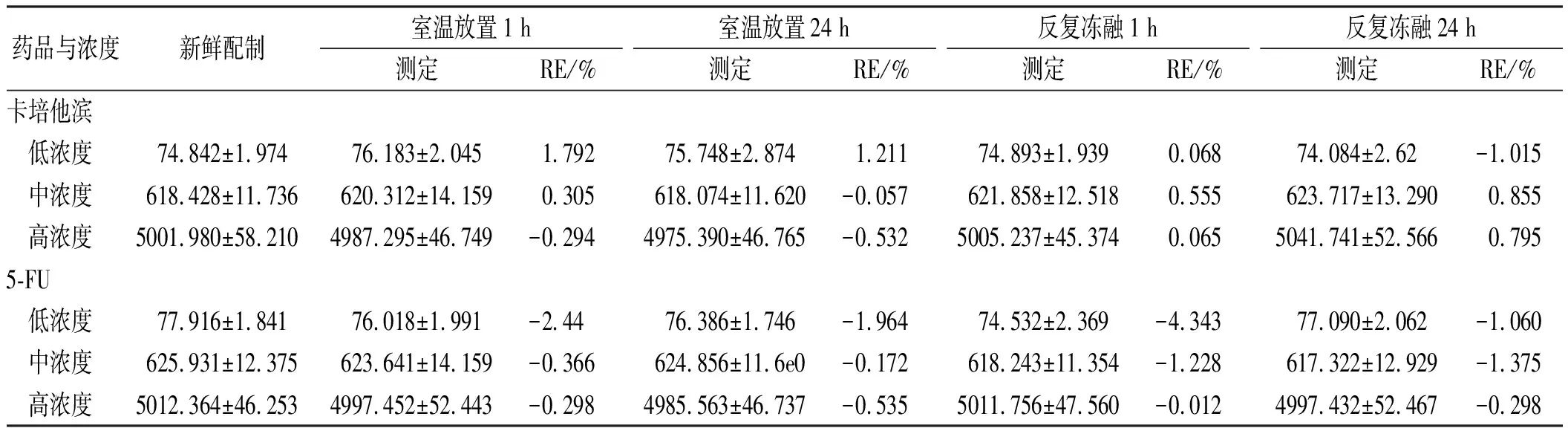
藥品與濃度新鮮配制室溫放置1 h測定RE/%室溫放置24 h測定RE/%反復凍融1 h測定RE/%反復凍融24 h測定RE/%卡培他濱 低濃度74.842±1.97476.183±2.0451.79275.748±2.8741.21174.893±1.9390.06874.084±2.62-1.015 中濃度618.428±11.736620.312±14.1590.305618.074±11.620-0.057621.858±12.5180.555623.717±13.2900.855 高濃度5001.980±58.2104987.295±46.749-0.2944975.390±46.765-0.5325005.237±45.3740.0655041.741±52.5660.7955-FU 低濃度77.916±1.84176.018±1.991-2.4476.386±1.746-1.96474.532±2.369-4.34377.090±2.062-1.060 中濃度625.931±12.375623.641±14.159-0.366624.856±11.6e0-0.172618.243±11.354-1.228617.322±12.929-1.375 高濃度5012.364±46.2534997.452±52.443-0.2984985.563±46.737-0.5355011.756±47.560-0.0124997.432±52.467-0.298
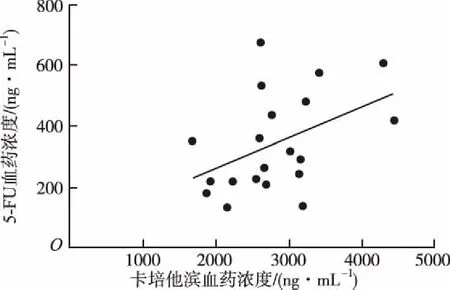
圖4 臨床患者卡培他濱與其活性代謝產物5-FU血藥濃度相關性
Fig.4Correlationofplasmaconcentrationofcapecitabineand5-fluorouracilinclinicalpatients
3 討論
卡培他濱是一種新型口服氟嘧啶核苷類似物,在體內轉變為5-FU發揮抗腫瘤作用,由于其不良反應相對5-FU較輕,近年來逐漸在臨床中替代5-FU使用。從生物藥劑學的角度,卡培他濱在口服給藥后約1.5 h內達到血藥峰濃度,稍后5-FU達到峰濃度。進入循環后,卡培他濱可廣泛分布于全身各組織當中,其中,在消化道、肝臟、腎臟組織中的藥物濃度較高,在腦組織內藥物濃度較低。卡培他濱主要在肝臟中代謝并經腎臟排泄,尿中排泄率為80%~90%,其藥物原型的排泄率僅為3%[6]。由于卡培他濱轉化為其活性代謝產物需要經過較多次的酶促反應,且其代謝酶均存在影響其活性的SNP位點,因此,同時檢測卡培他濱及其活性代謝產物5-FU的血藥濃度對評價卡培他濱的治療效果及預測其毒副作用具有重要的臨床意義。
目前,國內常用高效液相色譜法對卡培他濱或5-FU進行檢測[7-8]。但由于色譜法專屬性差、操作步驟繁瑣、檢測時間長,不僅增加檢驗難度,還降低該項目檢測臨床開展的適用性。而另一種主流治療藥物監測的化學法,采用抗原抗體反應,可檢測5-FU的血藥濃度,但尚無卡培他濱的相關試劑盒上市。而化學法的藥物濃度檢測,操作步驟亦較多,試劑盒成本較高,且抗原抗體反應易受到內源性物質或相關藥物代謝產物的干擾,從而影響檢測的準確度。而國外雖已采用LC-MS/MS法測定卡培他濱或5-FU,但分析方法存在諸多問題。如SALVADOR等[9]使用LC-MS/MS法同時測定人血漿中卡培他濱及其代謝物的濃度,所采用的洗脫方法對色譜柱傷害大,色譜運行時間長,且采用固相萃取法處理樣品,操作繁瑣,成本高,耗費大。HERMES等[10]使用LC-MS/MS法同時測定人血漿中5-FU及卡培他濱的濃度,其使用衍生化法處理樣品,雖色譜運行時間短但樣本處理過程操作繁瑣復雜,降低分析效率的同時還增加了成本。MONTANGE等[11]報道LC-MS/MS法同時測定人血漿中卡培他濱及其代謝物的濃度,色譜運行時間長達15 min,且樣品需重復測定,樣本需要量大(一次需使用500 μL),分析效率低,不利于臨床的應用及推廣。TSUME等[12]采用LC-MS/MS法同時測定生物樣品中5-FU及其代謝物的濃度,所采用的方法得到5-FU的定量下限為25 ng·mL-1,靈敏度低。
本研究建立一種快速同時檢測人血漿中卡培他濱及其活性代謝產物5-FU的LC-MS/MS的檢測方法,具有以下優點:①專屬性強,采用LC-MS/MS方法在固有設備特點中相較其他檢測設備具有更高的檢測專屬性,不易受到極性類似或結構類似內源性成分或代謝產物的影響。②靈敏度高,采用本方法對兩種成分進行檢測,達到在線性范圍內小于40 ng·mL-1的檢測限,并在低濃度區間內表現出較好的精密度與準確度。③樣品需求少,本方法檢測中僅需血漿樣品100 μL進行同管檢測,且檢測速度快,僅2 min即可完成1例樣品中卡培他濱及5-FU的同時檢測。④檢測方法學穩定,精密度、穩定性及回收率等均較為穩定,表明該方法適用于臨床血漿樣品檢測。⑤樣本處理過程簡單。
應用建立的方法對臨床患者血漿樣品進行檢測,結果表明,患者血漿中卡培他濱及5-FU的分布區間均較寬泛,表明卡培他濱的血藥濃度存在個體差異性,進而其活性代謝產物的濃度存在較大差異。卡培他濱與其對應樣品中代謝產物5-FU血藥濃度的相關性較差,證實卡培他濱與其活性產物間在代謝過程中可能存在代謝酶活性的個體差異。由于5-FU的血藥濃度對卡培他濱的臨床療效及不良反應均有較好的指導意義。因此,筆者建立同時檢測卡培他濱及5-FU血藥濃度的方法,一方面可以通過5-FU的血藥濃度評價并推測服用卡培他濱進行化療患者的臨床收益,對于濃度未在合理區間的患者及時調整劑量,另一方面同時對卡培他濱進行檢測,可以在調整劑量過程中更確切得知不同代謝酶活性患者在卡培他濱向5-FU代謝為程中的實際生物轉化情況,從而有利于實現更好的臨床療效并減少不良反應。
卡培他濱與5-FU的保留時間分別為0.610和0.611 min,若在傳統的HPLC條件下進行紫外檢測,兩色譜峰將無法分離,但通過MRM檢測模式具有色譜與質譜分離的能力,根據各自獨特的分子結構所產生的母離子和碎片離子,以質譜的高分辨能力,同時檢測不同的物質,最終形成圖譜,通過色譜工作站(B.04.01 SP2軟件)將卡培他濱及5-FU各自的色譜圖提取出來,兩藥的含量測定結果互不干擾。
綜上所述,采用LC-MS/MS法以乙腈提取血漿樣品來同時檢測卡培他濱與5-FU的濃度,是一種具有高靈敏度、高專屬性、簡單快捷且穩定的檢測方法。此法能快速檢測生物樣品中卡培他濱及5-FU,適用于卡培他濱制劑相關臨床治療中的治療藥物監測。

