克林霉素引起的急性腎損傷一例
戴魯筠 朱加明
1 臨床資料患者男,41歲,因“血尿、無尿、少尿伴血肌酐水平進行性升高12 d”入院。患者既往體格健壯,于2015年6月16日開始流涕、咳嗽,體溫38.4 ℃。6月17日于當?shù)匦l(wèi)生所就診,予鹽酸克林霉素1.2 g靜脈注射,注射期間患者感手指發(fā)麻,伴畏寒;注射后尿色變紅,伴下腹部、腰部脹痛和惡心。當日急診查血常規(guī):白細胞計數(shù)13.9×109/L,中性粒細胞比例0.844,中性粒細胞數(shù)絕對值為11.73×109/L。6月18日患者尿量<100 mL,伴明顯腰酸腰痛、胸悶、惡心嘔吐;血清尿素氮(BUN)18.62 mmol/L(正常參考值為2.9~8.2 mmol/L),血清肌酐(Cr)443.7 μmol/L(正常參考值為44~115 μmol/L);尿蛋白(+),尿潛血(+++),尿滲透壓295.36 mmol/L(正常參考值為600~1 000 mmol/L);總膽紅素、間接膽紅素、乳酸脫氫酶、肌酸激酶、淀粉酶水平均高于正常值。當晚復查血清BUN 23.7 mmol/L,血清Cr 731 μmol/L。中下腹部CT檢查:雙側腎周筋膜增厚模糊,提示炎性滲出可能。追問病史,患者于2015年3月體格檢查時測血清Cr 97 μmol/L;曾于外院行4次血液透析(簡稱血透)治療,第4次血透后患者尿量增至約400 mL/24 h。6月25日 患者至復旦大學附屬中山醫(yī)院就診,測血清BUN 13.9 mmol/L,血清Cr 1 201 μmol/L;腎臟超聲檢查:雙腎腎病(左、右腎長徑分別為110、115 mm)。病程中多次測血嗜酸性細胞數(shù)均無異常,免疫球蛋白E 124 U/mL(正常參考值為20~200 U/mL)。于2015年6月29日收入院,檢測血清BUN 22.2 mmol/L,血清Cr 1 944 μmol/L;蛋白(+/-),尿紅細胞(-);24 h尿蛋白0.18 g;3次尿相差顯微鏡檢查均偶見紅細胞;乙型肝炎病毒(HBV)、腫瘤標志物、風濕免疫指標均未見異常。7月1日行腎臟穿刺活組織病理學檢查:全片見13個腎小球,其中3個球性硬化、1個節(jié)段硬化,余腎小球體積略增大、毛細血管袢瘀血、毛細血管開放尚可;腎小球固有細胞數(shù)約70個/球(每個腎小球的肉眼計數(shù)腎固有細胞70~80個),系膜基質增多不明顯,系膜細胞增生不明顯,壁層上皮細胞增生與袢粘連,部分腎小球有囊壁纖維化;腎小管間質重度病變,小管數(shù)目減少,大量腎小管上皮細胞濁腫空泡變,部分壞死脫落,小管管壁可見炎性細胞浸潤,偶見小管上皮細胞再生,可見紅細胞管型、透明管型、顆粒管型,腎小管間質高度水腫,大量炎性細胞浸潤聚集成團,以單個核細胞為主,可見較多嗜酸性粒細胞;間質小動脈透明變,血管周圍可見炎性細胞浸潤。免疫熒光檢查:免疫球蛋白(Ig)G(-),IgA(+/-),IgM(-),補體(C)3(++),C4(-),C1q(-),Kappa輕鏈(-),Lambda輕鏈(-);少許IgA、C3呈顆粒狀、團塊狀,在系膜區(qū)彌漫分布。病理診斷:急性間質性腎炎伴腎小管壞死;局灶節(jié)段性腎炎(圖1)。為進一步明確診斷,抽取患者和健康志愿者的外周靜脈血,行克林霉素淋巴細胞轉化試驗,患者的試驗結果呈陽性。臨床診斷:急性腎損傷(AKI)3期,急性間質性腎炎伴腎小管壞死;局灶節(jié)段性腎炎。住院期間分別于6月30日、7月2和4日行血透治療;7月1和2日予甲潑尼龍琥珀酸鈉240 mg靜脈注射每日1次;明確病理診斷后于7月3和4日予甲潑尼龍琥珀酸鈉500 mg靜脈注射每日1次;7月5日起改為潑尼松龍60 mg口服每日1次,并輔以護腎、護胃、堿化尿液等治療。經(jīng)激素治療后,患者尿量逐漸增至3 000 mL/d以上,監(jiān)測血清Cr水平逐漸下降;7月13日復查血清Cr 248 μmol/L后出院。出院后繼續(xù)予激素60 mg口服每日1次,并規(guī)律減量;8月12日隨訪復查血清Cr水平降至134 μmol/L。患者于2018年8月7日至復旦大學附屬中山醫(yī)院腎內科門診隨訪,復查血清BUN 7.4 mmol/L,血清Cr 120 μmol/L。
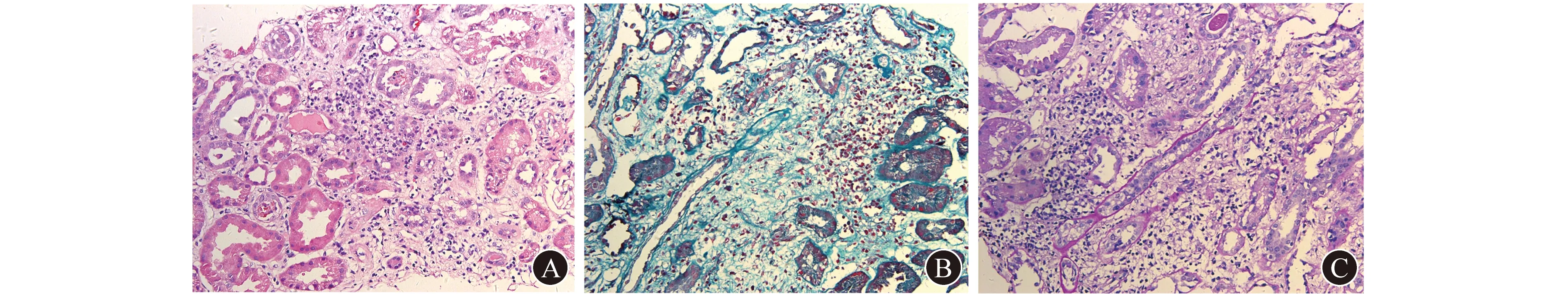
A H-E染色 B Masson染色 C 過碘酸雪夫(PAS)染色圖1 腎臟穿刺活組織病理學圖片(×200)
2 討 論該患者最終診斷為克林霉素引起的AKI,為AKI分期3期。入院時,詳細詢問其病史并完善相關檢查,該患者無容量不足、體液丟失、心功能不全、外傷等病史,故不考慮由腎前性因素引起的AKI。腎臟超聲、CT檢查無腎后梗阻證據(jù);既往無高血壓、糖尿病病史,腫瘤標志物、HBV-DNA、抗中性粒細胞胞漿抗體(ANCA)、抗腎小球基底膜抗體(GBM)抗體、自身抗體均為陰性,排除常見的自身免疫相關的急進性腎炎。結合患者的臨床癥狀與明確的克林霉素用藥密切相關,用藥后即肉眼見血尿、少尿、無尿和血清Cr水平快速升高,考慮由藥物引起的AKI可能性最大。入院后腎臟穿刺活組織病理學檢查示腎小管間質可見較多嗜酸性粒細胞,結合臨床表現(xiàn)和用藥史,提示過敏性急性間質性腎炎伴腎小管壞死,支持藥物腎毒性的診斷,最終經(jīng)克林霉素淋巴細胞轉化試驗證實。需要注意的是,用藥前患者在2015年3月體格檢查時血清Cr水平正常,但腎臟病飲食改良(MDRD)公式計算內生Cr清除率為76 mL/(min·1.73 m2),存在腎功能減退的基礎,且腎臟穿刺活組織病理學檢查提示局灶節(jié)段性腎炎。
克林霉素是林可霉素分子中第7位羥基被氯離子取代的半合成品,對革蘭陽性菌、厭氧菌有強大的抗菌作用。中國克林霉素注射液包括鹽酸克林霉素注射液和克林霉素磷酸酯注射液。在中國由克林霉素引起的AKI發(fā)生率顯著高于國外。國內一項針對2007—2014年的文獻回顧分析結果顯示,林可酰胺類占所有引起AKI藥物的3.6%,盡管病例數(shù)不多,但均由克林霉素引起[1]。
以“克林霉素+AKI”在2003—2019年的維普期刊中檢索由克林霉素所致AKI的相關文獻,再從中逐篇閱讀篩選,最終納入相關文獻5篇[2-6]。其中包括個案報道4篇,綜合報道1篇;病例數(shù)累計36例,男22例、女14例,中位年齡為39歲;克林霉素給藥途徑均為靜脈注射,中位用藥量1.6 g/d,部分為聯(lián)合用藥;用藥后最常見的癥狀為血尿(80.6%)、尿量減少或無尿(41.7%)、腰痛(19.4%),其余癥狀有惡心、嘔吐、腹脹,有1例患者出現(xiàn)大量腹腔積液;AKI發(fā)生時間為用藥后0.5 h~7 d;平均血清Cr水平為716.2 μmol/L,有13例患者進行血透治療。藥物治療包括激素、利尿劑、多巴胺、復方丹參液。僅1例患者行腎臟穿刺活組織病理學檢查,結果提示中度腎小管間質病變。所有患者治療后均轉歸良好。
有學者[7]報道24例由克林霉素引起的AKI患者,用藥量為1.0~1.5 g/d,AKI發(fā)病的中位時間為用藥后1 d(0.5 h~4 d)。15例患者出現(xiàn)肉眼血尿、皮疹、關節(jié)痛、外周血嗜酸性粒細胞數(shù)量增多罕見。63.2%的患者克林霉素淋巴細胞轉化試驗結果呈陽性。腎臟活組織病理學檢查證實為急性間質性腎炎和急性腎小管壞死。
急性腎小管壞死的最初臨床表現(xiàn)為少尿、無尿,尿液檢查時可見上皮細胞管型,尿鈉多>40 mmol/L,尿滲透壓<400 mmol/L。有學者[7]根據(jù)由克林霉素導致的AKI發(fā)病時間通常很短,推測克林霉素所致AKI的主要病理機制為直接的腎小管毒性作用。腎小管被結晶堵塞會提高急性間質性腎炎的發(fā)生率。克林霉素大部分在肝臟代謝,僅10%經(jīng)腎臟排泄,尿液中高濃度的克林霉素可在腎小管中凝結,導致腎小管梗阻。Fogazzi等[8]認為血尿,尤其是肉眼血尿是由藥物結晶所致。本例患者在靜脈注射克林霉素后即出現(xiàn)肉眼血尿,提示腎小管和腎臟受到損害。因此,早期出現(xiàn)的肉眼血尿是克林霉素腎毒性的臨床特征之一,需高度重視,當出現(xiàn)血尿時,應立即停止靜脈注射克林霉素,予以水化和堿化有可能減輕腎臟損害。
臨床上由藥物引起的急性間質性腎炎的癥狀不典型[9-10],難以與其他病因引起的AKI相鑒別,患者可有不適、乏力、食欲下降、惡心、“感覺發(fā)熱”和經(jīng)典的麻疹樣皮疹,尤其是軀干部的皮疹,對診斷藥物引起的急性間質性腎炎有很大的提示作用,但皮疹不敏感且不常見。Baker等[11]報道,急性間質性腎炎患者中有15%~50%表現(xiàn)為藥物引起的皮疹。血嗜酸性粒細胞數(shù)量增多常提示藥物過敏反應,有助于住院期間獲得的AKI的診斷,但血嗜酸性粒細胞診斷急性間質性腎炎的敏感性并不高,患者外周血嗜酸性粒細胞的比例和數(shù)值可完全正常[12]。僅5%~10%的急性間質性腎炎患者出現(xiàn)皮疹、發(fā)熱、血嗜酸性粒細胞增多三聯(lián)征[12-13]。Praga等[14]認為,急性間質性腎炎的發(fā)病機制是免疫誘導的對某些抗原,如腎小管基底膜成分、腎小管蛋白等的超敏反應,細胞介導的免疫反應在其中發(fā)揮了重要作用。病理組織學檢查見腎間質大量單個核細胞和嗜酸性粒細胞浸潤,進一步腎小管基底膜特異免疫熒光染色陰性排除了其他免疫性腎臟疾病。克林霉素淋巴細胞轉化試驗陽性表明外周血中可找到克林霉素特異的T淋巴細胞,可能進一步釋放炎性細胞因子。綜上所述,盡管本例患者無發(fā)熱、皮疹、嗜酸性粒細胞增多三聯(lián)征,但克林霉素淋巴細胞轉化試驗結果呈陽性,腎臟穿刺活組織病理學檢查見腎間質大量炎性細胞浸潤,以單個核細胞為主,可見較多嗜酸性細胞,腎小管上皮濁腫空泡變,均證實該患者的AKI由克林霉素所致,主要通過直接損害腎小管功能,以及激發(fā)淋巴細胞轉化引起。
AKI發(fā)展至腎衰竭期可選擇間歇性血透治療,如果容量負荷嚴重或血流動力學不穩(wěn)定,應首選連續(xù)性腎臟替代治療。目前認為,早期應用糖皮質激素治療對藥物所致的急性間質性腎炎患者的腎功能恢復有好處。Coca等[15]的研究結果顯示,治療組(靜脈注射甲潑尼龍250~500 mg/d治療3~4 d,再口服潑尼松治療8~12周)的血清Cr水平顯著低于對照組,需行透析治療的患者數(shù)量顯著少于對照組;腎功能未完全恢復正常的患者從停藥至接受激素治療的時間為(34±17)d,顯著長于腎功能完全恢復正常的患者的(13±10)d。而Clarkson等[13]的研究結果表明,糖皮質激素治療對于急性間質性腎炎患者腎功能恢復的速度和終線血清Cr水平并無益處。但值得注意的是,上述研究中糖皮質激素治療組從發(fā)病至腎臟活組織檢查的中位時間為4周(2~6周),所有患者糖皮質激素均在腎臟活組織檢查的4 d內使用。本例患者是在出現(xiàn)癥狀后的第15天起予糖皮質激素治療,同時在無尿期已行間歇性血透治療,隨訪期間患者的血清Cr水平逐漸好轉。
克林霉素在國內基層醫(yī)院的使用廣泛,因其具有厭氧作用,較多用于婦產科青霉素、頭孢類抗生素過敏時的替代治療,在臨床上對克林霉素引起的AKI應提高警惕,早期診斷和治療對腎功能完全恢復極其重要。

