以紅皮病為臨床表現的嗜酸性粒細胞增多性皮炎一例
李貝貝 閔仲生
臨床資料患者,男,68歲。因“全身紅斑、脫屑、瘙癢9年,泛發性紅斑反復發作4年”于2018年6月8日入院。患者9年前無明顯誘因下出現四肢、軀干紅斑,伴瘙癢,至當地醫院就診,診斷為“濕疹”,經治療后好轉(具體用藥不詳),隨后病情反復,偶起新疹,未予重視。4年前無明顯誘因皮疹突然增多,并融合成片,局部脫屑,瘙癢癥狀加重,外院診斷“紅皮病”,查嗜酸粒細胞百分比30.3%,嗜酸粒細胞計數2.60×109/L,予甲潑尼龍40 mg/d輸液治療三天,病情有所好轉,停藥后皮疹復起。當地醫院查骨髓細胞形態學:各階段嗜酸性細胞核比例增高,桿狀核比例減低,各階段細胞形態大致正常,提示嗜酸細胞增多癥。染色體JAK-2、BCR-ABL均正常,FISH-FIP1L1/PDGFA融合基因未做,后數次至我院皮膚科及血液科門診就診,多次復查嗜酸粒細胞計數及百分比均明顯增高,診斷“嗜酸性粒細胞增多性皮炎”,先后予糖皮質激素、沙利度胺、曲尼司特及口服中藥治療(具體不詳),皮疹控制不佳,反復發作,遂由門診收住院。分別于2014年先后4次入住我科。2014-04皮膚活檢結果:(左腹皮膚)表皮角化不全,棘層增生,表皮突下延,表皮基底及真皮淺層小血管周圍淋巴、漿、單個核細胞浸潤(圖1)。免疫組化:CD3(+)(圖2a),CD20(灶性+)(圖2b),CD45RO(+)(圖2c),CD68(局部+)(圖2d),CD79a(灶性+)(圖2e),lyso(局部+)(圖2f),mpo(-)。免疫組化結果示:(左腹皮膚)表皮基底及真皮淺層T淋巴細胞優勢增生,伴少量單核細胞、B細胞等浸潤。后均未再次行皮膚及骨髓活檢。第1次治療方案為糖皮質激素聯合雷公藤,第2、3次因上呼吸道感染皮疹加重,搔抓后破潰,糜爛明顯,治療予以甲潑尼龍80 mg日1次靜滴、環孢素軟膠囊75 mg日2次、先后予頭孢呋辛、頭孢米諾注射液抗感染、復方甘草酸苷、白芍總苷、酮替芬、地氯雷他定、康復新液濕敷及對癥支持治療,期間患者收縮壓波動在140~165 mmHg,心內科會診后予纈沙坦氫氯噻嗪片80/12.5 mg日1次控制血壓,因患者反復低鉀改為纈沙坦膠囊80 mg日1次。病情好轉后激素逐漸減量改為小劑量口服維持治療。后持續服用環孢素軟膠囊、甲潑尼龍片、地氯雷他定片等,控制尚可。2個月前患者軀干及雙上肢皮疹加重,現再次入住我科。患者一般情況尚可,無發熱盜汗,無咽喉腫痛,無關節疼痛等。既往體健,無銀屑病及其他特殊病史,無家族性類似病史。查體:T:36.7℃,P:87次/分,R:18次/分,BP:131/60 mmHg,雙側腹股溝淋巴結(蠶豆大小)腫大,無口腔潰瘍,兩肺聽診呼吸音清,未聞及明顯干濕啰音,無胸膜摩擦音,心尖搏動正常,心率87次/分,律齊,各瓣膜聽診區未聞及明顯病理性雜音。腹部柔軟,無壓痛及反跳痛,肝脾肋下未及,Murphy征陰性,肝腎區無叩擊痛,移動性濁音陰性。腸鳴音正常,無血管雜音。皮膚科檢查:軀干、雙上肢(圖3)、雙大腿皮膚彌漫性潮紅腫脹,干燥伴細小鱗屑,膚溫略高,四肢可見抓痕和少量血痂,局部可見色素沉著。
實驗室檢查:WBC 12.02×109/L,L% 78.0%,EOS 9.0%,EOS計數1.08×109/L。生化:尿素8.57 mmol/L,尿酸195.9 μmol/L,高密度脂蛋白膽固醇2.01 mmol/L,低密度脂蛋白膽固醇3.18 mmol/L,載脂蛋白A 11.67 g/L,乳酸脫氫酶357 U/L。尿常規、心肌酶、肌鈣蛋白I測定、輸血前篩查、ANA抗體譜11項、腫瘤指標均未見異常。糞常規寄生蟲蟲卵(-)。胸部CT:右肺中葉胸膜下小結節,建議隨訪復查;右肺中葉點狀鈣化灶。超聲心動圖:左心房擴大,室間隔高限,主動脈瓣關閉不全(輕度),二、三尖瓣關閉不全(輕度),左室舒張功能減退。前列腺彩超:前列腺結石。腎、輸尿管彩超未見異常。肝膽胰脾彩超:膽囊壁毛糙。T細胞亞群:CD4 322個/μL(低),CD8 146個/μL(低),CD3 526個/μL(低),CD4/CD8 2.21(正常)。提示細胞免疫低下,數值持續降低發生感染性疾病可能性升高。治療:熱毒寧20 mL/d,甲潑尼龍40 mg/d靜滴(6天后減量為30 mg/d,7天后減量為20 mg/d),環孢素軟膠囊75 mg/d,鹽酸左西替利嗪片、富馬酸酮替芬片,輔以護胃、補鈣、補鉀對癥治療,本院制劑黃芩油膏外用改善皮損等。中醫上予清熱涼血,利濕解毒湯劑口服。治療2周后皮疹明顯好轉出院。復查EOS計數、EOS百分比均正常。出院后甲潑尼龍逐漸減量,至今維持環孢素軟膠囊75 mg/d,甲潑尼龍片12 mg/d,同時口服中藥,回訪半年皮疹未發,控制良好。
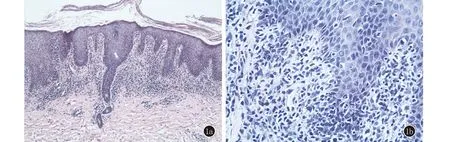
1a、1b:表皮角化不全,棘層增生,表皮突下延,表皮基底及真皮淺層小血管周圍淋巴、漿、單個核細胞浸潤(HE,×100;×400)
圖1紅皮型嗜酸性粒細胞增多性皮炎患者皮損組織病理
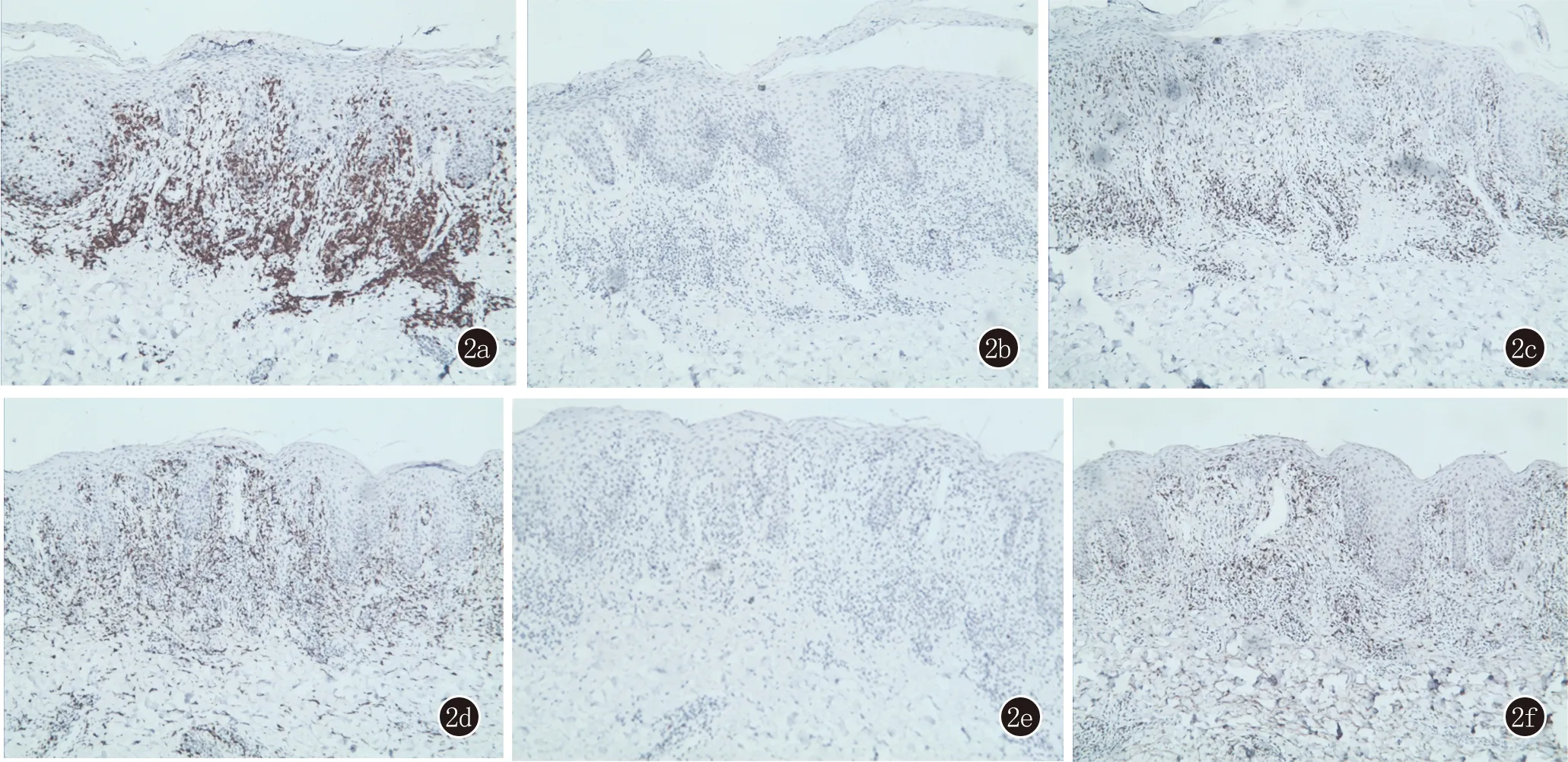
2a:CD3(+);2b:CD20(灶性+);2c:CD45RO(+);2d:CD68(局部+);2e:CD79a(灶性+);2f:lyso(局部+)
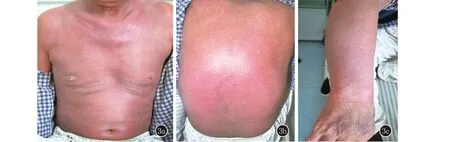
胸腹部、背部(3a、3b)及上肢(3c)皮膚彌漫性潮紅腫脹,干燥伴細小鱗屑,局部可見色素沉著
討論嗜酸性粒細胞增多性皮炎(hypereosinophilic dermatitis,HED)是以外周血和/或骨髓嗜酸性粒細胞持續增多、皮膚組織嗜酸性粒細胞浸潤為特征;屬于嗜酸性粒細胞增多綜合征(hypereosinophilic syndrome,HES)疾病譜的良性端,預后較好,HES疾病譜的惡性端是淋巴瘤甚至慢性嗜酸性粒細胞白血病。發病原因尚不明確,可能與超敏反應、自身免疫關系密切。HES可侵犯全身各個系統,造成靶組織、靶器官的嗜酸性粒細胞廣泛浸潤,包括心血管系統、呼吸系統、神經系統、消化道系統等,臨床表現多種多樣,可出現發熱乏力、咳嗽胸悶、頭暈癲癇、腹痛腹瀉、肝脾腫大等,但無明顯特異性。目前主流的分類方法將HES分為髓系增殖型HES(M-HES)、淋巴細胞型(L-HES),此外還包括家族型、重疊型、不確定型及伴隨型[1],L-HES通常以皮膚受累為主[2],故一般認為HED是淋巴細胞型HES。M-HES 患者主要特征為位于4號染色體的 FIP1L1-PDGFRA融合基因陽性,并出現各種染色體異常。此型皮膚黏膜均可受累,常伴多臟器損害,死亡的主要原因是心力衰竭,部分可發展為慢性嗜酸性粒細胞白血病,預后差。L-HES包括T淋巴細胞單克隆性增生和無T淋巴細胞單克隆性增生,以FIP1L1-PDGFRA融合基因陰性,具有表型為CD3-CD4+CD8-或CD3+CD4-CD8-、可產生大量IL-5的異常T淋巴細胞為特征[3-5]。TCR基因重排可見單克隆性表達。此型一般為良性進程,少數患者可發展為T細胞淋巴瘤。皮膚組織病理上HES的主要改變為真皮血管周圍明顯嗜酸性粒細胞及單一核細胞浸潤。但這種改變隨著取材標本部位的不同而具有差異性。
通常HED僅累及皮膚,無明顯內臟損害,好發于中老年男性,臨床特征為皮疹多形性、瘙癢性、易反復發作、可泛發全身。皮疹類型一般分為2種:常見型,紅斑、血管性水腫、丘疹、斑丘疹、斑塊、結節等;少見型,苔蘚樣變、紅皮型、水皰[6]、離心性環狀紅斑、血管炎等。臨床上容易誤診為濕疹、癢疹、蕁麻疹、特應性皮炎等。王媛等[7]對32例HED患者臨床分析中發現有9例皮疹表現為紅皮型。所以當紅皮病患者血嗜酸粒細胞明顯升高而又可排除結締組織病、寄生蟲感染、藥物過敏、腫瘤性疾病等原因引起的嗜酸粒細胞升高時,可以考慮是否為嗜酸性粒細胞增多癥。既往文獻報道中約60%的HES患者可發生心血管損害,高嗜酸性粒細胞心肌炎、高嗜酸性粒細胞心肌心內膜纖維化是HES患者死亡的主要原因[8]。張力等[9]回顧性分析30例HED患者臨床資料,結果顯示83.33%患者伴有LDH及a-羥丁酸脫羧酶升高。這提示我們對于HED患者應長期隨訪,患者宜適當加強本病意識。當心肌酶標志物異常時,在排除既往是否患有心臟疾病或其他原因引起的繼發性心肌受損后,應當考慮HSD是否向HES疾病譜另一端發展的可能。此時需要系統檢查排查疾病,臨床條件允許的情況下,除了再次骨髓活檢、皮膚活檢等常規檢查外,應當完善FIP1L1-PDGFRA融合基因檢測、染色體及TCR基因重排等檢查。
參考2012嗜酸粒細胞疾病和綜合征工作會議組對嗜酸性粒細胞增多癥(HE)提出的新共識[10],本例患者以反復發作的紅皮病為皮損表現,既往多次(間隔1個月)復查血象示EOS計數>1.5×109/L,骨髓活檢提示嗜酸性粒細胞增多癥,無明顯內臟受累表現,并且除外其他原因引起EOS增多所致的紅皮病,診斷符合紅皮型HED,由于經過治療,故本次入院時查EOS百分比、計數無明顯升高。第2次入住我科時一開始用甲潑尼龍80 mg/d靜滴1周,病情得以控制,破潰糜爛面愈合,后減量為60 mg/d,10天后皮疹仍消退不明顯,考慮不具備激素減量條件,且長期大劑量激素應用會出現廣泛的多系統不良反應,大大增加感染機會。查血漿皮質醇(8點)2.1 μg/dL,(16:00)2.8 μg/dL,(24點)2.00 μg/dL ;促腎上腺皮質激素(8點)0.17 pg/mL,(24點)0.01 pg/mL,根據皮質醇測定、促腎上腺皮質測定結果,提示PH軸抑制,為進一步控制病情,加用口服免疫抑制劑環孢素A 75 mg日2次,協同治療,同時防止激素減量過程中病情的反復。環孢素A是非骨髓毒性的免疫抑制劑[11]。對于骨髓儲備功能較差的紅皮型HED,可以考慮糖皮質激素聯合環孢素A治療。用藥過程中注意定期監測血藥濃度、血壓及電解質變化、肝腎功能、血常規、血脂、尿酸等。后面幾次復發入住我科期間治療方案均為甲潑尼龍40~80 mg/d靜滴聯合環孢素A 75~150 mg/d口服,病情控制后激素逐漸減量改為小劑量激素聯合環孢素口服維持治療。
HES治療方案應根據其分型而定,M-HES首選藥物為酪氨酸激酶抑制劑甲磺酸伊馬替尼;而HED的一線藥物是糖皮質激素,它通過抑制各類促嗜酸性粒細胞成熟和活化的細胞因子和趨化因子(IL5,IL3,GM-CSF) 的作用誘發嗜酸性粒細胞的程序性凋亡[12]。細胞毒藥物如雷公藤、環磷酰胺、甲氨蝶呤、環孢素A等是二線藥物,此外還有干擾素、肌注卡介菌多糖核酸、光療等。中、小劑量糖皮質激素單用或聯合免疫抑制劑,通過逐漸減量,并予小劑量糖皮質激素維持,是目前治療 HED 最有效的治療方案[9]。由于本病的好發年齡為中老年男性,許多患者合并有高血壓、糖尿病等慢性病,長期服用糖皮質激素會導致血壓、血糖升高,加重或誘發感染、胃黏膜損傷、骨質疏松、股骨頭壞死等副作用,故患有基礎疾病的人群更應密切關注血壓、血糖,必要時加用降壓藥,預防不良事件的發生發展。此外,進一步研究嗜酸性粒細胞增多的病因、發病機制,從而尋找更安全有效的藥物,仍是醫療工作者需要面臨的難題。

