胸腔鏡下肺楔形切除與解剖性肺段切除對IA1期非小細胞肺癌治療效果的比較
劉昌平,鐘一鳴
(江油市人民醫院,四川 綿陽 621700)
肺癌目前已成為嚴重威脅人類健康的惡性腫瘤之一,其發病率與死亡率逐年增高[1-2],其中非小細胞肺癌(non-small cell lung cancer,NSCLC)是肺癌最常見的病理類型。隨著高分辨率CT的普及與人們健康體檢意識的提高,越來越多的早期NSCLC被發現。傳統的早期NSCLC手術方式為肺葉切除及系統性淋巴結清掃[3]。近年來,多項研究[4-5]表明胸腔鏡下肺段切除較肺葉切除有相似的預后,且創傷更小,越來越多的胸外科醫生青睞于應用解剖性肺段切除治療早期NSCLC。但這也引起我們的思考:對于某個階段的早期NSCLC,肺楔形切除是否即可達到與解剖性肺段切除相似的預后。本文就胸腔鏡下肺楔形切除與解剖性肺段切除對IA1期NSCLC治療效果進行比較分析。現報告如下。
1 資料與方法
1.1 一般資料
選取2015年1月至2018年5月在江油市人民醫院胸外科接受胸腔鏡下肺楔形切除或解剖性肺段切除、術后病理分期不超過IA1期(IASLC第八版TNM分期[6])的NSCLC患者94例,根據手術方式分為楔形切除組(n=50)與肺段切除組(n=44)。 納入標準:(1)術前胸部CT檢查為周圍型單發肺結節;(2)腫瘤直徑≤1 cm;(3)肺部結節磨玻璃成分成份>50%的或隨訪腫瘤倍增時間≥400 d;(4)患者既往無其他惡性腫瘤病史,無長期服用免疫抑制劑病史。排除標準:(1)術后病理不為NSCLC的患者;(2)術后病理證實分期>pT1aN0M0 IA1期(IASLC第八版TNM分期)的NSCLC的患者;(3)意識障礙或精神異常,無法配合治療者;(4)術中中轉開胸患者;(5)術后接受化療患者。患者一般資料比較見表1。兩組患者年齡、性別、吸煙史及肺部腫瘤直徑比較,差異均無統計學意義(P>0.05),具有可比性。

表1 兩組患者的一般資料比較
1.2 手術方式
1.2.1 體位與切口選擇 胸腔鏡下肺楔形切除與解剖性肺段切除均采用相同的體位和手術切口。全麻插管后,選擇健側臥位,腋下墊枕或加用折刀體位,術側上臂固定于頭側,取腋中線第7肋間切口,長約1~1.5 cm,單肺通氣,置入胸腔鏡,在胸腔鏡監視下于腋前線第4或第5肋間作2~3 cm切口作為主操作孔,選擇肩胛下角線第8或第9肋間作1.5 cm切口作為副操作孔,用超聲刀及電凝鉤分離胸腔黏連。
1.2.2 肺楔形切除術 首先對病灶所在肺葉進行探查,距離病灶邊緣≥2 cm或>腫瘤直徑行楔形切除肺結節,切除物送術中快速冰凍病理檢查,若病理回報為惡性腫瘤,進一步行N1、N2淋巴結采樣,其中包括至少3個縱膈引流區淋巴結[7]。如采樣淋巴結冰凍結果陰性,常規處理后結束手術;如采樣淋巴結任意一組陽性,進一步行肺葉切除及系統性淋巴結清掃,患者出組。止血,沖洗胸腔,確定無肺部漏氣及活動性出血后留置胸引管、關胸。
1.2.3 解剖性肺段切除術 若術前影像學顯示病灶位置較深,或術中無法直接用手指探及,則直接行解剖性肺段切除術。若病變部位靠近肺表面,手指可探查觸及,則先行肺楔形切除術中送快速冰凍病理檢查;若病理回報為惡性腫瘤,再行解剖性肺段切除術.對不同肺段。手術操作流程略有不同:一般情況下,先游離靜脈切斷目標段靜脈,在進一步游離切斷肺段動脈及段支氣管,采樣膨脹-萎陷法及段間靜脈辨認段間平面[8],沿段間平面切除該目標靶段,注意病灶離切緣≥2 cm或≥腫瘤直徑,必要時可犧牲臨近肺段少量肺組織以保證切緣腫瘤組織陰性。切除標本送快速冰凍病理檢查,若病理回報為惡性腫瘤,且切緣陰性;進一步行N1、N2淋巴結采樣,其中包括至少3個縱膈引流區淋巴結。如采樣淋巴結冰凍結果陰性,常規處理后結束手術;如采樣淋巴結任意一組陽性,進一步行肺葉切除及系統性淋巴結清掃,患者出組;止血,沖洗胸腔,確定無肺部漏氣及活動性出血后留置胸引管、關胸。
1.3 觀察指標
分析兩組的手術時間、術中出血量、術后引流量、術后住院時間、術后并發癥、術后局部復發率、累積生存率等,并進行統計學分析。
1.4 統計學分析
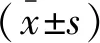
2 結果
2.1 兩組患者治療情況比較
肺楔形切除組患者手術時間、術中出血量、術后住院時間均小于肺段切除組患者,差異均具有統計學意義(P<0.01)。見表2。
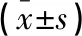
表2 兩組患者的治療情況比較
2.2 兩組患者術后并發癥比較
肺楔形切除組患者術后肺漏氣的發生率少于肺段切除組,差異具有統計學意義(P<0.05),肺楔形切除組術后肺不張、心律失常的發生率也少于肺段切除組,但差異無統計學意義(P>0.05)。見表3。

表3 兩組患者的術后并發癥比較[n(%)]
2.3 預后情況
12~24個月隨訪期間,肺楔形切除組內局部復發1例(2.00%),肺段切除組無局部復發患者,組間比較差異無統計學意義(χ2=0.89,P=0.35)。肺楔形切除組和肺段切除組患者均無死亡,兩組患者累積生存率100%。
3 討論
隨著外科微創理念逐步深入人心,胸外科醫生們越來越注重在根治性切除肺癌的同時設法保留更多健康肺組織[9-10]。理論上,胸腔鏡下肺楔形切除較胸腔鏡下解剖性肺段切除保留了更多肺功能,同時手術時間及創傷更少,這對心肺功能不全的患者尤為重要,也為術后局部腫瘤復發或其他部位新發肺結節的患者提供類良好的二次手術機會。
已有部分研究[11-12]報道胸腔鏡下解剖性肺段切除較肺楔形切除預后更優,但并未對腫瘤直徑進行細分并進一步分析。本研究根據最新的肺癌TNM分期,選擇了腫瘤直徑≤1 cm的IA1期病例作為研究對象,探究在早期肺癌中的某個階段,肺楔形切除是否即可達到肺癌根治性切除的效果。收集數據中提示,二者12~24個月內局部復發率和累積生存率無差異。提示胸腔鏡下肺楔形切除的短期預后與解剖性肺段切除相似。術后,局部肺內淋巴結肺楔形切除組的手術時間、術中出血量、術后住院時間均小于肺段切除組,認為這受術者操作熟練度影響,隨著操作者熟練度提高,解剖性肺段切除的手術時間、出血量等可能會逐步減少。術后并發癥的對比分析提示肺楔形切除組術后肺漏氣的發生率低于肺段切除組,考慮到胸腔鏡下解剖性肺段切除手術步驟較楔形切除繁瑣困難,術中牽拉暴露等操作可能損傷其他健康肺組織造成術后漏氣,肺段切除時處理段間平面也增加了手術后漏氣的可能[13],但隨著術者操作熟練度的提升和手術時間縮短,此并發癥發生率可進一步降低。
肺楔形切除組鐘存在1例局部復發患者,本例患者于隨訪第20個月出現手術區域實性結節,且雙肺出現多發磨玻璃結節,第23個月復查手術區域實性結節有所增大,PET/CT提示惡性病變。分析原因:(1)肺楔形切除較肺段切除對肺內淋巴結清掃更不徹底,術后淋巴結轉移存在假陰性,即本例患者真實分期可能大于IA1期;(2)患者隨訪期間出現雙肺多發磨玻璃結節,不除外局部原發肺癌。
本研究提示胸腔鏡下肺楔形切除與解剖性肺段切除治療IA1期NSCLC有相似短期預后,但肺楔形切除具有手術時間短、術中出血少、術后住院時間短、術后并發癥少的優勢,對于心肺功能差、需多次手術的NSCLC患者具有更實際意義。但其長期預后需更大樣本量、更長隨訪時間的隨機對照研究進一步證實。

