骨科手術部位金黃色葡萄球菌感染及耐藥性變化
宋彥 應弋陽 李炎
骨科住院患者大多需要手術治療,較多為開放性損傷,且急診手術較多,因此骨科住院患者手術部位感染(surgical site infection,SSI)在臨床中并不少見,為骨科術后較為嚴重的并發癥之一,一旦感染常需要長期、反復住院,多次手術,不但增加患者的治療費用與心理負擔,還會嚴重影響患者預后。金黃色葡萄球菌(SA)作為骨科手術部位感染的常見致病菌,其致病力強,傳播速度快,常呈現多重耐藥,給臨床治療帶來較大難題。為了解骨科患者SA感染的情況,作者現對骨科手術患者的金黃色葡萄球菌的分離結果及耐藥性進行對比性分析。現報道如下。
1 資料與方法
1.1 菌株來源 來自本院骨科2015年1月至2017年12月住院患者手術部位細菌學檢驗標本(創面分泌物、穿刺液、壞死組織等)。其中骨科住院患者手術部位分離病原菌分別為192、214和313株(剔除重復菌株)。質控菌株為金黃色葡萄球菌ATCC29213,購自衛生部臨床檢驗中心。
1.2 儀器與試劑 法國生物梅里埃公司VITEK 2微生物全自動細菌鑒定分析儀(簡稱VITEK 2)及配套卡片;分離培養基哥倫比亞血瓊脂平板和藥敏培養基MH瓊脂平板為法國生物梅里埃公司生產;藥敏紙片為英國Oxiod公司生產。
1.3 細菌鑒定及藥敏 常規培養分純后用VITEK 2和配套革蘭氏陽性卡片進行鑒定及藥敏試驗。耐甲氧西林金黃色葡萄球菌(MRSA)菌株的篩選利用VITEK 2自動檢測并經頭孢西丁紙片法確認,判斷標準參考CLSI2015標準。
1.4 統計學方法 采用SPSS 18. 0 統計軟件。三年間細菌的分離率和耐藥率的比較采用χ2檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 三年間SA和MRSA分離情況比較 見表1。
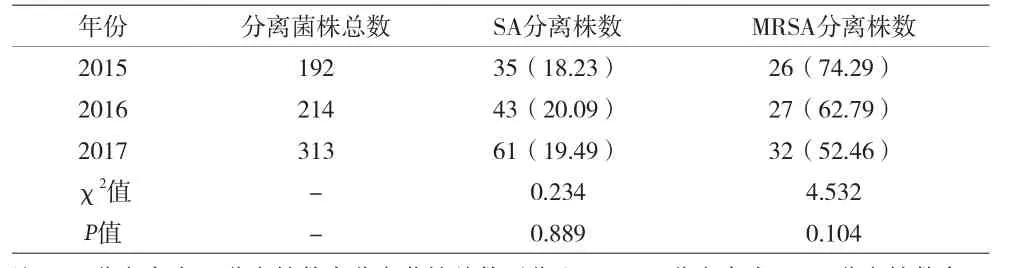
表1 三年間SA和MRSA分離情況比較[n(%)]
2.2 三年間SA對抗菌藥物耐藥率比較 見表2。
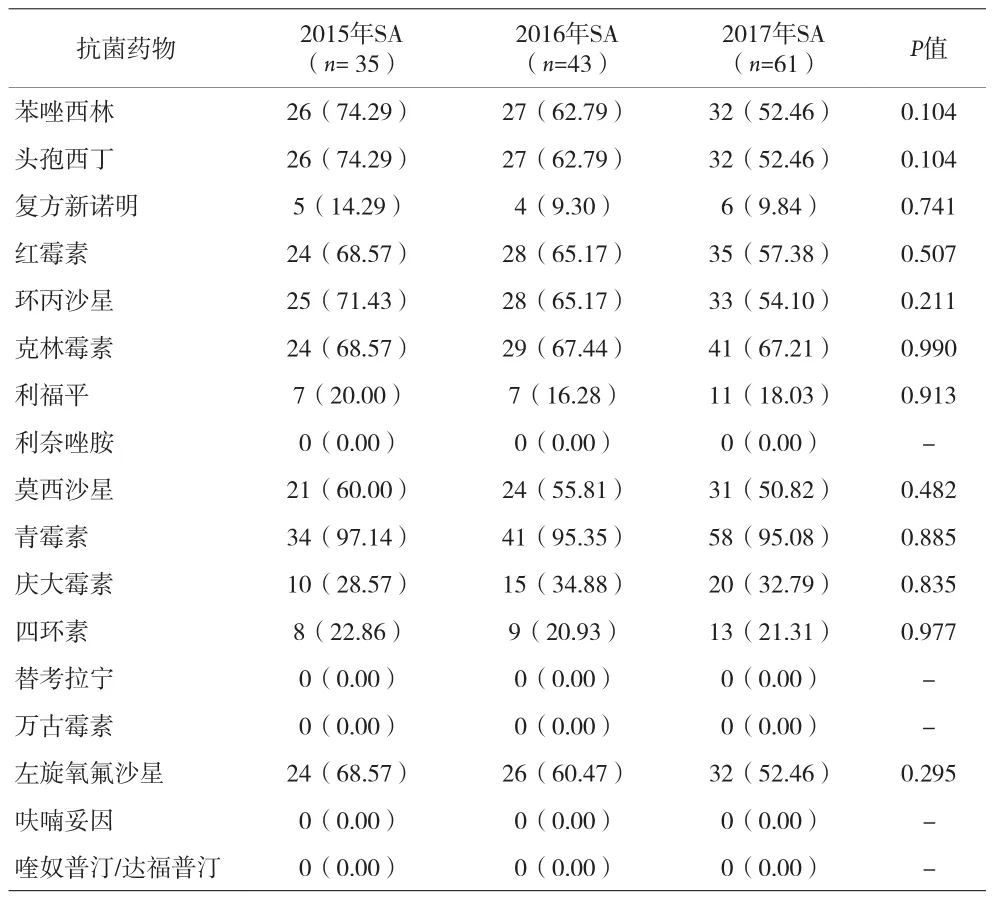
表2 三年間SA對抗菌藥物耐藥率比較[n(%)]
3 討論
SSI是骨科手術后最常見且較嚴重的并發癥之一,不但會增加患者的住院時間、手術次數及醫療費用,嚴重者還會影響患者肢體功能,增加致殘率與病死率。目前已經明確,引起骨科SSI有多方面的因素,且較復雜。其中,SA引起的骨科SSI是臨床最常見的原因。SA廣泛存在于自然界和人體的皮膚、鼻咽、腸道中,是發生院內感染的重要致病菌,當機體抵抗力低下時,容易經破損的皮膚和黏膜侵入人體,同時也常引起骨科手術部位的感染和定植。近年來隨著青霉素類、氨基糖苷類、喹諾酮類、四環素類、大環內酯類藥物在臨床的廣泛應用,一度造成了SA耐藥率的急劇增高[1],甚至還出現了耐萬古霉素SA[2-3],給臨床抗感染的治療帶來了較多困難。
本資料對醫院骨科過去三年SA引起的SSI,以及病原菌的檢出和耐藥情況進行了回顧性分析,結果顯示三年間SA的檢出并無明顯差異,但MRSA的構成呈下降趨勢,這也和全國耐藥檢測網監測的結果一致[4],這可能是由于近年來全國各醫療機構對細菌耐藥問題日趨重視,隨著手衛生、MRSA患者隔離以及抗菌藥物合理化使用等措施的實施和推廣,MRSA的防控也逐見成效。但骨科SSI 52.5%的MRSA檢出率還是明顯高出35.3%的全國平均水平[4],究其原因可能與骨科手術和病原菌的特點相關。骨科手術類型較多,如內固定、置換術和人工假肢等的使用會增加以SA為代表的菌群的反復感染和定植,從而在抗菌藥物反復使用的過程中不斷的誘發其耐藥性產生。此外,三年間SA對苯唑西林、環丙沙星、莫西沙星和左氧氟沙星的耐藥率雖呈下降趨勢,但其耐藥率仍>50%,因而在懷疑SA引起的SSI時,經驗性的選擇此類抗菌藥物,仍存在較大的治療失敗的風險。但萬古霉素、替考拉寧、利奈唑胺等具有較高敏感性,可以作為嚴重和反復感染的選擇用藥。
SA為代表的細菌易粘附于內置物上形成生物膜[5],因生物膜內低氧和低葡萄糖,細菌在生物膜內處于靜止期。體外研究[6]發現,大多數細菌具有最小殺菌濃度(MBC),MBC在靜止期較對數形成期明顯升高。高的靜態MBC和粘附于表面的細菌效果不佳,預示抗菌藥物治療內置物相關感染的失敗。此外,一些細菌亞群聚居于生物膜深部,此時細菌的代謝可降至一定水平,導致抗菌藥物療效甚微。治療內置物相關感染應考慮到此類特點。內置物周圍感染抗菌藥物治療方法已有報道[7]。若充分考慮到導致治療失敗的各種因素,使用合適的抗菌藥物,很多內置物周圍感染可以在保留內置物的情況下治愈。
綜上所述,骨科手術部位感染的影響因素多且復雜,以SA為代表細菌對各種抗菌藥物的敏感性有較大差異,應該嚴格按照細菌培養和藥敏試驗結果應用抗菌藥物,動態觀察細菌分布及耐藥率的變遷,為臨床治療和經驗性用藥提供依據。此外,臨床SA具有較高的同源性[5]。因此,應該繼續嚴格執行洗手、消毒和隔離等基本制度,以預防和減少交叉感染的出現。

