腹腔鏡與開腹經腹會陰直腸切除術治療低位直腸癌的療效對比:基于傾向性匹配分析
徐逸昕,奚誠,葉年源,王一波
(江蘇大學附屬武進醫院普外科,江蘇常州213002)
隨著全直腸系膜切除和放化療技術的發展,直腸癌患者的復發情況以及長期生存得以明顯改善[1]。Jacob等[2]在 1991年報道了首例腹腔鏡下結腸切除術。隨著器械設備和手術技術的發展,腹腔鏡結直腸切除手術得以迅猛發展,并且有著與開腹手術相同的遠期效果以及更好的近期療效[3]。目前,研究微創(腹腔鏡、機器人)與開腹治療結直腸癌療效對比的隨機對照試驗很多,但是微創手術治療低位直腸癌能否表現出同樣的優勢仍未明確。故本研究擬對比腹腔鏡與開腹手術治療低位直腸癌患者的療效。
1 對象與方法
1.1 研究對象
通過檢索電子病歷,收集2012年1月至2016年1月于江蘇大學附屬武進醫院普外科連續就診的低位直腸癌患者的臨床病理資料,共158例。其中,男90例,女68例,年齡38~90(65.0±11.5)歲。
1.2 入組標準和排除標準
入組標準:初發低位直腸癌;接受手術治療,術式為腹腔鏡或者開腹經腹會陰直腸切除術(abdominoperineal resection,APR);術前有完整的檢驗、檢查資料。排除標準:術前行新輔助放療、化療;術前行內鏡治療;同期行其他手術;腹腔鏡手術術中中轉開腹;資料缺失。
1.3 手術方法
所有患者在術前均行常規術前檢查,排除手術禁忌。腸鏡以及病理明確診斷低位直腸癌者,必須行APR。手術均按照全直腸系膜切除原則[4]進行:①近端游離至腸系膜下動靜脈根部,于根部離斷腸系膜下動脈并鉗夾離斷下靜脈,清掃該處淋巴脂肪組織;遠端切開腹膜返折,切斷并結扎左右側韌帶,游離直腸癌至膀胱精囊腺后方至肛提肌表面;于乙狀結腸中段切斷腸管,于腸旁血管弓下方切除腸系膜。②左下腹壁切除直徑3 cm的圓形皮膚、皮下組織,十字切開腹外斜肌腱膜,分離腹內斜肌、腹橫肌于腹膜外分離隧道到達側腹壁,將近端結腸鉗出,并固定于腹壁形成人工肛門。③環形荷包縫合閉鎖肛門,距離肛緣3 cm做梭形切口,切開皮膚、皮下組織,注意保護尿道(陰道),切除肛管及坐骨肛管間隙內淋巴脂肪組織、肛提肌及直腸,取出標本。④沖洗、檢查腹腔,放置腹腔引流管,依次關閉腹部以及會陰部切口。
1.4 觀察指標
患者臨床病理特征、手術相關情況:年齡,性別,體質量指數,合并癥指數,腹部手術史,其他腫瘤病史,各項檢驗指標(血紅蛋白、中性粒細胞、淋巴細胞、白蛋白以及球蛋白),腫瘤相關特征(位置、直徑、TNM分期、分化程度以及神經脈管侵犯情況),手術時間,出血量,術前術后檢驗結果差值、術后并發癥情況及嚴重程度,術后輸血情況,經口進食恢復時間,術后住院時間以及住院總費用。
1.5 判定標準
腫瘤分期:使用 AJCC/UICC第七版直腸癌TNM分期系統[5]。術后并發癥嚴重程度按照Clavien-Dindo分級標準[6]進行劃分:Ⅰ級為僅需要簡單藥物或者物理治療;Ⅱ級為需要特殊藥物(特殊抗菌藥物、營養支持制劑和其他),輸血和完全腸外營養;Ⅲ級為產生并發癥需要有創治療介入(手術、介入栓塞和內鏡等);Ⅳ級為病情危重、需要進入ICU監護;Ⅴ級為并發癥導致患者死亡;≥Ⅲ級定義為嚴重并發癥。
1.6 隨訪
隨訪頻率:術后第1年每3個月復查1次,第2年每4個月復查1次,此后每半年復查1次。隨訪內容:癌胚抗原、糖類抗原19-9、腸鏡、腹部B超以及全腹部增強CT。隨訪截止時間為2017年1月。中位隨訪時間29個月(12~60個月)。
1.7 傾向性匹配分析
使用Logistic回歸分析和以下協變量進行傾向性匹配分析:年齡、性別、體質量指數、術后化療情況、術前合并癥情況、各項血液檢驗結果和腫瘤病理情況。
1.8 統計學方法
采用SPSS 22.0統計軟件進行傾向性匹配和數據分析。計量數據符合正態分布以均數±標準差(±s)表示,兩組間比較采用獨立樣本t檢驗;計數資料組間比較采用χ2檢驗或者Fisher精確檢驗;等級資料組間比較采用Mann-WhitneyU檢驗;Kaplan-Meier法繪制生存曲線并采用Log-rank檢驗比較預后差異。
2 結果
2.1 基線資料
共有158例患者符合入組條件(腹腔鏡組84例,開腹組74例)。按照入組與排除標準進行篩選:腹腔鏡組排除者中,術前行ESD 2例,新輔助放療、化療2例,同期行其他手術3例,資料缺失2例;開腹組排除者中,術前行ESD 3例,新輔助放療、化療1例,同期行其他手術4例,資料缺失2例。最終,腹腔鏡組符合條件75例,開腹組符合條件64例。
傾向性匹配分析前,兩組血紅蛋白水平(P=0.007)、白蛋白水平(P=0.011)和腫瘤位置(P=0.002)差異存在統計學意義。傾向性匹配分析后,兩組各項臨床病理特征差異均無統計學意義(P>0.05)。見表1。
2.2 兩組患者生存情況比較
兩組患者均得到完全隨訪,經Log-rank檢驗提示,術后3年生存率分別為腹腔鏡組76.5%,開腹組75.1%,差異無統計學意義(P>0.05)。見圖1。
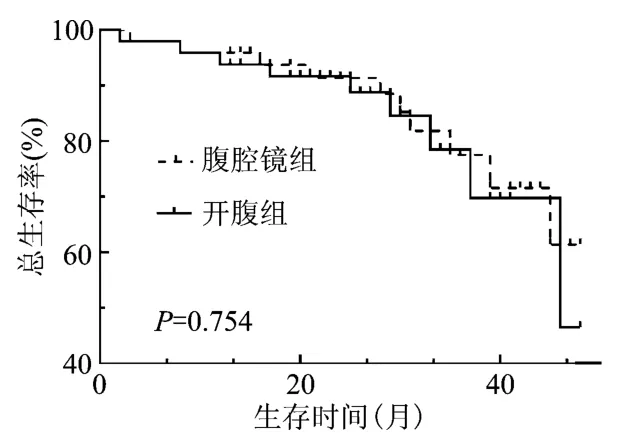
圖1 兩組患者的生存情況對比
2.3 兩組患者手術情況以及術后臨床病理特征比較
與開腹組相比,腹腔鏡組術中出血量較少,手術后血紅蛋白、白蛋白消耗更少,術后并發癥中腹腔感染、切口感染率更低,并發癥程度較輕,恢復經口進食時間和術后住院時間更短,但住院費用較高(P均<0.05)。兩組手術方式清掃的淋巴結數目差異無統計學意義(P>0.05)。見表2。
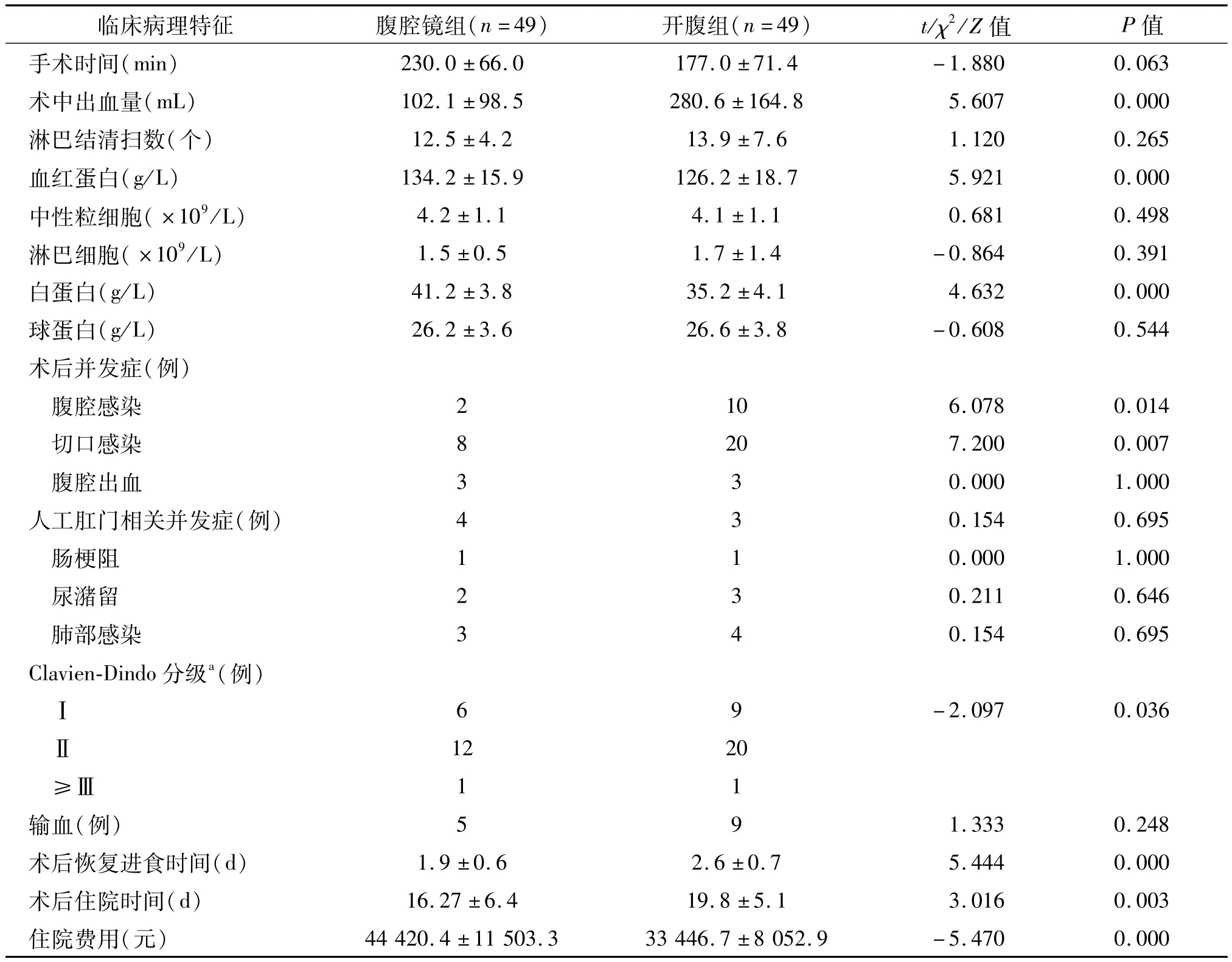
表2 兩組患者術后臨床特征對比
3 討論
既往對于直腸癌根治術的回顧性分析只是簡單地對比實驗組與對照組患者的術前資料,便得出基本資料無明顯差異;繼而通過比較兩組患者的術后資料,便得出兩種手術方法孰優孰劣的結論,這樣的結論是有失偏頗的。Honda等[7]最近也闡述了該觀點:在進行兩種治療方式的回顧性分析對比前,需要盡量多地將患者的術前資料放入傾向性匹配分析模型中(包括術前檢驗、檢查資料以及腫瘤分期情況等),排除兩組患者的差異,然后再進行患者預后的對比;這樣使得入組人群的基線資料更加平衡,從而減少了對結果的干擾。
我們發現除去一些基線資料,以下問題依然會影響患者預后,需要在進行研究前排除入組之間的差異:①貧血、營養狀態、機體炎癥狀態,這是由于患者的整體狀況可能會影響手術醫師的術式選擇。有報道稱,行微創直腸切除術的患者整體營養狀態要比開腹手術患者好[8];②已明確的可以預測患者生存情況的各種預后指數[9];③腫瘤的病理學特征[10]。
隨機對照研究證實,與開腹手術相比,腹腔鏡直腸切除術的短期療效更加優異[11]。本研究也發現腹腔鏡組術后并發癥嚴重程度較輕,術后恢復進食時間和住院時間較短。在進行術后并發癥亞組分析時,腹腔鏡組腹腔、切口感染率較低,分析原因如下:①腹腔鏡設備可以有助于手術醫生更加仔細地辨認盆腔解剖結構;開腹手術由于盆腔位置低、空間狹窄,手術醫生以及助手往往無法很好地解剖。②微創手術切口小,腹腔顯露時間短,患者的內環境受影響程度低;③腹腔鏡手術中超聲刀的止血效果較一般電刀要好。手術中的出血量與術后輸血往往與患者的術后并發癥發生率密切相關[12]。本研究同樣發現腹腔鏡組的出血量較少,血紅蛋白、球蛋白和白蛋白消耗更低,并發癥也較開腹組少。手術清掃淋巴結數目是評價手術效果的重要標準,并且與患者的長期生存密切相關[13]。本研究中腹腔鏡組與開腹組淋巴結清掃數目差異無統計學意義,同時兩組患者的長期預后也無明顯差異。
腹腔鏡手術療效優異,但住院費用較高。本研究中腹腔鏡組住院費用明顯高于開腹組。研究證實,行腹腔鏡直腸手術患者的近期與中期費用負擔較高[14]。由于我國的醫療保險并不是全額支付,所以在選擇手術方式時也必須將經濟因素納入考慮范圍,不能一味追求技術的先進性。
本次研究雖然運用傾向性匹配分析將兩組患者的術前差異縮減至最小,但是證據強度仍然無法與隨機對照研究相比。且本次研究為單中心,樣本量偏少,可能存在統計學誤差。所以,下一步應開展大規模多中心隨機對照研究。
綜上所述,腹腔鏡經腹會陰直腸切除術與開腹手術相比,在近期療效方面有較大優勢,但醫療費用較高,在為低位直腸癌患者選擇手術方式時需要制定個體化方案。

