亞硫酸二甲酯對銅腐蝕性能的研究
(連云港堿業有限公司,江蘇 連云港 222042)
銅在有色金屬中產量排名第二,被廣泛應用于各行各業,其優點是質地堅硬,不易腐蝕,且耐高溫、耐高壓,被認為是耐腐蝕的金屬之一。但是實際情況中,由于一些苛刻的使用條件以及長時間使用,銅也不可避免地會被腐蝕,例如銅在加工過程中會接觸某些有機酯,而酯類中的硫元素會明顯侵蝕銅表面形成銅綠,嚴重影響銅的性能和美觀,因此解決銅的腐蝕問題已經成為國內外學者研究的重點。馬玉紅[1]等人研究指出烴類物質并不會對銅產生腐蝕,其他非烴類物質如酸、硫化物以及水在許多過程中不可避免地會腐蝕銅。王吉會[2]研究表明S2-和NaCl的混合介質對銅有一定的腐蝕行為,其中S2-通過改變銅的表面結構從而能夠加劇腐蝕。Brumis V[3]和K. P. FitzGerald[4]的研究表明銅在SO2的作用下會生成銅綠,生成的銅綠會轉化成(Cu4SO4(OH)6)堿式硫酸銅,其中內層的Cu2O和水層也會反應成堿性硫酸銅。Aastrup T[5]和Zakipou[6]的研究表明強氧化力的O3也會導致SO2和NO2的協同反應,因此在SO2和NO2的氣氛中形成的酸會嚴重侵蝕銅的表面。
本文重點研究銅在生產和使用過程中存在的腐蝕行為,其中亞硫酸二甲酯的成分和結構類似于腐蝕銅的有機酯、潤滑油等物質,且含有硫結構的亞硫酸二甲酯對銅有一定的侵蝕能力,故選取將銅片浸泡在亞硫酸二甲酯水解溶液中,并觀察其腐蝕現象。最后通過光學顯微鏡、掃描電鏡SEM、能譜EDS現代分析測試技術獲取其微觀的腐蝕形貌以及腐蝕區域的元素組成,對銅在不同酸堿度溶液中的腐蝕性能進一步分析研究,探討銅的腐蝕機理和腐蝕性能。
1 試驗部分
1.1 試驗原料
本試驗所采用的原材料為99.97 wt%的商業高純紫銅,銅板紫銅呈磚紅色,其物理性能見表1;亞硫酸二甲酯無色透明液體,分子式是C2H6O3S,99%分析純,廠家上海阿拉丁生化科技股份有限公司,亞硫酸二甲酯溶解于NaOH水溶液中,使其反應生成Na2SO4和Na2SO3,其性能見表2;助劑:NaOH,分析純,上海化學試劑有限公司;有機溶劑:無水乙醇,分析純,上海迪凱化學試劑有限公司。

表1 銅的主要物理性能
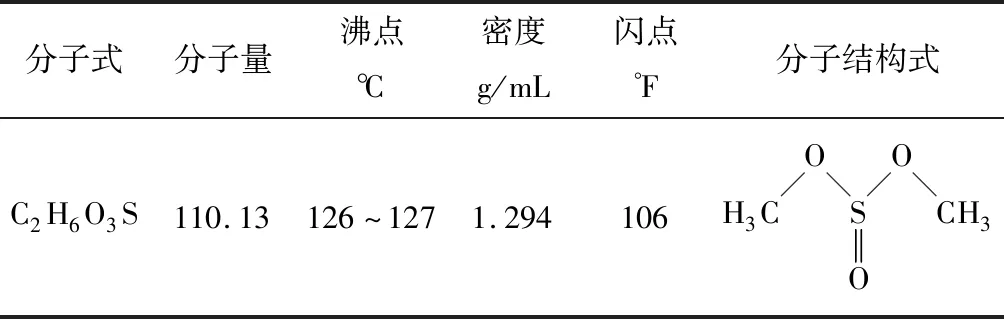
表2 亞硫酸二甲酯的主要物理性能
1.2 試驗制備工藝和方法
1.2.1 水解溶液制備
在圓底燒瓶(如圖1)中加入10 mL亞硫酸二甲酯和10 mL NaOH(0.5 mol/L)水溶液,連通冷凝管及冷凝裝置,冷凝管上端用氣球密封,防止氣體泄漏,利用調溫電熱器加熱,加熱溫度控制在70~100 ℃,加熱約2 h后冷卻至室溫。
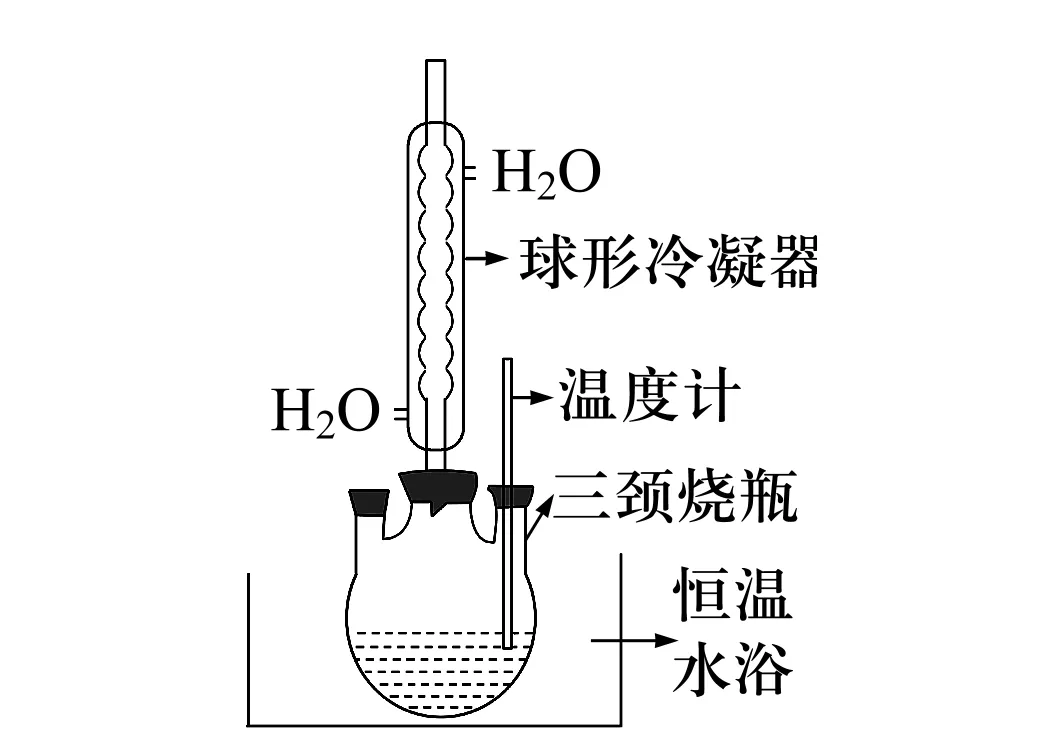
圖1 制備水解溶液裝置圖
1.2.2 試樣銅制備
線切割截取8×8 mm的紫銅,用鑲嵌機進行鑲嵌,利用600~1 200目的砂紙在打磨機上打磨,拋光機拋光至鏡面。
1.2.3 試樣SEM觀察
試驗采用日本電子公司生產的JSM-5900型掃描電鏡進行顯微觀察,通過SEM觀察樣品的產物和形貌。掃描電壓為15 kV,分辨率為3~6 nm。
1.2.4 試樣X-射線衍射儀分析
采用美國熱電公司ARLX′TRA型X射線衍射儀。儀器的技術指標及性能特點為:2.2 kW,Cu Kα靶、步進0.02°。儀器工作參數:管電壓45 kV,管電流30 mA。掃描速率為10°/min。
1.3 試驗方案
試驗是將銅片按標準制樣,進行打磨、拋光,將制得的樣品放入到亞硫酸二甲酯的水解溶液中進行浸泡,利用光學顯微鏡OM、掃描電鏡SEM觀察其腐蝕形貌,通過能譜EDS分析腐蝕區腐蝕產物的成分,對其在不同酸堿度溶液中的腐蝕性能進一步分析研究,如圖2。
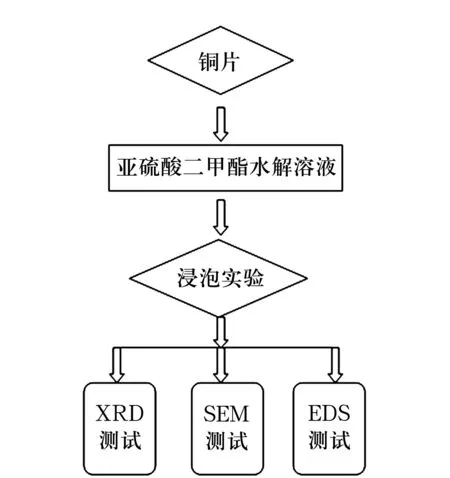
圖2 試驗過程示意圖
其中腐蝕介質為制備得到的水解溶液,將制備的銅樣品放入水浴鍋中進行熱循環浸泡試驗(40 ℃恒溫加熱16 h、25 ℃恒溫加熱8 h),浸泡20 d后取出紫銅試樣,利用用光學顯微鏡OM觀察和掃描電鏡SEM觀察其腐蝕形貌,利用能譜EDS分析腐蝕產物的成分。
2 結果與討論
2.1 腐蝕產物性能與表征
通過上述試驗工藝和方法,將銅片浸泡在不同酸堿度亞硫酸二甲酯水解溶液中,15 d的腐蝕形貌如光學顯微鏡圖3和圖4所示。

圖3 銅片在堿性水解溶液中的腐蝕圖
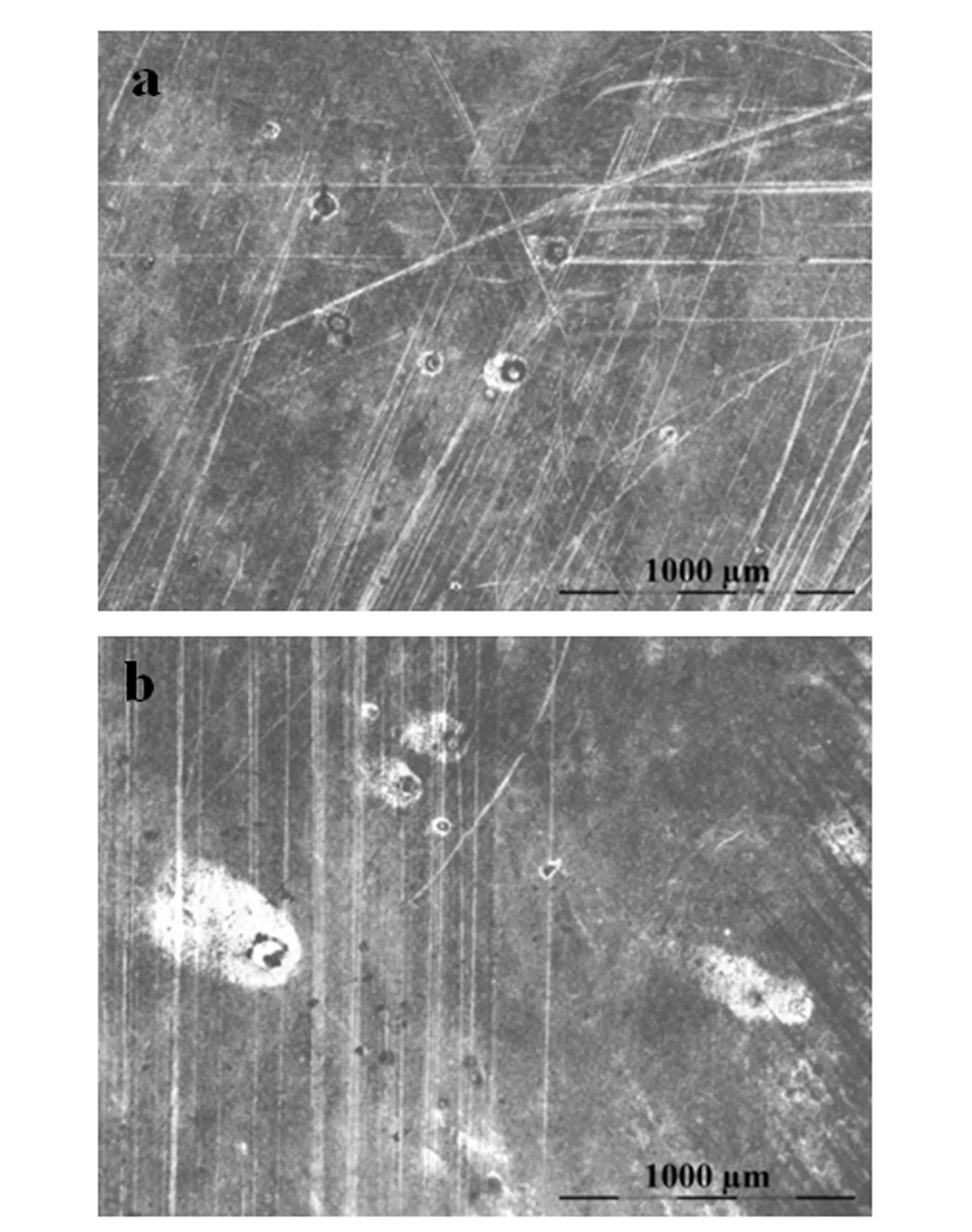
圖4 銅片在中性水解溶液中的腐蝕圖
通過圖3(a)中可以明顯觀察到銅片表面中局部腐蝕區域且顏色變深,同時在圖3(b)也可以觀察到銅片腐蝕面積增加,其腐蝕趨勢是愈加密集且右半部分中變色更加明顯,這表明堿性亞硫酸二甲酯對銅有一定的侵蝕能力,對比圖3(a)中閉合環狀的腐蝕痕跡和圖3(b)自上而下的痕跡,這說明銅在該溶液中的腐蝕主要以點蝕和局部腐蝕為主,且隨著點、線延續腐蝕區域和腐蝕產物也會逐漸增加,而銅片在使用過程中受到的腐蝕經常是雜亂無章的,見圖4。
通過圖4可以觀察到:中性條件下亞硫酸二甲酯腐蝕能力高于堿性條件,具體表現在中性條件下銅片表面腐蝕區域更嚴重范圍更廣。從圖4可以看到中性溶液的腐蝕表面有較多的點、線,表面腐蝕嚴重,開合環狀的腐蝕痕跡無規律的分布在銅的表面,腐蝕形貌更加明顯,同時在腐蝕區域會觀察到銅表面會產生其他顏色腐蝕物。
2.2 XRD分析
將銅片浸泡在不同酸堿度亞硫酸二甲酯水解溶液中15 d和20 d,得出XRD圖譜見圖5和圖6。
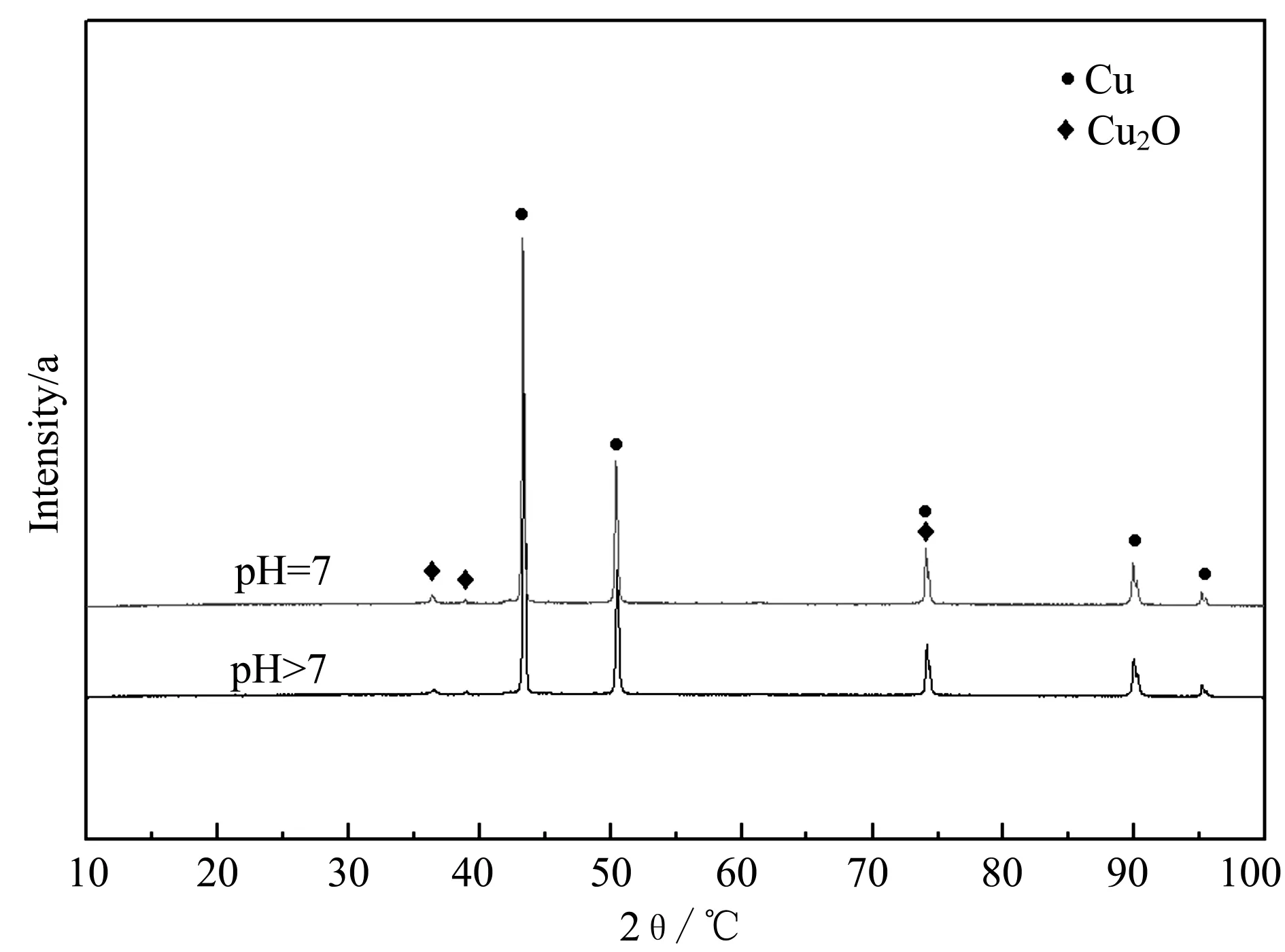
圖5 銅在水解溶液(堿性+中性)浸泡15 d后的XRD圖譜
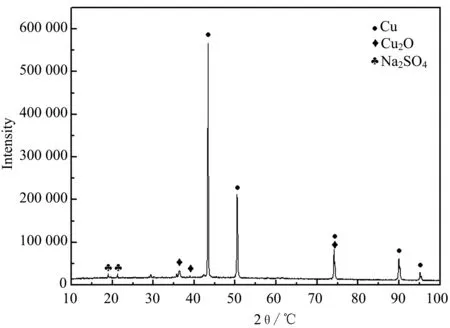
圖6 銅在水解溶液中浸泡20 d后XRD圖譜
通過圖5可以看出,銅在堿性和中性的亞硫酸二甲酯水解溶液中的產物無明顯差異,均以Cu2O為主,而從圖6可以看出,銅在浸泡20 d后,除了銅和氧化亞銅外,在溶液中還檢測到了Na2SO4。根據試驗過程,可以推測:水解溶液中硫的存在形式為亞硫酸根,但是亞硫酸根不穩定,易被水中O2氧化,進而進一步形成了穩定的硫酸根,發生的化學反應如下所示:
2.3 SEM與EDS分析
將銅分別浸泡在堿性和中性亞硫酸二甲酯水解溶液中15 d后,得出SEM圖(見圖7、圖8)和EDS圖(見圖9、圖10及圖11)。

圖7 銅在堿性水解溶液中浸泡后的SEM圖
通過圖7可以觀察到銅表面除了有幾處明顯的腐蝕坑外,其余部分主要以點蝕坑為主,而且在點蝕坑周圍可以看到許多淺色的顆粒狀腐蝕產物。為能準確的了解腐蝕區域的腐蝕產物,利用EDS能譜儀分析腐蝕微區的成分,分別選取如下3點:點蝕坑內;腐蝕產物顆粒的周圍;腐蝕坑內。背散射電子掃描結果見圖8。

圖8 銅在堿性水解溶液中浸泡后的EDS圖

編號CuOSi區域169.4319.3411.22區域272.1817.6510.17區域354.9126.0319.06
根據表3所示,3處區域的元素組成,除了銅元素外,都以氧元素居多,這表明腐蝕產物以銅的氧化物為主,而三處的Si主要來自于試驗中所用到的玻璃器皿中的SiO2。除去SiO2中的氧元素,點3處氧元素最多,點1處其次,點2處最少,這表明銅的氧化物主要分布在銅表面未被腐蝕處。

圖9 銅在中性水解溶液浸泡15 d后的SEM圖
從圖9可以觀察到,銅在中性水解溶液中浸泡15 d后,相比在堿性溶液中銅在中性條件下表面腐蝕范圍更廣,區域內出現大面積的腐蝕。具體表現形式為:銅表面不僅存有腐蝕坑洞外,還出現了裂縫腐蝕,嚴重破壞了銅的表面。為進一步研究腐蝕區域的腐蝕與S元素是否有關,試驗中分別對腐蝕區域進行EDS能譜分析如圖10所示,得出表4。

圖10 銅在中性溶液中腐蝕表面1

編號CuOS區域188.359.522.13區域290.957.511.55
根據圖10、表4可以明顯看出:銅在中性溶液中的腐蝕發現了硫元素,且1處腐蝕區域比2處表面含量多,同時腐蝕區域氧含量也比表面多,1處的腐蝕率達到了11.65%,比2處高出2.59%,可以得出結論S元素的增加加速了銅的腐蝕。
為論述試驗結果,本文進一步選取了不同的腐蝕區域和未腐蝕區域進行EDS能譜分析如圖11所示,得出表5,結果如下。

圖11 銅在中性溶液中腐蝕表面2
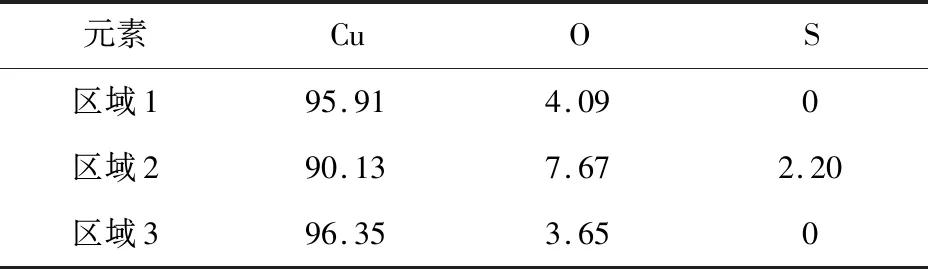
元素CuOS區域195.914.090區域290.137.672.20區域396.353.650
從圖11可以看出圖中腐蝕區域2處要比1處腐蝕面積大將近一倍。而根據表5中的數據來看,在2處的腐蝕區域腐蝕率達到了9.87%,分別比腐蝕區域1處和未腐蝕區域3處腐蝕率高出5.78%和6.22%。而且只在2處發現了S元素且氧含量比1處和3處都多,說明S元素的存在確實加快了2處的腐蝕。
3 結 論
1)亞硫酸二甲酯在堿性條件下水解的產物是亞硫酸鹽和甲醇,銅在亞硫酸二甲酯水解的腐蝕產物是Cu2O,與水解溶液的酸堿性無關。
2)銅在堿性水解溶液中的腐蝕以點蝕和局部腐蝕為主,且與S元素無關,腐蝕產物主要分布在未被腐蝕的表面處;銅在中性水解溶液中腐蝕以裂縫腐蝕為主,腐蝕面積大,且S元素加快腐蝕率。
3)隨著的堿性的增加,銅的耐蝕性性能降低,腐蝕速率加快,在中性溶液中的腐蝕速率最快,腐蝕率可達到了11.65%,且銅的耐蝕性能隨著浸泡時間增長有所提高。

