量子生物學或有助于破解生命中的最大謎題
編譯 蔡立英
從酶促反應的驚人速度到人腦的運作,科學家在對許多生物學謎題的探索中都發現了量子效應存在的證據。

在英國謝菲爾德大學的一個物理實驗室中,數百個光合細菌被置于兩面相距不到1微米的鏡子之間。物理學家大衛·科爾斯(David Coles)和他的同事正在用白光照射這一充滿微生物的空隙,他們可以通過調節鏡子之間的距離來調節白光在細胞周圍反射的方式。根據2017年發表的研究結果,這種精妙的裝置可以使光子與少數細胞中的光合作用結構發生相互作用,而且研究團隊通過微調實驗裝置就可以改變這種相互作用。
研究人員可以像這樣控制細胞與光的相互作用,這本身就是一項了不起的成就。但是,2018年,研究團隊對這一發現作出了更令人驚訝的闡釋。當科爾斯和幾位合作者重新分析實驗數據時,他們發現細菌和光子之間相互作用的性質比他們最初的分析結果更奇特。前后兩篇論文的共同作者之一、英國牛津大學的物理學家弗拉特科·韋德拉爾(Vlatko Vedral)表示:“這對我們來說似乎是一個無法回避的結論,那就是我們間接證實了量子糾纏。”
量子糾纏是指兩個或多個粒子相互依存的狀態,不管它們之間相距多遠。 這是亞原子世界的諸多反直覺的特性之一,比如電子和光子等粒子同時表現為粒子和波,同時占據多個位置和狀態,并能穿過看似不可穿透的勢壘。這種尺度下的物理過程是用量子力學復雜的數學語言描述的,并且經常產生看似違背常識的效應。正是使用這種語言,韋德拉爾及其同事們在謝菲爾德大學的實驗數據中,檢測到了光子和細菌之間發生量子糾纏的特征。
研究人員已經在無生命物體中多次證明了量子糾纏的存在。2017年,有科學家報告稱,他們設法維持了相隔1 200千米的光子對之間的相互依存性。但是,如果韋德拉爾及其同事們提出的假設是正確的,也就是說,這種現象也存在于細菌中,那么該研究可能標志著人類首次在生物體內觀察到量子糾纏,并且為日益增多的證據又增加了佐證,證明量子效應在生物學中并不像人們過去以為的那樣罕見。
在生命系統的雜亂世界中,也許能觀察到量子現象,這在歷史上一直是一種邊緣的觀念。雖然量子理論準確地描述了構成所有物質的單個粒子的行為,但長久以來,科學家們認為,數十億個粒子在環境溫度下的集體運動會淹沒任何奇特的量子效應,并且大量粒子的集體行為可以通過牛頓等人確立的更為人熟知的經典力學得到更好的解釋。實際上,量子現象的研究者通常會僅僅為了消除背景噪聲,而把粒子隔離在接近絕對零度的溫度下——這一溫度下幾乎所有的粒子運動都停止了。
英國薩里大學的理論物理學家吉姆·艾爾-哈利利(Jim Al-Khalili)指出:“環境溫度越高,粒子運動越快,背景噪聲越嘈雜,這些量子效應就消失得越快。”他在2014年與他人合著了一本名為《神秘的量子生命》(Life on the Edge)一書,向非專業讀者介紹了所謂的“量子生物學”。“因此,量子效應竟然堅持存留于細胞內,這幾乎是荒謬的,反直覺的。不過,如果量子效應確實存留于細胞內——而且有很多證據支持,在某些現象中的確如此,那么生命一定有其特殊的運作機制。”
現在,不止是艾爾-哈利利和韋德拉爾,還有越來越多的科學家也認為,量子世界的效應可能是解釋生物學中一些最大謎題(從酶催化效率到鳥類導航乃至人類意識)的關鍵,甚至可能受制于自然選擇。
牛津大學的物理學家基婭拉·馬萊托(Chiara Marletto)與科爾斯和韋德拉爾合作,發表了關于細菌中量子糾纏的論文,她指出:“整個領域都試圖證明這一點,那就是,量子理論不僅適用于這些生物系統,而且還有可能測試這些系統是否利用量子物理學來發揮其功能。”
生物學反應中的量子效應
20世紀80年代中期,美國加州大學伯克利分校的生物化學家朱迪思·克林曼(Judith Klinman)確信,關于酶催化的傳統解釋是不完整的。當代理論認為,在形狀匹配的基礎上,酶與底物按照經典力學規律發生相互作用,依照規律將底物聚集在其活性位點,并穩定分子結構的過渡態,從而把反應速率加速到萬億倍或更高。但是,克林曼從酵母中提取酶進行體外實驗時,卻得到了奇怪的結果。
在催化苯甲醇氧化成苯甲醛時,醇脫氫酶會將氫原子從一個位置移動到另一個位置。出乎意料的是,當克林曼和她的同事們用較重的同位素氘和氚替代底物中的特定氫原子時,反應快速放緩。雖然酶催化的經典解釋允許適度的同位素效應,卻無法解釋克林曼觀察到的反應速率的大幅下降。克林曼表示:“我們所看到的現象偏離了現有理論。”
她的團隊一直在深入研究此問題,后來在1989年,他們基于已經在酶研究者之中流傳的想法,提出了一個假設:催化反應涉及一種稱為“量子隧穿”(quantum tunneling)的量子“戲法”。艾爾-哈利利解釋道,量子隧穿就像踢足球穿過一座山,這里所說的足球是指電子或其他粒子,而山則是指阻礙反應發生的能壘(energy barrier)。“在經典世界,你必須狠踢一腳才能讓足球翻過山頂到達另一邊,”他說,“而在量子世界,你不必如此費勁,你可以把足球踢到半山腰,足球就會突然消失,但會在另一邊出現。”
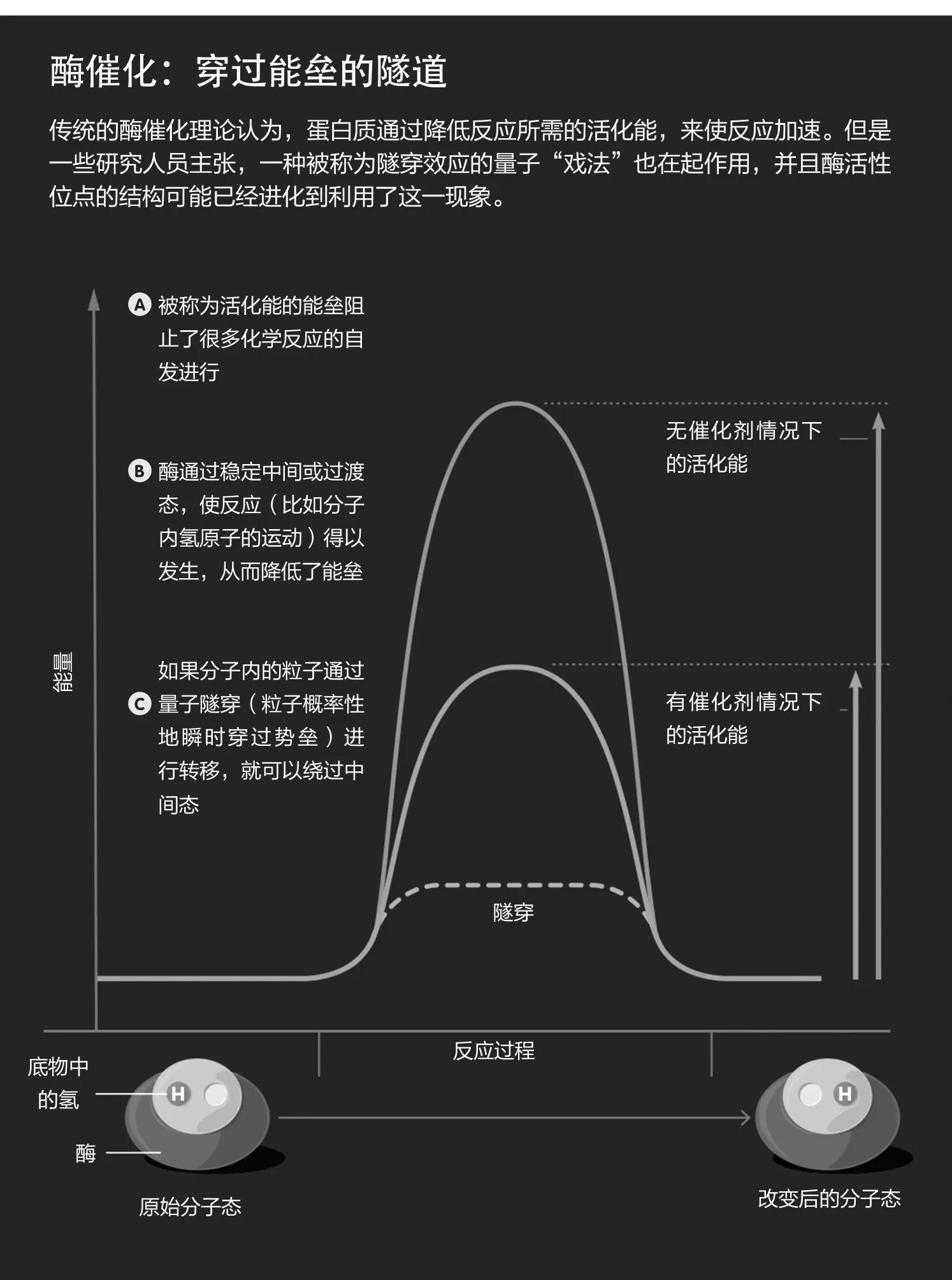

克林曼的團隊在這篇論文和后來的論文中提出,在苯甲醇氧化以及很多其他反應的催化過程中,氫轉移是在量子隧穿效應的幫助下進行的。這有助于解釋為什么氘和氚經常會延緩反應——因為更重的粒子隧穿能力更差,而且會使同一分子中的其他粒子的隧穿變得更難。艾爾-哈利利說,克林曼研究團隊觀察到的效應已被其他實驗室復制到多種酶上,從而為生物系統中的量子效應假說提供了一些最有力的證據。
雖然現在人們普遍接受量子隧穿效應會在生物催化中發生,但研究人員對于量子隧穿效應在生物催化中的重要程度,以及它是否受自然選擇影響存在分歧。例如,美國科羅拉多州立大學的化學家理查德·芬克(Richard Finke)指出,無論酶是否存在,一些反應都表現出相似程度的同位素效應,這暗示著酶不太可能經過了特別的進化適應,來增強其催化反應中的量子隧穿效應。目前還不清楚量子隧穿在多大程度上加速了反應。一些研究人員認為,在主要由經典力學主導的過程中,量子隧穿效應通常只不過發揮微弱的推動作用。
但克林曼認為,發生在酶中的量子隧穿效應遠比想象的重要。她說:“酶可以產生促進隧穿的非常精確且緊湊的活性位點結構。”她指出,例如,在催化過程中,酶會改變構象,使氫供體和受體位點足夠接近——彼此間距約0.27納米,從而促進量子隧穿效應。
她的研究團隊通過改變酶的活性位點,并觀察反應速率和同位素效應如何在體外發生變化,來驗證他們的這一想法。例如,2019年早些時候,該團隊創造了一種大豆脂氧合酶的變體,使反應底物以不利于氫隧穿的方式略微錯位。突變酶的催化能力比野生型低4個數量級,并且突變酶對氘取代氫更加敏感。
研究人員仍在量化量子隧穿效應在催化中的作用,克林曼強調,使用突變和計算建模等多種方法來確切了解蛋白質如何加速反應很重要。研究人員開展了酶的進化實驗,在實驗中反復選擇蛋白質來增強酶的催化能力,這也可以讓我們深入了解量子隧穿效應在催化中的作用大小——盡管近期至少有一項此類嘗試尚無定論。2018年,一個研究團隊把涉及氫轉移的一個酶促反應中的酶進行了演變,得出的研究報告稱,在整個演變過程中,量子隧穿效應“沒有觀察到顯著變化”。
對上述問題的探討,呼應了另一場正在進行的對話,那就是關于量子現象在地球上另一個關鍵的生物過程——光合作用過程中的重要性。當韋德拉爾及其同事正在研究細菌的光合作用結構是否與光子糾纏時,其他研究團隊則一直在研究另一種量子效應如何促使光合作用的能量轉移效率最大化。
在植物和一些微生物的捕光反應期間,光子激發葉綠素分子中包含的電子,產生一種稱為“激子”(exciton)的實體。這些激子繼而從一個葉綠素分子轉移到下一個,直到它們抵達反應中心——這是一簇可以捕獲和儲存能量的蛋白質。
激子在轉移過程中可能會失去能量,這意味著它們在葉綠素分子之間繞路越多,到達反應中心的能量就越少。物理學家早在幾十年前就曾提出,如果這個轉移過程是量子相干的,那么就可以避免這種能量浪費。也就是說,如果激子可以像波而不是像粒子那樣傳播,它們就可以同時嘗試通往反應中心的所有路徑,而只采用最高效的那條。
2007年,由兩位化學家——加州大學伯克利分校的格雷厄姆·弗萊明(Graham Fleming)和華盛頓大學圣路易斯分校的羅伯特·布蘭肯希普(Robert Blankenship)領導的研究團隊稱,他們在從綠硫細菌中提取的葉綠素分子復合物中,觀察到了量子相干性,綠硫細菌是一種常見于缺乏光照的深海中的光合微生物。研究人員使用了一項技術對樣品吸收和釋放的能量進行分析,并在溫度冷卻至77 K的復合物中,檢測到一種稱為“量子拍”(quantum beating)的信號,他們將這種振蕩解釋為量子相干性的證據。在接下來的幾年里,他們和其他研究團隊在環境溫度下復制了這一研究結果,并將其擴展到海藻和菠菜的葉綠素復合物中。
這些研究結果是否反映了量子效應對光合作用中的能量轉移作出了有意義的貢獻仍值得探討。例如,在2017年,德國研究人員再次研究了綠硫細菌并報告,發現其量子相干效應持續時間不到60飛秒(即6×10-6秒),時間太短不足以協助能量轉移到反應中心。但是2018年,另一個研究團隊認為,葉綠素復合物中存在多種類型的相干性,有些量子相干確實顯現出持續足夠長的時間,從而在光合作用中發揮作用。其他一些科學家提示說,一些細菌可以通過產生不同形狀卻非常關鍵的光捕獲蛋白來開啟或關閉量子相干效應。這些研究發現再次引發了學界的猜測:光合作用結構可能像酶一樣,已經進化到利用了量子現象的程度。
布蘭肯希普指出,光合作用中的量子相干效應如今已是一個被廣泛接受的現象。正如酶中的量子隧穿效應一樣,“此時最關鍵的討論是,量子相干效應是否真正影響系統的效率或其他方面,產生真正的生物學益處。我認為這個問題目前還沒有定論。”


動物學謎題的量子解釋
每年冬天,歐洲大陸北部的知更鳥都會向南遷徙數百公里到達地中海,這是一種通過磁覺(magnetoreception)——具體來說,就是鳥類探測地球磁場方向的能力——實現的導航壯舉。但是,試圖解釋這種第六感的早期研究,比如鳥類依賴內部磁鐵礦晶體進行導航的研究假說等都未能獲得實驗上的證據支持。
直到20世紀90年代末期,這個問題引起了索斯滕·里茨(Thorsten Ritz)的注意,他當時還是美國伊利諾伊大學厄巴納-香檳分校的一名研究生(后來,他就職于加州大學爾灣分校),在已故生物物理學家克勞斯·舒爾滕(Klaus Schulten)的指導下,研究光合作用中的量子效應。他對隱花色素特別感興趣,這是一種在鳥類視網膜中發現的光敏蛋白質。里茨說,現在已經有“很好的證據”證明隱花色素在鳥類磁覺中的作用。因此,在2000年,專注于研究這種蛋白質的里茨、舒爾滕和伊利諾伊大學的另一位同事,在舒爾滕早期理論工作基礎上,發表了后來被稱為“自由基對模型”(radical-pair model)的理論假說,來解釋磁覺可能的運作機制。
里茨、舒爾滕等人提出,隱花色素蛋白質中的反應會產生一對自由基分子,每個分子各自都有一個孤電子,相互之間會發生量子糾纏,它們的行為對諸如地球磁場等弱磁場的朝向很敏感。自由基對相對于磁場的朝向變化,理論上可以觸發下游的化學反應,從而使得信息以某種方式傳遞到大腦。
里茨繼而與最早論述歐洲知更鳥磁覺的生物學家伉儷羅斯維塔·維爾奇科(Roswitha Wiltschko)和沃爾夫岡·維爾奇科(Wolfgang Wiltschko)合作,對該假說產生的一系列預測進行實驗驗證。例如,在2004年發表的一項研究中,該研究團隊將知更鳥置于振蕩的磁場中,根據“自由基對模型”的預測,該實驗中磁場振蕩所采取的頻率和角度可能會破壞自由基對對地球磁場的敏感性。實驗發現,這么做有效地破壞了知更鳥的導航能力。
從那時起,“自由基對模型”從各種磁覺理論假說中脫穎而出,獲得越來越多的理論支持。2018年,針對一種隱花色素Cry4的分子特性和表達模式的兩項研究指出,該蛋白質可能是斑胸草雀和歐洲知更鳥的磁感應受體。
要確定鳥類磁覺是否真的以這種方式起作用,并且揭示自由基對的孤電子之間的量子糾纏是否重要,還有待更多的深入研究。里茨表示,科學家們也還沒有完全了解隱花色素如何將磁場信息傳遞給大腦。同時,他的研究團隊正專注于突變實驗,這可能有助于揭示隱花色素的磁敏感性。2018年秋天,牛津大學的化學家彼得·霍爾(Peter Hore)和德國奧登堡大學的生物學家亨里克·穆里岑(Henrik Mouritsen)領導的研究目標類似的項目“量子鳥類”(QuantumBirds),獲得了歐洲研究委員會(ERC)的資助。
在動物感覺生物學中,磁覺不是引起量子物理學家興趣的唯一謎題,研究人員希望破解的另一個科學上神秘的感覺是嗅覺。傳統理論認為,氣味分子與嗅覺神經元上的蛋白質受體結合,從而觸發嗅覺。可是,實際中,一些形狀幾乎相同的氣味分子卻產生完全不同的氣味,而另一些立體化學構型不同的氣味分子卻產生相似的氣味,這些不能自圓其說的現象都使傳統理論面臨挑戰。
20世紀90年代中期,英國倫敦大學學院的生物物理學家盧卡·都靈(Luca Turin,現在是一位受人尊敬的香水評論家)提出,嗅覺受體可能不僅對形狀敏感,而且對氣味分子化學鍵的振動頻率敏感。他認為,當氣味與受體結合,如果氣味分子的化學鍵以某一頻率振動,就可以促進受體內電子的量子隧穿效應。根據他的模型,這種電子轉移會觸發嗅覺神經元中的信號級聯,最終向大腦發送神經脈沖。
倫敦大學學院的物理學家詹尼·布魯克斯(Jenny Brookes)以數學方式闡述了這個問題,并證明它在理論上是可行的。她指出,該理論的實驗證據還難以捕捉,但這也正是這一理論令人興奮的部分原因所在。近年來,研究人員一直在尋找與酶反應中相似的同位素效應。如果量子隧穿效應發揮重要作用,那么,含有較重氫同位素的氣味分子應該與正常分子的氣味不同,因為它們的化學鍵的振動頻率較低。
不同團隊的研究結果并不一致。2013年,都靈的研究團隊報告指出,人類可以區分含有不同同位素的氣味劑。兩年后,其他研究人員未能重現這一結果,并稱該理論“難以置信”。但這一理論并沒有過時。2016年,另一個團隊報告指出,蜜蜂可以區分含有不同同位素的氣味,而最近的理論研究則提出了一系列新的預測來幫助測試該理論模型的有效性。
在實驗證據不足的情況下,理論工作也引起了研究人員對量子生物學解釋的興趣。例如,一些研究人員推測,在光合作用中起作用的量子相干效應,也可能影響視覺和細胞呼吸等廣泛的生物現象。另一些人則提出,質子隧穿效應(proton tunneling)可以促進DNA中的自發突變,盡管艾爾-哈利利及其同事的理論研究表明,至少對他們建模的腺嘌呤-胸腺嘧啶堿基對來說,這不太可能。
詭異的量子效應可能在人類大腦中發揮作用,這一想法也許是量子物理學在動物世界最極端的延伸了。加州大學圣巴巴拉分校的物理學家馬修·費舍爾(Matthew Fisher)認為,神經元具有能夠像量子計算機一樣運行的分子機器,不是使用0或1這樣的經典比特,而是運用可以同時處于0和1狀態的信息單位——量子比特來工作。
費舍爾提出,大腦的量子比特編碼在波斯納分子(Posner molecules)內的磷酸根離子態上,波斯納分子是在骨骼中發現的磷酸鹽和鈣簇,也可能存在于某些細胞的線粒體內。他的團隊最近的理論工作認為,不同波斯納分子中的磷酸根離子態可以相互糾纏持續數小時甚至數天,也許因此能夠進行快速和復雜的計算。費舍爾最近獲得資助,建立了一個稱為“量子大腦”(QuBrain)的國際合作項目,通過實驗尋找這些量子糾纏效應。很多神經科學家對該項目能否取得積極成果表示懷疑。
讓量子生物學發揮作用
量子生物學中的大多數想法仍然很大程度地受到理論驅動而不是實驗支持,但現在許多研究人員正試圖縮小兩者之間的差距。韋德拉爾的團隊計劃在2019年晚些時候,收集更多關于細菌中量子糾纏現象的數據,荷蘭代爾夫特理工大學的物理學家西蒙·格勒布拉切爾(Simon Gr?blacher)也提議在緩步動物中進行量子糾纏實驗。2017年,艾爾-哈利利和《神秘的量子生命》一書的共同作者——薩里大學的生物學家約翰喬·麥克法登(Johnjoe McFadden)一起,幫助建立了量子生物學博士培訓中心,以鼓勵跨學科探討并推進研究工作。麥克法登說:“在更廣泛的科學家和研究資助者群體中,如果你說你正在研究生物學中的量子力學,那么現在別人不會認為你是徹底瘋了,只是會覺得這有點古怪。”
接受《科學家》雜志采訪的其他研究人員也強調,無論理論機制是否獲得實驗支持,量子生物學的推測本身都是有價值的。“隨著技術微型化發展,我們可以從生物世界的豐富信息寶庫中汲取靈感,”理論物理學家和量子計算研究員、科技公司SAP Africa的創新總監阿德里安娜·馬雷(Adriana Marais)說,“這是一個探究生命是什么的絕佳機會,同時也是從生物世界吸取經驗,學習如何以最優方式在這種微尺度下設計工藝流程的絕佳機會。”
量子生物學在現實世界的應用,包括從更高效的太陽能電池到新型生物傳感器技術。2018年,一個研究團隊提出了一個“仿生鼻子”的設計,部分基于嗅覺的量子理論,用以檢測微量濃度的氣味劑。霍爾和其他人強調,用以解釋磁覺的自由基對機制或許可以應用于探測弱磁場的裝置。
“我們可以利用獲得的信息來設計基于這些原理的系統,”里茨說,“即使事實證明這并不是鳥類磁覺的機理。”

