提高多中心臨床研究倫理審查效率和質量的探索及思考
王晶晶 范士志 廖祥麗 段鴻彥 朱劍武
中圖分類號 R951 文獻標志碼 A 文章編號 1001-0408(2019)23-3196-04
DOI 10.6039/j.issn.1001-0408.2019.23.05
摘 要 目的:探索提高多中心臨床研究倫理審查效率和質量的方法。方法:《關于深化審批制度改革鼓勵藥品醫療器械創新的意見》《藥品注冊管理辦法(修訂稿)》政策出臺后,結合我中心實際與實踐,分析我中心提高倫理審查效率和質量的方法、完全備案制方式可能存在的問題以及提高多中心臨床研究倫理審查效率和質量的途徑。結果與結論:我中心采取了多樣化的審查方式(會議審查、快速審查、備案制等),通過對研究項目實施分級管理及差異化審查流程,制訂備案制操作細則等方式提高審查的效率和質量,跟蹤審查和實地訪查次數有所增加。我中心倫理委員會在探索過程中,認為完全實行備案制會出現組長單位倫理審查質量難以評估、各中心研究資質及條件不一等問題。為提高多中心臨床研究倫理審查的效率和質量,可采用提高中心倫理的審查質量、加強各中心倫理委員會間的溝通與互認、建立倫理委員會秘書初審制等措施,實現效率與質量的平衡。
關鍵詞 多中心臨床研究;倫理備案制;倫理審查質量;倫理審查效率
Exploration and Reflection on Improving the Efficiency and Quality of Ethical Review in Multi-center Clinical Trial
WANG Jingjing1,FAN Shizhi2,LIAO Xiangli1,DUAN Hongyan1,ZHU Jianwu3(1.Office of Ethics Committee, Daping Hospital of Army Medical University, Chongqing 400042, China;2.Dept. of Cardio-vascular Surgery, Daping Hospital of Army Medical University, Chongqing 400042, China;3.Medical Research Department, Daping Hospital of Army Medical University, Chongqing 400042, China)
ABSTRACT ? OBJECTIVE: To explore the ways to improve the efficiency and quality of ethical review in multi-center clinical trial. METHODS: After issuing the policy of Opinions on Deepening the Reform of Approval System and Encouraging the Innovation of Pharmaceutical Medical Devices and Measures for the Administration of Drug Registration (Revised Version), combined with the practice of our center, the methods to improve the efficiency and quality of ethical review, the possible problems of complete filling system and the way to improve the efficiency and quality of ethical review in multi-center clinical trial were analyzed in our center. RESULTS & CONCLUSIONS: Our center adopted a variety of review methods (conference review, rapid review, filing system, etc.), implemented hierarchical management and differential review process for research projects, and formulated defined rules of filling system operation and other ways to improve the efficiency and quality of review, doubled the review efficiency, increased the number of follow-up review and field visit. In the process of exploration, the ethics committee of our center believes that the complete implementation of the filing system will lead to problems such as the difficulty to evaluate the quality of the ethical review of the leader unit, different research qualifications and conditions of each center, etc. In order to improve the efficiency and quality of the ethical review of multi-center clinical research, the measures are can be adopted, such as improving the quality of the ethical review of the center, strengthening the communication and mutual recognition of the ethics committees of each center, and establishing the preliminary review system of the secretary of the ethics committee, so as to realize the balance of efficiency and quality.
KEYWORDS ? Multi-center clinical trial; Ethical filling system; Ethical review quality; Ethical review efficiency
2003年版《藥物臨床試驗質量管理規范》[1](GCP)第六十五條指出,多中心臨床試驗是由多位研究者按同一試驗方案在不同地點和單位同時進行的臨床試驗。研究項目需要獲得所有參研單位的倫理審查批件,每家單位逐一獨立審查,這一過程常需要耗時超過半年,嚴重影響項目的開展進度。2017年10月8日,中共中央辦公廳、國務院辦公廳印發《關于深化審批制度改革鼓勵藥品醫療器械創新的意見》[2](以下簡稱《意見》)。《意見》明確指出,要完善倫理委員會機制、提高倫理審查效率。同年10月23日,食品藥品監督管理局發布的《藥品注冊管理辦法(修訂稿)》[3]中也提到,多中心臨床試驗認可組長單位或區域倫理批準。筆者在本文中對本機構提高倫理審查效率和質量的方法,完全備案制方式可能存在的問題及提高多中心臨床研究倫理審查效率和質量的途徑三方面進行研究,以希望提高倫理審查的效率和質量。
1 我中心提高倫理審查效率和質量的方法
我中心倫理委員會既往標準操作規程中規定,對于多中心臨床研究均需要獨立會議審查,不接受中心倫理批件。這種方式審查效率極低,上述新規出臺后,倫理委員會辦公室積極響應,結合自身實際,從以下幾個方面修訂標準操作規程,以提高倫理審查的效率。
1.1 建立多樣化的審查方式
單一會議審查常規情況下屬于定期會議,不能滿足大量項目同時進行初始審查,極易造成審查項目積壓。所以我院將初始審查的審查方式由單一會議審查調整為會議審查、快速審查和備案制:(1)會議審查。屬于定期會議,需要滿足法定到會人數,且每次審查項目數量有限。 (2)快速審查。由兩名委員進行審查,如意見一致,則下發批件;若意見不一致,則需要轉為會議審查。 (3)備案制。認可組長單位批件,不再重復審查,直接簽發批件。
1.2 對項目進行分級管理及差異化審查流程
倫理辦公室根據研究性質和風險程度對項目進行分類,以此來選擇不同的審查方式,這樣可以滿足不同研究項目的審查需要,縮短等待審查的時間,待審項目能得到及時的受理和審查。
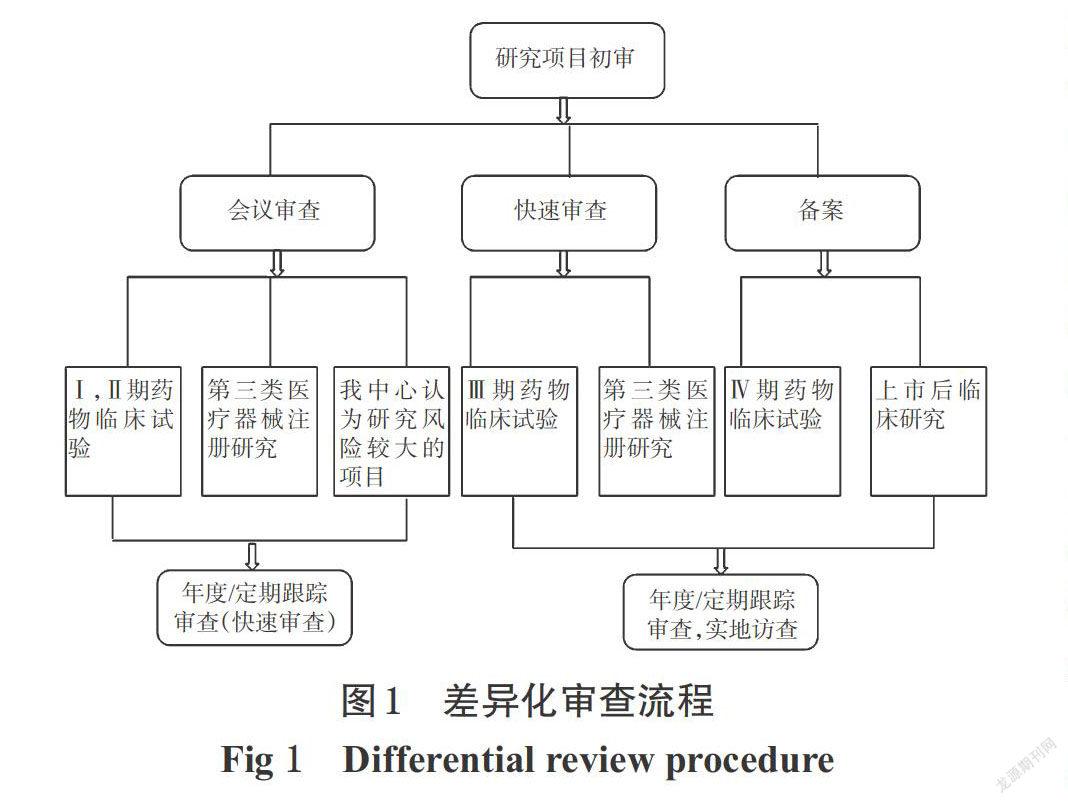
同時為進一步保證研究的倫理規范性,對于初審采用快速審查或備案制的研究項目,縮短跟蹤審查頻率,每6個月進行一次本中心進展情況的審查,必要時采取實地訪查的方式。差異化審查流程見圖1。
1.3 規定備案制操作細則
因備案制為新增的審查方式,修訂后的標準操作規程對其操作流程進行了以下規定:(1)辦公室秘書進行仔細的形式審查,對項目類別、研究藥物及器械分類、組長單位批件及批準的文件一一進行審核,確保所遞交的材料與組長單位倫理批件批準的文件一致。(2)如有針對本單位的個性化材料,可單獨送審,由委員進行快速審查。(3)形式審查通過的項目,符合備案要求的,填寫備案申請表,倫理秘書遞主任委員審核確認,若同意,則附審查批件。
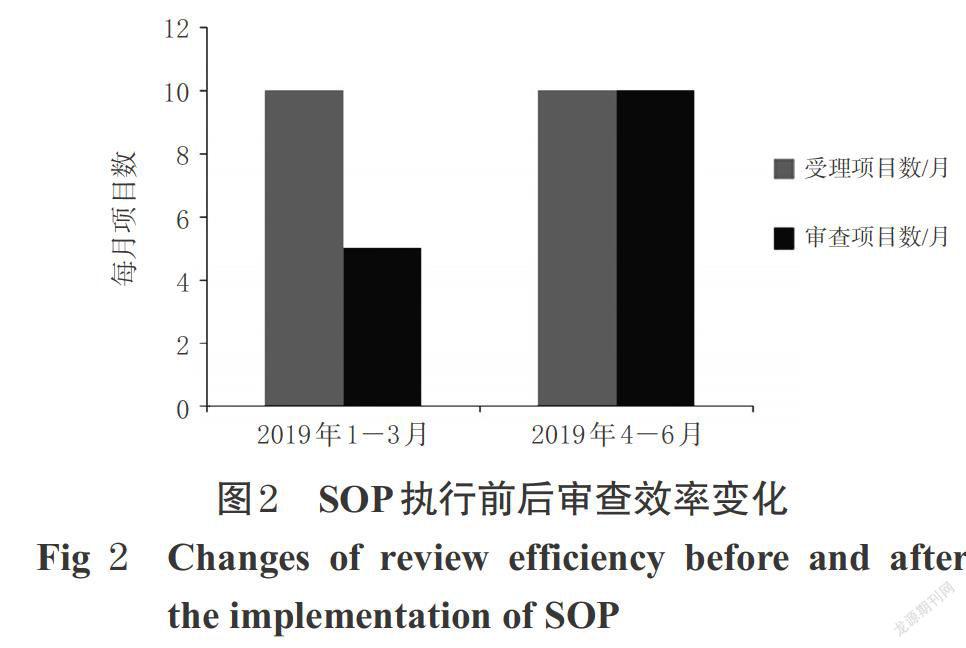
自2019年4月修訂后的本中心倫理委員會《標準操作規程》(SOP)執行以來,我中心初始審查的效率提高了一倍,同時跟蹤審查和實地訪查的次數有所增加,實地訪查的次數由既往的每半年一次,增加至每3個月一次。由此可見,我中心的分級管理、差異化審查方式可在保證審查質量的情況下,提高倫理審查效率。SOP執行前后審查效率變化見圖2。
2 完全備案制方式可能存在的問題
我中心倫理委員會在探索過程中,認為完全備案制會存在如下問題。
2.1 組長單位倫理審查質量難以評估
目前由于缺乏官方的評估認證標準,國內各機構倫理委員會的資質無從考量。我國醫學倫理領域第一家也是唯一一家經國務院批準的官方認證機構就是針對中醫藥領域的世界中醫藥學會聯合會(WFCMS),其開展的認證也是我國醫學倫理領域唯一的國家認證項目。認證對象是“開展涉及人的中醫藥研究的組織機構”[4],而在化學藥領域,國內尚無任何官方認證機構。此外,大部分倫理委員會的倫理審查流程和標準尚未統一,雖然部分倫理委員會已通過國際認證,如發展倫理委員會審查能力的戰略行動(WHO/SIDCER)、美國人體研究保護項目認證協會(AAHRPP)等,規范程度較高,但這類高水平的倫理委員會仍是少數[5]。
2.2 各中心研究資質及條件不一
2010年11月,國家食品藥品監督管理局在發布的《藥物臨床試驗倫理審查工作指導原則》[6]中指出,多中心臨床研究,各分中心倫理委員會需審查本中心的研究資質及研究條件是否滿足試驗要求,特別是研究風險較大的項目,如前期研究發生多例嚴重不良事件、研究對象為危重癥患者,由于各中心研究資質及條件不一樣,完全不進行初始審查,直接備案,難以保證研究開展的質量。
3 提高多中心臨床研究倫理審查效率和質量的途徑
我中心在探索提高倫理審查質量和效率的過程中,思考總結了以下方法。
3.1 提高中心倫理的審查質量
組長單位高質量的倫理審查是參加單位不再重復審查的重要前提,這是受試者安全與權益能得到保護的關鍵。接受組長單位倫理審查結論,將不會再有其他倫理委員會去發現問題并進行補救,那么將對組長單位倫理審查提出更高的要求。如果組長單位倫理委員會審查質量不過關,所有參加單位的試驗受試者都將面臨權益與安全保護的問題。中國臨床研究能力提升與受試者保護高峰論壇(CCHRPP)《臨床研究倫理協作審查共識( 試行版) 》[7]提出了“主審倫理委員會”的概念,并對“主審倫理委員會”的資格進行了規定。也就是說,承擔多中心臨床試驗主要倫理審查職責的倫理委員會必須滿足相應的資格要求。組長單位倫理委員會不會自然而然就成為主審倫理委員會,而是要滿足相應資格要求才能成為令各參加單位信服的主審倫理委員會,這樣受試者的安全權益才能得到保證[8]。
故為提高中心倫理的審查質量,可推行設立國家級的倫理認證機構,建立涵蓋全部中西醫院的認證分級機制。通過認證的機構倫理委員會才可擔任中心倫理的職責。并且相關部門應制訂出符合我國國情的中心倫理審查具體操作指南,將中心倫理的審查要點、標準、流程等統一規定。這樣各分中心也可評估中心倫理審查質量,從而在本中心采取適宜的審查方式[9]。
3.2 建立并加強各中心倫理委員會間的溝通與互認
3.2.1 建立各中心倫理委員會間的溝通機制 中心倫理與分中心倫理審查,缺一不可。應明確職責劃分,加強溝通交流,增強協作意識。與中心倫理建立相互合作的“有審有備有溝通”的機制。可采取各中心倫理委員會聯合建立工作微信群、定期舉辦年會等方式[10]。
3.2.2 設立主審倫理委員會+副審倫理委員會制 由主審倫理委員會負責對多中心臨床研究項目的科學與倫理合理性承擔主要審查職責[11],確保審查全面充分高質量,參加單位的倫理委員會承擔副審倫理委員會職責,即在主審倫理委員會審查意見基礎上,側重對研究在本機構的可行性以及知情同意書的本地化要求等進行審查。如分中心可以對知情同意書審查并作出“本土化”的要求[12],以適應本地的受試者閱讀和理解,同時分中心對項目進展過程中的嚴重不良事件、方案違背、年度定期跟蹤審查、修正案等均需進行重點審查,對于本中心臨床研究實施全過程進行嚴格的倫理監管,才可保證臨床研究的倫理審查質量。
3.2.3 倫理審查互認 推行建立倫理審查結果互認制度,制定按照疾病分類的倫理審查標準和操作細則,在全國統一執行,實現倫理審查任務分流。例如北京友誼醫院與北京佑安醫院、北京地壇醫院聯合,開展了基于消化、肝病學科的倫理協作審查和互認試點的簽約,省去了不必要的重復審批,節省了臨床試驗的時間[13]。
3.3 實行倫理委員會秘書初審制
對于實行“備案制”的項目,不能只是簽收備案,倫理秘書收到材料后,應加倍仔細進行形式審查,如我中心倫理秘書對于送審材料與中心倫理批件均一一核對,同時針對本單位的相關材料還需及時送審。倫理辦公室在對研究風險評估等沒有充分把握時,還需聘請相關專業的獨立顧問。
所以秘書的工作能力也是倫理委員會工作質量的關鍵要素之一。應加強對倫理委員會秘書的培訓,提高崗位勝任力。培訓內容可以結合現行法規指南,以及臨床研究的設計、倫理審查的程序、受試者保護、知情同意書要點等多方面,同時衛生行政部門可提供針對倫理秘書的強制性繼續教育課程,設定定期考核機制等方式[14],進一步提高秘書的倫理形式審查的能力,尤其對送審資料是否具有重大倫理問題的辨別力,正確判斷能否簽收該項目資料,以及如何對研究項目采取合適的審查方式,做好備審工作的把關人。
多中心臨床研究是目前臨床試驗的常態,如何將《意見》落地,提高倫理審查效率,并保證倫理審查質量,是國內研究機構開展多中心臨床試驗的共同要求,本單位對此的實踐僅在初始階段,有待隨著實踐發展進一步深入。政府監管部門可建立與完善倫理委員會認證制,各研究單位可以積極探索,結合自身實際,借鑒國內外先進做法,通過制定個性化的備案制度、建立多種形式的倫理協作審查模式、加強自身倫理審查制度建設等方式,實現效率與質量的平衡。
參考文獻
[ 1 ] 國家食品藥品監督管理局.藥物臨床試驗質量管理規范[S]. 2003-09-01.
[ 2 ] 中共中央辦公廳,國務院辦公廳.關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見[S]. 2017-10-08.
[ 3 ] 國家食品藥品監督管理局.藥品注冊管理辦法(修訂版)[S]. 2017-10-23.
[ 4 ] 馬長永,馬曉,徐輝.關于建立我國倫理審查委員會認證制度的展望與思考[J].中國醫學倫理學,2016,29(1):10-13.
[ 5 ] U.S Food and Drug Administration. Guidance for industry using a centralized IRB review process in multicenter clinical trials[EB/OL].[2017-12-02].http://www.fda.gov/RegulatoryInformation/Guidances/ucm127004.htm.
[ 6 ] 國家食品藥品監督管理局.藥物臨床試驗倫理審查工作指導原則[S]. 2010-11-08.
[ 7 ] 中國臨床研究能力提升與受試者保護高峰論壇(CCHRPP)臨床研究倫理協作審查共識(試行版)[EB/OL].[2019- 05-20].http://www.sohu.com/a/213407638_776163.
[ 8 ] 周吉銀,劉丹,曾圣雅,等.我國多中心臨床試驗組長單位倫理審查制度的挑戰[J].中國醫學倫理學,2018,31(9):1157-1161.
[ 9 ] 嚴晉,劉瑜鐘,筱華,等.效率與質量的平衡:構建多中心臨床試驗倫理審查協調體系與平臺的設想[J].中國新藥與臨床雜志,2017,36(10):586-592.
[10] 陸麒,姜柏生.區域倫理委員會的定位、職能與發展[J]. 醫學與哲學,2018,39(12A):1-5.
[11] 柳正植,崔英子,齊彩繽,等.多中心藥物臨床試驗中牽頭單位的職責[J].長春中醫藥大學學報,2016,32(4):844- 846.
[12] 王艷橋,喬潔,陸麒,等.國內多中心臨床試驗的中心倫理審查模式初探[J].醫學與哲學,2016,37(3A):28-31,35.
[13] 黃旭,汪秀琴.關于多中心臨床試驗倫理協作審查的思考[J].中國新藥雜志,2018,27(11):1290-1293.
[14] 李浩,孔德香.我院倫理委員會工作現狀分析及對策探討[J].中國醫療管理科學,2018,8(5):27-30.
(收稿日期:2019-06-29 修回日期:2019-10-18)
(編輯:劉明偉)

