2型糖尿病合并甲狀腺功能減退對血清脂聯素、8-異前列腺素F2α的影響
2型糖尿病(type 2 diabetes mellitus,T2DM)嚴重危害人類健康。我國T2DM患病率高達10.9%,糖尿病前期患病率為35.7%[1]。T2DM病人中甲狀腺功能減退(甲減)患病率為7.59%[2]。近年來研究表明,炎癥反應和氧化應激共同參與T2DM的發病過程[3],但其和T2DM合并甲減關系的報道仍較少。脂聯素是近年來研究的熱點,被認為是一種新的炎癥標志物,同時有抗胰島素抵抗、抗動脈粥樣硬化等作用,在調節代謝方面有重要作用[4]。8-異前列腺素F2(8-iso-PGF2α)是氧化應激較好的標志物之一[5]。本研究擬探討T2DM合并甲減對血清脂聯素、8-iso-PGF2α的影響。
1 對象與方法
1.1 對象和分組 選取2015年3月至2018年3月在我院內分泌科住院的T2DM病人172例為研究對象,其中男103例,女69例,年齡40~85歲,平均(65.25±7.97)歲。根據甲狀腺功能將172例病人分為T2DM伴甲減組(73例)和單純T2DM組(99例)。甲狀腺功能減退診斷標準:促甲狀腺激素(thyroid stimulating hormone,TSH)≥4 mIU/L,游離三碘甲狀腺原氨酸(FT3)、游離甲狀腺素(FT4)降低(FT3<2.8 pmol/L,FT4<11.5 pmol/L)。納入標準:(1)年齡<90歲;(2)符合1999年WHO T2DM診斷標準[6];(3)簽署知情同意書。排除標準:(1)有精神疾病或其他原因不能配合檢查者;(2)患有急性感染、嚴重高血壓、高血壓性心臟病、冠心病、心臟瓣膜病、風濕性心臟病、腫瘤、心功能3級以上者;(3)嚴重肝、腎功能受損者;(4)患有血液系統、風濕免疫系統疾病者;(5)近1個月使用糖皮質激素、非甾體類抗炎藥及免疫抑制劑者;(6)合并酮癥酸中毒、高糖高滲狀態等T2DM急性并發癥者。本研究經我院倫理委員會批準。
1.2 一般資料及血清學指標收集 收集病人年齡、性別、體質量指數(BMI)、吸煙史、收縮壓、舒張壓及降壓藥物使用情況等基本資料。所有病人于清晨空腹抽取肘靜脈血3 mL,室溫3000 r/min 離心 20 min,用EP管收集離心所得血清,置于-80 ℃ 超低溫冰箱保存待測,檢測8-iso-PGF2α、糖化血紅蛋白、總膽固醇(TC)、甘油三酯(TG)、高密度脂蛋白(HDL-C)、低密度脂蛋白(LDL-C)、甲狀腺功能(FT3、FT4、TSH)等指標,其中TC、TG、HDL-C、LDL-C采用全自動生化分析儀檢測,甲狀腺功能采用化學發光法檢測,由我院檢驗科完成。人脂聯素試劑盒購自美國R&D公司,8-iso-PGF2α試劑盒購自上海索萊寶生物科技有限公司,均采用ELISA 方法檢測,由專人嚴格按試劑盒說明書操作。
2 結果
2.1 2組病人一般情況比較 2組病人年齡、性別、吸煙、BMI、血壓、血糖、血脂、降壓藥物使用情況比較,差異無統計學意義(P>0.05)。T2DM伴甲減組病人8-iso-PGF2α高于單純T2DM病人,脂聯素低于單純T2DM組(P<0.05)。見表1。
2.2 糖尿病合并甲減對脂聯素、8-iso-PGF2α的影響 分別以脂聯素、8-iso-PGF2α為應變量,采用多重線性回歸調整年齡、性別、BMI、糖化血紅蛋白、血脂等混雜因素后,結果顯示T2DM合并甲減對脂聯素有負向影響,對8-iso-PGF2α有正向影響(P<0.05)。見表2。
表1 2組病人一般情況比較
注:與T2DM伴甲減組比較,*P<0.05,**P<0.01

表2 T2DM合并甲減對脂聯素、8-iso-PGF2α的影響
注:調整年齡、性別、BMI、吸煙、血壓、血糖、血脂
2.3 TSH和脂聯素、8-iso-PGF2α的相關性 T2DM伴甲減病人中,TSH的自然對數(LnTSH)和脂聯素呈負相關,和8-iso-PGF2α呈正相關(P<0.05)。見表3。
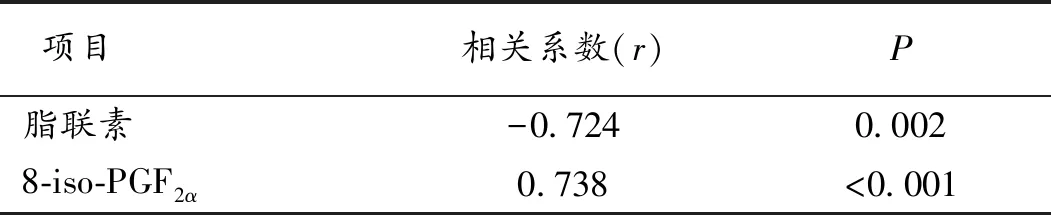
表3 LnTSH和脂聯素、8-iso-PGF2α的相關分析
3 討論
T2DM和甲減都是常見的內分泌系統疾病,二者共存也較常見[7]。本研究發現,T2DM伴甲減組較單純T2DM組脂聯素水平更低,多重線性回歸調整了年齡、性別、BMI、糖化血紅蛋白、血脂等混雜因素后,脂聯素和T2DM合并甲減負相關。既往研究表明,單純T2DM[8]、單純甲減[9]及妊娠糖尿病合并亞臨床甲減病人[10]的傳統炎性因子如白細胞介素-1(IL-1)、IL-6、腫瘤壞死因子-α(TNF-α)均增高。脂聯素是一種由脂肪細胞分泌的新炎性介質,具有抗炎作用,是目前新的調節炎癥反應的藥物靶點之一[11]。T2DM病人脂聯素水平低[12]。甲減大鼠模型的脂聯素也降低[13]。本研究發現,T2DM伴甲減組較單純T2DM組脂聯素水平更低,說明T2DM病人合并甲減后進一步降低了脂聯素的表達,具有協同作用。脂聯素水平下降,和傳統炎癥因子反應增高不同,說明T2DM合并甲減不僅存在促炎作用增強,還存在抗炎作用減弱。T2DM合并甲減后脂聯素進一步降低可能的機制是:(1)長期甲減病人相對缺氧會影響右心功能,導致交感神經系統活性增強,兒茶酚胺分泌增多,通過G(S)蛋白-PKA依賴途徑抑制脂聯素基因表達[14]。(2)甲減病人IL-6、TNF-α等傳統炎性因子增高,可抑制過氧化物酶增生物激活受體(PPAP)介導的脂聯素基因啟動子表達[15]。
本研究發現,T2DM伴甲減病人8-iso-PGF2α水平較高,說明T2DM合并甲減后氧化應激反應更明顯。有報道顯示,T2DM病人氧化應激反應增高[16]。但TSH水平和氧化應激關系的研究仍較少,且存在一定爭議。Coria等[17]報道,與甲功正常者相比,甲減病人中一氧化氮水平升高,而亞臨床甲減病人中無明顯改變,且甲減病人的對氧磷酶活性無明顯改變。而?ztürk等[18]報道,甲減和亞臨床甲減病人的氧化應激水平均增高。本研究單因素及多因素分析均顯示TSH和氧化應激呈正相關。
T2DM合并甲減發病率較高,但目前臨床上對其認識不足,應引起重視。本研究為T2DM合并甲減的調節炎癥、抗氧化及改善代謝紊亂等治療提供一定理論依據,具有重要的臨床意義。但本研究為橫斷面研究,未能證實T2DM合并甲減同脂聯素、氧化應激間的因果關系,需要進一步深入研究。

