乳腺癌組織長鏈非編碼RNA UCA1和BCAR4表達與輔助化療效果的相關性研究 *
王 碧,吉茂禮
(1.陜西省核工業二一五醫院檢驗科,陜西咸陽 712000;2.商洛市中心醫院檢驗科,陜西商洛 726000)
輔助化療可以使一部分乳腺癌患者獲得病理學完全緩解,延長患者的生存期[1]。研究表明,長鏈非編碼RNA(long non-coding RNA,lncRNA)尿路上皮癌相關1(urothelial carcinoma-associated 1,UCA1)和乳腺癌雌激素耐受基因4(breast cancer anti-estrogen resistance 4,BCAR4)與乳腺癌化療的耐藥機制有關[2]。本研究采用實時逆轉錄-聚合酶鏈反應(real-time reverse transcription-polymerase chain reaction,RT-PCR)技術分析30例乳腺癌患者組織UCA1和BCAR4的表達,旨在探討兩基因標志物與乳腺癌輔助化療效果的相關性。
1 材料與方法
1.1 研究對象 選取2016年12月~2018年12月在陜西省核工業二一五醫院和陜西省商洛市中心醫院接受輔助化療的局部晚期乳腺癌穿刺或活檢標本30例進行分析。年齡39~74歲,中位年齡52歲。依據化療效果分為有效組(20例)和無效組(10例)。所有患者均經病理組織學診斷為原發性乳腺癌,患者白細胞>3 000×109/L,符合輔助化療標準。排除標準:并發高血壓、糖尿病等慢性疾病,并發血液病或其他惡性腫瘤。本研究經陜西省核工業二一五醫院和陜西省商洛市中心醫院醫學倫理委員會審核批準,并得到所有患者的知情同意。
1.2 試劑和儀器 RT-PCR引物以及RNA提取試劑盒、逆轉錄試劑盒以及PCR試劑盒均購自廣州復能基因有限公司。血清CA153水平檢測采用羅氏Modular○RP800生化分析儀。
1.3 方法 血清CA153水平檢測采用電化學發光技術,參考值為0~25 ng/ml。組織UCA1和BCAR4表達檢測應用RT-PCR技術。
1.3.1 乳腺癌輔助化療:所有患者均行DA方案化療:多西他賽75 mg/m2,1次/3周,吡柔阿霉素50 mg/m2,1次/3周,環磷酰胺600 mg/m2,1次/3周,共化療6周。依據輔助化療的療效行保乳手術或乳房切除術。乳腺癌輔助化療療效評價標準[3],完全緩解:腫瘤完全消失,包括腋窩淋巴結;部分緩解:最長的腫瘤直徑減少30%;疾病進展:最長的腫瘤增長20%或出現新的腫瘤轉移灶;無變化:所有情況無變化。完全緩解和部分緩解者被納入有效組,疾病進展和無變化者被納入無效組。
1.3.2 標本收集與處理:所有患者于輔助化療后采集空腹靜脈血4 ml,分離血清于-80℃保存,用于CA153水平檢測。收集輔助化療后的穿刺或活檢標本,用于UCA1和BCAR4表達檢測。
1.3.3 RT-PCR:按照miRVana miRNA分離試劑盒說明書操作,提取乳腺癌組織的總RNA。引物采用ABI公司Primer Express Softwarev2.0設計,由華大基因公司合成。以U6作為內參照。BCAR4引物序列:F5’-CTGGTGTCGTGGA GTCGGCAATTCAGTGA-3’,R5’-GACCC AAIACGAGTCGGCAATTCAACT-3’。UCA1引物序列:F5’-CAAGGTTCATGACACTTGC-3’。R5’-GTCAATCCWCGCTGTAGCA-3’。U6引物序列:F5’-ACTTCTGAATGAGTGCTTCAG-3’,R5’-UGAAGCGCCTGGTGTTTAAACG-3’。PCR反應條件:預變性95℃10 s,95℃10 s,60℃20s,72℃10s共40個循環。以2-△Ct求得UCA1和BCAR4的相對表達量,△Ct=目的基因循環數-U6的循環數。
1.4 統計學分析 資料采用SPSS21.0軟件進行分析。UCA1,BCAR4和CA153的異常率分析以及乳腺癌臨床病理特征分析采用χ2檢驗,UCA1,BCAR4和CA153的表達或水平分析采用t檢驗。相關性分析采用Person法。以P<0.05為差異有統計學意義。
2 結果
2.1 乳腺癌組織UCA1,BCAR4及血清CA153分析結果比較 見表1。與無效組比較,有效組組織UCA1,BCAR4表達和血清CA153水平顯著降低,有效組三標志物的異常率也顯著降低。以上比較的差異均有統計學意義(均P<0.01)。乳腺癌輔助化療的有效率為66.6%。
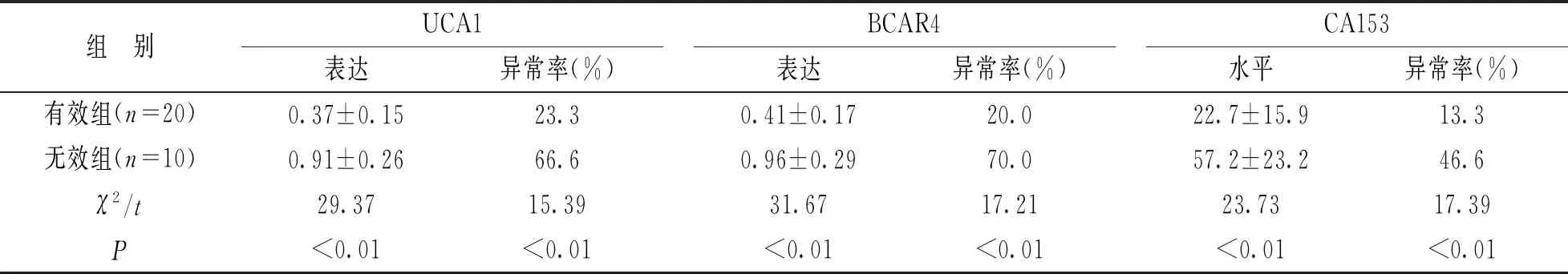
表1 乳腺癌組織UCA1,BCAR4及血清CA153分析結果比較
2.2 相關分析 見表2。在乳腺癌輔助化療無效組中,組織UCA1和BCAR4表達呈正相關性(r=0.839,P<0.01),兩標志物分別與血清CA153水平呈正相關性(r=0.817~0.832,均P<0.01)。組織UCA1表達與乳腺癌患者的年齡無相關性(P>0.05),而與腫瘤組織學分級和淋巴結轉移具有顯著相關性(均P<0.05)。BCAR4表達與乳腺癌患者的年齡和腫瘤組織學分級無相關性(均P>0.05),而與乳腺癌的淋巴結轉移有相關性(P<0.05)。

表2 乳腺癌臨床病理特征分析(%)
3 討論
輔助化療可以使乳腺癌患者獲得病理學緩解,但仍然有一部分的患者面臨進展的風險,并可能因此失去保乳手術的機會[4]。研究表明lncRNA中的BCAR4和UCA1與乳腺癌化療的耐藥機制密切相關。VAN AGTHOVEN等[1]研究認為BCAR4的高表達可能促進雌激素依賴型乳腺癌細胞的生長,上調組織BCAR4表達可以增加乳腺癌細胞對雌激素的敏感性,促進乳腺癌細胞對化療藥物的抵抗。研究表明,人類表皮生長因子受體(ErbB)是一種原癌基因,其在許多腫瘤組織中呈現高表達。組織中高表達的ErbB2和ErbB3可以刺激腫瘤細胞增殖,增強腫瘤細胞的侵襲性[5]。研究發現,上調人乳腺癌ZR-75-1細胞株內的BCAR4表達可以促進ErbB2和ErbB3的磷酸化,增強腫瘤細胞對雌激素的依賴作用,進而刺激腫瘤細胞的增殖[6]。有研究采用RT-PCR技術分析80例乳腺癌患者的結果顯示,BCAR4在乳腺癌組織中的表達顯著高于癌旁組織,而沉默BCAR4表達則可以抑制乳腺癌細胞的遷移和侵襲[7]。本研究結果顯示乳腺癌輔助化療有效組中BCAR4的基因表達較無效組顯著降低,BCAR4在有效組的異常率也顯著降低(P<0.01)。提示輔助化療可能降低乳腺癌細胞對雌激素的敏感性,促進乳腺癌細胞的凋亡。目前,有關BCAR4在乳腺癌輔助化療中的研究甚少,有待進一步地深入研究。
最近的研究證實UCA1對乳腺癌呈現明顯的促癌作用,并且調控多種腫瘤細胞如非小細胞肺癌、乳腺癌及肝癌細胞的化療敏感性。研究表明UCA1是乳腺癌的原癌基因,其在雌激素受體陽性及陰性的乳腺癌細胞中均呈現較高的表達[8]。LIU等[9]研究發現UCA1表達與乳腺癌的病理分級和死亡率呈正相關性。他們的研究認為UCA1通過調節Wnt信號通路影響腫瘤細胞的化療敏感性,在他莫昔芬耐藥的腫瘤細胞中Wnt信號活性和UCA1表達明顯增加。最近的報道認為,不均一核糖核蛋白Ⅰ可以促進乳腺癌細胞中UCA1的過表達,其作用機制可能為乳腺癌細胞中過表達的UCA1與p27競爭性結合不均一核糖核蛋白Ⅰ,導致p27表達受到抑制,進而促進乳腺癌細胞的生長[10]。LIU等[9]采用RT-PCR方法評估乳腺癌患者組織UCA1的表達,他們發現抑制UCA1表達則增強了乳腺癌細胞對化療藥物的敏感性并誘導更多的癌細胞凋亡,提示UCA1可能與乳腺癌化療的耐藥機制有關。本研究分析30例乳腺癌患者的結果顯示,有效組UCA1的基因表達和異常率與無效組比較顯著下調(P<0.01)。提示輔助化療可以使乳腺癌患者獲得部分緩解或完全緩解,進而延長患者的生存期。
CA153已被公認為乳腺癌的相關腫瘤標志物,其在乳腺癌組織中的表達明顯增高,并且在轉移病灶中也具有較高的異常率[11]。本研究的分析結果發現乳腺癌輔助化療有效組血清CA153水平及異常率較無效組顯著降低(P<0.01)。進一步地分析顯示UCA1和BCAR4表達有正相關性,且UCA1和BCAR4表達與CA153水平均有正相關性(P<0.01)。UCA1表達與腫瘤組織學分級和淋巴結轉移具有顯著相關性(P<0.05)。BCAR4表達與乳腺癌的淋巴結轉移有相關性(P<0.05)。以上提示UCA1和BCAR4可能參與了乳腺癌的發生和發展,其在乳腺癌組織中的差異性表達可以監測輔助化療的效果。
綜上所述,UCA1和BCAR4表達可能與乳腺癌輔助化療的耐藥機制有關,下調UCA1和BCAR4表達可以促進輔助化療的效果并有效緩解腫瘤的進展。

