討論目視比色法和分光光度法測鐵的分析
(連云港堿業有限公司,江蘇 連云港 222042)
鐵含量的分析法有目視比色法和可見分光光度法。目視比色法即用眼睛觀察比較溶液顏色深淺來確定物質含量的分析方法。目視比色法測定的準確度較差,相對誤差約為5%~20%,但由于它所需儀器簡單,操作簡便,仍廣泛應用于準確度要求不高的一些中間控制分析中,更主要的是應用在限界分析中。限界分析是指要求確定樣品中待測雜質含量在規定的最高含量限界以下。我公司重堿崗位中和水中鐵含量的分析符合此條件。可見分光光度法是生成有色化合物即"顯色"以后測定。顯色反應能否滿足分光度法的要求,除了選擇顯色劑以外,控制好反應條件是十分重要的。
1)顯色劑用量。顯色劑的適宜用量可通過試驗來確定。
2)溶液酸度。溶液的酸度對光度測定有顯著影響,必須控制溶液的pH值在一定范圍內,才能獲得恒定的有色配合物,得到正確的測定結果。
3)溫度的影響。溫度對光的吸收及顏色的深淺都有影響,因此在繪制標準曲線和進行樣品測定時,應溫度保持一致。
4)顯色時間。加入顯色劑后,有色配合物的形成需要一定時間,生成的有色配合物也很穩定,這類反應在完全顯色后放置一些時間進行測定。
5)共存離子的干擾及消除方法。溶液中有共存離子Fe3+時,加入還原劑抗壞血酸將Fe3+還原成Fe2+。
可見分光光度法在定量分析領域有著更為重要和廣泛的應用。我公司的成品純堿中鐵的分析適用此方法。
1 硫氰酸銨目視比色法
1.1 主題內容與應用范圍
本法則得樣品中的Fe2+、Fe3+均以Fe2O3計。
本法適用于中間產物的的Fe2O3分析。
1.2 原理
在酸性溶液中二價鐵和三價鐵都轉變成三價鐵離子,加入硫氰酸銨生成紅色絡合物,此顏色深淺與三價鐵離子的濃度成正比,可比色定量。
1.3 試劑
1.3.1 鹽酸溶液:1+1
1.3.2 甲基橙指示劑:1 g/L
1.3.3 硝酸溶液:1+1.7
1.3.4 10%硫氰酸銨溶液:稱取10.0 g NH4SCN溶于90 mL熱的純水中,溶解后,搖勻,備用
1.3.5 鐵標準溶液:1.00 mL含0.01 mg鐵
1.4 步驟
1)用移液管移取搖勻的樣品10.00 mL于250 mL燒杯中,加甲基指示劑(1 g/L) 1滴,用1+1鹽酸溶液中和至溶液呈紅色,加硝酸溶液(1+1.7 )1 mL,加純水20 mL,加熱蒸至溶液體積約剩10 mL,定量轉移至50 mL比色管中,向比色管中加10% NH4SCN溶液 5 mL,加純水至刻度,搖勻。
2)在另一比色管中,加硝酸溶液(1+1.7)1 mL,加10% NH4SCN 5 mL,加適量純水稀釋,用Fe標準溶液(1.00 mL含0.01 mg鐵)滴定至顏色和體積都與第1.4節1)中溶液相同。
1.5 計算
式中:V——滴加Fe標準溶液的體積,mL;
0.01——Fe標準溶液1 mL相當于Fe的毫克數。
注:若樣品溶液中Fe2O3的含量高時,可減少取樣體積。
2 分光光度法
2.1 主題內容與適用范圍
本標準規定了碳酸鈉中鐵含量的測定。
本標準適用于碳酸鈉生產過程中碳酸鈉中鐵含量的測定。
2.2 原理
用抗壞血酸將試樣中的三價鐵離子還原成二價鐵離子、在乙酸一乙酸鈉緩沖體系中,二價鐵離子與鄰菲啰琳,生成橙紅色絡合物、在最大吸收波長(510 mm)下用分光光度計測量其吸光度再從工作曲線中查出相應的百分含量。
2.3 試劑和溶液
本標準所用試劑和水、在沒有注明其他要求時,均指分析純試劑和蒸餾水或相應純度的水。
2.3.1 鹽酸:1+1溶液
2.3.2 鹽酸:1+11溶液
2.3.3 氨水:1+7溶液
2.3.4 對硝基酚:1 g/L溶液
2.3.5 乙酸-乙酸鈉緩沖溶液:pH≈4.5
2.3.6 稱取136 g乙酸鈉溶于水并稀釋至1000 mL為a溶液
2.3.7 量取120 mL冰乙酸稀釋至1 000 mL為b溶液
2.3.8 取a、b兩溶液以1:1的體積混合
2.3.9 抗壞血酸:20 g/L溶液此溶液使用期為十天,出現混濁時溶液不能使用
2.3.10 鄰菲啰琳: 2 g/L溶液,當有顏色產生時不能使用
2.3.11 硫酸鐵銨:稱取0.864 g硫酸鐵銨[NH4Fe(SO4)2·12H2O],溶于水,加10 mL硫酸溶液(1+3),移入1 000 mL容量瓶中,稀釋至刻度
2.3.12 鐵標準溶液:1 mL含Fe 0.100 mg
2.3.13 將2.3.12節中鐵標準溶液稀釋10倍,即得1 mL含Fe 0.0100 mg
2.3.14 無水碳酸鈉:優級純
2.4 測定步驟
2.4.1 標準參比溶液的配制
分別取7個100 mL干凈小燒杯,加10 mL水濕潤,依次加入0.00 mL、1.00 mL、2.00 mL、4.00 mL、6.00 mL、8.00 mL、10.00 mL鐵標準溶液(見2.3.13節),一滴對硝基酚指示劑(見2.3.4節),緩慢加入鹽酸溶液(見2.3.1節),至明顯黃色退去并過量五滴,煮沸2至3 min,冷卻后,滴加氨水(見2.3.3節)使溶液又呈現明顯黃色,再滴加鹽酸(見2.3.2節)至明顯黃色退去,再過量1.0 mL,將溶液移入100 mL容量瓶中,用水稀釋至刻度搖勻。
2.4.2 顯色
分別移取參比液(見2.4.1節)20.00 mL各置于50 mL容量瓶中,加2.5 mL抗壞血酸溶液(見2.3.9節)。10.0 mL乙酸-乙酸鈉緩沖液(見2.3.5節)和5.0 mL鄰菲啰琳溶液(見2.3.10節)用水稀釋至刻度搖勻。
2.4.3 吸光度的測定
使用分光光度計和1 cm的比色皿在510 nm波長時以水為對照進行吸光度的測定。
2.4.4 工作曲線的繪制
從測得的各個吸光度中減去試劑空白試驗的吸光度以鐵含量為橫坐標,以對應的吸光度為縱座標,繪制工作曲線。
2.4.5 測定
稱取試樣10.0 g,置于干凈小燒杯中,按照工作曲線制作程序測定吸光度,再從曲線上直接查出試樣中的鐵的百分含量。
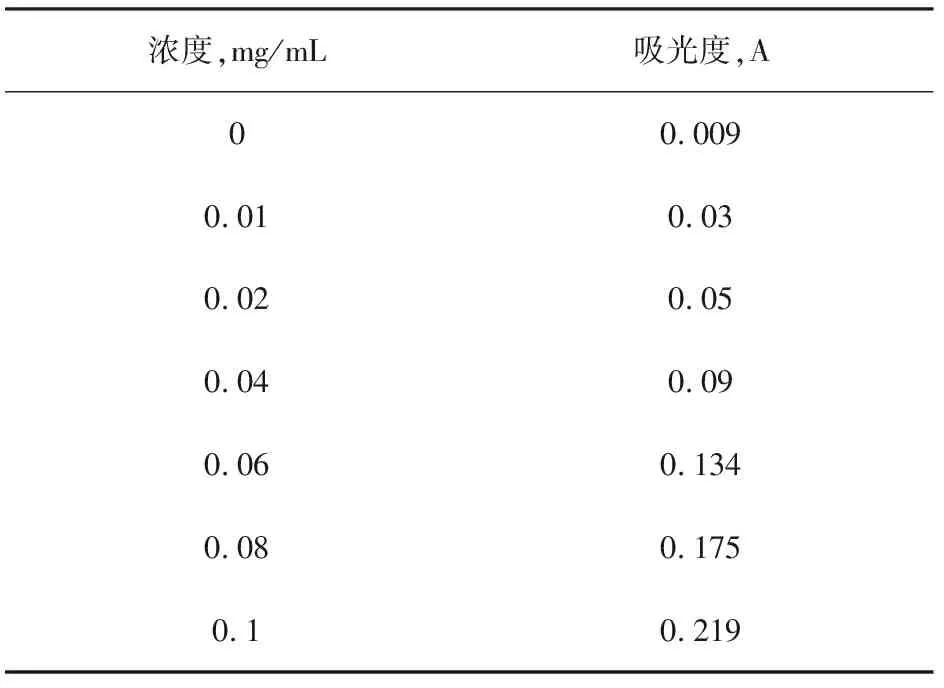
表1 吸光度測量結果
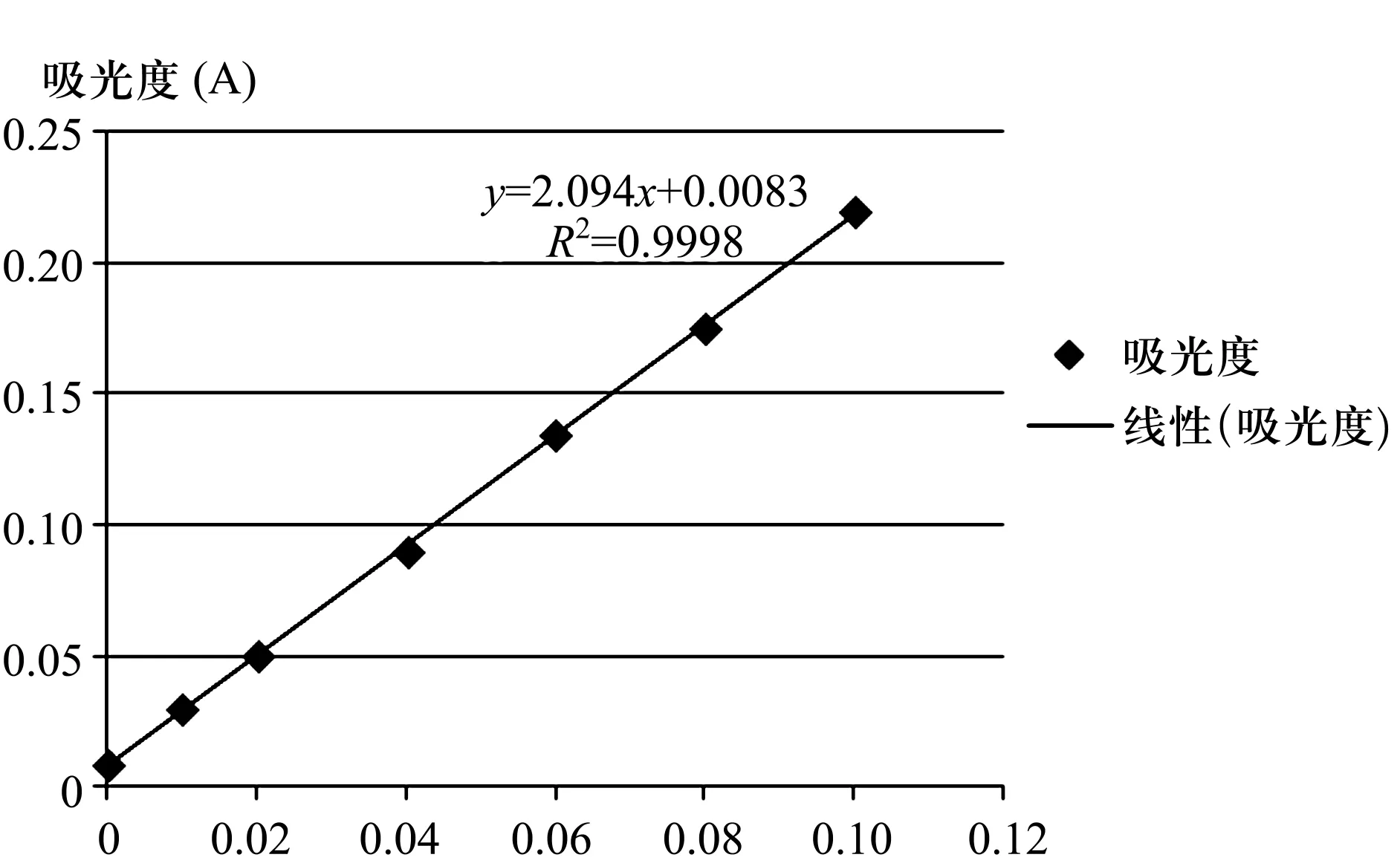
圖1 吸光度曲線
3 兩種方法對鐵含量分析對比
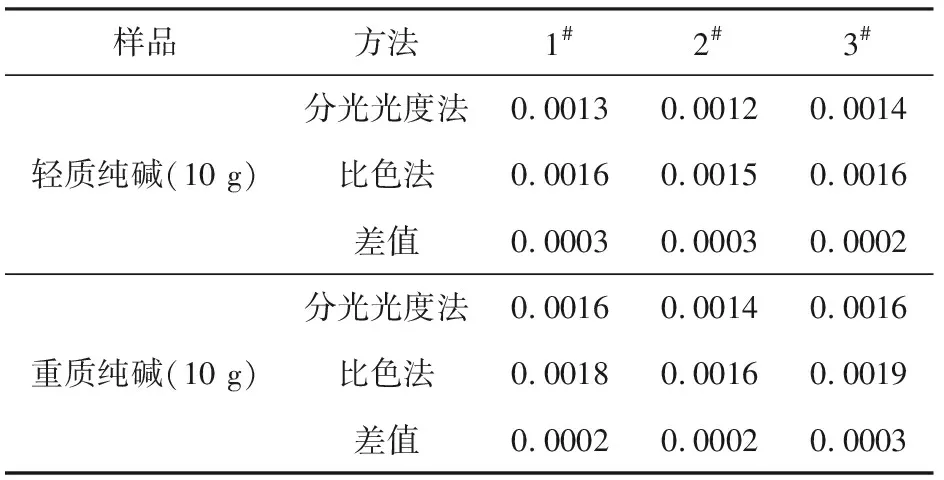
表2 對成品堿鐵含量分析的對比
試驗結論:從表2和表3數據上來看,比色法測定數據偏高,測定誤差較大,精密度、準確度都較低。
4 兩種方法的優劣性比較
從以上分析來看,比色分析法采用肉眼觀測,測定過程簡便,快捷,標準溶液、所需試劑的配制較容易,準確度、精密度要求低。中控分析中中和水的分析要求分析頻次高、速度快,精密度要求不高,便于中間控制的及時調節,比色分析法成本較低,所以中間控制宜采用目視比色法。
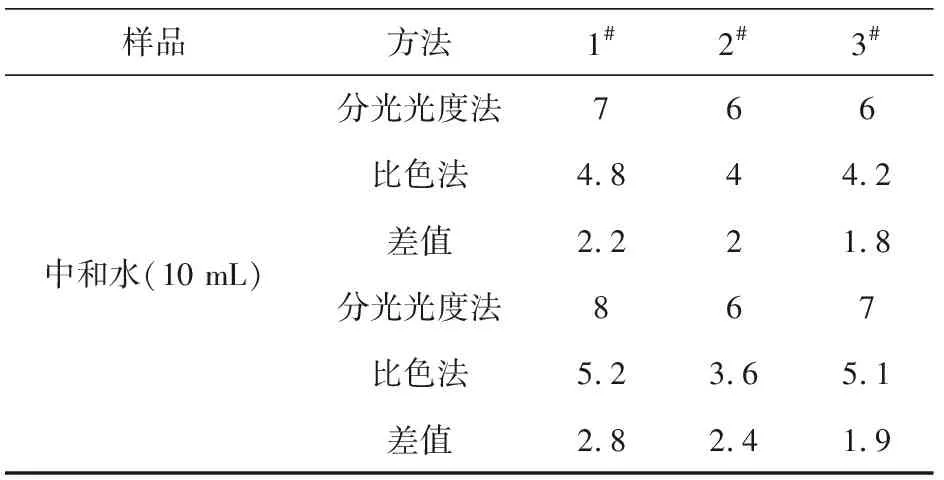
表3 對中和水鐵含量分析的對比
分光光度法采用儀器分析,分析過程要求仔細、精確、酸度控制要求高,儀器操作對操作人員的水平也有較高的要求,操作人員要懂得對儀器的使用、維護、保養、測定注意事項,數據的誤差要求小,精密度、準確度都要高。純堿質量的出廠檢驗或者仲裁檢驗的準確度和精密度要求均較高,因此宜采用分光光度法。
鐵含量的測定是純堿成品分析出廠檢驗指標中一項重要控制項目之一,鐵含量的高低直接影響純堿的白度,對外觀有重要的影響。而成品鐵含量的高低直接取決于中和水中鐵含量的多少,中和水中鐵含量高,重堿的鐵含量就高,進一步影響成品堿鐵份含量的高低。中控分析中鐵含量測定要求高頻次、及時、快速、準確,所以選用目視比色法就能滿足生產的要求。成品中鐵含量的分析要求準確度高,合格品和不合格品的劃分對經濟效益的影響較大,所以選用鐵曲線法(可見分光光度法)較合適。

