角鯊烯/γ-環糊精包合物制備及分子模擬
張光杰,谷令彪,周民生,袁 超,劉金洲
(1.安陽工學院生物與食品工程學院,河南 安陽 455000;2.齊魯工業大學食品科學與工程學院,山東 濟南 250353)
角鯊烯又名鯊烯、三十碳六烯、魚肝油萜,化學名為2,6,10,15,19,23-六甲基-2,6,10,14,18,22-二十四碳六烯,由Tsujimoto于1906年在黑鯊魚肝油中發現,是一種高度不飽和烴類化合物[1]。在常溫下,角鯊烯為油狀的無色液體,不溶于水,難溶于冰醋酸、乙醇和甲醇,易溶于四氯化碳、乙醚、丙酮、石油醚等有機溶劑,因其含6 個非共軛雙鍵,因此極不穩定,很容易氧化。角鯊烯具有提高體內超氧化物歧化酶活性、增強機體免疫能力、改善性功能、抗衰老、抗疲勞、抗腫瘤等多種生理功能[2],因此,被廣泛應用于醫藥、化妝品和食品行業[3],但由于其水溶性較差、易被氧化等,使其在具體應用過程中受到了嚴峻挑戰。雖然已有膠囊產品問世,但多數以保健品形式銷售,產品品種單一。筆者前期研究發現可以通過環糊精分子包埋技術改善其水溶性并已成功應用于營養果凍的研發制作。
環糊精是由環糊精葡萄糖殘基轉移酶[4]作用于淀粉、糖原、麥芽寡聚糖等葡萄糖聚合物后形成的由6~12 個D-吡喃葡萄糖基以α-1,4-糖苷鍵連接而成的低聚糖,由于其具有內疏水外親水的特性,所以可通過氫鍵、范德華力、疏水作用等分子間作用力與多種有機化合物形成包合物,并可改變被包合物的物理及化學性質。常見的環糊精種類主要有α-、β-、γ-環糊精。其中,γ-環糊精因其分子內腔空間較大而被廣泛應用于食品及醫藥[5-7]等領域。而有關環糊精包埋角鯊烯的文獻鮮有報道,已有研究制備了角鯊烯/環糊精包合物[8],但是并未對其包合機理進行相關研究。
鑒于此,本實驗通過水溶液法結合冷凍干燥法制備角鯊烯/γ-環糊精包合物,并對其進行相溶解度、傅里葉變換紅外光譜(Fourier transform infrared spectroscopy,FTIR)分析、氫譜核磁共振(hydrogen nuclear magnetic resonance,1H NMR)分析及分子模擬,以期探索包合物的形成機理,改善角鯊烯在水溶性環境中的溶解效果,并為擴大角鯊烯的應用范圍提供理論依據及參考。
1 材料與方法
1.1 材料與試劑
角鯊烯標準品(純度>99%) 北京寰宇科創生物科技發展有限公司;γ-環糊精(純度>99.0%) 東京化成工業株式會社;正己烷(色譜純) 天津賽孚瑞科技有限公司。
1.2 儀器與設備
2010-Plus氣相色譜儀(配有氫火焰離子檢測器和色譜工作站) 日本島津企業管理有限公司;Tensor II FTIR儀、AM-400型1H NMR分析儀 德國布魯克科技有限公司;FA2004B電子天平 上海佑科儀器儀表有限公司;KQ-200VDE型三頻數控超聲波清洗器 昆山市超聲儀器有限公司;TH70-85-2磁力攪拌器 余姚市東方電工儀器有限公司。
1.3 方法
1.3.1 包合物的制備
采用水溶液法參考相關文獻[9]制備包合物。稱量一定量的γ-環糊精溶于25 mL蒸餾水中,使其形成40 mmol/L的γ-環糊精溶液,將角鯊烯緩慢滴加在γ-環糊精溶液中(參照文獻[8]按照主客物質的量比為3∶1添加)并超聲振蕩15 min。在40 ℃條件下磁力攪拌72 h即可得到包合物溶液。靜置1 h,用吸油紙去除溶液表面未包合的角鯊烯油滴,置于-60 ℃、100 Pa條件下凍干,得到角鯊烯/γ-環糊精包合物粉末。
1.3.2 包合物的表征
1.3.2.1 相溶解度測定
參照相關文獻[10-11]對包合物進行相溶解度測定。稱取一定量的γ-環糊精溶于25 mL蒸餾水中,分別配制濃度為0、10、20、30 mmol/L和40 mmol/L的環糊精溶液,并按主客物質的量比1∶1.5的比例向其中滴加過量的角鯊烯,超聲振蕩15 min,分別在25、40 ℃及55 ℃條件下磁力攪拌72 h,得到包合物溶液。取5 mL包合物溶液,向其中加入10 mL正己烷,超聲萃取10 min。靜置后經0.45 μm有機濾膜過濾后用氣相色譜檢測得到包合物中角鯊烯含量。
氣相色譜條件參照相關文獻[12-14],具體條件如下:Rtx-5毛細管柱(30 m×0.25 mm,0.25 μm);升溫程序:150 ℃維持1 min,15 ℃/min升溫至250 ℃維持12 min;載氣為99.999% N2,空氣流速400 mL/min,氫氣流速40 mL/min,分流比1∶10;進樣口溫度250 ℃;進樣口壓力204 kPa;氫火焰離子檢測器溫度290 ℃;進樣量1 μL;定量方法為峰面積歸一化外標法。
以環糊精的濃度為橫坐標,角鯊烯的溶解度為縱坐標,繪制相溶解圖,并計算包合常數、增溶因子(S/S0,S及S0分別為角鯊烯在環糊精溶液及水中的溶解度)[15]及熱力學參數,按式(1)~(3)計算:
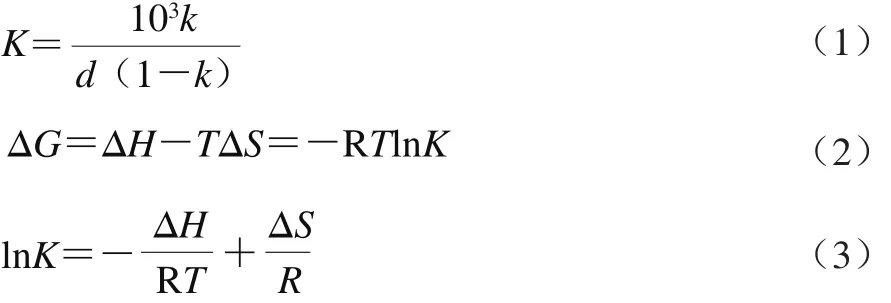
式(1)中:K為包合常數/(L/mol);k為相溶解度圖中線性回歸方程的斜率;d為相溶解度圖中線性回歸方程的截距/(mmol/L)。
式(2)中:ΔG為反應的吉布斯自由能/(J/mol);Δ H為反應的焓變/(J/m o l);R為氣體常數,8.314 J/(K·mol);T為熱力學溫度/K;ΔS為反應的熵變/(J/(K·mol))。
根據式(3),將lnK對1/T作圖,通過線性擬合得到直線的截距可計算ΔS。
1.3.2.2 FTIR分析
將約1 mg樣品(γ-環糊精和角鯊烯/γ-環糊精包合物)置于盛有約100 mg干燥溴化鉀的瑪瑙研缽中充分混合并研磨成細粉末。然后將樣品裝入模具中壓成片狀,并置于FTIR儀中進行測試。通過向溴化鉀片劑中加入1滴角鯊烯制備角鯊烯片劑樣品。
1.3.2.31H NMR分析
用核磁共振波譜儀在500 MHz、25 ℃條件下記錄1H NMR譜。將角鯊烯、包合物和γ-環糊精分別溶解在氘代二甲基亞砜中,置于內徑為5 mm的核磁管中,分別進行測試。并根據包合物1H NMR圖譜中呈現的各基團圖譜的積分面積計算包合物中主客物質的量比[16-17]。
1.3.3 分子模擬
用Hyperchem8.0構建角鯊烯、γ-環糊精及不同主客物質的量比(1∶1、2∶1、3∶1、4∶1、5∶1)包合物的分子結構模型,并選擇PM3方法用共軛梯度優化器對各分子模型的能量進行最小化運算,直到得到0.01 kcal/(mol·?)的均方根值[18]。模擬條件為300 K,1 個大氣壓,最小能量模型的ΔE按式(4)計算:

式中:E主、E客和E包分別為γ-環糊精、角鯊烯和包合物的計算能量/(kcal/mol)。
2 結果與分析
2.1 相溶解度分析

圖1 角鯊烯在不同溫度下γ-環糊精溶液中的相溶解圖Fig. 1 Phase dissolution diagrams of squalene in γ-cyclodextrin solutions at different temperatures
由圖1可知,在25、40 ℃及55 ℃下,在0~40 mmol/L范圍內,角鯊烯在γ-環糊精溶液中的相溶解圖為AL型[19],即形成的包合物主客物質的量比為1∶1,不同于文獻[8]報道的γ-環糊精與角鯊烯可形成主客比近似為2.68∶1的包合物,這可能與包合物制備條件不同有關。

表1 角鯊烯在不同溫度下γ-環糊精溶液中的包合常數、增溶因子及熱力學參數Table 1 Inclusion constants, solubilization factors and thermodynamic parameters of squalene in γ-cyclodextrin solution at different temperatures
包合過程是一個動態平衡的過程,即包合與解離同時存在。而包合常數K值是決定包合物性質的一個重要參數,其大小能夠反映環糊精和角鯊烯形成包合物過程中結合力的強弱,所以,K值可對包合過程作出定量描述。一般K值越大說明環糊精的包合效果越明顯,增大客體分子溶解度的能力越強。由表1可看出,包合常數K隨著溫度的升高而增大,表明所形成的包合物越來越穩定,這是由于分子熱運動隨溫度的升高變得更加劇烈,有利于角鯊烯進入環糊精的空腔內,從而使反應向有利于包合的方向進行,這與相關研究[20-21]結論一致。
通過比較表1中各增溶因子可知,在本實驗條件下,γ-環糊精對角鯊烯的增溶效果隨溫度的升高和濃度的增加而增強,且最大可使角鯊烯的溶解度提高為原來的309 倍。這個結果可能與溫度升高使分子運動更加劇烈及環糊精濃度增加使主客體包合的幾率增加有關。
由表1可看出,ΔH為正值,表明包合反應為吸熱反應,ΔS為正值,表明包合過程是無序化程度升高的熵增加的過程。由熱力學第2定律可得,當環糊精的空腔容納疏水性客體分子前需要脫去水殼,此時會釋放結合水,進而被客體分子取代,這個過程會引起熵的正變,說明疏水作用在整個包合過程中起著重要作用[22]。此外,該過程是吸熱反應,但客體分子與環糊精空腔內壁之間通過范德華力和分子間氫鍵力的相互作用是放熱反應。本實驗中,熵增加期間吸收的熱量可能大于主-客體絡合反應釋放的熱量,從而導致正焓變[23-24],即溫度升高所帶來的無序化增加較之包合過程釋放的反應熱而引發的焓變更為明顯,因此,熵增加對整個包合反應的影響更大些。ΔG為負值表明包合反應是一個自發過程[25],ΔG隨著溫度的升高而呈負增加,表明溫度的升高增加了形成包合物的自發傾向,而溫度升高也是增加無序化(熵增加)的過程。因此,從能量變化可以推斷,無序化增加(熵增加)是角鯊烯分子進入環糊精空腔的主要驅動力。
2.2 FTIR分析

圖2 角鯊烯(A)、包合物(B)及γ-環糊精(C)的FTIR圖譜Fig. 2 FTIR spectra of squalene (A), inclusion complex (B) and γ-cyclodextrin (C)
FTIR可通過分子的振動和旋轉躍遷識別和分析化合物。主體和客體分子的IR吸收峰的變化可以提供關于包合物形成的重要信息。
如圖2A線所示,2 968 cm-1和2 853 cm-1處非常強的吸收峰為—CH3的伸縮振動峰,2 919 cm-1處為—CH2—的不對稱伸縮振動峰,1 669 cm-1處為=CH—的伸縮振動峰,1 444 cm-1處為與雙鍵相連的CH2的變形振動峰,1 381 cm-1處為—CH3中C—H的變形振動峰,836 cm-1處為=CH—中C—H的非平面搖擺振動峰,上述結果與文獻[26]報道一致。
另外,包合物的紅外光譜(圖2B線)與γ-環糊精(圖2C線)非常相似。γ-環糊精的主要特征吸收峰有:3 384 cm-1左右為γ-環糊精上—OH的伸縮振動;2 926 cm-1為—CH3及—CH2—中C—H的伸縮振動;1 645 cm-1左右為結合水的振動;1 367、1 336、1 304 cm-1為—CH3及—CH2—中C—H的彎曲振動;1 156 cm-1左右為C—O—C的反對稱伸縮振動;1 079、1 026 cm-1左右為C—C或C—O的伸縮振動,此結果與文獻[27]報道相符。而在包合物的紅外譜圖中角鯊烯的部分特征吸收峰(2 919、1 669 cm-1及1 444 cm-1)消失,這些譜帶由于與更強的γ-環糊精譜帶重疊而被掩蓋。然而,在836 cm-1處的吸收峰表現出強度降低及輕微的偏移,這可能與角鯊烯分子中雙鍵上的C—H的非平面搖擺振動在包含物形成后受限制并且包合物中的客體含量較低有關。上述信息表明角鯊烯分子中的雙鍵進入γ-環糊精的空腔,間接證實了角鯊烯被γ-環糊精成功包埋。
2.3 1H NMR分析
1H NMR可以提供關于客體分子在環糊精腔內空間位置的有價值的信息。H-3和H-5是環糊精腔內壁中的質子,當客體分子進入環糊精空腔時,由于客體分子與環糊精疏水內腔之間的相互作用,會使H-3和H-5質子的化學位移發生變化[28]。結合圖3、表2可以看出,角鯊烯分子進入γ-環糊精分子空腔后,γ-環糊精的質子發生明顯的化學位移,角鯊烯的質子在包合物的圖譜上峰高和峰面積也發生很大變化。γ-環糊精的質子H-3和H-5、OH-2和OH-3及OH-6均發生明顯偏移,分析原因可能是包合物形成后,角鯊烯分子進入γ-環糊精空腔內部,由于客體分子雙鍵環電流的影響使得位于γ-環糊精空腔內壁的H-3和H-5電子屏蔽作用減小,移向低場,化學位移值增大,且二者化學位移相差不大,可見角鯊烯分子進入γ-環糊精空腔內的入口(大口端或小口端)是沒有明確的選擇性的[29-30]。同時由于角鯊烯分子上雙鍵的屏蔽效應,使得OH-2、OH-3及OH-6周圍的電子云密度增加,化學位移減小,移向高場,這些變化表明包合物已成功形成。結合上述紅外光譜分析結果及角鯊烯的結構特點,可以推測角鯊烯的部分雙鍵結構進入γ-環糊精空腔內部。而對于H-2和H-4,由于δ3.3附近水分的強質子峰(可能與樣品未充分干燥有關)的存在覆蓋了H-2和H-4的質子信號,無法對其進行準確分析。

圖3 角鯊烯(A)、包合物(B)及γ-環糊精(C)的1H NMR圖譜Fig. 3 1H NMR spectra of squalene (A), inclusion complex (B) and γ-cyclodextrin (C)

表2 γ-環糊精及角鯊烯分子中特征基團的化學位移Table 2 Chemical shifts of characteristic groups in γ-cyclodextrin and squalene molecules
另根據包合物1H NMR圖譜中呈現的各基團圖譜的積分面積計算包合物中主客物質的量比約為3.45∶1,此結果既不同于上述相溶解度結果顯示的1∶1,也不同于相關文獻[8]報道的2.68∶1。這進一步印證了環糊精分子包合客體分子是一個復雜的動態過程,不同的客體分子結構、主客體的相對用量、不同的包合條件都會影響到包合物的分子結構。上述主客物質的量比差異可能是由于分子結構呈鏈狀的角鯊烯分子在溶液環境中的分子熱運動很容易進入γ-環糊精相對寬廣的內腔,但是也很容易“溜走”,即包合解離同時存在,并且相溶解度實驗中角鯊烯過量,因此更多的包合物主客物質的量比近似為1∶1形式;而本研究中用于1H NMR分析的角鯊烯/γ-環糊精包合物樣品在制備過程中是按照主客物質的量比3∶1添加的,可以有更多γ-環糊精空腔可供選擇,且一旦形成多個環糊精分子包合同一個角鯊烯分子的包合物結構,相對于主客物質的量比1∶1的包合物要穩定一些,另3.45∶1的主客物質的量比為平均值,說明形成的包合物是含有多個主客物質的量比的混合物;與文獻[8]報道的2.68∶1的差異主要與包合物的制備條件(主客物質的量比、包合時間、溫度、主客體攪拌的激烈程度等)差異有關。
2.4 分子模擬結果

圖4 角鯊烯(A)、γ-環糊精(B)及不同主客物質的量比的包合物分子(C~F)模擬模型Fig. 4 Molecular simulation models of squalene (A), γ-cyclodextrin (B)and inclusion complex (C-F) with different host to guest molar ratios

表3 不同主客物質的量比包合物的最小能量模型的ΔETable 3 ΔE of minimum energy model for inclusion complexes with different host to guest molar ratios kcal/mol
目前,基于分子力學的分子模擬已被廣泛應用于表征包合物與環糊精的三維結構[31]。通過上述FTIR和1H NMR分析,可以基本確定角鯊烯/γ-環糊精包合物的主客體分子結合形式,角鯊烯鏈狀分子通過大口端(或小口端)進入γ-環糊精空腔,且部分雙鍵位于γ-環糊精的H-3及H-5附近,而其余長鏈部分位于空腔外。通過Hyperchem 8.0構建并優化的角鯊烯和γ-環糊精的結構見圖4A、B,不同主客物質的量比的包合物分子模型及其ΔE分別見圖4C~F及表3。結果表明,角鯊烯分子呈稍彎曲的鏈狀時較為穩定,且隨著主客物質的量比的增加,角鯊烯分子將γ-環糊精分子均勻地“串聯”在一起形成包合物分子,包合物的ΔE逐漸降低,分子結構趨于穩定,但是當主客比增加到5∶1時,E包及ΔE突然增大為正值,且包合物分子模型中主客體相互遠離(圖4未顯示),包合物變得不穩定。究其原因可能是由于雖然角鯊烯鏈狀分子可以同時“串聯”多個γ-環糊精分子,但是當“串聯”的γ-環糊精分子過多時會導致相鄰的環糊精分子間斥力增大,而主客體結合的作用力又比較弱,導致分子間距離突然增大,并影響到整個包合物的穩定。因此,從分子模擬角度而言,最佳主客物質的量比為4∶1,這與上述1H NMR圖譜積分分析的的結果(3.45∶1)較為接近。
3 結 論
應用水溶液法結合冷凍干燥法制備角鯊烯/γ-環糊精包合物,并通過相溶解度、FTIR、1H NMR分析及分子模擬對γ-環糊精包合角鯊烯的機理進行研究。結果顯示,角鯊烯被γ-環糊精成功包埋,且在客體分子過量的情況下,可與γ-環糊精形成主客物質的量比1∶1的包合物,而當γ-環糊精過量時,可形成主客物質的量比3.45∶1的包合物。相溶解度及熱力學參數分析結果表明,γ-環糊精對角鯊烯增溶效果明顯,最大可提高至原來的309 倍;包合常數隨溫度升高而增大,整個包合過程釋放的反應熱較小,呈自發的吸熱反應,溫度升高導致的無序化增加(熵增加)是包合反應的主要驅動力。分子模擬結果表明,包合物的分子結構為角鯊烯鏈狀分子將γ-環糊精環狀分子均勻地“串聯”在一起,且最佳主客物質的量比為4∶1,但大于4∶1后包合物分子結構突然變得不穩定,具體機理仍有待進一步研究。本研究對于進一步闡明環糊精包合角鯊烯的機理具有重要的指導意義,并可為擴大角鯊烯在食品、化妝品及醫藥等領域水溶性環境中的應用提供理論依據及參考。

