十溴二苯乙烷對部分血糖內分泌干擾的計算機輔助理論研究
張天慶,楊秀榕,曾凡剛,張嚴,*
1. 中央民族大學生命與環境科學學院,北京 100081 2. 中國人民大學環境學院,北京 100872
十溴二苯乙烷(decabromodiphenyl ethane, DBDPE)是一種高效、環保的溴代阻燃劑,長期以來被人們認為難以進入環境以及生物體內并產生蓄積。然而,在2003年,Kierkegaard等[1]首次從下水道淤泥中檢測出DBDPE。隨后一些調查表明DBDPE已廣泛分布在水、空氣和土壤中[2-7]。何明靖等[7]通過對鹵系阻燃劑在東江魚體中的生物富集研究發現DBDPE在東江魚體內的富集能力較強,余樂洹等[8]在我國北京地區的紅隼體內發現DBDPE的存在,任子賀等[9]在對水生和陸生生物體中鹵系阻燃劑的差異性富集研究中,發現DBDPE在鯰魚和家鴿中存在,綜合以上以及其他的調查研究可知,DBDPE已經廣泛存在于生物體內。另外,有研究表明DBDPE已進入食物鏈中[10-11]。Wang等[12]在對中國北京室內塵埃中溴系阻燃劑研究中發現,DBDPE已經成為主要的溴系阻燃劑,并且DBDPE的中值水平不僅比其他新型溴系阻燃劑高出幾個數量級,而且比3種傳統溴系阻燃劑高出3~27倍。另外,還有研究表明人會通過呼吸、飲食等方式攝入DBDPE[13]。目前,DBDPE使用量逐年增長,在環境和生物體內的蓄積程度呈上升趨勢,而且帶來的健康風險性較高,因此部分學者對其展開了毒理學和流行病學研究。
Jin等[14]使用斑馬魚作為體內模型評價了DBDPE的毒理學效應,結果顯示,在短期暴露于不同濃度DBDPE污染的沉積物時,斑馬魚的死亡率和畸形率均未受影響,但是DBDPE對斑馬魚幼魚具有低神經毒性,該研究結果揭示了DBDPE在實際環境中的潛在風險。韓倩等[15]通過DBDPE對草魚幼魚肝臟和肌肉組織氧化應激效應的影響研究發現,DBDPE暴露影響草魚幼魚肝臟組織的抗氧化防御系統,可以誘導草魚幼魚產生氧化應激效應。Sun等[16]對BALB/c小鼠進行不同劑量的DBDPE灌胃給藥,30 d后,處死小鼠,取血、肝臟和甲狀腺,分離肝微粒體,測定血糖、胰島素和甲狀腺激素水平,結果表明,DBDPE除了可引起一定程度的肝臟損傷和肝功能不全外,還具有內分泌干擾活性,而且DBDPE的內分泌干擾活性會影響血糖代謝水平,但目前其作用機制尚未得出。為了探究其具體機制,縮短研究時間,降低研究成本,本文采用計算機輔助研究的方法對DBDPE影響血糖的代謝機制進行探究,為后續的實驗研究提供理論依據。
當前已進行的體內外研究和流行病學研究結果顯示,內分泌干擾物(EDCs)可通過干擾生物體內分泌過程來影響機體的生理過程,其發揮干擾作用時,一是直接作用于機體內受體,干擾機體對外源性化學物質的代謝,進而引起機體本身的代謝紊亂;二是直接作用于機體特異性代謝受體,形成同型二聚體或異二聚體,進而與特定的靶基因結合,干擾下游基因的表達,進而干擾胰島素等激素水平,從而影響機體的正常代謝[17]。機體的內分泌通路中與血糖相關的有芳香烴受體介導、雌激素、孕激素、甲狀腺激素和雄激素等內分泌通路[18-21],因此,本文采用上述通路所提及的與血糖相關的受體進行研究,以探究出DBDPE是否與這些受體結合而發揮干擾內分泌作用而影響機體正常代謝,進而影響機體血糖代謝。具體過程是將DBDPE與雌激素受體(estrogen receptors, ERs)包括ERα和ERβ、孕激素受體(progesterone receptor, PR)、甲狀腺激素受體(thyroid hormone receptor, TR)包括TRα和TRβ、雄激素受體(androgen receptor, AR)、芳香烴受體(aryl hydrocarbon receptor, AhR)進行分子對接實驗(圖1)。另外,基于DBDPE類似物(均為EDCs)分子的三維結構以及Richards[22]和Chen等[24]提供的這些分子的EC50(根據實驗要求將該活性數值轉換為-logEC50),采用比較分子力場分析法(CoMFA)構建3D-QSAR模型,CoMFA是構建3D-QSAR模型的主要方法之一,由于其預測能力強,模型形象直觀而受到廣泛應用[23,25]。在進行實驗時,首先綜合考慮CHARMM力場和靜電場等對這些分子進行場疊合,再對能量網格電位進行濾波,去除高度相關的描述符,之后使用剩余的描述符來建立偏最小二乘(PLS)模型,即3D-QSAR模型,以此預測未知內分泌干擾物的干擾活性,這為實驗研究提供了理論依據。
1 材料與方法(Materials and methods)
1.1 實驗材料
DBDPE及其類似物的結構數據來源于PubChem數據庫,分子對接實驗所需的全部受體結構來源于PDB蛋白質晶體結構數據庫,DBDPE類似物的活性數據來源于Richards[22]和Chen等[24]等的研究。所有分子對接計算以及構建3D-QSAR模型均在寶德RR2510N計算機工作站完成,所用軟件采用美國Accelrys公司研發的Discovery Studio(DS)3.5分子設計軟件包,計算中選用的各項參數除特別說明外均使用缺省值。

圖1 實驗所需受體結構與十溴二苯乙烷(DBDPE)結構注:Erα為雌激素受體α,來源于文獻[26];Erβ為雌激素受體β,來源于文獻[27];PR為孕激素受體,來源于文獻[28];TRα為甲狀腺激素受體α,來源于文獻[29];TRβ為甲狀腺激素受體β,來源于文獻[30];AhR為芳香烴受體,來源于文獻[31];AR為雄激素受體,來源于文獻[32]。Fig. 1 Receptor structure and decabromodiphenyl ethane (DBDPE) structure in receptor-ligand interactionsNote: ERα is estrogen receptor α and refers to literature [26]; ERβ is estrogen receptor β and refers to literature [27]; PR is progesterone receptor and refers to literature [28]; TRα is thyroid hormone receptor α and refers to literature [29]; TRβ is thyroid hormone receptor β and refers to literature [30]; AhR is aryl hydrocarbon receptor and refers to literature [31]; AR is androgen receptor and refers to literature [32].
1.2 實驗方法
1.2.1 分子對接實驗
本部分以ERα為例,用DS3.5軟件首先進行DBDPE與ERα的預處理,具體過程是:利用Small Molecules模塊中Prepare or Filter Ligands功能對DBDPE進行結構優化并將其定義為配體分子;點擊Chemistry進行ERα的加氫處理,在蛋白質的結構面板內刪掉水分子,利用Define and Edit Binding Site功能定義ERα為受體分子,并找到結合位點(12個)。
然后進行分子對接實驗,具體過程是:
(1)用DS3.5軟件中Receptor-Ligand Interactions模塊的Lib Dock功能進行剛性對接實驗,在調整參數時,除Max Hits to Save參數設為10(以縮短計算時間),其余均為默認值,對接結果顯示,ERα的12個結合位點中有5個能夠與DBDPE完成剛性對接;
(2)用Receptor-Ligand Interactions模塊中的Ligand Fit功能在剛性對接得到的5個結合位點的基礎上進行半柔性對接實驗,在調整參數時,輸入的結合位點更改成能夠完成第一步對接的5個結合位點,結果只有2個結合位點能夠完成半柔性對接;
(3)用Receptor-Ligand Interactions模塊中的Flexible Docking功能在半柔性對接得到的2個結合位點的基礎上進行全柔性對接實驗,根據實驗結果的打分函數來評估ERα與DBDPE的結合情況。
1.2.2 構建3D-QSAR模型
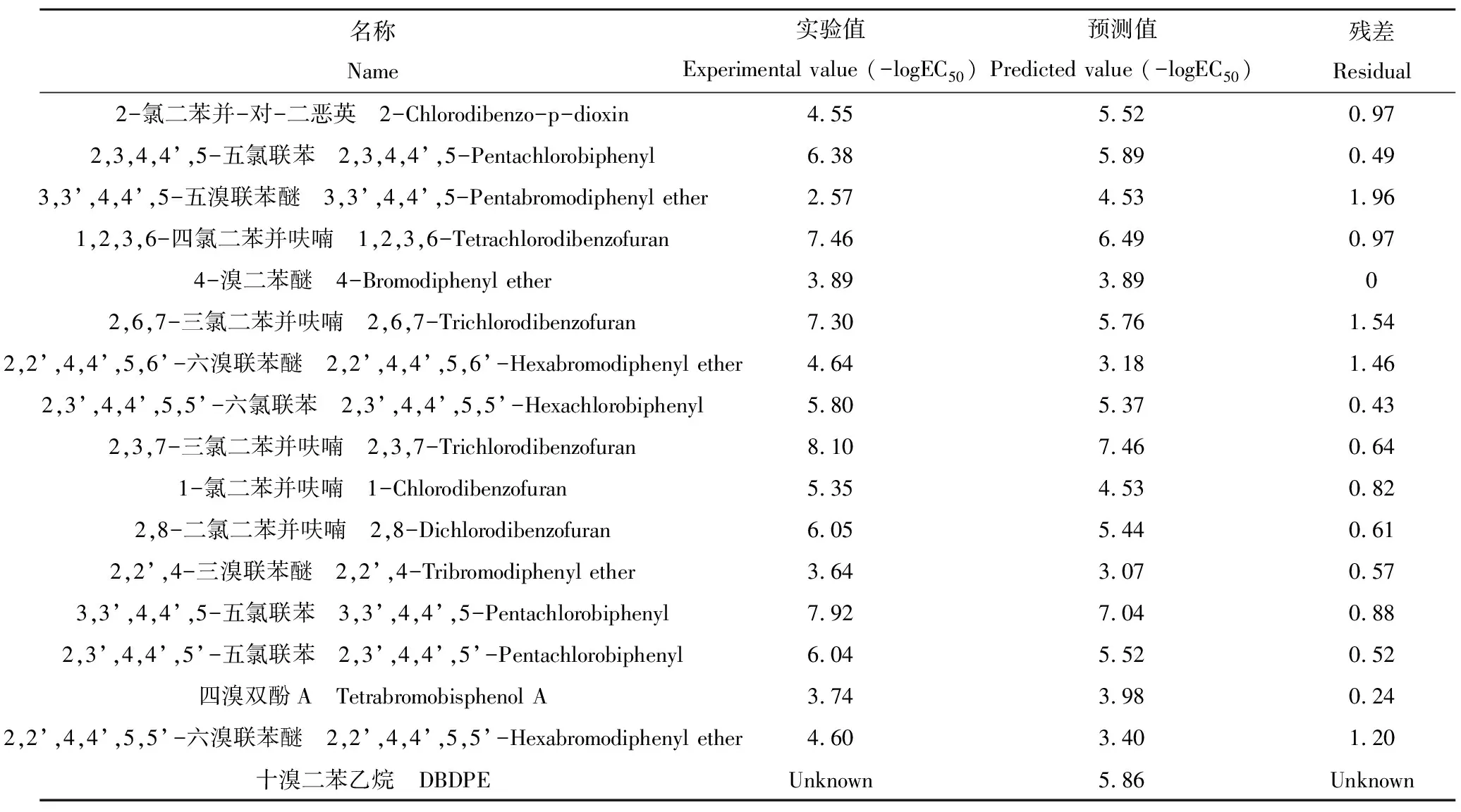
軟件中導入DBDPE的類似物,輸入半最大效應濃度的負對數值(-logEC50),進行預處理,再將其分為訓練集(如表1)和測試集,利用Small Molecules模塊中的Create 3D QSAR Model功能構建DBDPE類似物的3D-QSAR模型。
2 結果與討論(Results and discussion)
2.1 分子對接結果
在剛性對接的過程中,DBDPE能夠在ERα的5個結合位點、ERβ的6個結合位點、PR的4個結合位點、TRα的2個結合位點、TRβ的1個結合位點、AR的2個結合位點以及AhR的2個結合位點處與相應受體結合。在半柔性對接的過程中,DBDPE能夠在ERα的2個結合位點,ERβ的2個結合位點,PR的3個結合位點,TRα的1個結合位點處與相應受體結合(表2)。

表1 訓練集的分子結構和活性數據Table 1 The structure and activity data of training set molecules

續表1名稱Name-logEC50結構Structure2,2’,4,4’-四氯聯苯2,2’,4,4’-Tetrachlorobiphenyl4.092,3,7,8-四氯二苯并呋喃2,3,7,8-Tetrachlorodibenzofuran8.122,3,4,5-四氯聯苯2,3,4,5-Tetrachlorobiphenyl4.853,3’,4,4’-四氯聯苯3,3’,4,4’-Tetrachlorobiphenyl7.372,3,6,8-四氯二苯并呋喃2,3,6,8-Tetrachlorodibenzofuran7.662,3,3’,4,4’-五氯聯苯2,3,3’,4,4’-Pentachlorobiphenyl5.852,2’,4,4’,5,5’-六氯聯苯2,2’,4,4’,5,5’-Hexachlorobiphenyl5.102,3,3’,4,4’,5-六氯聯苯2,3,3’,4,4’,5-Hexachlorobiphenyl6.301,2,4-三氯二苯并-對-二惡英1,2,4-Trichlorodibenzo-p-dioxin5.881,2,4,6,7,8-六氯二苯并呋喃1,2,4,6,7,8-Hexachlorodibenzofuran6.08
注:活性數據來源于文獻[22-25];-logEC50為半最大效應濃度的負對數值。
Note: The active data are derived from the literature [22-25]; -logEC50is the negative value of the half maximum effect concentration.

表2 DBDPE與內分泌干擾物受體的剛性對接和半柔性對接結果Table 2 Lib Dock and Ligand Fit results between DBDPE and endocrine disruptor receptors
在全柔性對接實驗中,利用了多種打分函數來評估配體與受體的全柔性分子對接結果,主要參考值是配體與受體之間的相互作用能(CDOCKER interaction energy, CIE)。CIE越低表示配體與受體結合越強,對接結果越好,CIE越高則相反。DBDPE與4種受體的全柔性對接結果列于表中(表3~6),配體與受體全柔性分子對接的相互作用如圖2~5所示(注:每種受體只列出一個對接結果最好的結合位點)。
從表3可知,CIE最高為-26.22 kJ·mol-1,最低為-43.65 kJ·mol-1,說明對接過程所需的相互作用能非常小,對接結果是合理可靠的。
選取CIE最低的構象1(結合比較穩定),二者的相互作用二維圖如圖2所示,其中DBDPE與ERα側鏈上的520號賴氨酸、381號絲氨酸與515號精氨酸存在氫鍵相互作用(藍色箭頭表示DBDPE與側鏈上氨基酸存在氫鍵相互作用),與520號賴氨酸存在π-陽離子相互作用(由橙色線表示)。氫鍵相互作用以及π相互作用的存在對配體與受體結合的穩定情況具有重要作用。
從表4可知,CIE最高為-32.58 kJ·mol-1,最低為-42.59 kJ·mol-1,說明對接過程所需的相互作用能非常小,對接結果是合理可靠的。
選取CIE最低的構象4(結合比較穩定),二者的相互作用二維圖如圖3所示,其中DBDPE與ERβ側鏈上的329號精氨酸和383號蘇氨酸存在氫鍵相互作用,與464號組氨酸存在π-π相互作用,與386號精氨酸存在π-陽離子相互作用。氫鍵相互作用以及π相互作用的存在對配體與受體結合的穩定情況具有重要作用。
從表5可知,CIE最高為-40.72 kJ·mol-1,最低為-53.77 kJ·mol-1,說明對接過程所需的相互作用能非常小,對接結果是合理可靠的。
選取CIE最低的構象1(結合比較穩定),二者的相互作用二維圖如圖4所示,其中DBDPE與PR側鏈上的777號酪氨酸、728號絲氨酸和822號賴氨酸存在氫鍵相互作用,氫鍵相互作用的存在對配體與受體結合的穩定情況具有重要作用。
從表6可知,CIE最高為-37.57 kJ·mol-1,最低為-42.78 kJ·mol-1,說明對接過程所需的相互作用能非常小,對接結果是合理可靠的。
選取CIE最低的構象1(結合比較穩定),二者的相互作用二維圖如圖5所示:其中DBDPE與TRα側鏈的330號絲氨酸存在氫鍵相互作用,氫鍵相互作用的存在對配體與受體結合的穩定情況具有重要作用。
在分子對接實驗中,DBDPE與ERα、ERβ、PR和TRα的對接結果較好,說明DBDPE是通過與這

表3 DBDPE與ERα的全柔性對接結果Table 3 Flexible docking results between DBDPE and ERα
注:CIE表示配體與受體之間的相互作用能。
Note: CIE stands for CDOCKER interaction energy.
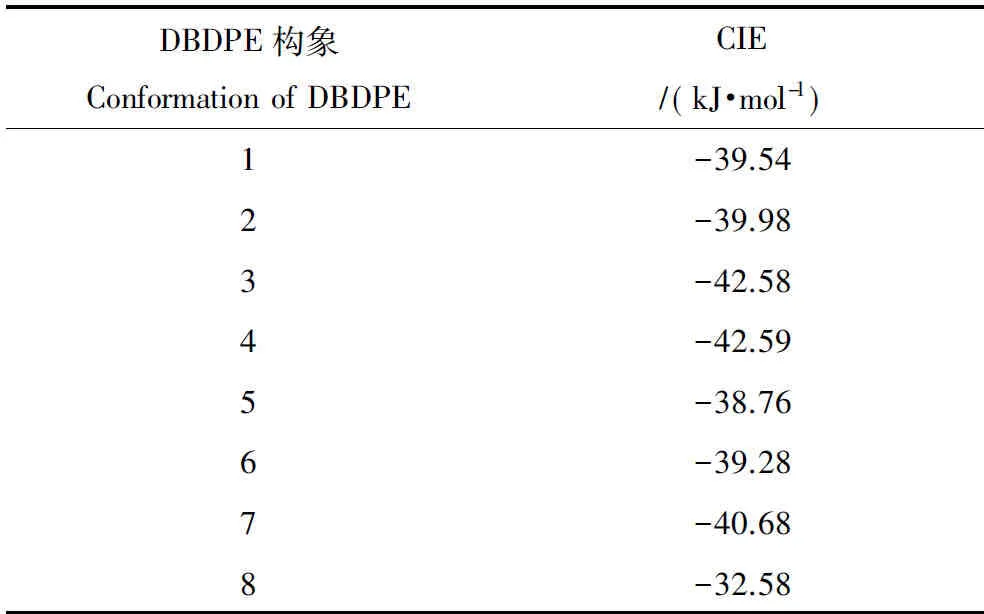
表4 DBDPE與ERβ的全柔性對接結果Table 4 Flexible docking results between DBDPE and ERβ

圖2 DBDPE與ERα的相互作用二維圖Fig. 2 X-Y scheme of interaction between DBDPE and ERα

圖3 DBDPE與ERβ的相互作用二維圖Fig. 3 X-Y scheme of interaction between DBDPE and ERβ

表5 DBDPE與PR的全柔性對接結果Table 5 Flexible docking results between DBDPE and PR

表6 DBDPE與TRα的全柔性對接結果Table 6 Flexible docking results between DBDPE and TRα
些受體結合而發揮內分泌干擾活性作用,進而影響血糖代謝水平,另外根據DBDPE與不同激素受體的對接結果可得出DBDPE對生物內分泌干擾在性別方面存在差異。
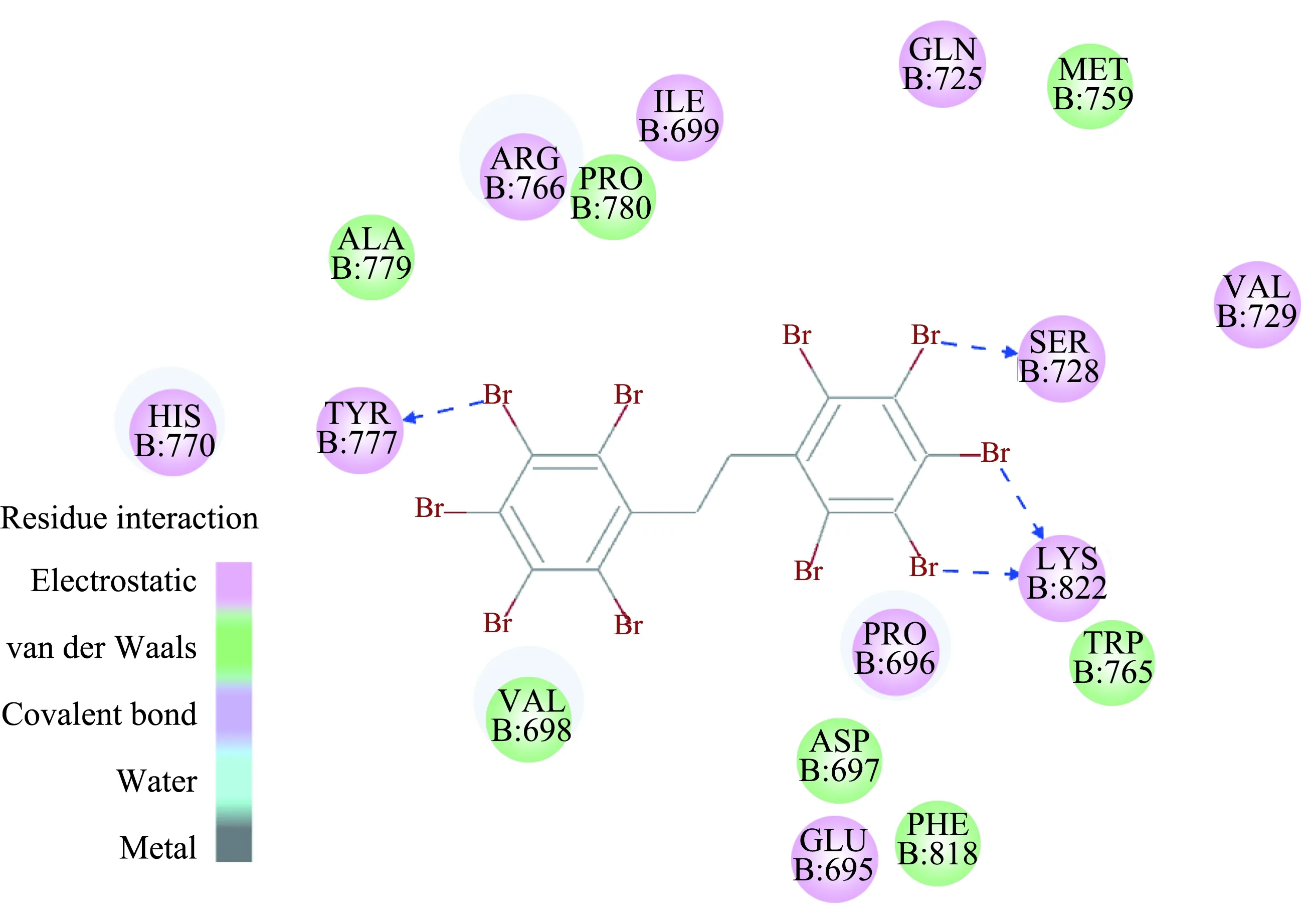
圖4 DBDPE與PR的相互作用二維圖Fig. 4 X-Y scheme of interaction between DBDPE and PR

圖5 DBDPE與TRα的相互作用二維圖Fig. 5 X-Y scheme of interaction between DBDPE and TRα
2.2 3D-QSAR模型
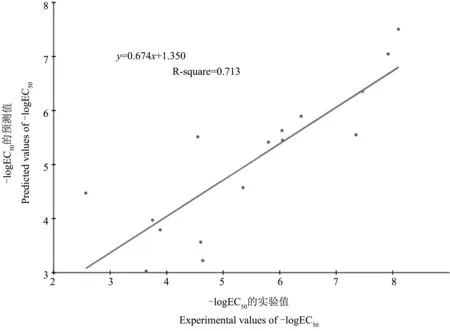
建立的模型通過訓練集的實驗值與預測值的回歸曲線(圖6)來表示,在此曲線中,橫坐標是實驗值,縱坐標是預測值,R-square值為0.989,R-square是可決系數,反映模型對樣本數據的擬合程度,范圍是0 通過測試集的測試(表7),我們可以看到實驗值與預測值的殘差并不大,這也說明結果較好,于是我們又利用模型得到DBDPE的預測值(-LogEC50),是5.86,與其他類似物相差較小。通過以上結果,我們得出結論:我們構建的3D-QSAR模型置信度較高。另外,本實驗所找的DBDPE類似物大多數屬于內分泌干擾物,它們通過發揮內分泌干擾活性作用影響血糖代謝水平,由于預測的值與其類似物的值較為接近,所以我們可以得出:與DBDPE類似的其他內分泌干擾物在血糖的內分泌干擾方面具有相近的作用。 圖6 訓練集的實驗值與預測值的回歸曲線Fig. 6 Regression curve of experimental value and predicted value of training molecules 圖7 外部驗證實驗的測試集的回歸曲線Fig. 7 Regression curve of test set for external validation test 綜上所述:通過DS 3.5中的分子對接功能將DBDPE與血糖內分泌代謝過程有關的受體進行對接,并利用DBDPE類似物的三維結構與活性數據構建3D-QSAR模型,最終得出如下結論: (1)DBDPE能夠與部分血糖內分泌受體(ERα、ERβ、PR和TRα)進行全柔性對接,相互作用能很強,說明對接結果較為穩定,這表示DBDPE是通過與這些受體結合,對后續的內分泌通路產生影響,進而影響血糖代謝水平。 (2)從對接結果發現,DBDPE能夠與雌激素受體和孕激素受體結合,而不能夠與雄激素受體結合,說明DBDPE對生物內分泌的影響在性別方面有一定的差異,這與前述的Sun[16]的實驗研究結果相符。 表7 測試集的實驗值與預測值的關系Table 7 The relationship between experimental value and predicted value of the test set molecules 注:各種化合物的實驗值來源于文獻[22-25]。 Note: The experimental values of various compounds are derived from document [22-25]. (3)通過構建3D-QSAR模型,預測出類似DBDPE未知內分泌干擾物的EC50,認為對生物代謝方面的影響具有一定的相似性。 目前,國內外開展的針對DBDPE的毒理學相關研究和評價資料比較少,且研究結果之間存在一定的差異,本文的計算機輔助研究為DBDPE在內分泌干擾方面的實驗研究提供了理論依據。