大黃魚TRIM25基因克隆和表達分析
周真真 景 斐 魏 可 張建設
(浙江海洋大學海洋科學與技術學院, 國家海洋設施養殖工程技術研究中心, 舟山 316022)
先天免疫反應是脊椎動物抵御微生物入侵的第一道防線[1]。當脊椎動物被病原體感染時, 病原體高度保守的核糖核酸及蛋白分子成分即病原體相關分子模式(Pathogen-association molecular patterns, PAMPs)能夠快速被細胞模式識別受體(Pattern recognition receptors, PRRs)識別[2]。目前已有3種細胞模式識別受體被分析鑒定, 分別是Toll樣受體(TLRs)、NOD樣受體(NLRs)和RIG-I樣受體(RLRs)[3—7]。PRRs識別病原體PAMPs, 啟動下游一系列信號傳導通路, 誘導炎性細胞因子和Ⅰ型干擾素的產生。其中, RLRs是包漿中識別病毒dsRNA的主要受體家族, RLRs (如RIG-I)的表達受到多種分子的調節, 包括病毒dsRNA和病毒dsRNA模擬體poly(I:C)等[2]。而且RIG-I的CARDs結構域被E3泛素連接酶TRIM25 (Tripartite motif-containing 25)泛素化而激活, 這對于RIG-I信號通路的信號轉導至關重要[8]。
蛋白泛素化是在El泛素激活酶, E2泛素結合酶以及E3泛素連接酶作用下對靶蛋白泛素化修飾從而調控細胞內信號通路并激活細胞內先天免疫應答, 而E3泛素連接酶由于其特異性識別靶蛋白, 因此在蛋白泛素化修飾過程中發揮著至關重要的作用[9,10]。E3泛素連接酶在脊椎動物中普遍存在, 并且包括HECT結構域家族、U-box結構域家族和RING結構域家族[11,12]。TRIM蛋白屬于E3泛素連接酶的RING結構域家族, 參與多種生物學過程, 包括細胞分化、細胞周期調控、細胞凋亡和先天免疫反應[13,14]。TRIM家族蛋白在結構上從N端到C端包含保守的RING結構域、1—2個B-box結構域、Coiled-coil結構域, 另外在C末端還有可變的蛋白結構域[15—18]。其中, RING結構域參與鋅原子的結合并促進對靶蛋白的泛素化, 提高蛋白的穩定性[19];B-box結構域為TRIM蛋白的特征結構域且能提高TRIM蛋白E3泛素連接酶活性[20,21]; Coiled-coil結構域可以促進TRIM蛋白間同源或異源的寡聚反應[22];C末端的PRY/SPRY結構域通過與RIG-I相互作用導致下游抗病毒信號明顯增加, 從而誘導干擾素的產生[23]。TRIM家族在哺乳動物中被廣泛研究,TRIM家族基因參與哺乳動物機體多種生命活動[13,24],例如, 與HIV-I病毒相關的TRIM5[25], 神經元特異性蛋白TRIM22[26]以及與先天免疫相關的TRIM25[8]、TRIM15[27]和TRIM21[28]等。
近幾年TRIM家族成員在魚類中被研究, 在斑馬魚(Danio rerio)基因組中發現240種TRIM家族基因成員或類似TRIM基因[29], 其中包含魚類特有的TRIM亞家族基因 finTRIM/ftr (Fish novel large multigene TRIM gene)。在大西洋鮭(Salmo salar)[30]、斜帶石斑魚(Epinephelus coioides)[31]和尼羅羅非魚(Oreochromis niloticus)[32]等硬骨魚類中發現病毒和病毒模擬體poly(I:C)誘導TRIM25基因表達, 而且TRIM25基因在體外過表達可抑制病毒復制, 在培養的魚類細胞中可以增強干擾素信號基因表達[32]。這些研究充分表明TRIM25基因可能在硬骨魚類抗病毒免疫應答中發揮重要作用。
大黃魚(Larimichthys crocea)是我國一類重要的海洋經濟魚種[33,34]。近年來, 大黃魚遭受細菌、寄生蟲和病毒等的危害, 對大黃魚養殖產業造成嚴重的影響[35,36]。因此, 為建立控制大黃魚疾病的有效措施, 需要更深入地研究大黃魚抗病分子機理。為研究大黃魚抗病免疫機制, 本研究選擇大黃魚TRIM家族中的TRIM25基因進行初步研究。因此,本研究對大黃魚TRIM25基因編碼區進行分子克隆,并研究該基因的分子特征以及在poly(I:C)感染后的表達分析。
1 材料與方法
1.1 實驗動物
實驗所用大黃魚是來自中國浙江省舟山市, 用于實驗的每條大黃魚約重100 g。實驗大黃魚需在25℃水箱中暫養2周左右, 每天至少投喂2次。實驗大黃魚麻醉后被處死, 取頭腎、脾臟、肝臟和外周血等組織, 并將取出的各組織在-80℃凍存。每組實驗設置3個平行。
1.2 poly(I:C)的用法
病毒dsRNA模擬體poly(I:C)原液(Sigma-Aldrich)溶解在1 mg/mL的磷酸鹽緩沖液(PBS)中, 通過腹腔向大約重100 g的大黃魚體內注射0.25 mg poly(I:C), 對照組注射等量無菌PBS溶液。在poly(I:C)注射入大黃魚后, 分別在3h、6h、12h、24h和48h時間點以及注射PBS的對照組取外周血、頭腎、脾臟和肝臟主要免疫組織, 在-80℃凍存。
1.3 TRIM25基因克隆
采用Trizol試劑(Invitrogen, USA)從凍存的大黃魚各個組織(-80℃保存)中提取總RNA, 總RNA純度用1%瓊脂糖凝膠電泳檢測, 通過NanoDrop 2000核酸蛋白檢測儀對總RNA濃度測定, RNA樣品OD值一般在1.8—2.1視為純度極高。然后按照SuperScriptTMIII反轉錄酶試劑盒(Invitrogen, USA)說明書將5 μg總RNA反轉錄合成第一鏈cDNA。
根據大黃魚轉錄組獲得TRIM25基因編碼序列,針對TRIM25基因設計特異性的引物TRIM25-F/TRIM25-R (表 1), 以大黃魚脾臟cDNA作為模板,用EasyTaq?DNA Polymerase (全式金)進行聚合酶鏈式反應(PCR)。PCR反應體系(20 μL): 上下游引物各0.4 μL, 2.5 mmol/L dNTP Mixture 1.6 μL, 10×EasyTaq?Buffer 2 μL, EasyTaq?DNA Polymerase 0.2 μL, 模板0.4 μL, 加無菌去離子水15 μL; 設置PCR反應條件為: 95℃預變性5min; 95℃變性30s,58℃退火30s, 72℃延伸10s, 32個循環; 72℃終延伸10min。PCR產物利用1%瓊脂糖凝膠分離, 并利用普通瓊脂糖凝膠DNA回收試劑盒(天根, 中國)進行膠回收, 然后連接并克隆到pGEM-T載體上(Promega, USA), 通過藍白斑篩選獲得陽性克隆子, 送至上海華大基因測序。最后用DNAstar軟件拼接測序后的序列, 獲得大黃魚TRIM25基因完整編碼序列, 并命名為LcTRIM25。

表1 PCR引物信息Tab. 1 PCR primer sequences information
1.4 TRIM25基因生物信息學分析
LcTRIM25核苷酸序列通過MEGA7.0軟件翻譯為氨基酸序列[37], 并通過DNAMAN軟件對多個物種的TRIM25基因進行多序列比對。利用ExPAsy(https://web.expasy.org/protparam/)在線軟件對LcTRIM25蛋白進行序列分析。另外, 利用SMART在線軟件(http://smart.embl-heidelberg.de/)預測LcTRIM25蛋白結構域。TRIM25基因系統發育分析是在不同物種的TRIM25氨基酸序列基礎上, 采用MEGA7.0軟件中的一種自下向上(聚集)的聚類方法——相鄰連接(NJ)方法生成系統進化樹[38]。
1.5 實時熒光定量PCR表達分析
用Trizol方法提取凍存的poly(I:C)感染大黃魚的外周血、脾臟、頭腎和肝臟組織的總RNA,RNA濃度和純度的檢測同1.2, 使用SuperScriptTMIII反轉錄酶試劑盒進行反轉錄, 合成第一鏈cDNA。根據克隆獲得的LcTRIM25基因編碼序列, 利用primer premier 5.0設計熒光定量特異性引物TRIM25-RT-F/TRIM25-RT-R (表 1)。管家基因β-actin[39]為本實驗內參基因, 內參基因是LcTRIM25基因表達的內部參照物, 是實時熒光定量PCR (qRT-PCR)系統工作時的某種標準,β-actin熒光定量引物β-actin-RT-F/β-actin-RT-R (表 1)。
用SYBR?Premix ExTaq? (TaKaRa, Japan)試劑在ABI 7500快速實時PCR系統(Applied Biosystems, USA)上檢測LcTRIM25基因在各組織的相對表達量, 每組實驗設置3個平行。實時熒光定量20 μL PCR反應體系: 0.8 μL上下游引物、0.4 μL ROX Reference Dye II、10 μL TB Green Premix ExTaqII、1 μL cDNA模板, 7 μL DEPC水。熒光定量PCR反應結束, 利用2-ΔΔCt方法分析LcTRIM25基因表達量, 并通過SPSS軟件中方差分析(ANOVA)了解實驗組和對照組基因表達差異, 采用鄧肯(Duncan)多重比較法分析基因相對表達量[40]。采用均值±標準差(SE)分析實驗數據結果,P<0.05為具有顯著性差異,P<0.01為具有極顯著性差異。
2 結果
2.1 大黃魚TRIM25基因序列分析
經擴增、測序獲得LcTRIM25基因編碼序列全長為2097 bp, GenBank登錄號: MK327541, 編碼698個氨基酸。ExPAsy在線軟件預測LcTRIM25蛋白分子量為77.99 kD, 分子式為C3404H5402N966O1047S43,理論等電點是8.66, 富含絲氨酸(Ser, 11%)、亮氨酸(Leu, 8.6%)和賴氨酸(Lys, 7.6%)。利用在線軟件SMART預測蛋白結構域, LcTRIM25蛋白結構分析發現未包含信號肽, 包括3個高度保守的結構域, 分別是RING結構域(第20—57位氨基酸)、B-box2結構域(第151—191位氨基酸)、Coiled-coil結構域(第227—281位氨基酸)和可變的C末端PRY/SPRY結構域(第523—697位氨基酸)。
2.2 TRIM25蛋白多序列比對
經Blastx在線軟件分析發現LcTRIM25氨基酸序列與斜帶石斑魚TRIM25氨基酸序列同源性較高(67%)。另外, LcTRIM25氨基酸序列與人類(Homo sapiens, XM_005082.4)、小鼠(Mus musculus, NM_009546.2)、雞(Gallus gall, NM_001318458.1)、非洲爪蟾(Xenopus laevis, XM_018238270.1)、斑馬魚(NM_200175.1)和斜帶石斑魚(KX_258199.1)的TRIM25氨基酸序列利用DNAMAN軟件進行多序列比對。多序列比對結果發現TRIM25蛋白結構域序列相似性相對較高; 并且大黃魚和斜帶石斑魚TRIM25氨基酸序列具有較高同源性, 與Blastx分析結果相同。
2.3 TRIM25基因系統進化樹構建
收集來自GenBank數據庫中已發表的不同物種(兩棲動物、哺乳動物、爬行動物、鳥類和硬骨魚類)TRIM25基因序列。在TRIM25氨基酸序列基礎上, 構建系統進化樹(圖 1)。TRIM25系統進化樹顯示分為單獨的三支, 分別是哺乳動物、爬行動物和鳥類聚集為一支; 硬骨魚類聚為一支; 兩棲動物為一支。其中, 哺乳動物、爬行動物和鳥類各自為一小支, 說明哺乳動物, 爬行動物和鳥類的TRIM25基因同源性很高。另外, 系統進化樹表明大黃魚TRIM25基因與鱸形目斜帶石斑魚同源性較高, 親緣關系最近; 與兩棲動物、爬行動物、鳥類和哺乳動物同源性相對低。
2.4 LcTRIM25基因組織表達分析
本實驗采用qRT-PCR方法檢測健康大黃魚肌肉、皮膚、腦、腸、外周血、心臟、脾臟、頭腎、肝臟9個正常組織中LcTRIM25基因的表達。qRTPCR結果表明,LcTRIM25基因在被檢測的9個組織中廣泛表達, 但表達量相對較低(圖 2)。LcTRIM25基因在不同組織中的表達水平存在差異, 以表達量為1的肌肉組織為參考, 在肝臟中表達量最高, 約為對照組3倍, 在心臟中表達量最低, 約為對照組1/300倍(圖 2), 這種差異性表達可能是由不同的組織表達模式所誘導。
2.5 LcTRIM25基因在poly(I:C)感染后的時序表達
qRT-PCR結果顯示, 在poly(I:C)感染大黃魚后,LcTRIM25基因在各組織中(外周血、頭腎、脾臟和肝臟)的表達水平與對照組相比顯著升高(圖 3)。在外周血中LcTRIM25基因的表達量在24h達到最高,24—48h表達量逐漸降低(圖 3A); 在頭腎中LcTRIM25基因表達水平在12h達到最高峰后出現下降趨勢(圖 3B); 在脾臟中LcTRIM25基因表達量在6h到達峰值, 從6—48h期間表達量逐漸下降(圖 3C); 在肝臟中,LcTRIM25基因表達量從3—6h期間呈現下降趨勢, 在6—12h表達量逐漸上升并在12h達到最高值, 之后表達量呈現下降趨勢(圖 3D)。
3 討論
在之前的研究中根據TRIM家族成員結構域的組成以及進化角度將TRIM家族分為兩大類(Group1, Group2): Group1包含除SPRY結構域的多種C末端結構域, 進化較慢, 結構保守; Group2的特征是C端具有SPRY結構域并且僅具有B-box2結構域, 而且Group2的進化速度比Group1更快速[41—43]。在本研究中, 大黃魚TRIM25基因通過擴增、測序獲得其編碼序列全長2097 bp, 編碼698個氨基酸;蛋白結構預測發現LcTRIM25從N端到C端具有保守的結構域(RING、B-box2和Coiled-coil)和可變的C末端PRY/SPRY結構域; 另外, 多序列比對和系統進化樹分析表明LcTRIM25基因與鱸形目斜帶石斑魚TRIM25基因的同源性較高, 而且系統進化樹表明大黃魚與哺乳動物、爬行動物、鳥類和兩棲動物TRIM25基因同源性相對低。這可能是因為不同物種所處環境不同, 面對不同的環境選擇壓力, 導致不同的進化速度和進化方向[42]。這些分子特征分析說明大黃魚TRIM25基因屬于Group2 TRIM家族。
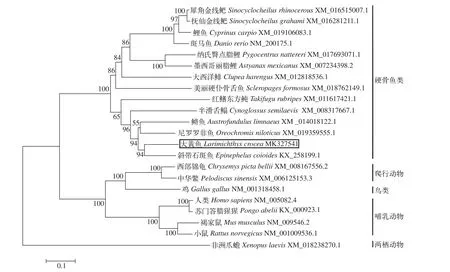
圖1 TRIM25基因系統進化樹(NJ)Fig. 1 Phylogenetic trees of TRIM25 gene (Neighbor-joining)
研究發現Group2的TRIM家族成員在病毒感染的先天免疫反應中發揮重要作用[42,44,45], 例如TRIM27通過靶向作用IKKs負調控參與抗病毒應答和炎癥反應的信號轉導[44],TRIM21在泛素化非降解途徑中有助于巨噬細胞天然免疫的激發[46]和TRIM5α被認為是先天性細胞對HIV-1抗性的物種特異性介質[47]等。在本研究中, qRT-PCR結果顯示LcTRIM25在健康大黃魚9個正常組織中廣泛存在,但表達水平相對較低, 這與斜帶石斑魚TRIM25基因[31]和韓國鳑鲏(Rhodeus uyekii)TRIM25基因[48]研究一致。LcTRIM25基因在肝臟中達到最高表達量,這可能是為了滿足肝臟在體內進行新陳代謝的需要, 而且在頭腎、腸和肌肉中表達量較高, 說明大黃魚TRIM25基因在免疫相關組織中高度表達。
另外, 早有研究證明硬骨魚類TRIM25基因對病毒感染具有快速響應模式。大西洋鮭感染傳染性鮭魚貧血病毒(ISAV)[30]和斜帶石斑魚感染poly(I:C)或石斑魚虹彩病毒(SGIV)時[31],TRIM25基因表達水平都呈現迅速上升后下降趨勢。本研究對LcTRIM25基因在健康大黃魚注射poly(I:C)后不同時間點的表達水平變化進行檢測。LcTRIM25基因在外周血、頭腎、脾臟和肝臟中表達量迅速增加, 均出現上升到達峰值后下降的趨勢; 其中頭腎和脾臟中LcTRIM25基因表達量在6h達到峰值; 肝臟中LcTRIM25基因表達量在12h達到峰值; 外周血中LcTRIM25基因在24h達到最高表達水平且上調幅度最大, 這可能是因為外周血是機體重要的免疫場所, 外周血中含有可以直接參與免疫反應的白細胞[32], 另外, poly(I:C)通過腹腔注射入大黃魚體內隨外周血液循環擴散到主要免疫組織, 組織感染poly(I:C)后迅速反應, 從而TRIM25基因在相關免疫組織中表達水平比在外周血中更快到達峰值, 而在血液循環過程中TRIM25基因一直持續表達。這說明大黃魚TRIM25基因可能在先天免疫應答過程中發揮重要作用。

圖2 LcTRIM25基因在大黃魚健康組織中的表達Fig. 2 Tissue specific expression of LcTRIM25 gene in healthy Larimichthys crocea
綜上所述, 經過分子克隆、測序首次確定大黃魚TRIM25基因編碼序列全長, 并檢測LcTRIM25基因在健康大黃魚以及感染poly(I:C)后的表達量變化。LcTRIM25基因在被檢測的健康大黃魚各個組織中均表達, 在肝臟中表達量最高; 健康大黃魚注射poly(I:C)后,LcTRIM25基因在免疫組織中表達水平迅速上調, 且不同組織中LcTRIM25基因表達模式具有差異性。初步推測大黃魚TRIM25基因可能在先天抗病毒免疫反應中發揮作用, 為研究Group2 TRIM家族成員在硬骨魚類中的抗病毒免疫應答提供理論參考。
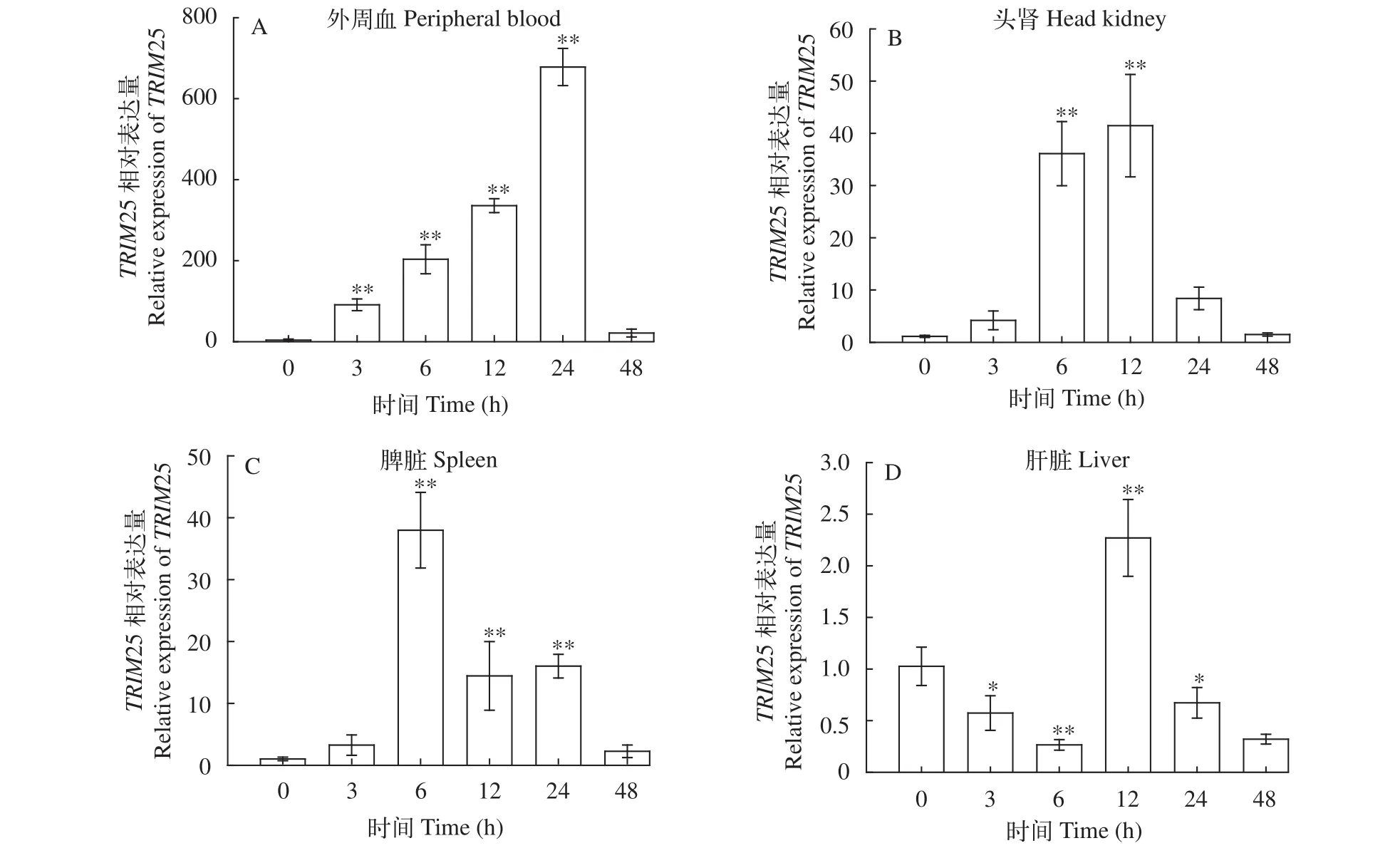
圖3 LcTRIM25基因在poly(I:C)刺激后的時序表達Fig. 3 The relative expression of LcTRIM25 gene after poly(I:C) challenge

