后腹腔鏡保留腎單位的腎部分切除術對T1期腎腫瘤的臨床效果
張少杰, 徐曉峰, 杜 泉, 李 楠, 肖 湘
(陜西省咸陽市中心醫院 泌尿外科, 陜西 咸陽, 712000)
腎腫瘤是泌尿外科中比較常見的腫瘤,其惡性腫瘤發生率高達94%[1], 只有極少數腫瘤屬于良性,一般患者早期會出現血尿、腰背酸痛及腹部淋巴結腫大等癥狀,腎腫瘤晚期常伴有消瘦、腹腔內出血。根據TNM分期[1], T1期腎腫瘤最大直徑不超過7 cm且局限于腎臟,雖然腫瘤直徑并不大,但若不及時處理,進一步惡化會危及生命。一般臨床常采用傳統開放式腎部分切除術,但創傷較大,術后恢復時間較長,且護理不當極易造成感染。隨著腔鏡技術的不斷發展,研究[2]發現后腹腔鏡保留腎單位的腎部分切除術(RLPN)在治療腎腫瘤方面取得了很好的成效。RLPN是一種經腹膜后途經利用腹腔鏡對腹膜后器官進行手術操作的一種微創手術,能最大程度保留部分腎功能的同時減少手術疼痛,提高生存質量,是目前臨床上治療腎腫瘤的有效手段之一。本研究觀察100例經臨床診斷為T1期腎腫瘤患者行RLPN術后的臨床效果,現報告如下。
1 資料與方法
1.1 一般資料
選取陜西省咸陽市中心醫院2013年6月—2018年6月收治的100例經臨床診斷為T1期腎腫瘤患者為研究對象,其中男60例,女40例;年齡25~60歲,平均(40.84±12.25)歲。根據隨機法平均分為對照組與觀察組。對照組男28例,女22例;年齡25~56歲,平均(38.15±80.23)歲;病程1~5年,平均病程(3.21±1.46)年;平均腫瘤直徑(3.12±2.35) cm。觀察組男32例,女18例;年齡29~60歲,平均(37.24±7.24)歲;病程1~4年,平均病程(3.15±1.06)年;平均腫瘤直徑(3.41±2.14) cm。2組基本資料差異無統計學意義(P>0.05)。所有患者均知情同意,經過醫學倫理委員會批準認可。
納入標準[3]: ① 實驗室檢查符合美國癌癥聯合會關于腎癌TNM分期中T1期腎腫瘤患者診斷標準; ② 健側肝、腎功能良好,且無其它血液系統疾病; ③ 未出現淋巴結腫大,腫瘤無遠處轉移; ④ 未出現明顯手術禁忌證。排除標準[3]: ① 腎臟解剖結構不清晰; ② 需要進行其他手術; ③實驗室檢查提示良性腫瘤。
1.2 方法
對照組給予開放式腎部分切除術。手術過程中取90 °健側臥位并妥善固定,常規消毒鋪無菌巾。在患者第11肋間處做一切口,進入后腹腔時在腎臟背側分離其脂肪組織,暴露出腎動脈并用鉗子將其夾閉,記錄手術開始時間。腫瘤組織周圍5 mm處切除腫瘤,用可吸收線縫合出血點,最后縫合創面。松開鉗端觀察創面情況,記錄術中失血量以及腎蒂血管阻斷時間,在體內留置引流管后關閉并縫合腹腔。術后觀察腫瘤組織性狀,并送至病理科檢驗。觀察組給予后腹腔鏡保留腎單位的腎部分切除術。患者行全身麻醉手術,手術過程中采用90 °健側臥位,用墊枕置于腰下妥善固定,消毒鋪無菌治療巾。在腋中線上兩橫指、腋前線及腋后線下建立后腹腔鏡三通道。在腰大肌處切開,分離腎周圍脂肪組織后暴露腎動脈,進而暴露腫瘤組織。用鉗子夾閉腎動脈后,在腫瘤組織周圍5 mm處切除腫瘤,用可吸收線縫合出血點,最后縫合傷口創面。
術后嚴密觀察引流液情況、術后失血量、血腫與切口感染情況以及疼痛情況。引流液不正常時應及時抗炎對癥處理; 術后失血過多應及時輸血處理; 血腫與切口感染應給予抗生素消炎治療,血腫切開引流等措施; 發生尿漏后需要植入輸尿管支架; 疼痛不能耐受時予以止痛藥肌注緩解。
治療療效根據美國《實用腫瘤雜志學》[4]腎腫瘤術后療效評價標準進行評價。肝、腎功能指標參照中華醫學會中《實用內科學》[5]肝、腎功能檢查指標后進行評價。生存質量根據1990年腫瘤患者生存質量評分(QOL)《草案》[6]生存質量評分標準進行評分。
2 結 果
2.1 2組療效比較
術后1周,對照組疾病進展8例,疾病穩定12例,部分緩解15例,完全緩解15例。觀察組分別為2、8、10、30例。觀察組總有效率為96.00%, 顯著高于對照組的84.00%(P<0.05)。
2.2 2組手術相關情況比較
手術治療后, 2組術中輸血率差異無統計學意義(P>0.05)。觀察組手術時間、術中出血量、術后住院時間、術后失血量、腎蒂血管阻斷時間優于對照組,差異有統計學意義(P<0.05), 見表1。
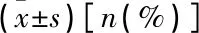
表1 手術相關情況比較
與對照組比較, *P<0.05。
2.3 2組肝、腎功能水平比較
2組患者手術前肝、腎功能比較差異無統計學意義(P>0.05); 觀察組術后尿素氮(BUN)、血肌酐(Scr)、尿酸(UA)、內生肌酐清除率(Ccr)、腎小球濾過率(GFR)低于對照組,差異有統計學意義(P<0.05)且2組術后尿蛋白均為陰性,見表2。
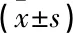
表2 2組肝、腎功能水平比較
BUN: 尿素氮; Scr: 血肌酐; UA: 尿酸; Ccr: 內生肌酐清除率; GFR: 腎小球濾過率。與術前比較,*P<0.05; 與對照組比較,#P<0.05。
2.4 2組生存質量評分情況比較
術前, 2組生存質量比較差異無統計學意義(P>0.05); 2組術后1、3、6個月生存質量評分均顯著下降,觀察組術后1、3、6月評分高于對照組,差異有統計學意義(P<0.05), 見表3。
2.5 2組隨訪術后生存情況比較
隨訪患者1、2、3年,觀察組生存率分別是100.00%、96.00%、90.00%, 均高于對照組,但差異無統計學差異(P>0.05), 見表4。
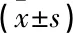
表3 2組生存質量評分比較 分
與術前比較, *P<0.05; 與對照組比較, #P<0.05。

表4 術后生存情況比較[n(%)]
2.6 2組并發癥及復發率
隨訪1年, 2組患者術后均出現并發癥,觀察組漏尿1例、血腫2例、切口感染1例、出血1例,對照組分別為2、2、3、2例。觀察組總并發癥發生率為10.00%, 低于對照組的18.00%, 觀察組復發率為8.00%, 低于對照組的12.00%, 但差異均無統計學意義(P>0.05)。
3 討 論
隨著外科鏡下縫合技術與不腔鏡技術的不斷進步,后腔鏡保留腎單位手術在腫瘤最大直徑小于7 cm的T1期腎腫瘤治療中有很好地發展前景,其中RLPN逐漸成為治療腎腫瘤的主要有效手段之一,該手術方式是一種新型微創手術[7-8]。術中醫生利用鏡頭能夠準確找到腫瘤壞死處并加以切除,提高手術成功率[9-11]。
本研究中觀察組腎蒂血管阻斷時間短于對照組,原因為RLPN在手術過程中利用無損傷鉗阻斷腎動脈,靜脈滴注肌酐來延長腎缺血時間,更大程度減少腎損傷,更好地保護腎功能。同時,觀察組手術時間、術中失血量、住院時間、術后失血量優于對照組,原因可能與RLPN在手術過程中定位精準、腎蒂阻斷時間短有關, RLPN手術對患者創傷小、手術時間短、腎缺血時間也相對較短,從而減少了患者術后失血量,縮短住院時間,與王衛平等[12-13]研究結論相一致。T1期腎腫瘤在健側腎功能完好的前提下,保留腎單位手術方式可以保護患腎的腎功能,降低全切術下孤立腎發生腎功能不全等的風險,而手術前后肝腎功能水平變化在一定程度上反映了患者預后以及手術成效。本研究2組患者術后肝、腎功能指標較術前降低,觀察組變化幅度大于對照組,表明RLPN術后患者肝腎功能恢復迅速,原因為手術不僅可以精準切除,而且可以縮短手術時間及腎缺血時間,更好地保護肝腎功能。2組患者術后1、3、6個月生存質量逐漸下降,但觀察組生存質量評分高于對照組,這可能與RLPN術定位精確度高,醫源性損傷小,術中腎缺血時間短,能更好保護患腎功能有關。隨訪1、2、3年后發現, 2組生存率逐年下降,其中觀察組生存率下降幅度較小。

