Fenton氧化法處理堿性大紅模擬廢水
何亞萍 黃升謀 湯亞飛


摘要:以堿性大紅模擬廢水為對象,采用Fe2+和Fe3+作為催化劑與H2O2構成芬頓體系進行了Fenton氧化反應,考查了pH值、反應時間、Fenton試劑配比與用量等影響因子對色度處理效果的影響。結果表明:最佳處理條件為:初始pH=3、C(Fe2+):C(H2O2)=1:5或C(Fe3+):C(H2O2)=1:5、反應時間為30min。當堿性大紅模擬廢水濃度為1000mg/L,初始H2O2濃度為5mmol/L時,最佳條件下Fe2+、Fe3+芬頓體系的脫色率去除效率分別為92.30%、95.68%。對比了Fe2+和Fe3+作為催化劑進行Fenton氧化反應的處理效果。說明Fe3+作為催化劑與Fe2+效果相近。
關鍵詞:堿性大紅;Fenton氧化法;Fe3+
中圖分類號:X703 文獻標識碼:A 文章編號:1674-9944(2019)22-0083-04
1 引言
染料作為紡織印染行業的一種重要染色工具,隨著工業社會的發展變遷,越來越廣泛地應用于生活的方方面面,不僅僅局限于紡織印染,在食品、醫藥、化妝品等行業也有應用[1]。染料地廣泛應用帶來大量染料廢水,廢水大多具有色度大,COD值高、成分復雜、毒性大、難降解等特點[2]。這些染料廢水如果不經處理,直接排人水體,會對自然環境帶來極大危害。因此,染料廢水的處理問題亟待解決。目前,已有大量學者對染料廢水的處理進行了研究,如電絮凝一生化法[3]、活性炭吸附法[4]、電化學法[5]等。雖然這類方法取得一定的效果,但并不是十分的理想。
Fenton氧化法作為一種最常見的高級氧化技術,因具有適用范圍廣、反應速率快、氧化能力強、反應體系條件溫和、反應設備簡單等優點[6]。采用Fenton氧化法來處理染料廢水,在水處理領域具有很好的應用前景,也是目前水處理領域研究的熱點[7~9]。芬頓氧化法常用的芬頓試劑是Fe2和H2O2,也有Cu2+、Co2+等作為芬頓催化劑[10,11],但關于Fe3+作為芬頓催化劑的研究很少。本文對Fe3+作為芬頓催化劑進行了研究,并與Fe2+的效果進行了比較。考察了催化劑投加量、H2O2投加量、pH值、反應時間、芬頓試劑配比對染料脫色效果的影響。
2 實驗
2.1 實驗材料和儀器
材料:工業染料堿性大紅,化學試劑FeSO4·7H2O、Fe2(SO4)3·xH2O、H2O2(30%)均為分析純;將堿性大紅用去離子水稀釋至廢水中堿性大紅濃度為1000mg/L,原水的pH值約為9.5。
儀器:752PC型紫外可見分光光度計、85-2恒溫磁力攪拌器、SHA-C數顯水浴恒溫振蕩器、PHS-3CpH計、BSA 124S電子天平等。
2.2 實驗方法
試驗取50mL水樣到250mL錐形瓶中,用H2SO4調整pH值后投加一定量的催化劑和H2O2,置于恒溫震蕩搖床一定時間。反應完成后用NaOH調整pH值為10后靜置60min,取上清液測定水樣的吸光度。
用分光光度計對堿性大紅模擬廢水進行全掃,在504.5~506.5nm波長處,有最大吸光度。選定505nm為最大吸收波長,在此波長下測溶液吸光度。脫色率的計算公式為:
式(1)中:δ為脫色率(%),A為1000mg/L堿性大紅模擬水樣的吸光度;A0為反應結束后上清液的吸光度。
3 結果與分析
3.1 s催化劑投加t對處理效果的影響
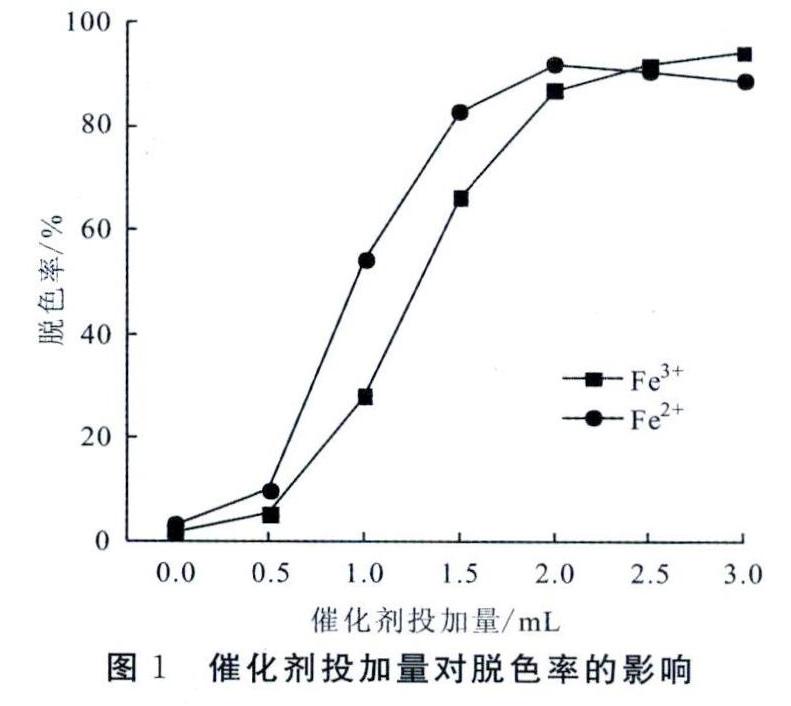
取50mL模擬廢水,不調pH值。固定0.2mol/L的H2O2投加量1.0mL,改變催化劑投加量,室溫下搖床震蕩30min。考察催化劑投加量對廢水脫色率的影響。結果見圖1。
由圖1可知,當H2O2投加量為1mL時,對于Fe2+、Fe3+而言,增加投加量,脫色率也隨之增加。Fe2+相較于Fe3+稍快達到最大脫色率。對Fe2+而言,催化劑投加量增加到2.0mL時,達到最大脫色率,繼續投加催化劑,脫色率表現為小幅度下降;而對Fe3+而言,增加催化劑投加量到2.0mL時,脫色率仍舊表現為上升,但上升幅度明顯下降。根據Fenton試劑機理可以看出當H2O2投加量一定時,·OH隨著Fe2+/Fe3+的增加而增加,所以污染物被快速降解;當Fe2+/Fe3+過量后導致H2O2分解為H2O和O2從而消耗T2O2。綜合考慮,確定2.0mL為Fe2+和Fe3+的最佳催化劑投加量。
3.2 H2O2投加,對處理效果的影響
取50mL模擬廢水,不調pH值。固定0.02mol/L的催化劑投加量2.0mL,改變H2O2投加量,室溫下搖床震蕩30min。考察H2O2投加量對廢水脫色率的影響。結果見圖2。
由圖2可知,當催化劑投加量為2.0mL時,對于Fe2+、Fe3+而言,增加H2O2投加量,脫色率也隨之增大,達到最大脫色率后變化不是太大。Fe2+和Fe3+的脫色率變化趨勢基本相似,都是在H2O2投加量為2mL之前迅速增大2.0mL之后增幅就降下來了。因為當H2O2濃度低時,·OH的量隨著H2O2的增加而增加;當H2O2濃度過高,過量的H2O2不但不能通過分解產生更多的自由基,反而在反應一開始就把Fe2+迅速氧化為Fe3+,使得氧化反應在Fe3+的催化下進行,這樣既消耗H2O2的用量,又抑制了·OH的產生。綜合考慮確定2.0mL為H2O2的最佳投加量。
3.3 初始pH對處理效果的影響
取50mL模擬廢水,調節不同pH值。固定0.02mol/L的催化劑投加量1.0mL,0.2mol/L的H2O2投加量1.0mL,室溫下搖床震蕩30min。考察初始pH對廢水脫色率的影響。結果見圖3。
由圖3可知,當對于Fe2+和Fe3+而言,廢水的脫色率隨pH值變化而變化的趨勢基本相似,但Fe2+較于Fe3+對色度的去除效果略好。Fe2+和Fe3+都在pH=3時有最大脫色率,溶液的pH值對Fenton反應至關重要,這主要是由于H2O2和鐵離子本身的化學性質決定的。Fenton反應的最佳pH值在2.5~3.5。pH值較高時Fe3+相對不活躍造成Fenton試劑的反應活性降低,生成的·OH也較少;較高的pH值還會導致H2O2自身的分解,從而影響Fenton氧化的速率。因此pH值太高或者太低都不利于Fenton降解有機物,故確定3為最佳初始pH。
3.4 反應時間對處理效果的影響
取50mL模擬廢水,調節pH=3。固定0.02mol/L的催化劑投加量1.0mL,0.2mol/L的H2O2投加量1.0mL,改變室溫下搖床震蕩時間。考察反應時間對廢水脫色率的影響。結果見圖4。
由圖4可知,對于Fe2+和Fe3+而言,廢水脫色率隨時間變化而變化的趨勢基本相似,均隨反應時間的增加而增加,但Fe2+較于Fe3+去除效果略好。Fe2+在5min時就能達到68.78%的去除率,而Fe3+在20min時才達到63.95%的去除率,再一次表明芬頓反應Fe2+做催化劑比Fe3+啟動的更快。Fe2+和Fe3+的脫色率增長幅度在30min后都明顯降低,故確定最佳反應時間為30min。
3.5 Fenton試劑投加,對處理效果的影響
根據以上實驗結果可以計算出此時Fenton試劑C(Fe2+):C(H2O2)=1:5,C(Fe3+):C(H2O2)=1:5。取50mL模擬廢水,調整pH=3,離子濃度為0.02mol/ L,H2O2濃度為0.2mol/L。按計算配比投加不同量的Fenton試劑,室溫下搖床震蕩30min。考察芬頓試劑投加量對廢水脫色率的影響,結果見表1和圖5。
根據表1和圖5可知,按C(Fe2+),C(H2O2)=1:5、C(Fe3+):C(H2O2)=1:5投加,隨著Fenton試劑投加量的增加脫色率均增大。當Fe2+(Fe3+)和H2O2的投加量分別為1.5mL和3mL時達到最大值。由圖5可知,在Fe2+(Fe3+)和H2O2的投加量分別為2.5mL和1.25mL時,脫色率的增長幅度基本為0,綜合考慮確定Fenton試劑Fe2+(Fe3+)的最佳投加量為2.5mL,H2O2的最佳投加量為1.25mL。即此時Fe3+、Fe2+的脫色率分別為95.68%、92.30%。
4 結論
(1)Fenton處理模擬廢水實驗結果表明,初始pH值為3,C(Fe2+),C(H2O2)=1:5、C(Fe3+):C(H2O2)=1:5,反應30min為最佳處理條件。當廢水濃度為1000mg/L,按最佳條件投加0.02mol/L的Fe2+(Fe3+)2.5mL,0.2mol/L的H2O21.25mL(體系初始H2O2濃度為5mmol/L)時,Fe2+、Fe3+芬頓體系的脫色率分別為92.30%、95.68%。
(2)增加H2O2和Fe2+(或Fe3+)均有利于Fenton氧化法去除色度,而過量的H2O2和Fe2+(或Fe3+)反而制約Fenton處理效果;酸性條件下有利于Fenton降解有機物,初始pH太高或者太低都不利與Fenton處理效果;一定范圍內延長反應時間有利于色度的去除,但過長的反應時間對Fenton處理效果沒幫助。
(3)在相同條件下Fe2+和H2O2構成的芬頓體系與Fe3+與H2O2構成的芬頓體系的對廢水的脫色率變化趨勢大體相似,但總體而言Fe3+作為催化劑的脫色效果與Fe2+相近。
參考文獻:
[1]陳文華,李剛,許方程,等.染料廢水污染現狀及處理方法研究進展[J].浙江農業科學,2014,1(2):1~5.
[2]李竹亮,張湘濤.淺析染料廢水及其治理[J].科學技術創新,2010(12):114
[3]孫金勇,莊云龍.電絮凝—生化法聯合處理染料廢水的研究[C]//中國化學會.第二屆全國環境化學學術報告會論文集.北京:中國化學會,2004.
[4]張小璇,葉李藝,沙勇,等.活性炭吸附法處理染料廢水[J].廈門大學學報(自然科學版),2005,44(4):542~545.
[5]劉艷,左燕君.電化學法處理染料廢水的脫色實驗研究[J].環境與發展,2018(1):84~85.
[6]吳支備.劉飛.高級氧化技術在水處理中的研究進展[J].山西建筑,2016,42(8):156~157.
[7]葉招蓮.芬頓試劑催化氧化酸性大紅GR染料廢水的研究[J].江西化工,2003(1):55~58.
[8]曾旭,曾德芳.芬頓氧化深度處理印染廢水的實驗研究[J].廣州化工,2018(1):92~94.
[9]孟寧,歐曉霞,秦雷云,等.芬頓氧化法降解水溶液中甲基橙的研究[J].綠色科技,2018(8):61~63.
[10]周午陽,張朝升,孫志民,等.Cu2+助芬頓法處理高濃度鄰苯二甲酸二甲酯廢水[J].環境工程學報,2014,8(7);2789~2794.
[11]Ling S K,Wang S,Peng Y.Oxidative degradation of dyes in wa-ter using Co2+/H2O2and Co2+/peroxymonosulfate[J].Jour-nal of Hazardous Materials,2010,178(1):385~389.
收稿日期:2019-10-20
基金項目:湖北省高等學校優秀中青年科技創新團隊計劃項目(編號:T201616)
作者簡介:何亞萍(1992-),女,碩士研究生,研究方向為環境化學。
通訊作者:黃升謀(1962-),男,博士,研究方向為環境生化學。

