重癥患者碳青霉烯類藥物血藥濃度監測分析
徐銀麗,郭曉芳,江翊國,梁 培
(1.南京醫科大學附屬蘇州科技城醫院藥學部,江蘇 蘇州 215153;2.南京鼓樓醫院重癥醫學科,江蘇 南京 210008;3.南京鼓樓醫院藥學部,江蘇 南京 210008)
碳青霉烯類抗菌藥物是非典型β-內酰胺類抗菌藥物,通過與青霉素結合蛋白(penicillin-binding protein,PBP)緊密結合,阻礙細胞壁的合成,使細菌迅速腫脹、溶解發揮作用,是時間依賴性抗菌藥物,主要經腎排泄,常用于耐藥陰性菌感染的治療[1-2]。不同的碳青霉烯類藥物抗菌譜、抗菌活性、PK/PD均存在一定差異,不同病理生理狀態也會影響其藥代動力學。本研究目的為監測重癥患者使用常規劑量碳青霉烯類藥物時,血藥谷濃度是否能達到目標范圍,為重癥患者個體化用藥提供數據基礎,優化給藥方案,提高治療的有效性和安全性[3]。
1 材料和方法
1.1 研究對象
采用回顧性研究方法,收集2017年1月至2018年12月某三甲醫院ICU收治的使用碳青霉烯類藥物并監測血藥濃度的重癥患者信息,共計122例患者,排除以下患者:(1)年齡< 16歲;(2)碳青霉烯類藥物過敏史;(3)用藥時間< 48 h;(4)僅監測40%給藥間隔(40%T)血藥濃度而未監測血藥谷濃度;(5)檢驗結果缺失。最終入組85例,比阿培南組17人、亞胺培南組50人、美羅培南組18人。
1.2 治療
藥物信息如下:注射用比阿培南(商品名稱:天冊,0.3 g)、注射用亞胺培南西司他丁鈉(商品名稱:泰能,0.5 g∶0.5 g)、注射用美羅培南(商品名稱:美平,0.5 g)。靜脈滴注給藥,比阿培南組劑量0.3 g,q 12 h ~ 0.6 g,q 8 h不等,5人行連續腎臟替代療法(continuous renal replacement therapy,CRRT)治療;亞胺培南組劑量0.5 g,q 12 h ~ 1 g,q 8 h不等,19人行CRRT治療;美羅培南組劑量0.5 g,q 12 h ~ 1 g, q 8 h不等,10人行CRRT治療。病程中動態監測腎功能,根據肌酐清除率、CRRT治療情況,個體化計算初始劑量并及時調整[4]。CRRT模式除2例連續靜靜脈血液透析濾過(continuous veno-venous hemodia fi ltration,CVVHDF)以外,其他均為連續靜脈血液濾過(continuous veno-venous hemo filtration,CVVH),血液流速180 ~ 250 mL·min-1,置換液流速1000 ~ 3000 mL·h-1。
1.3 數據采集
收集患者年齡、性別、身高、體重、APACHE Ⅱ評分、SOFA評分、主要感染診斷、肝酶、血肌酐、白蛋白、給藥劑量及血藥谷濃度等數據。
1.4 血藥濃度測定
1.4.1 樣本采集 由護士在第4次給藥開始前在患者靜脈抽取2 mL靜脈血標本測定血藥谷濃度(CRRT患者于非泵入側靜脈抽取)。
1.4.2 血藥濃度測定 采用高效液相色譜法,儀器:Agilent 1200型高效液相色譜儀,Agilent 1200色譜工作站(Agilent公司)。血漿前處理:亞胺培南及比阿培南取血后30 min內、美羅培南取血后1 h內,3000 r·min-1離心5 min,取上清液300 μL,加入100 μL穩定劑,旋渦混勻,-80 ℃凍存待測。檢驗方法參照該院及外院相關研究,由血藥濃度監測實驗室進行方法學檢查[5-7]。
1.5 評價指標
碳青霉烯類藥物為時間依賴性藥物,評價其抗菌效果的主要參數是血藥濃度維持在細菌最低抑菌濃度(minimum inhibitory concentration,MIC)以上的時間。療效最大化一般需要40%T > MIC,重癥患者或耐藥菌感染將100%T > MIC甚至100%T > 4MIC設置為目標靶值時可獲得更好的殺菌效應[8]。
1.6 統計學處理
2 結果
2.1 一般資料
單因素方差分析結果顯示患者年齡、性別、身高、體重、APACHE Ⅱ評分、SOFA評分均無顯著性差異(P > 0.05)。主要感染診斷有:膿毒血癥(23人次)、重癥肺炎(18人次)、腹腔或腸道感染(16人次)、血流感染(13人次)、顱內感染(8人次)、重癥胰腺炎(5人次)、復雜皮膚及軟組織感染(燒傷)(3人次)、肝膿腫(2人次)等,同一患者可能存在多部位感染。APACHE Ⅱ評分:急性生理與慢性健康評分。SOFA評分:全身性感染相關性器官功能衰竭評分。詳見表1。
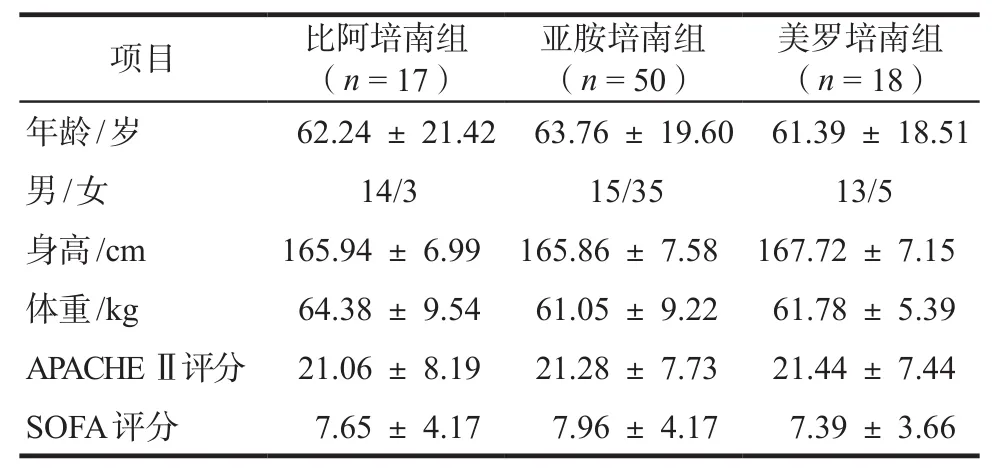
表1 患者一般資料Tab 1 General information of patients
2.2 血藥谷濃度
各組血藥谷濃度結果見表2。各組數據符合正態分布,進行單因素方差分析,美羅培南組血藥谷濃度高于亞胺培南組和比阿培南組,差異有統計學意義(P = 0),后兩組間差異無統計學意義。亞胺培南組和美羅培南組各有3例患者,因檢出耐藥菌(MIC ≥ 16 μg·mL-1),延長滴注時間至3 h,此類患者血藥谷濃度高于各組血藥谷濃度均值。
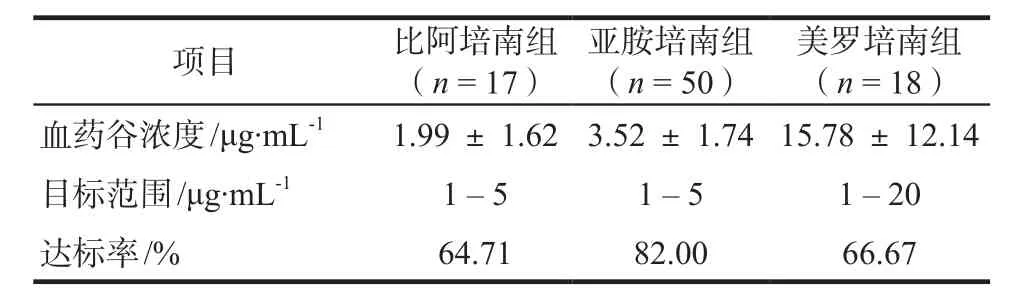
表2 各組血藥谷濃度測定結果Tab 2 Results of serum trough concentrations of each group
2.3 CRRT對血藥谷濃度的影響
根據患者腎功能及CRRT條件,個體化調整給藥劑量。各組CRRT與非CRRT血藥谷濃度分別進行單因素方差分析,結果見表3,差異均無統計學意義(P= 0.71、0.76、0.96)。在及時個體化調整劑量的情況下,CRRT未對碳青霉烯類血藥谷濃度產生顯著影響。
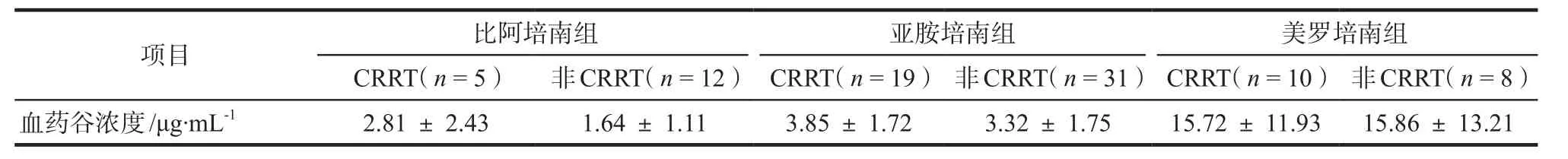
表3 CRRT治療對碳青霉烯類血藥谷濃度的影響Tab 3 In fl uence of CRRT on serum trough concentration of carbapenems
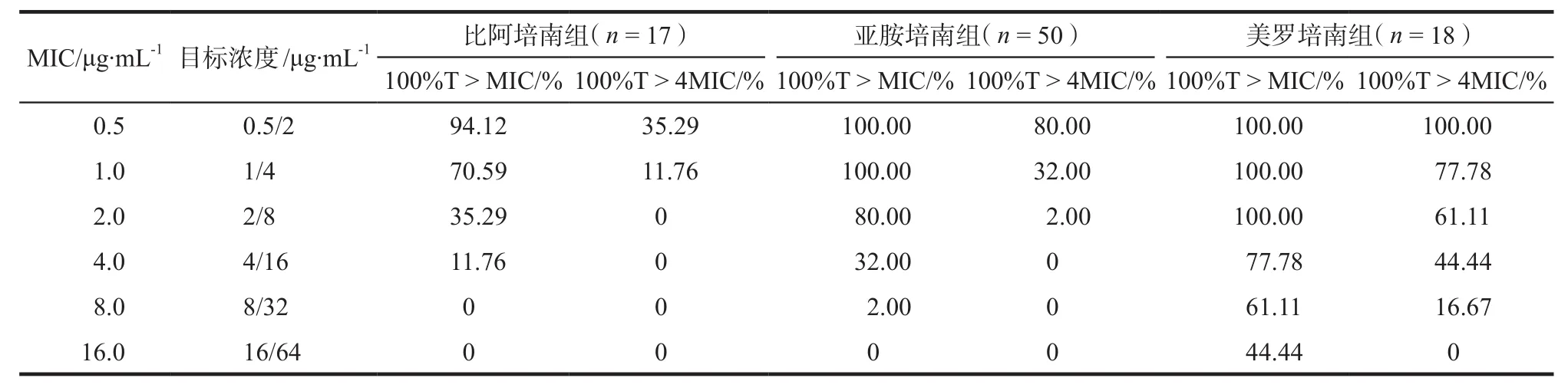
表4 各組PK/PD達標率比較Tab 4 Comparison of PK/PD compliance rate of each group
2.4 PK/PD達標率
不同MIC值時的PK/PD達標率見表4,各組微生物檢出結果見表5,美羅培南組有較高的PK/PD達標率。
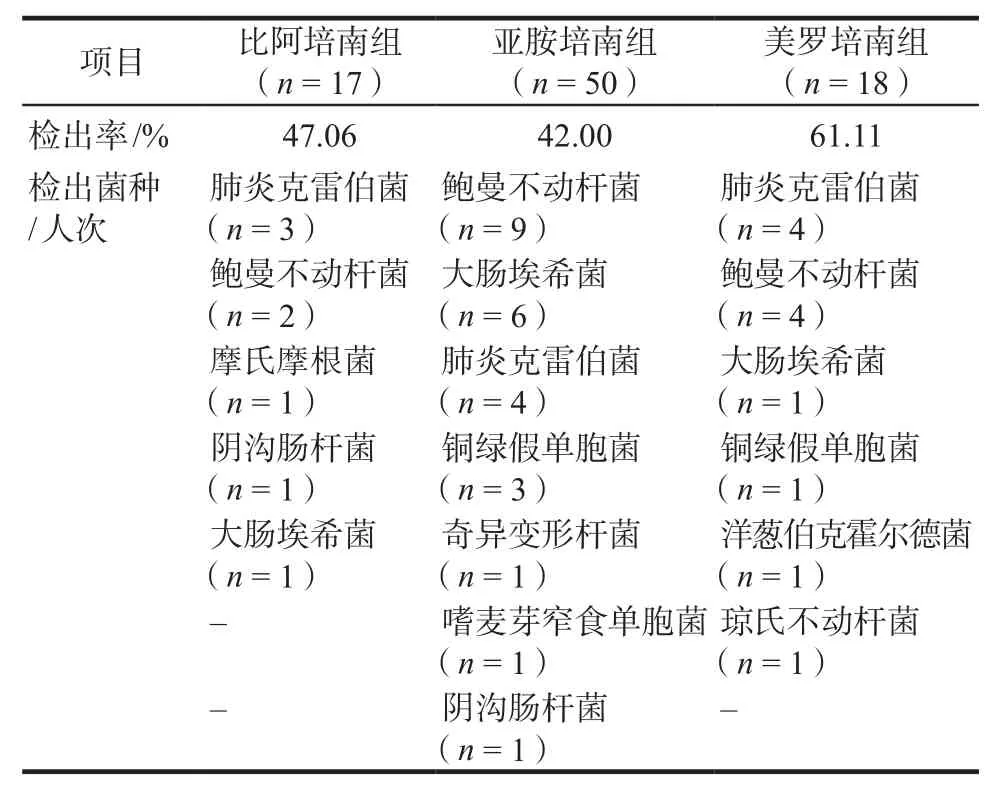
表5 各組微生物檢出結果Tab 5 Etiological results of each group
2.5 碳青霉烯類藥物對肝腎功能的影響
各組間用藥后肝腎功能指標見表6。各組間用藥后各指標比較,差異均無統計學意義(P > 0.05),未出現因藥物性肝腎功能損害而停藥的患者。
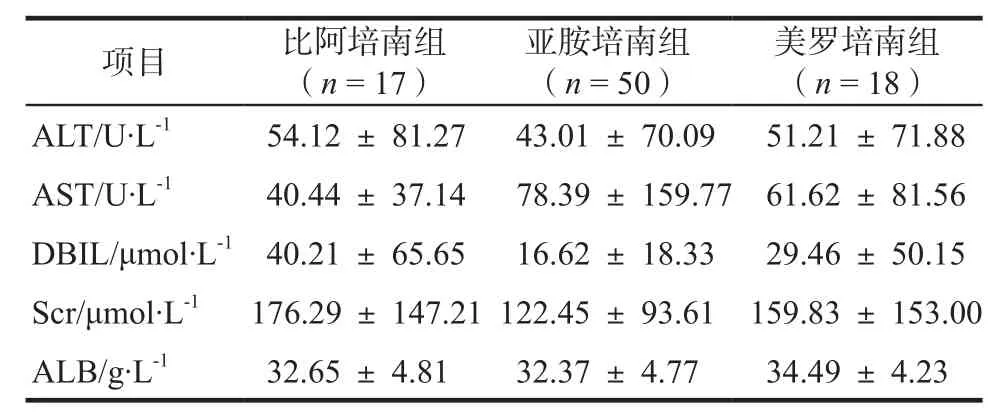
表6 各組用藥后肝腎功能比較Tab 6 Comparison of liver and kidney function after administration of each group
2.6 轉歸
比阿培南組3人死亡,14人好轉。亞胺培南組10人死亡,40人好轉。美羅培南組6人死亡,12人好轉。無患者出現惡心、嘔吐、腎功能損傷等不良反應。亞胺培南組有1人出現中性粒細胞減少,3人出現抽搐,其血藥谷濃度分別為:3.87 μg·mL-1、5.33 μg·mL-1、6.25 μg·mL-1、7.25 μg·mL-1,2人直接停藥,2人改用美羅培南。比阿培南組、亞胺培南組、美羅培南組血藥谷濃度數據經驗證均符合正態分布(Kolmogorov-Smirnov結果P = 0.056、0.062、0.191),分別進行線性回歸分析,線性回歸相關系數分別為R = 0.848、0.289、0.531,R2= 0.719、0.083、0.282,比阿培南組線性相關程度最強,詳見表7。預測變量中僅比阿培南組Scr水平與血藥谷濃度呈顯著相關性(P = 0.003)。
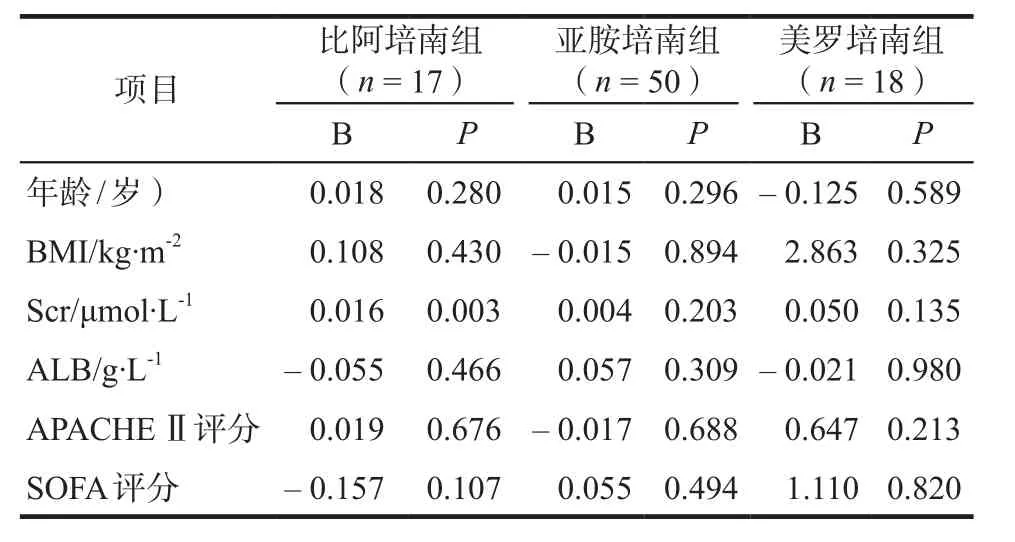
表7 血清藥物谷濃度的線性回歸分析Tab 7 Linear regression analysis of serum trough concentration
3 討論
3.1 重癥患者的特殊病理生理狀態
重癥感染患者通常存在器官功能障礙、心排量高、休克等特殊病理生理狀況,可引起抗菌藥物藥代動力學參數改變,抗菌藥物的合理應用可直接影響患者預后。重癥感染患者以膿毒癥居多,高劑量可確保更高的AUC和T > MIC,使患者獲益更多[3,9]。對于器官功能損害的患者,為避免藥物蓄積加重器官功能損害,也需調整劑量。通過TDM可幫助調整給藥劑量、頻次、輸注時長,優化給藥方案[10-11]。
3.2 基于TDM的碳青霉烯類給藥方案優化
本研究中的藥敏試驗僅做對亞胺培南的MIC值,檢出菌中44.17%為敏感菌(MIC ≤ 1 μg·mL-1),這要求碳青霉烯類藥物血藥谷濃度維持在較高水平,才能達到較好的治療效果。通常有效血藥濃度范圍可將MIC敏感值(1 μg·mL-1)作為下限,當碳青霉烯類藥物血藥濃度達到MIC的4 - 5倍時,殺菌效果趨于飽和,增加劑量并不增加療效,假設MIC = 1 μg·mL-1,通常可將5 μg·mL-1設為上限。亞胺培南致癲癇發生率高于美羅培南,小鼠亞胺培南血藥濃度2 μg·mL-1左右即可引起癲癇,人體研究極少[12-13];比阿培南上市時間短,研究數據稀缺,無明確的致毒性血藥濃度數據;美羅培南與腦神經細胞γ-氨基丁酸受體親和力較弱,神經系統損害較少,治療窗較寬,有研究表明美羅培南50%致腎毒性和癲癇的血藥濃度分別為44.45 μg·mL-1和64.2 μg·mL-1[14]。本研究所在醫療機構將比阿培南、亞胺培南目標濃度范圍定為1 - 5 μg·mL-1,美羅培南定為1 - 20 μg·mL-1。此目標范圍尚不是金標準,各醫療、監測機構并不統一,仍在不斷完善中,并不是判斷有效性和安全性的唯一標準。本研究中比阿培南組和美羅培南組均未出現不良反應,亞胺培南組4人出現不良反應,其中2人改用美羅培南后未出現不良反應。綜合考慮,在MIC相同的情況下,對于腎功能不全易造成藥物蓄積或顱內感染者,美羅培南的有效性和安全性可能更好。
目前,臨床使用比阿培南的常規劑量是0.3 g,q 12 h或q 8 h,但已有研究指出常規劑量并不能達到較好的臨床療效及細菌清除率,日本傳染病協會/日本化療學會(JAID/JSC)發布的呼吸道傳染病治療指南(2016)指出,對于治療產ESBL的克雷伯菌,比阿培南的推薦劑量可達到0.3 - 0.6 g,q 8 h - q 6 h。本研究中比阿培南血藥谷濃度PK/PD達標率低,與劑量較低密切相關。碳青霉烯類均為親水性抗菌藥物,主要經腎排泄,血流動力學不穩定者,液體復蘇或使用血管活性藥物、CRRT等器官支持治療均可加快液體代謝,導致血藥濃度下降[15]。監測血藥谷濃度可驗證其是否在目標范圍內,并通過及時調整劑量提高治療的有效性與安全性。
3.3 研究局限性
因本研究中患者病理生理狀態多樣,血流動力學狀態個體差異大,樣本量少,結果存在一定局限性。線性回歸分析發現僅比阿培南組Scr水平與血藥谷濃度呈顯著相關性(P = 0.003)。亞胺培南和美羅培南組血藥谷濃度與各預測變量無顯著相關性,但Scr的P值最小,提示腎功能可能是一項重要因素,擴大樣本量是深入研究的前提。
綜上,根據藥物品種、特殊的病理生理狀態、血藥谷濃度等可制定碳青霉烯類藥物的個體化給藥方案。美羅培南血藥谷濃度及PK/PD達標率均高于比阿培南和亞胺培南,對于腎功能損傷或顱內感染等特殊患者可能具有更好的療效和安全性。

