我院外科預防使用質子泵抑制劑的干預效果分析
陳 婧,王 明,尹東鋒
(新疆軍區總醫院藥劑科臨床藥理室,新疆 烏魯木齊 830000)
近年來,為預防外科手術后應激性潰瘍的發生,質子泵抑制劑(proton pump inhibitor,PPI)的過度使用現象日益突顯,在增加藥品不良反應發生率的同時,也導致了醫療費用的不合理支出。用藥患者多為常規手術患者,并無應激性潰瘍(stress ulcer,SU)發生的高風險因素[1]。現將我院外科使用質子泵抑制劑預防應激性潰瘍的情況進行干預前后的對比,分析用藥合理性,為外科合理使用PPI提供參考。
1 資料與方法
1.1 資料來源
基于PASS系統,提取我院2018年1 - 6月(干預前)與2018年7 - 12月(干預后)普外科、肝膽外科、骨科、耳鼻喉科、神經外科、泌尿外科、頜面外科、心胸外科、燒傷科、肛腸科使用質子泵抑制劑的病歷,共計2633例,其中干預前預防性使用質子泵抑制劑1651例,不合理的有1124例,不合理率68.08%,干預后預防性使用982例,不合理的有503例,不合理率51.22%。
1.2 評價標準
參考美國衛生系統藥師協會[2](American society of health-system pharmacists,ASHP)、中國藥典:臨床用藥須知[3]、《應激性黏膜病變預防與治療—中國普通外科專家共識》[4]、《應激性潰瘍防治專家建議(2015版)》[5],對此次分析的預防性使用的病歷進行用藥指征、用藥品種、用法用量、用藥時間、相互作用的合理性評價。
具有以下一項危險因素以上的患者應采用預防措施:(1)機械通氣超過48 h;(2)凝血機制障礙[國際標準化比值(INR) > 1.5,血小板< 50×109·L-1或部分凝血酶原時間>正常值2倍];(3)原有消化道潰瘍或出血病史;(4)嚴重顱腦、頸脊髓外傷;(5)嚴重燒傷(燒傷面積> 30%);(6)嚴重創傷、多發傷;(7)各種困難、復雜的手術;(8)急性腎功能衰竭或急性肝功能衰竭;(9)急性呼吸窘迫綜合征(acute respiratory distress syndrome,ARDS);(10)休克或持續低血壓;(11)膿毒癥;(12)心腦血管意外;(13)嚴重心理應激,如:精神創傷、過度緊張等。若同時具有以下任意兩項危險因素時也應考慮使用預防藥物:(1)ICU住院時間> 1周;(2)糞便隱血持續時間> 3 d;(3)大劑量使用糖皮質激素(劑量 > 氫化可的松250 mg·d-1);(4)合并使用非甾體類抗炎藥。
根據SU防治建議,下列情況列為SU的高危人群:(1)高齡(年齡≥65歲);(2)嚴重創傷(顱腦外傷,燒傷,胸、腹部復雜困難的大手術等);(3)合并休克或持續低血壓;(4)嚴重全身感染;(5)并發多臟器功能障礙綜合征(MODS)、機械通氣> 3 d;(6)重度黃疸;(7)合并凝血機能障礙;(8)臟器移植術后;(9)長期應用免疫抑制劑與胃腸道外營養;(10)1年內有潰瘍病史。
1.3 統計學處理
采用SPSS19.0軟件進行統計分析,組間比較采用χ2檢驗,以P < 0.05為差異有統計學意義。
2 結果
2.1 PPI總體使用情況
2018年6月23日經全院合理用藥專題會議及OA系統發布關于《合理使用注射用質子泵抑制劑的情況說明》一周后進行干預。我院干預前后總體PPI使用率有所下降,見表1。抽查的10個外科科室干預前后使用PPIs的分布情況詳見表2。干預前后不同PPI制劑的例數及排序情況見表3,涉及藥品包括注射用蘭索拉唑、注射用泮托拉唑、注射用奧美拉唑、注射用艾司奧美拉唑(因住院醫師開具PPI口服制劑數量極少,此次分析選擇忽略PPI口服制劑),干預前與干預后相比使用率均有所下降,使用量最大的為注射用蘭索拉唑。
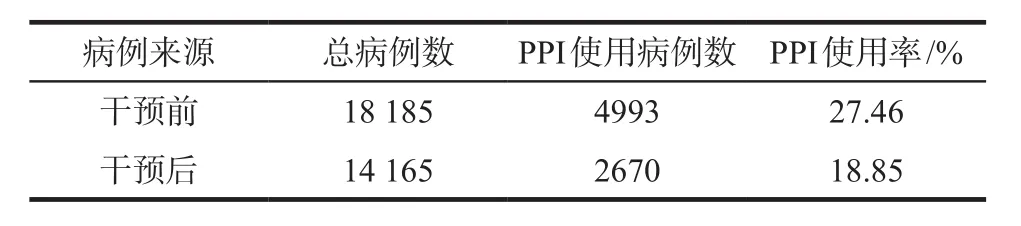
表1 我院干預前后PPI使用率Tab 1 PPI utilization rate before and after intervention in our hospital
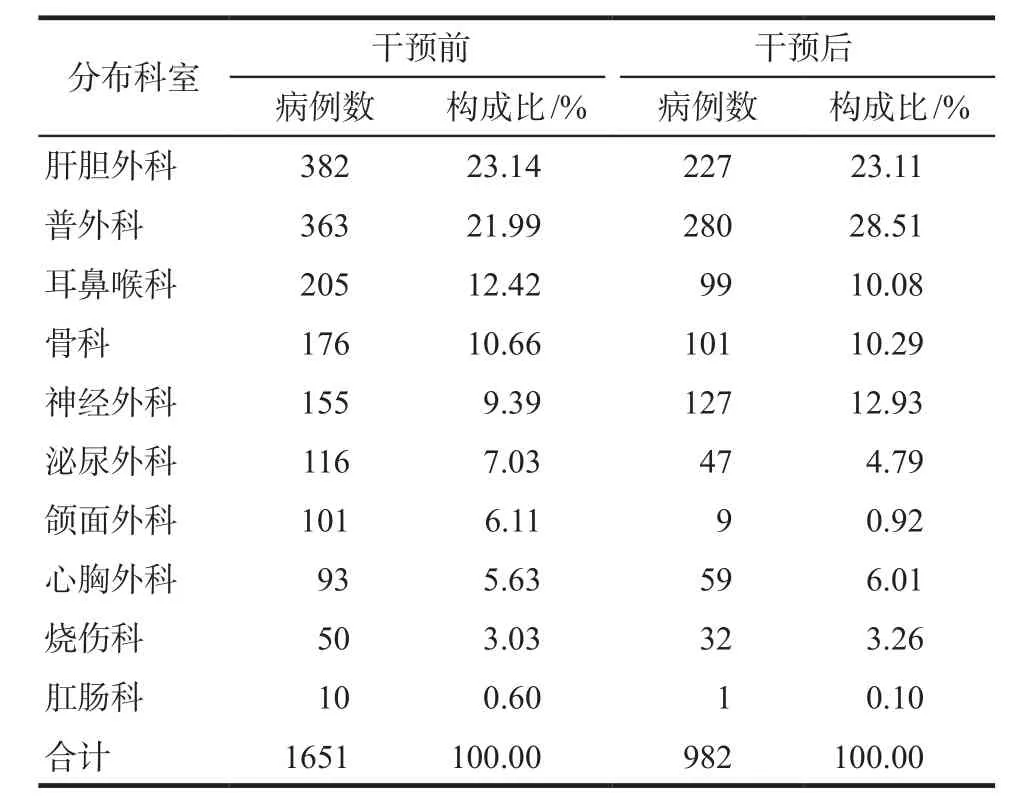
表2 外科使用PPI科室分布情況Tab 2 Distribution of departments using PPI in surgery
2.2 PPI干預前后預防用藥不合理情況分析
本次調查預防用藥不合理情況分別為:無適應證用藥、溶媒選擇不當、療程偏長、相互作用和用法用量不當。其中無適應證用藥為預防用藥不合理情況的主要原因,占80%以上。干預后不合理率各項不合理例數均顯著低于未干預前(P < 0.05),不合理率有所下降,且存在統計學意義,詳見表4。
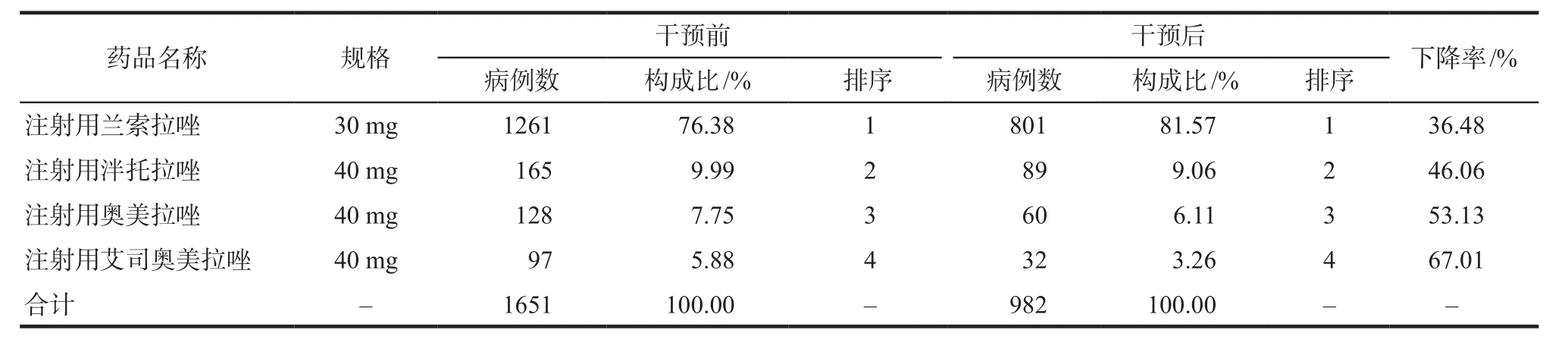
表3 干預前后不同PPI制劑構成比及排序Tab 3 Constituent ratio and order of different PPI preparations before and after intervention
3 討論
3.1 無適應證用藥
無適應證用藥是PPI濫用的主要原因[6]。通過此次分析發現, PPI臨床應用最多的是預防應激性潰瘍,特別是外科圍手術期,無論患者是否存在應激性潰瘍的高風險因素,都常規給予PPI進行預防。有些不存在高風險因素患者的骨折切開復位與內固定術、全膝關節置換術;腹腔鏡下膽囊切除術、腹腔鏡下保膽取石術;喉鏡下扁桃體切除術、鼻內鏡下鼻中隔矯正術等;輸尿管鏡輸尿管結石碎石取石術;肛腸科回腸造瘺術;頜面外科咽部間隙感染切開引流術等,這些手術在做好充分的術前準備及排除高危因素的前提下,術后應激性潰瘍的發生率是非常低的,故不建議患者預防性使用PPI。需加強對醫務人員的藥學培訓,更新用藥知識,避免藥物的過度使用。
3.2 用藥時機及療程
用藥療程偏長是過度使用PPI的另一個主要表現。當調查顯示在預防SU時,全部患者選擇靜脈給藥,且大部分在手術后才開始用藥,導致用藥時機不規范。SU的發生大多集中在原發病發生的3 ~ 5 d內,當患者病情穩定可耐受腸內營養或已進食、臨床癥狀開始好轉或轉入普通病房后可改為口服用藥或逐漸停藥[7]。本次調查中,較多患者預防用藥大于3 ~ 5 d,最長達15 d,有的甚至從手術前用至出院。因我院下半年臥床患者比上半年較多,導致干預后療程偏長的情況比上半年發生率較高。所以,臨床醫師應嚴格把握預防SU的用藥指征,及時停藥,避免加重患者經濟負擔,并減少長期用藥帶來的風險。
3.3 用法用量及溶媒選擇
此次調查中,PPI基本為靜脈給藥。PPI在酸性溶液中不穩定,輔料常用氫氧化鈉來調節pH值,溶媒宜選用0.9%氯化鈉注射液100 mL,靜脈滴注,溶媒體積過大,滴注時間過長,容易出現含量下降、變色、沉淀等情況。本調查中存在蘭索拉唑、泮托拉唑及艾司奧美拉唑使用5%葡萄糖注射液作為溶媒,溶媒量大于100 mL的不合理用藥情況較多,還存在蘭索拉唑q 8 h給藥及單次用藥劑量過大的不合理用藥情況。PPI預防用藥的推薦劑量如下:奧美拉唑40 mg,艾司奧美拉唑40 mg,蘭索拉唑30 mg,泮托拉唑40 mg,推薦頻次均為qd[8]。大劑量艾司奧美拉唑推薦用于急診消化道出血,使用方法為80 mg靜推后,以8 mg·h-1的速度持續靜脈泵入或靜脈滴注[9]。因此,需加強對臨床科室的用藥干預,結合信息化管理,實時預警,避免藥物的濫用。
3.4 藥物相互作用
由于大多數PPI是經CYP2C19和CYP3A4代謝,對細胞色素P450系統均有競爭性抑制效應。而CYP2C19同時參與氯吡格雷的代謝,使其轉化為活性代謝產物而發揮抗血小板作用。本研究結果顯示,PPI在臨床使用過程中多存在藥物間相互作用,如:奧美拉唑與氯吡格雷的相互作用所占比例較高,少數為神經外科癲癇患者使用卡馬西平;頜面外科、耳鼻喉科患者使用激素都可與PPI產生相互作用,臨床藥師均建議臨床換用泮托拉唑進行治療。研究[10]報道,奧美拉唑、蘭索拉唑與氯吡格雷合用會顯著增加患者復發心肌梗死的風險。Hata等[11]學者認為,蘭索拉唑會增強華法林的抗凝作用和增加出血的風險,與其合用時,應監測PT值和INR。潑尼松與埃索美拉唑均為CYP3A4酶的底物,使潑尼松活化受影響,而降低了其療效[12]。卡馬西平也可通過CYP3A4酶,使奧美拉唑的清除率降低[13]。因此建議臨床醫師在選用PPI時,應結合患者個體情況考慮選用合適的PPI,使患者的治療得到應有的療效。
3.5 藥品不良反應
近年來,對PPI不良反應的研究報道越來越多,同時也引起了社會的關注[14]。如骨折、腎病、微觀結腸炎、低鎂血癥和肺炎等[15-19],同時可增加艱難梭狀芽胞桿菌感染和慢性肝臟疾病的風險[20-21]。有研究[22]顯示,PPI用于預防性治療危重患者SU時,其不良反應發生風險顯著高于組胺H2受體拮抗劑。PPI使用不當的主要原因之一為低風險的胃十二指腸潰瘍和非重癥監護病房的患者預防應激性潰瘍,并且往往是被絕大多數醫生認為是一種無害和相對廉價的可治療任何消化問題的基本防范藥品[23]。本次調查中,我院2018年僅有1例患者出現不良反應,在使用注射用艾司奧美拉唑15 min后出現全身皮疹,停藥后皮疹消失。PPI在臨床的應用須引起廣大臨床醫師的關注。
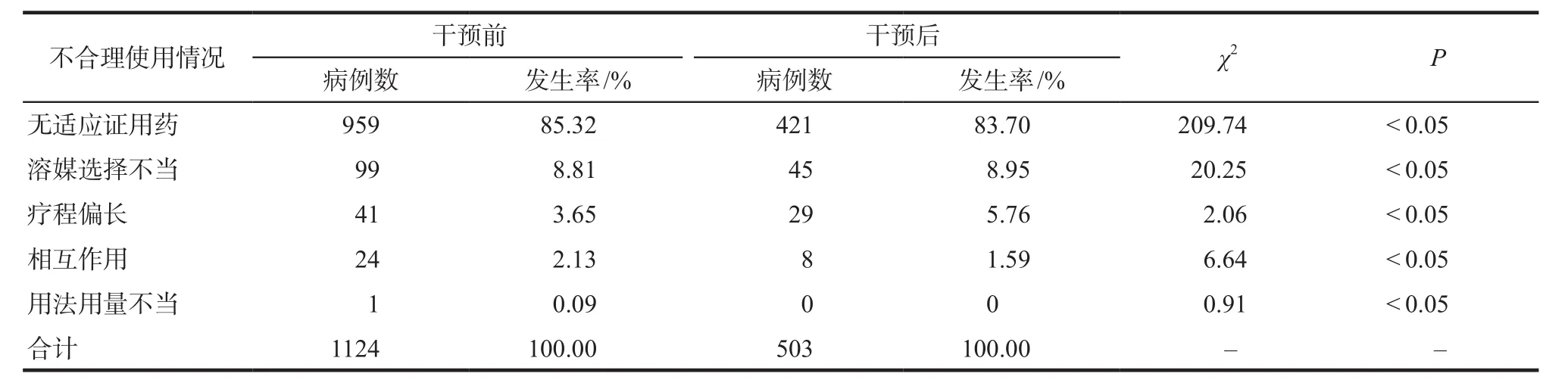
表4 干預前后不合理用藥使用情況統計Tab 4 Statistics of irrational drug use before and after intervention
綜上,通過對我院外科PPI使用合理性的分析,發現臨床仍存在PPI使用不合理的情況,多為無適應證用藥。作為藥學人員應加大處方點評、醫囑審核力度,為醫務人員和患者提供用藥咨詢和宣傳合理用藥知識。同時,建議臨床醫師在選用PPIs時應謹慎:(1)要嚴格用藥前的適應性評估;(2)根據評估結果,結合患者具體情況,制定個體化用藥方案;(3)同時注意在患者用藥期間密切觀察,尤其是聯合用藥時,以保證其療效,減少不良反應的發生,避免過度使用造成醫療資源的浪費。

