足月妊娠口服低劑量米索前列醇引產母嬰結局臨床分析
盧運萍 鐘向真 王潔文 李俊鋒 梁靜兒 黎瑞彬
廣東省東莞市第五人民醫院婦產科 523000
隨著二胎政策的開放,產婦由于高齡常常合并妊娠期高血壓、妊娠期糖尿病等各種疾病,或由于自身體質因素妊娠足月后不能自行發動有效規律的宮縮等,嚴重危害了孕產婦和胎兒的健康[1]。臨床上,引產是各種高危妊娠的有效處理手段,而引產是否成功的關鍵所在是子宮頸的成熟度[2]。常用的促進子宮頸成熟度的干預方法分為應用縮宮素和米索前列醇等藥物刺激,或者宮頸擴張球囊和Foley尿管等物理刺激[3]。有大量研究報道了各種干預手段對孕產婦引產結局以及新生兒的影響,結論不一,臨床上到底采用哪種最優方案還有待定論[4]。相比于各種物理刺激,藥物刺激具有起效迅速的優點,而大量關于米索前列醇的研究報道中,用藥方案均為陰道后穹窿局部置藥,相比于靜滴縮宮素的用藥方案,能更有效促進宮頸成熟,縮短產程,改善母嬰結局[5],但是引產過程中常出現宮縮過強甚至有子宮破裂的報道。本文通過給予75例孕產婦口服低劑量米索前列醇引產的方式來探索其在足月分娩引產中的效果,現報道如下。
1 資料與方法
1.1 一般資料 將2016年1月—2018年12月于我院產科住院分娩的150例具有引產指征、無應用催產素和口服米索前列醇禁忌證的晚期妊娠婦女作為觀察對象,納入標準:(1)孕周≥37周;(2)單胎、足月、胎膜完整,且胎位為頭先露;(3)具有下列引產指征中的至少1項:① 孕周≥41周;② B超診斷羊水過少,羊水指數(AFI)≤5cm;③患有妊娠期高血壓;④患有妊娠期糖尿病;⑤患有其他需要終止妊娠的疾病;⑥宮頸成熟度Bishop評分≤6;⑦無應用催產素和口服米索前列醇禁忌證。排除標準:(1)前置胎盤;(2)胎盤早剝;(3)子宮疾病手術史;(4)產前有出血史;(5)存在生殖系統感染;(6)頭盆不稱;(7)合并惡性腫瘤;(8)合并重要臟器的功能不全;(9)存在精神障礙;(10)凝血功能異常;(11)嚴重妊娠合并癥、并發癥不適宜陰道分娩者。150例晚期妊娠的孕產婦根據隨機數字表法分為觀察組75例和對照組75例,兩組在平均年齡、平均孕周、初始宮頸Bishop評分等一般資料比較上差異無統計學意義(P>0.05),具有可比性,見表1。
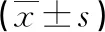
表1 兩組患者的一般資料比較
1.2 用藥方法 觀察組用藥方法為將0.2mg米索前列醇完全溶解于100ml生理鹽水中,給予產婦8ml(16μg)/次,每8h口服1次,每次口服米索前列醇前進行宮頸Bishop評分,連續口服3d,若有規律宮縮,即每5~6min 1次,每次持續30s,則停止給藥。對照組用藥方法為將2.5U縮宮素溶解于500ml 0.9%氯化鈉中緩慢靜滴3d,初始速率為8滴/min,然后根據產婦的宮縮、胎心率情況,每30min增加4滴/min,直至出現有效的宮縮,即10min內3次,每次持續30~60s,最大滴速不超過40滴/min,每隔8h進行宮頸Bishop評分;兩組產婦期間如果宮頸Bishop評分≥6分者,進行人工破膜,破膜后1~2h無有效宮縮予靜滴催產素引產,以成功陰道分娩視為引產成功。用藥3d宮頸Bishop評分<6分或仍然沒有進入臨產的孕產婦,轉剖宮產。
1.3 評估指標 包括每組的陰道分娩率=(總例數-轉剖宮產例數)/總例數×100%;宮頸成熟度Bishop評分;臨產時間(開始引產到臨產的時間);總產程;分娩時間(開始引產到分娩的時間);產后出血量;新生兒Apgar評分、臍動脈血氣pH值、新生兒窒息率。
1.4 統計學方法 所有數據均采用SPSS21.0來分析處理。計量資料采用(均數±標準差)表示,兩組間比較采用student-t檢驗,計數資料采用[n(%)]表示,組間比較采用χ2檢驗。當P<0.05時認為差異有統計學意義。
2 結果
2.1 兩組孕產婦陰道分娩率及臨產前Bishop評分比較 觀察組陰道分娩70例,轉剖宮產5例,陰道分娩率為93.33%(70/75);對照組陰道分娩62例,轉剖宮產13例,陰道分娩率為82.67%(62/75);觀察組的陰道分娩率明顯高于對照組,差異有統計學意義(χ2= 4.040,P=0.044)。臨產前,觀察組的宮頸Bishop評分(10.03±1.72)分明顯高于對照組的(7.92±1.45)分,差異有統計學意義(t=8.123,P=0.001)。
2.2 兩組孕產婦分娩情況比較 觀察組的臨產時間、總產程、分娩時間以及產后出血量明顯少于對照組,以上差異均有統計學意義(均P<0.05),見表2。
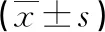
表2 兩組孕產婦分娩情況比較
2.3 兩組新生兒情況比較 觀察組的新生兒Apgar評分和臍動脈血氣pH值明顯高于對照組,差異均有統計學意義(均P<0.01);兩組均無重度窒息新生兒,且輕度窒息新生兒例數無明顯差異(P>0.05),見表3。
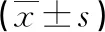
表3 兩組新生兒情況比較
3 討論
米索前列醇是前列腺E的衍生藥物,其經口服后迅速吸收入血,藥代動力學監測顯示在口服2min后即可在外周血中檢測到米索前列醇,15min后血藥濃度即可到達峰值,90min后可以完全被吸收,其從血液中清除的半衰期約為30min,主要排出途徑為腎臟。大量的動物及人體實驗結果顯示米索前列醇對胎盤和胎兒無明顯副作用[6]。米索前列醇能使妊娠各時期的子宮肌產生強烈的收縮,其中妊娠晚期的子宮肌對米索前列醇最為敏感,且其收縮力的大小具有劑量依賴性,而米索前列醇用藥發生嚴重并發癥的主要原因在于用藥劑量過大或用藥指征不符合[7]。有研究顯示,米索前列醇用藥劑量過大可以引起宮縮過強和羊水糞染,胎兒產生宮內窘迫,嚴重時甚至導致羊水栓塞和子宮破裂等危及生命的并發癥[8]。因此,米索前列醇在臨床應用中都推薦以小劑量應用為主。
較多的用法是小劑量米索前列醇局部放置于陰道后穹窿,用藥期間應該密切監測宮縮以及胎心率,一旦出現宮縮過強或者胎心持續異常時,立刻取出殘余米索前列醇,給予孕產婦吸氧處理,必要時可以應用宮縮抑制劑,如口服硝苯地平或滴注25%的硫酸鎂松弛子宮。在米索前列醇應用效果的研究中,有報道顯示相比于靜滴催產素引產,小劑量米索前列醇引產的成功率更高,且安全性好,母嬰均無明顯的不良反應[9]。一項大樣本量的循證醫學研究結果顯示,使用米索前列醇進行引產的晚期妊娠婦女與靜滴催產素引產相比,宮縮過強以及胎兒宮內窘迫等不良反應發生率更低,引產成功率高[10]。在本文中,采用的口服低劑量米索前列醇引產的方式,相比于陰道后穹窿局部放置的應用方法,其用藥劑量更小,引起宮縮過強以及胎兒宮內窘迫等不良反應發生率更低。結果顯示,口服低劑量米索前列醇引產可以提高陰道分娩成功率,縮短臨產時間、總產程和分娩時間,減少產后出血量,且新生兒的Apgar評分、臍動脈血氣pH值更高(均P<0.01)。最近有新的研究報道顯示新生兒發生血清總膽紅素升高與孕產婦應用米索前列醇引產有一定的相關性[11],針對該科學問題還需要擴大樣本量的進一步研究來證實。
總之,口服低劑量米索前列醇引產可以有效促進宮頸成熟,縮短產婦的臨產、分娩和產程,且對母嬰的安全性高,值得在臨床推廣應用。

