羧甲基殼聚糖對鈾的促排及腸道菌群的影響
姚亦天,吳梓茹,歐陽杰,張曉燕,李仁艷,李 昊,潘媛媛,黃德娟
(東華理工大學 化學生物與材料學院,江西 南昌 330013)
鈾的毒性表現在化學毒性和放射性毒性兩方面。人體攝入鈾的途徑主要有吸入含鈾氣溶膠、攝入被鈾污染的水或食物;植物方面,鈾溶液能對大豆幼苗細胞DNA造成損傷,影響其萌發率、生根等[1];動物方面,長期接觸低劑量鈾,動物會發生基因突變,生殖功能和造血系統也會受到損害,鈾主要會對蓄積器官(腎臟、骨組織)及敏感器官(睪丸)產生毒害。
人體腸道內微生物數量達100萬億個[2],超過1 250種,統稱為腸道菌群。這個巨大而復雜的微生物群落從消化、營養吸收、能量供給、免疫調節和抵抗疾病等多方面影響人和動物的生理與病理狀況[3]。調整腸道菌群失調的較好方法是益生元補菌,促進雙歧桿菌、乳桿菌等腸道有益菌的增殖,維持腸道菌群平衡。多糖類物質因能夠增強肌體健康、延緩細胞衰老而得到廣泛研究[4-5]。重金屬的攝入會造成動物和人體腸道菌群結構發生特異改變;反之,腸道菌群及其代謝產物又為宿主抵御重金屬進入肌體提供“屏障”功能[6]。
殼聚糖(chitosan)是自然界中唯一的堿性多糖,主要來源于節肢動物、軟體動物的外殼及真菌的細胞壁,無毒無害,生物相容性好,具有抗腫瘤和增強肌體免疫功能的作用,可以抑制真菌、酵母菌和細菌等的繁殖[7];同時殼聚糖能與鈾形成螯合物[8]。但殼聚糖不溶于水,使其應用受到很大限制,其衍生物羧甲基殼聚糖在水溶性及生物活性等性能方面都有提高[9];但羧甲基殼聚糖對體內鈾染毒的解毒效果尚未見有報道。因此,從小鼠體質量變化、體內菌群數量、肝腎中鈾含量等方面研究羧甲基殼聚糖對染鈾小鼠的解毒效果,以期為鈾解毒提供安全無害的方法,也為進一步開發殼聚糖的生物活性提供新思路。
1 試驗部分
1.1 動物、試劑與儀器
SPF級昆明小鼠48只,雄性,6~8周齡,體質量30~40 g,購于南昌大學撫州醫學分院。
0.2 mg/mL鈾溶液,偶氮胂Ⅲ,鹽酸,乙二胺四乙酸二鈉(Na2-EDTA),無水乙醇,濃硝酸,過氧化氫溶液,生理鹽水,質量分數為10%的羧甲基殼聚糖,LBS(乳桿菌)培養基,EMB(大腸桿菌)培養基,BS(雙歧桿菌)培養基,EC(腸球菌)培養基。
可調式電熱板,手提式不銹鋼壓力蒸汽滅菌鍋,紫外可見分光光度計,凈化工作臺,光照培養箱,臺式離心機,電子天平,生物解剖器,電熱鼓風干燥箱,聚四氟乙烯坩堝。
1.2 試驗方法
1.2.1 分組與處理
將48只小鼠隨機分為3組,每組各16只。
空白組:腹腔注射生理鹽水2周+灌胃生理鹽水2周;
中毒組:腹腔注射鈾溶液2周+灌胃生理鹽水2周;
試驗組:腹腔注射鈾溶液2周+灌胃羧甲基殼聚糖2周。
每周結束后,3組各解剖4只,通過3組間相互對照,觀察鈾對小鼠的毒害作用及羧甲基殼聚糖的解毒效果。
1.2.2 體質量稱量
每天在喂食前稱量各小鼠體質量,觀察不同組別間小鼠的外貌特征(如眼睛、皮毛)。
1.2.3 腸道微生物的培養
每2~3 d收集一次鼠便,梯度稀釋,在超凈工作臺中涂布接種4種主要腸道微生物(雙歧桿菌、乳桿菌、大腸桿菌、腸球菌),放入培養箱中于37 ℃下培養48 h。
1.2.4 肝腎中鈾質量分數測定
每周解剖一批小鼠,取其肝腎,用分光光度法在652 nm波長下測定鈾的吸光度,再推算鈾質量分數。
1.3 數據處理
每組小鼠體質量以平均值±標準誤差表示,用單因素方差分析法比較各組間小鼠體質量、菌群數量、肝腎中鈾質量分數的差異,用sigmapolt 12.0軟件對這些變量進行作圖對比分析。
2 試驗結果與討論
2.1 狀態及體質量變化
1)注射鈾溶液后,部分小鼠死亡,存活小鼠體質量有明顯下降,與空白組(生理鹽水組)有極顯著差異;存活小鼠出現毛發變粗糙、無光澤,尾巴顆粒狀凸起,食欲不振等癥狀:這應是鈾對小鼠肌體造成了毒害作用。繼續給鈾,中毒組小鼠體質量有所回升,但依然與空白組有顯著差異。因此推測,如繼續給鈾,小鼠會逐漸對鈾耐受,從而出現體質量變化不大的情況(圖1)。
2)停止腹腔注射鈾,中毒組與試驗組體質量均有回升,而空白組在第4周基本無變化。對3組曲線走勢分析,在第4周時試驗組體質量逐漸偏離中毒組,而靠近空白組。表明小鼠停止鈾染毒后,灌胃羧甲基殼聚糖對體質量回升更有效(圖2)。
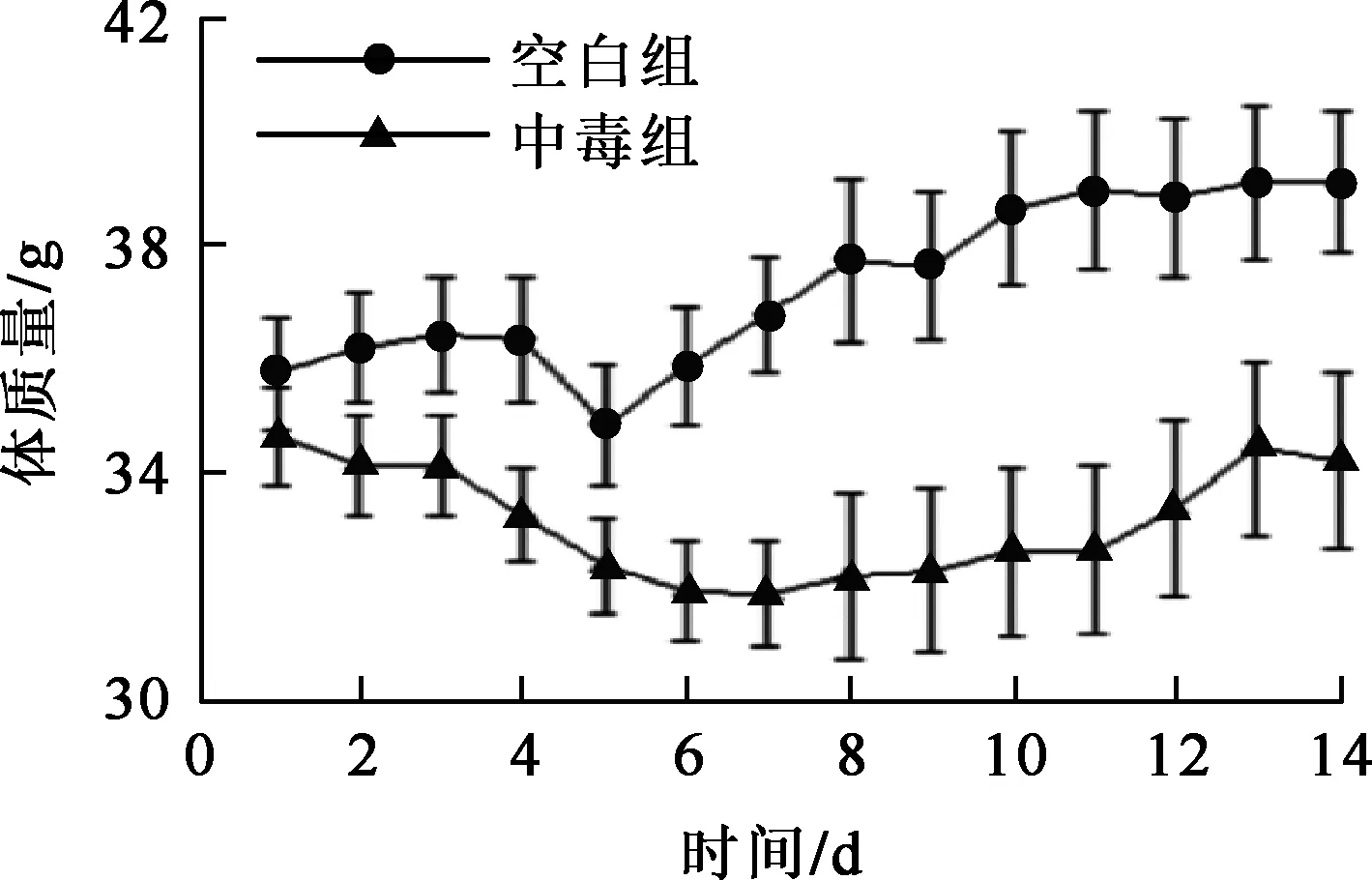
圖1 第1、2周小鼠體質量變化
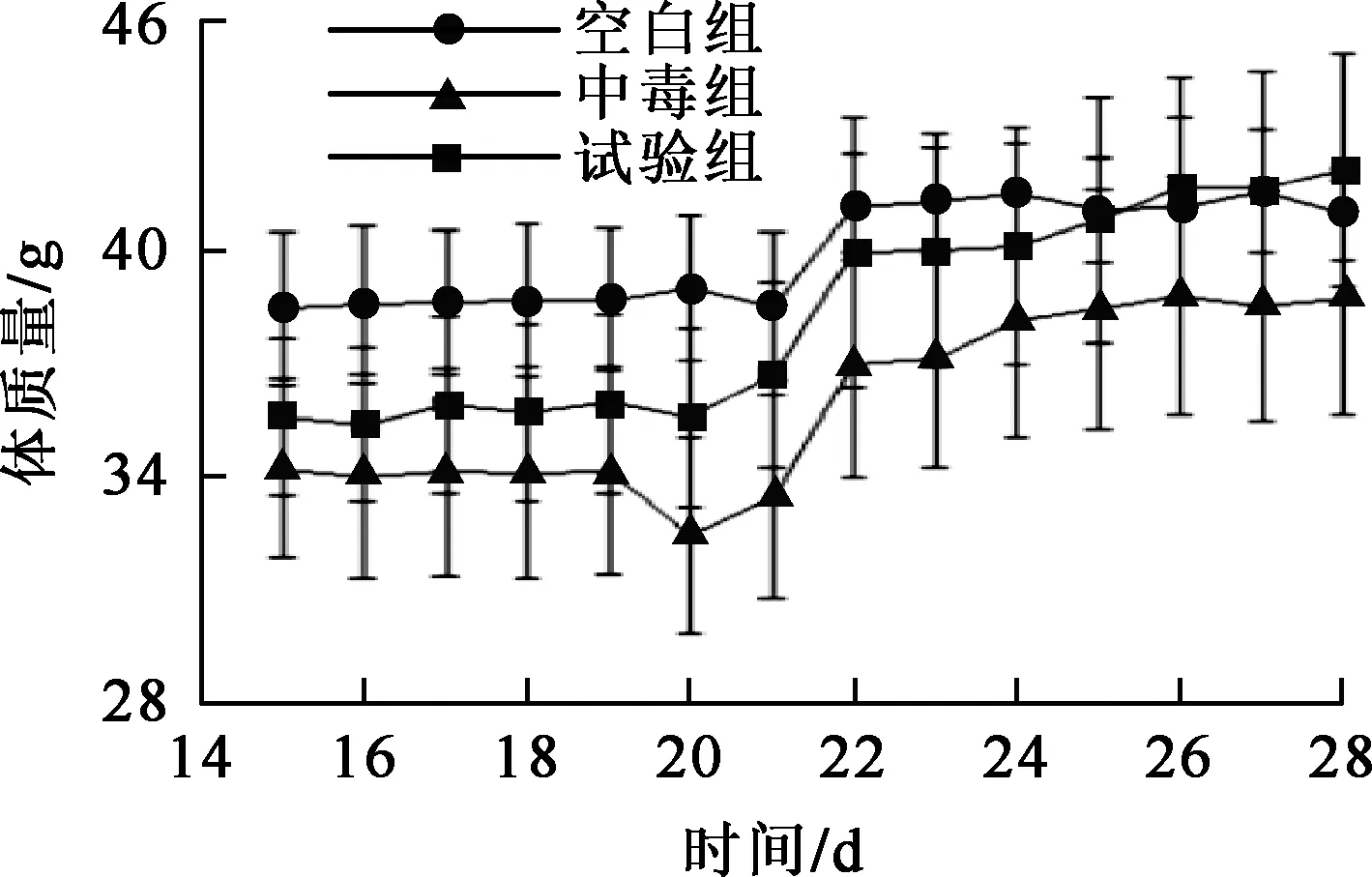
圖2 第3、4周小鼠體質量變化
2.2 腸道菌群數量變化
1)鈾染毒后的第1、2周內,小鼠體內的主要菌群(乳桿菌、雙歧桿菌、腸球菌、大腸桿菌)與空白組均無顯著差異,這與文獻[10]的結論一致,推測鈾損傷肌體與腸道菌群無必然聯系。
2)灌胃羧甲基殼聚糖后,第3周3組小鼠的腸道菌群無顯著變化;第4周試驗組乳桿菌數量升高,并與其余2組形成顯著差異(圖3);而雙歧桿菌、腸球菌、大腸桿菌在第4周仍無顯著差異(圖4~6)。
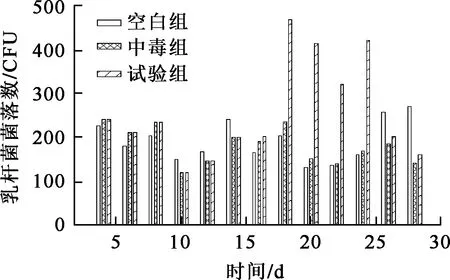
圖3 4周內3組小鼠腸道中乳桿菌數的變化
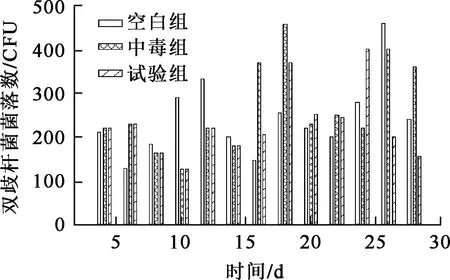
圖4 4周內3組小鼠腸道中雙歧桿菌數的變化
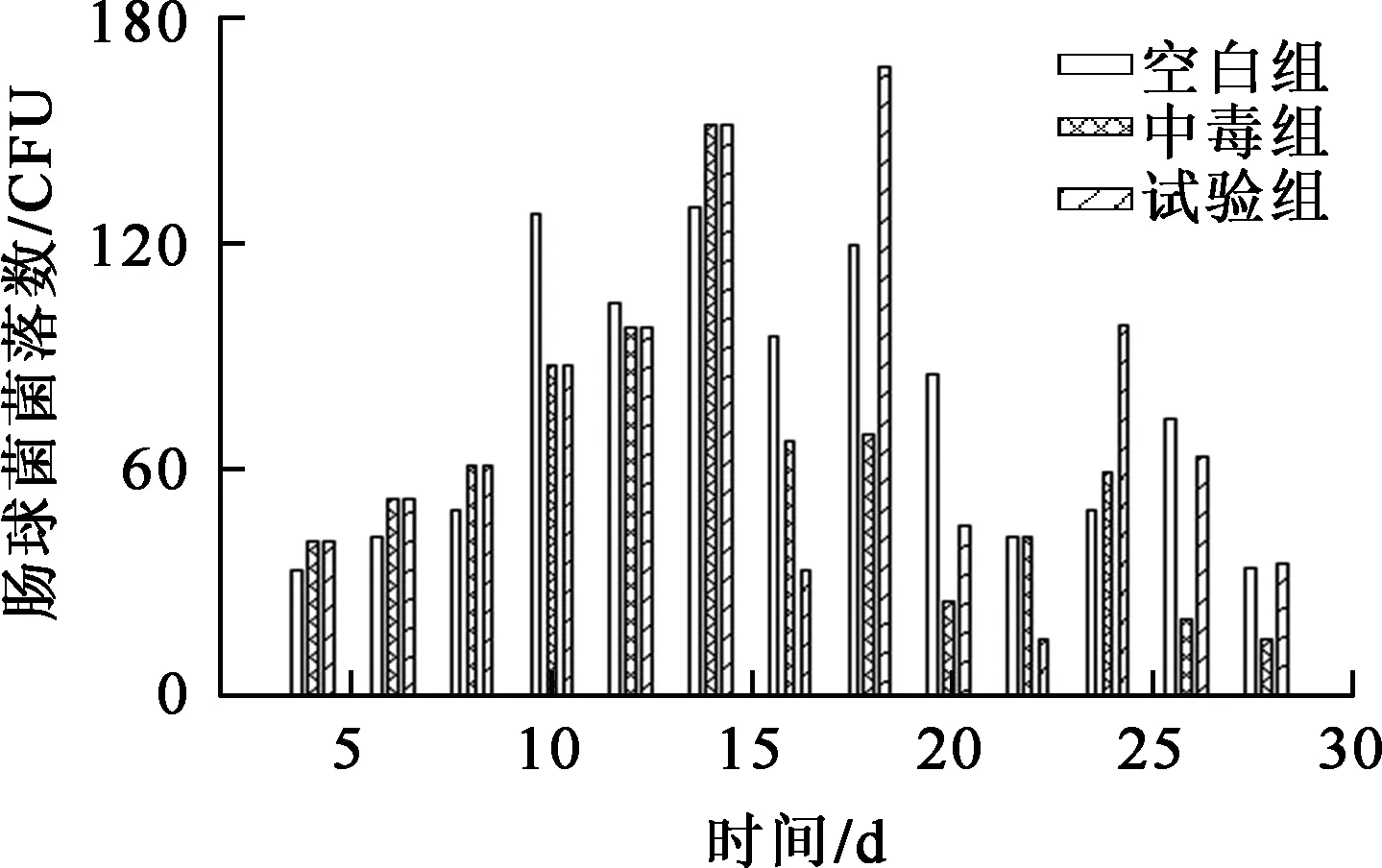
圖5 4周內3組小鼠腸道中腸球菌數的變化
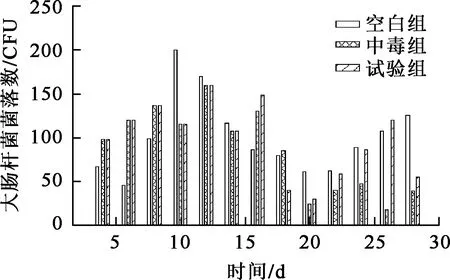
圖6 4周內3組小鼠腸道中大腸桿菌數的變化
由圖3看出,即使在鈾染毒不利情況下,灌胃羧甲基殼聚糖仍然對小鼠腸道乳桿菌產生了促進增長作用[11]。乳桿菌是人體腸道中的正常優勢菌,其代謝產物使腸道環境偏酸性,有利于宿主消化和吸收[12];乳桿菌可以抑制病原菌,防止病原菌附著于腸上皮細胞表面,維持人體腸道微生態平衡[13];乳桿菌還能夠增加腸道中淋巴細胞數[14],增強肌體免疫力。可以推測,羧甲基殼聚糖促進了乳桿菌的增長,從而在一定程度上使小鼠更快恢復健康。
2.3 肝腎中鈾質量分數變化
4周內中毒組、試驗組小鼠腎臟和肝臟中鈾質量分數變化情況如圖7、8所示。結果表明:
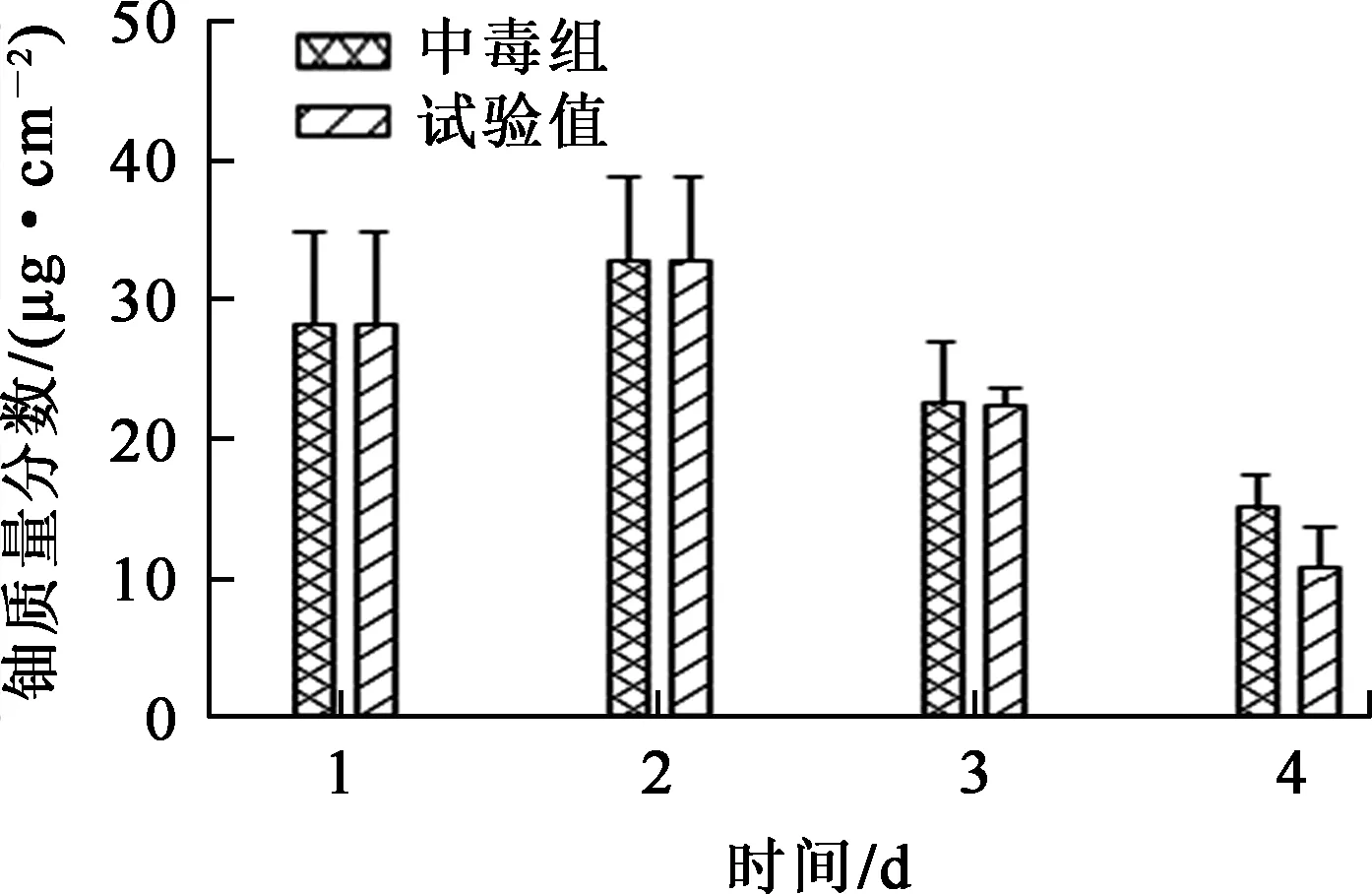
圖7 4周內中毒組、試驗組小鼠腎臟中鈾質量分數變化
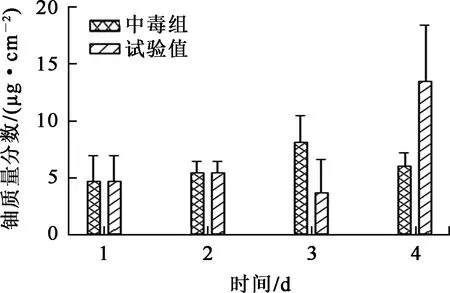
圖8 4周內中毒組、試驗組小鼠肝臟中鈾質量分數變化
1)腹腔注射小鼠第1周,中毒組、試驗組小鼠的腎臟中鈾質量分數明顯升高,與空白組有極顯著差異,而肝臟中鈾質量分數升高幅度不大,與空白組無明顯差異;第2周,中毒組、試驗組小鼠腎臟中鈾質量分數依然與空白組有極顯著差異,肝臟中鈾質量分數相比第1周有所升高,與空白組形成明顯差異。這說明鈾在腎臟中的富集比在肝臟中的富集速度快,且富集量也多,相對于肝臟來說,腎臟是鈾的主要富集器官。這與文獻[15]的結論一致。
2)灌胃羧甲基殼聚糖的2周內,圖7中試驗組的腎臟鈾質量分數呈現更快的下降趨勢,但與中毒組尚未形成顯著差別;圖8中試驗組的肝臟鈾質量分數反而上升,與預期不符,有待進一步分析。
2.4 肝腎鈾質量分數與體質量之間的關系
試驗中發現,小鼠灌胃羧甲基殼聚糖后,肝臟中鈾質量分數不降反升,且肝臟變黑且顏色較腎臟更深;但從小鼠生理狀況看,該組小鼠恢復健康情況更佳:因此推測,羧甲基殼聚糖與鈾形成螯合物會在小鼠肝臟中匯集,導致肝臟中鈾質量分數升高;但因形成螯合物,使得鈾酰離子無法再解離出來,從而對小鼠僅有低毒害作用。
基于以上推測,采取演繹推理法,從另一個角度分析試驗組數據,驗證試驗組注射羧甲基殼聚糖2周內的體質量變化與鈾在肝腎中富集量之間的關系。
以試驗組4只小鼠第29天體質量減去第15天體質量作為體質量變化值,以肝腎試驗組對空白組的吸光度表示鈾質量分數相對值;考慮到肝臟中鈾酰離子與羧甲基殼聚糖形成螯合物的假設,則肝臟中鈾質量分數相對值減去腎臟中鈾質量分數相對值即為螯合物相對值(見表1)。

表1 螯合物相對值與小鼠體質量的變化
以螯合物相對值為x軸,體質量變化值為y軸,繪制回歸曲線,獲得回歸方程及相關系數,結果如圖9所示。可以看出:肝臟中,螯合物相對值與體質量變化呈正相關關系(R2=0.971 6),可認為鈾酰離子與羧甲基殼聚糖在肝臟中形成了無毒性或低毒性的螯合物。
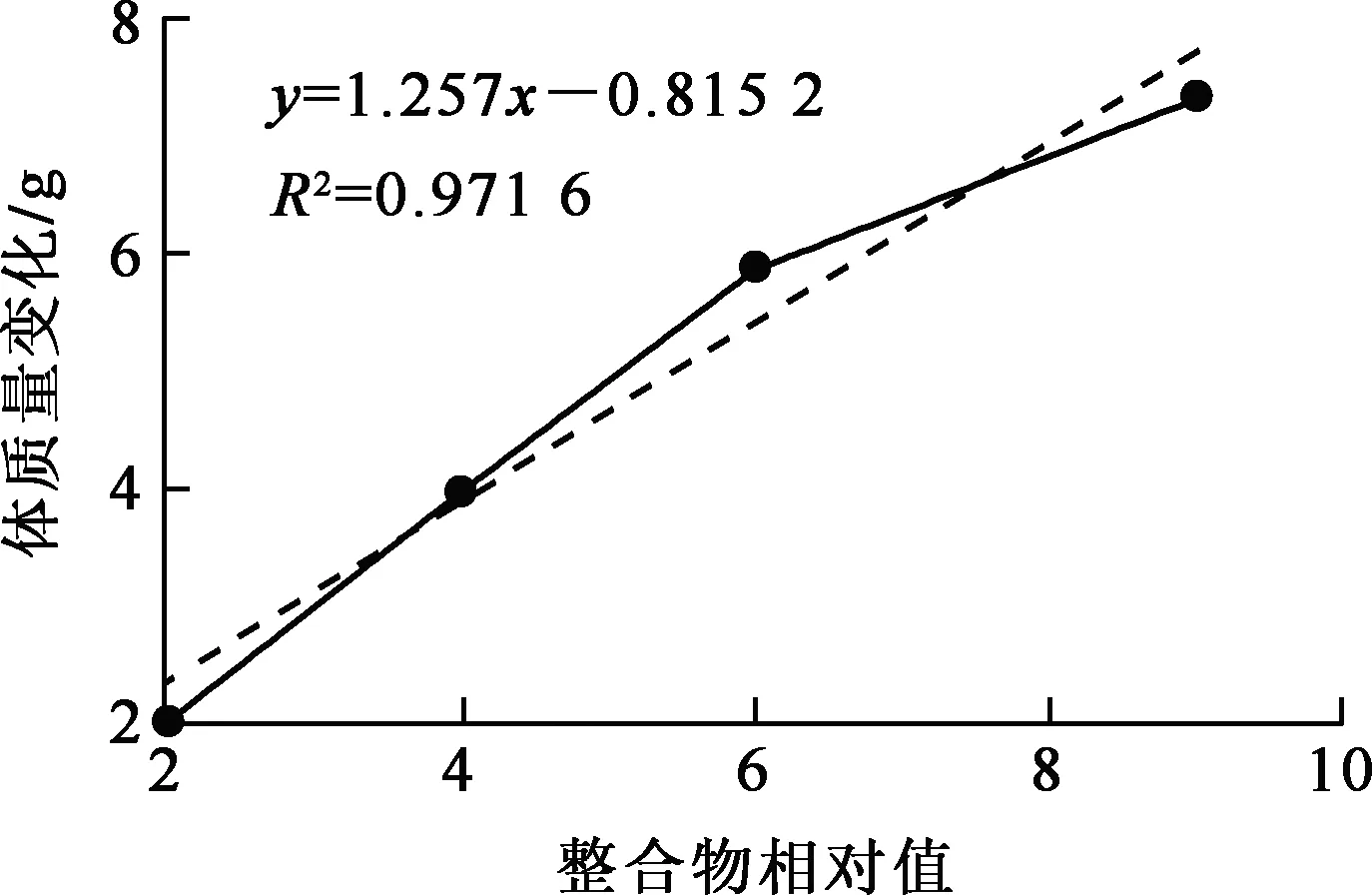
圖9 小鼠體質量變化-螯合物相對值的回歸曲線
3 結論
從小鼠體質量及外貌特征(皮毛等)的變化來看,鈾染毒對小鼠有危害作用,出現部分個體死亡情況;小鼠肝腎中的鈾有顯著積累,但腸道菌群無顯著變化。對鈾染毒后的小鼠灌胃羧甲基殼聚糖,小鼠有恢復健康跡象,并且腎臟中鈾質量分數呈下降趨勢,腸道中乳桿菌數量也有所增加。可以推斷,羧甲基殼聚糖對鈾染毒有促排、解毒正向作用,并且可作為腸道菌群的一種益生元,促進乳桿菌增殖。
目前的鈾促排化合物均不能達到理想效果,因此根據與鈾的配合能力強、毒副作用小、生物相容性好、天然等特點,研究殼聚糖衍生物——羧甲基殼聚糖,進一步提高其水溶性、對鈾的吸附能力,可為鈾促排劑的研發提供新材料,也為開發益生元及尋找新的生物活性物質提供理論依據。
對含鈾廢水的處理、鈾的體外吸附等問題已有研究,殼聚糖及其衍生物對腸道菌群的影響近年來也有許多研究,但機體鈾中毒后,水溶性殼聚糖對鈾的解毒效果、腸道菌群的影響尚未見有報道。尋找一種生物相容性好、吸附性能好、毒副作用低的鈾促排劑,同時將水溶性殼聚糖開發為益生元,加入到食品中,具有重要意義。

