加壓流化床反應器中煤焦化學鏈氣化實驗與數值模擬研究
郭欣桐, 常國璋, 譚曉莉, 胡修德, 郭慶杰
(寧夏大學 省部共建煤炭高效利用與綠色化工國家重點實驗室 化學化工學院,寧夏 銀川 750021)
合成氣作為應用廣泛的原料氣,有“萬物源頭”的美譽。中國新型煤化工產業的蓬勃發展,對煤制合成氣關鍵技術提出了高效清潔的要求[1]。傳統煤氣化技術常采用空氣、富氧氣體或純氧與煤的燃燒為氣化反應供熱,存在燃燒損失大,化學能利用率低的問題[2]。
化學鏈氣化(CLG)是一種新型的煤氣化技術,具有使CO2內分離的優點,且利用載氧體(OC)的氧化熱實現自熱平衡,省去空分裝置,達到降低能耗和環保的要求,受到了國內外學者們的廣泛關注[3-5]。隨著化學鏈氣化技術發展的逐漸成熟,其工業化應用成為目前的研究熱點之一。其中,操作壓力不僅是煤氣化反應速率及氣體產物組成的重要影響因素,而且加壓還可提升氣化爐的生產能力。因此,研究加壓條件下的煤化學鏈氣化過程的規律對其工業化應用具有重要意義。
煤焦氣化速率慢是制約化學鏈氣化系統整體效率的重要問題[6],因此,燃料反應器的設計及其內部反應機理一直是研究的熱點。Liu等[7]對燃料反應器中的煤氣化反應特性進行了研究,發現氣化劑-煤和煤-載氧體間的傳質限制是反應速率的控速步驟。Wei等[8]研究了Fe基載氧體的反應性能和褐煤與載氧體比例對合成氣評價的影響,結果表明:載氧體晶格氧的釋放促進了合成氣的產生;當氣化劑-煤的傳質受限時,過量的載氧體對化學鏈氣化更為有利。Zhang等[9]對比了加壓燃料反應器分別選用流化床和固定床運行方式的性能差異,發現煤和載氧體的反應性能與操作壓力和所采用的操作方式密切相關。其中,固定床中的氣化速率和CO2濃度要明顯高于流化床反應器。綜上分析,煤、載氧體和氣化劑構成的多相反應體系存在著傳質、流體動力學和反應平衡之間的相互影響,采用宏觀實驗的方法難以掌握單一因素的作用規律。
數值模擬是一種有效的研究方法,可將煤化學鏈氣化復雜體系模型解耦,以掌握其多相流動特性和多相反應行為間的影響規律,但目前未見相關研究報道。由于化學鏈氣化與化學鏈燃燒(CLC)的技術原理和工藝裝置類似,因此可借鑒當前化學鏈燃燒的CFD模擬研究方法。Wang等[10]將煤和Fe基載氧體顆粒擬流體化,對循環流化床提升管中的氣-固相流動和化學反應過程進行了CFD模擬,得到了氣、固組分濃度以及各反應速率的分布特征。Su等[11]采用雙流體模型對其課題組開發的5 kWth燃煤化學鏈燃燒(CLC)雙循環流化床系統進行了熱態模擬,從流動規律和燃燒效率著手優化了運行工況。以上是針對煤CLC系統進行的模擬研究,與化學鏈氣化的運行工況及評價指標截然不同。CLC為滿足CO2捕集率的最大化,載氧體與煤物料的配比遠高于化學鏈氣化工藝,因此在顆粒濃度分布、煤氣化反應速率與載氧體還原反應速率比值上有較大差異[12]。此外,操作壓力對于顆粒流態化以及宏觀反應行為也會產生影響,而針對加壓煤化學鏈氣化的相關實驗和模擬研究還未見報道。
隨著計算顆粒流體動力學(CPFD)的發展,在歐拉流體模型和拉格朗日運動模型的基礎上,提出了將相同性質的顆粒視為“顆粒微團”的簡化計算方法,可表現不同屬性顆粒流動特征,且最大程度節約了計算成本[13]。
筆者以Fe2O3/Al2O3為載氧體,以實驗用加壓流化床反應器為原型,建立了CPFD熱態模擬反應器模型進行模擬,結合實驗,對加壓流化床系統中的煤焦加壓化學鏈氣化過程進行研究,分析加壓下煤焦和載氧體的多相流動及其對化學鏈氣化反應的影響,得到了加壓下不同價態Fe基載氧體還原反應速率對化學鏈氣化性能和合成氣品質的影響規律。
1 實驗和模擬部分
1.1 實驗部分
以內蒙鄂爾多斯煙煤為原料,在管式爐中以 20 K/min 的速率升至1223 K,恒溫30 min制焦,破碎篩分出粒徑為20~120 μm的煤焦。以Fe(NO3)3·9H2O(分析純,國藥控股化學試劑有限公司產品)為前驅體,以γ-Al2O3(分析純,國藥控股化學試劑有限公司產品)為載體,采用浸漬法在363 K下混合攪拌12 h,然后在393 K下干燥12 h,接著在1233 K下煅燒3 h制備質量分數為40% 的Fe2O3/Al2O3復合載氧體。經破碎篩選,得到與煤焦相同粒徑(20~120 μm)的復合載氧體樣品。煤和煤焦的工業分析和元素分析見表1。
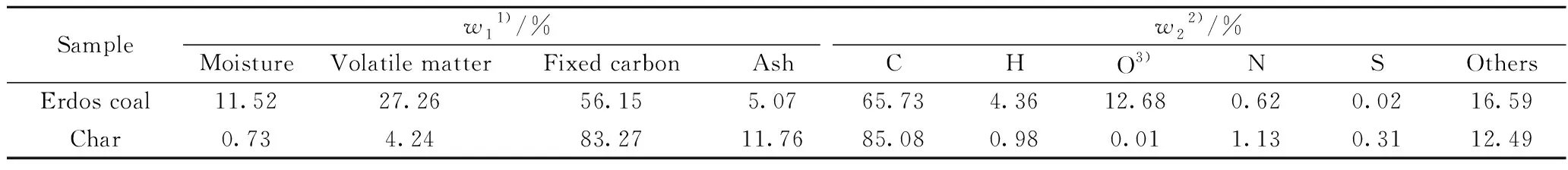
表1 煤和煤焦工業分析和元素分析Table 1 Proximate and ultimate analyses of coal and char
圖1為實驗用加壓流化床反應器,由進料器、供氣裝置、反應器、加熱爐(控溫系統)、蒸汽發生器、冷凝分離器、流量計、氣體分析及數據采集等裝置所構成。流化床反應器主體高800 mm,內徑30 mm,反應溫度以管芯反應床料中部為準。蒸汽發生器由柱塞恒流泵和預熱爐組成,通過調節去離子水的流量,精確控制蒸汽質量流率。
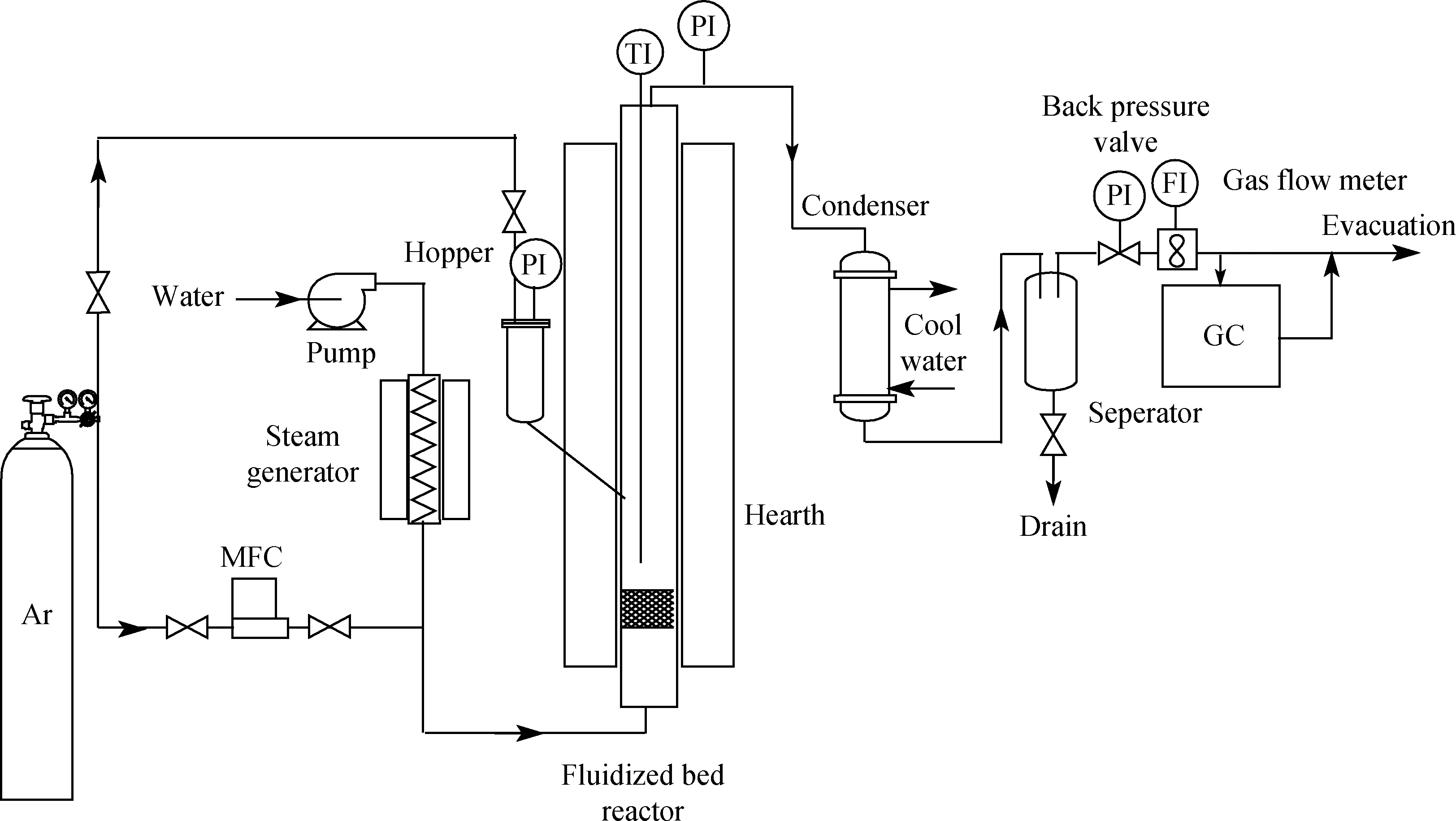
圖1 加壓流化床反應器裝置示意圖Fig.1 Schematic diagram of a pressured fluidized bed reactorMFC—Mass flow controller; TI—Temperature indicator; PI—Pressure indicator; FI—Flux indicator; GC—Gas Chromatography
將2 g煤焦和35 g載氧體顆粒混合均勻后加入料斗內,組裝反應器各部件,確認氣密性良好后,用氬氣吹掃置換系統內的空氣;調節系統總壓升至實驗所需壓力(0.1~0.5 MPa);蒸汽發生爐和反應床升至1193 K后打開柱塞泵,注入水蒸氣(H2O: 85%,Ar: 15%,均為體積分數);操作氣速均設定為0.14 m/s。反應器內氣相濃度平衡后,將料斗中煤焦和載氧體顆粒吹入反應器床層進行流化。
反應器的干燥氣體產物取樣后立即用氣相色譜(GC7820,北京中科惠分儀器有限公司產品)進行組分分析。實驗結束后,用Ar吹掃冷卻反應器,收集還原態載氧體進行表征分析。
1.2 模擬部分
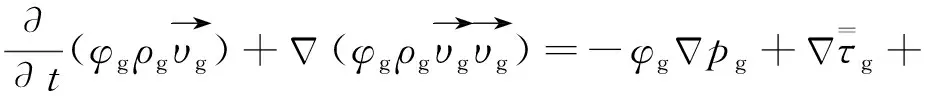
1.2.1 多相流流體動力學模型
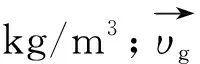
(1)
式(2)為各氣相組分的輸運方程,其中wi,g為氣相中組分i的質量分數,%;氣相組分i在氣-固相間的傳質速率用方程等號右側項表示,其中Ji,g為氣相中組分i的擴散通量[15],kg/(m2·s)。
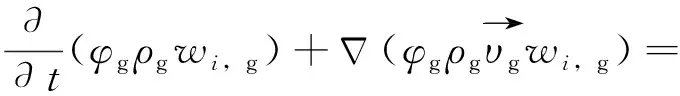
(2)
(3)
(4)
因加壓條件下流化床反應器內的顆粒分布發生改變,所以選取兼具密相和稀相區均適用的Wen-Yu/Ergun Blend模型,如式(5)和(6)所示。其中:φp為顆粒相體積分數,%;φcp為顆粒緊密充填時的體積分數,%;曳力系數(Cd)是雷諾數(Re)的函數[17];ρp為顆粒密度,kg/m3;rp為顆粒半徑,m;D1和D2分別表示顆粒相體積分數小于0.75φcp和大于0.85φcp時的氣-固相間曳力作用,kg/(m3·s)。
(5)
(6)
連續相和顆粒相的能量守恒方程分別如式(7)和(8)所示。其中,Hg為氣相的焓值,J/kg;Qgp為顆粒相與流體相間的對流傳熱,W/m2;λg為導熱系數,W/(m2·K);TBulk為顆粒相主體溫度,K;Tp為顆粒溫度,K;mp為顆粒質量,kg;Cp為顆粒相比熱容,J/(kg·K);h為熱傳遞系數,J/(m·K);Ap為顆粒比表面積,m2/kg;fh為顆粒相傳熱比。煤焦和載氧體單顆粒的溫度變化通過氣-固相間換熱和吸收的反應熱(HR,J/kg)表示。
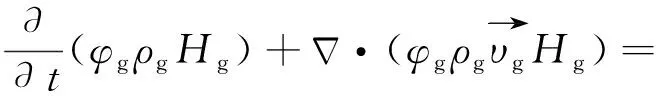
(7)
(8)
式(9)為顆粒相的Lagrange離散運動方程,其中F為其他作用力相源,N;τp為顆粒相的應力張量,Pa[18];g為重力加速度,m/s2。
(9)
1.2.2 多相反應動力學模型
燃料反應器中多相復雜反應體系包括煤焦氣化反應、水煤氣變換反應、甲烷化反應及載氧體還原反應。筆者所在課題組在前期研究中發現,煤焦氣化產物中CH4摩爾分數小于1%(如圖4所示),因此模型中未引入甲烷化反應及其與載氧體的還原反應。
(1)煤焦氣化反應
在煤焦氣化過程中,氣化劑為H2O和CO2,如式(10)和(11)所示。
C(s)+H2O(g)→CO(g)+H2(g)
(10)
C(s)+CO2(g)→2CO(g)
(11)
當煤焦氣化反應決速步驟受動力學控制時,使用式(12)的Langmuir-Hinshelwood方程形式計算煤焦氣化速率(Rg,mol/(s·m3))[19]。
(12)
由表1知,煤焦的固定碳和灰分總質量分數達95%,因此水分和揮發分的熱解過程未加考慮。式(12)中:crea為氣化劑濃度,mol/m3;cpro為氣化產物濃度,mol/m3;mc為加入煤焦質量,g;drea為反應器內徑,m;h為反應器高度,m;k為反應速率常數,m3/(mol·s),由表2通過阿倫尼烏斯方程獲取。

表2 煤焦氣化動力學參數Table 2 Kinetic parameters of coal char
(2)水煤氣變換反應
如式(13)所示,氣相產物CO可以與氣化劑H2O發生水煤氣變換反應,產生CO2和H2,從而改變氣相產物中的組分比例。煤氣化工業生產中,常采用該方法對合成氣中氫/碳比進行調節。
CO(g)+H2O(g)→CO2(g)+H2(g)
(13)
水煤氣變換反應速率(Rs,mol/(s·m3))如式(14)所示,其中yH2O、yCO2、yH2、yCO分別表示H2O、CO2、H2和CO的摩爾分數[11],%;E=218 kJ/mol,A=1.89×107m1.5/(mol0.5·s),α=0.5,β=1,R=8.314 J/(K·mol);平衡速率常數Keq由式(15)獲取[20]。
(14)
(15)
(3)Fe2O3/Al2O3載氧體的還原反應
Fe2O3載氧體隨晶格氧釋放深度的不同,被還原為Fe3O4、FeO以及Fe 3種還原態。實驗中氣化劑H2O的體積分數為85%,采用XRD對還原態載氧體分析(圖11),未觀察到單質Fe,因此對Fe3O4和FeO進行多相反應動力學模擬,反應過程如式(16)~(19)所示。
H2(g)+3Fe2O3(s)→2Fe3O4(s)+H2O(g)
(16)
CO(g)+3Fe2O3(s)→2Fe3O4(s)+CO2(g)
(17)
H2(g)+Fe2O3(s)→2FeO(s)+H2O(g)
(18)
CO(g)+Fe2O3(s)→2FeO(s)+CO2(g)
(19)

(20)
(21)
(22)
式(22)為載氧體還原反應速率(Rr,mol/(s·m3))計算公式,式中mOC為載氧體加入量,g;其他動力學參數如表3所示。

表3 載氧體還原反應動力學參數[10,21]Table 3 Reduction kinetic parameters of oxygen carriers
1.2.3 條件設定
按照圖1的加壓流化床反應器建立了三維反應器幾何模型。對模擬的網格結構、適當的單元數和時間步長進行了測試和確定,考察了反應器出口氣體組分濃度與網格數的關系。結果表明:網格數設定為1235時,模擬結果穩定。
采用降速法模擬了混合顆粒(煤焦和載氧體)床層壓降(Δp,Pa)與表觀氣速(U,cm/s)的流化關系,如圖2所示,獲取了雙組分混合顆粒體系的初始流化速度(Uif)、臨界分離速度(Ubf)、完全流化速度(Uff)和最小流化速度(Umf)。由圖2可知,隨著表觀氣速的增大,混合顆粒的流化曲線可分為4個流化狀態:固定床狀態A、輕顆粒流化重顆粒靜止狀態B、不完全流化狀態C和完全流化狀態D。相對應的3種雙組分顆粒混合狀態可分為完全分離狀態(U=Ubf)、部分混合或部分分離狀態(Ubf
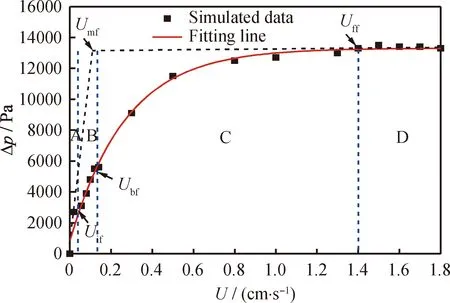
圖2 混合顆粒(煤焦和載氧體)床層壓降隨表觀氣速變化的流化曲線Fig.2 Fluidization curves between pressure drop and velocity of binary mixtures
采用阿基米德準數(Ar)式(23)和終端沉降雷諾數(Ret)式(24),通過式(25)分別得到了煤焦和載氧體顆粒的終端速度ut,Char=5.0 cm/s,ut,OC=11.6 cm/s。
(23)
(24)
(25)
其中:?為運動黏度,m2/s。設定的表觀操作氣速(14.0 cm/s)遠大于煤焦顆粒終端速度(5.0 cm/s),是其2.8倍,接近湍流狀態(典型湍流狀態時U是ut的3倍)。因此,該表觀操作氣速下存在煤焦顆粒被氣流帶出的現象。為防止未反應完的煤焦被氣流帶出,在實驗反應器出口處安裝了過濾器,阻止顆粒的流出。同理,模擬反應器的出口處進行了邊界條件設置:只允許氣相流出,禁止顆粒流出。其他初始條件及邊界條件與實驗工況保持一致,如表4所示。
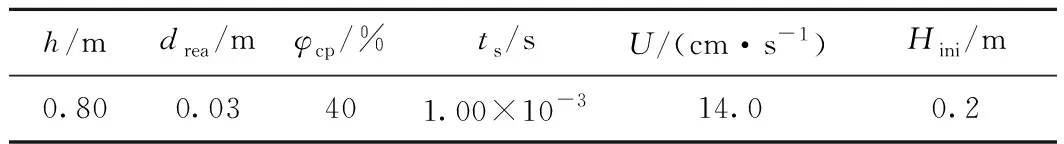
表4 模型初始條件及邊界條件Table 4 Initial and boundary conditions of model
2 結果與討論
2.1 模擬結果
圖3為30 s時的顆粒種類分布、顆粒溫度、壓力梯度(pg,Pa)及水蒸氣的體積分數(φH2O,%)分布。壓力梯度為出口壓力與局部壓力的差值。Hrea為反應器軸向高度,m。由圖3可知,煤焦和載氧體顆粒混合均勻,未出現明顯分層;顆粒溫度穩定在設定溫度±3 K范圍內;壓力梯度小于0.028 MPa;水蒸氣體積分數近似等于85%。因此,模擬邊界條件以及初始設置滿足實驗工況要求。
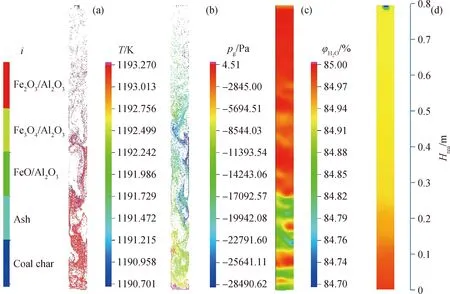
圖3 穩定流形時的顆粒種類分布、顆粒溫度、壓力梯度及水蒸氣的體積分數分布特征Fig.3 The characteristics of stable fluidization pattern(a) Particle specie; (b) Particle temperature; (c) Pressure gradient; (d) Volume fraction of H2O
為確保模擬結果的準確性,對模擬壓力p在0.1~0.5 MPa下的模擬反應結果進行驗證。模擬反應開始25 s后,在0.1 s時間步長內,濃度值標準偏差在1%以內波動。因實驗中氣體產物捕集操作時存在時間誤差,所以實驗和模擬的產氣分析結果取2 min內的平均值進行比較,反應時間10 min時反應器出口各氣體組分摩爾分數(y)對比結果如圖4 所示(除去H2O和Ar)。由圖4可知,模擬結果隨壓力的變化趨勢與實驗結果基本一致,H2、CO、CO2摩爾分數的相對誤差分別為4.16%、11.36%、21.73%,模擬結果與實驗值的偏差在可接受的誤差范圍內。因此,建立的煤焦加壓化學鏈氣化反應模型可靠,模擬結果可信。
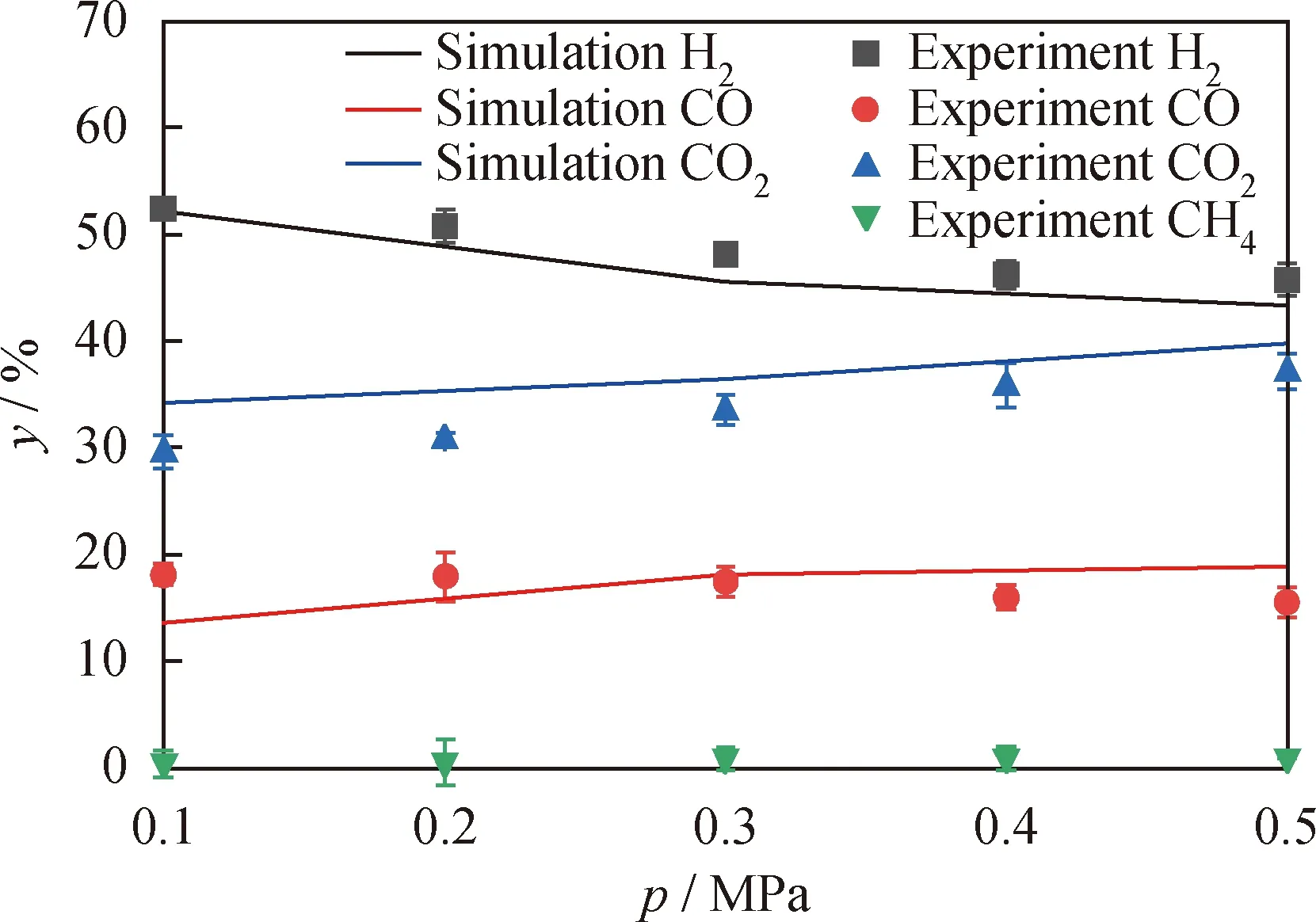
圖4 不同壓力下反應器出口氣體組分摩爾分數模擬結果和實驗值的對比Fig.4 The comparison of simulated and experimental molar fraction of gas components at reactor outlet under different pressures t=10 min
2.2 操作壓力對煤焦和載氧體混合顆粒流態化特征的影響
為研究煤焦和載氧體顆粒的加壓流動形態,考察燃料反應器內顆粒體積分數及壓降分布隨壓力的變化。圖5為模擬壓力在0.1~0.5 MPa下的瞬態顆粒體積分數。由圖5可以看出,壓力升高,連續相對顆粒相的曳力作用增大,煤焦和載氧體顆粒的流形由柱塞逐步轉變為湍流流態化,促進了煤焦顆粒與氣化劑的接觸。湍流過程中煤焦和載氧體顆粒的碰撞接觸,使載氧體與氣化產物間的還原反應在煤焦顆粒的四周均勻發生。此外,0.1~0.2 MPa時密相區和稀相區的分界清晰;隨著壓力的繼續升高,分界逐步模糊;壓力大于0.3 MPa時出現了過渡區。這說明加壓促進了流態化的穩定,床層中氣泡逐漸變小。
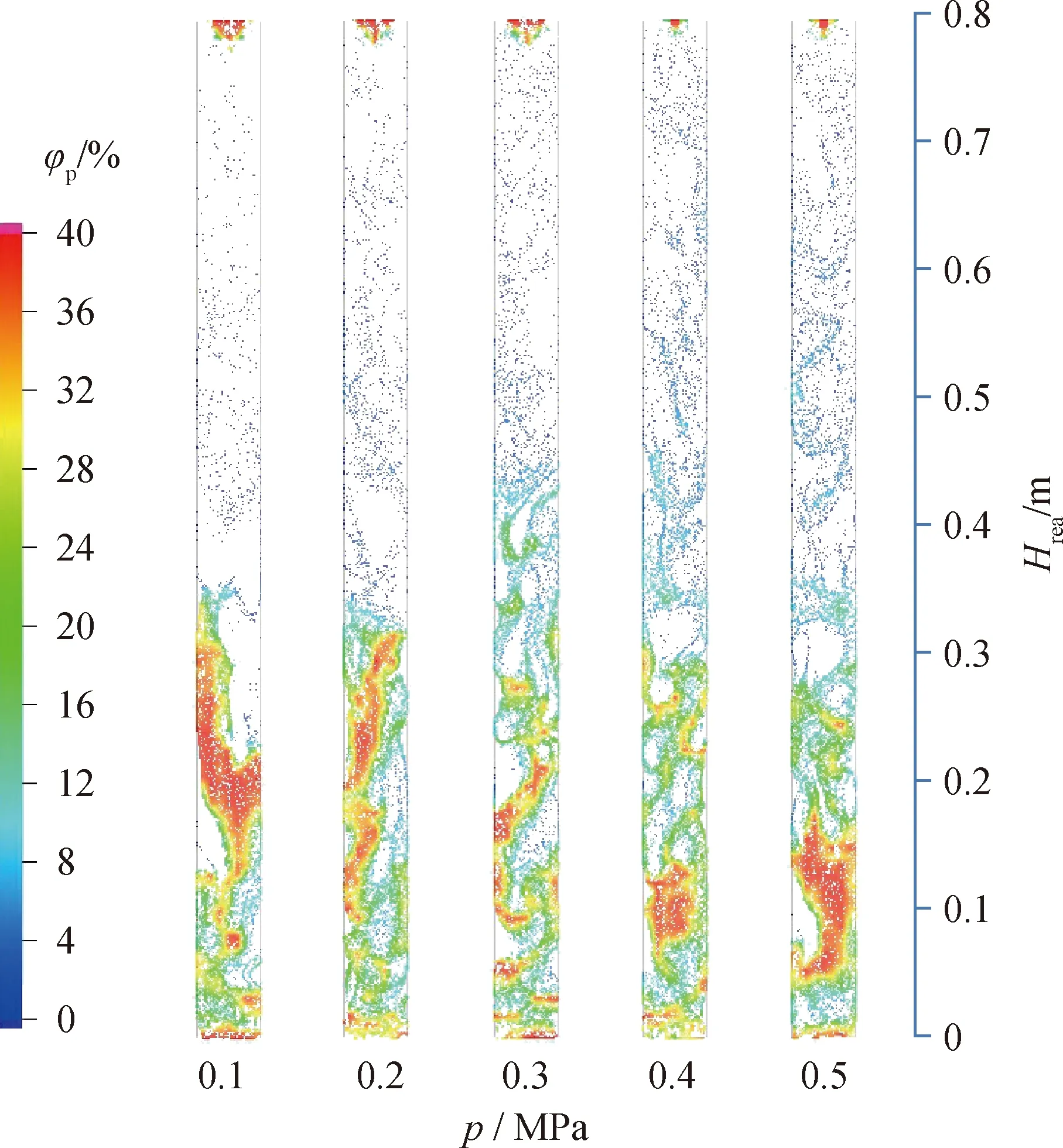
圖5 瞬態顆粒體積分數隨壓力的變化Fig.5 The variation of instantaneous particles volume fraction with pressures
圖6為不同模擬壓力下,反應器內軸向壓降(Δp,kPa)分布。由圖6知,同一模擬壓力下,隨著軸向高度的升高,壓降逐步增大,壓降變化范圍為25~31 kPa。隨著模擬壓力的增大,相同軸向高度處壓降增大,但軸向高度上的壓降曲線漸趨于線性。這與圖5中加壓時床層氣泡變小及流態化更加穩定的現象一致。
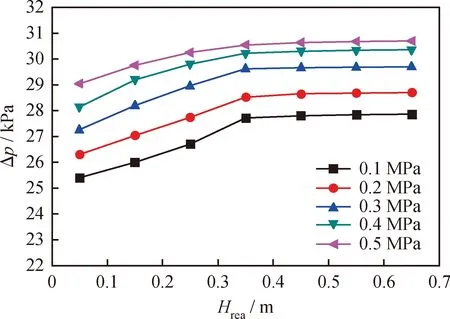
圖6 不同模擬壓力條件下反應器軸向壓降分布Fig.6 The axial pressure drop distribution under different simulated pressures
圖7為不同軸向高度截面的顆粒體積分數隨操作壓力的變化趨勢。與瞬態截面圖趨勢一致,加壓后顆粒分布更加均勻,且各軸向高度截面上的顆粒體積分數呈現增長趨勢。但是,當操作壓力大于0.3 MPa時,軸向0.05 m截面的顆粒體積分數出現拐點,隨壓力的升高而降低。通過對瞬態截面圖的觀察,分析原因為氣力輸送能力的提高,使反應器布風板上部的密相區向更高的區域延伸[22]。因此,加壓對燃料反應器內軸向的顆粒體積分數有提升作用,同時可使壓力梯度和顆粒分布更加平滑均勻,有利于燃料反應器內流形的穩定。
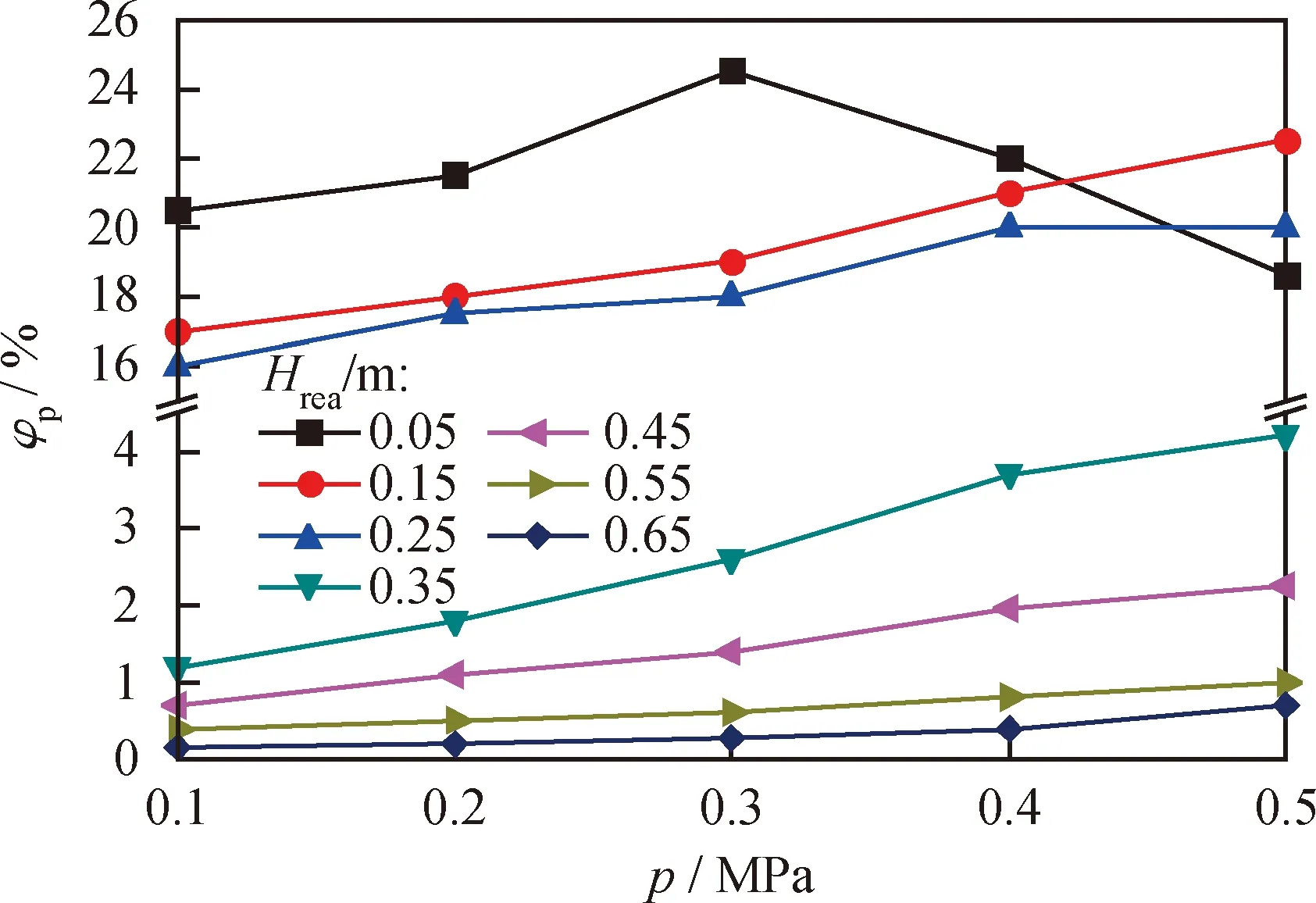
圖7 不同軸向高度顆粒體積分數隨壓力的變化Fig.7 The particle volume fraction with pressures at different axial heights
2.3 顆粒分布對反應的影響
分別對密相區(Hrea=0.15 m)、過渡區(Hrea=0.35 m)及稀相區(Hrea=0.55 m)的加壓反應特性進行考察。圖8為3個顆粒分布區域中合成氣摩爾分數(ysyn)隨壓力的變化(除去H2O和Ar)。由圖8(a)知,隨著壓力的升高,3個區域呈現了3種變化:密相區合成氣摩爾分數由78.5%降低至71.9%;過渡區合成氣摩爾分數在0.3 MPa處出現拐點,先增后減;稀相區合成氣摩爾分數變化較小。操作壓力為0.1~0.2 MPa時,燃料反應器內合成氣摩爾分數沿軸向高度呈下高上低趨勢;當操作壓力大于0.3 MPa時,密相區合成氣摩爾分數已低于過渡區,且3個區域的合成氣摩爾分數均隨著壓力的增大而減小。而在圖8(b)中,隨著3個區域顆粒體積分數和系統壓力的改變,合成氣摩爾分數在81.8%~83.7%范圍內小幅變化。相同的壓力條件下,顆粒體積分數是3個區域最大的差異變量,因此在化學鏈氣化中顆粒體積分數是影響合成氣摩爾分數的關鍵因素,可通過操作壓力對顆粒分布的影響,實現對合成氣品質的調控。
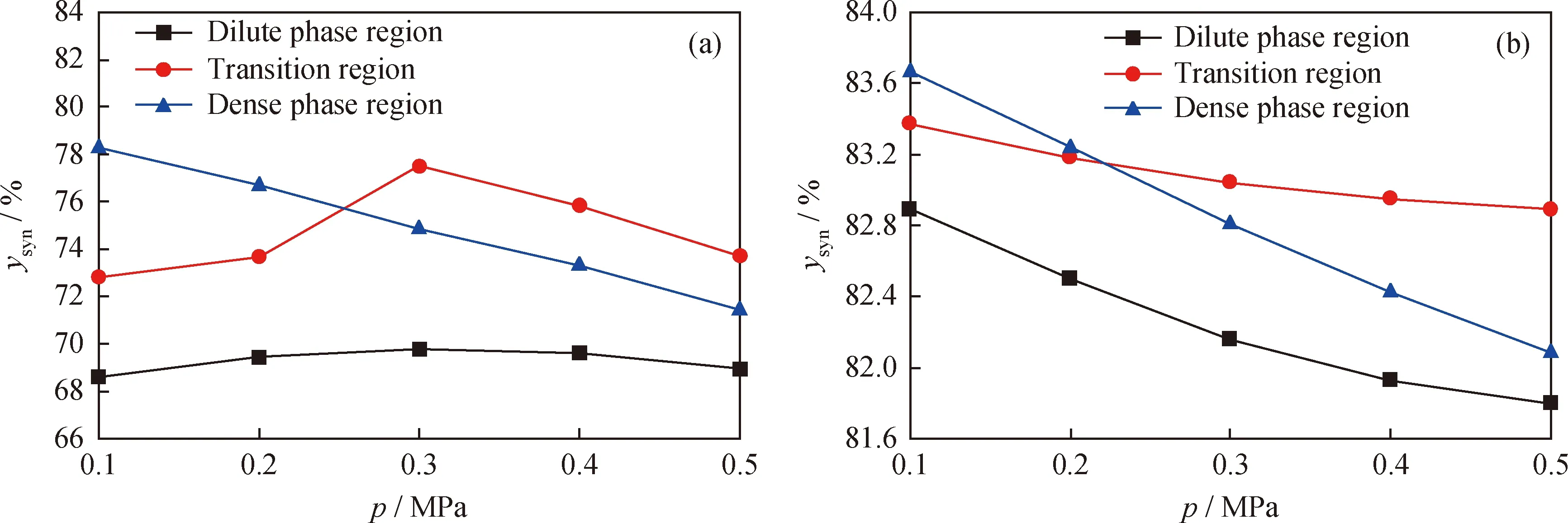
圖8 3個顆粒分布區域中的合成氣摩爾分數隨壓力的變化Fig.8 The molar fraction of syngas with pressures in each particle distribution region(a) Coal char and Fe2O3/Al2O3; (b) Coal char and SiO2
利用多相反應動力學模型對化學鏈氣化復雜反應體系進行解耦,得到了各獨立反應速率的變化特征,如表5所示。由表5可以看出,煤焦氣化速率(Rg)和載氧體還原反應速率(Rr)隨著顆粒體積分數增加而增大,而水煤氣變換反應速率(Rs)沒有明顯變化;3種反應速率均隨著操作壓力的增大而增大,在相同壓力下,Rs明顯低于Rg和Rr。表5中,在0.1~0.5 MPa壓力范圍,3個顆粒分布區中煤焦氣化速率、載氧體還原反應速率、水煤氣變換反應速率的最大變化范圍分別為0.246、1.07和0.05 mol/(s·m3)。因此,加壓流化床反應器中操作壓力以及顆粒流態的改變對水煤氣變換反應速率無顯著影響,主要通過煤焦氣化反應和載氧體還原反應的耦合作用實現對合成氣組分比例的調控。相較于載氧體還原反應速率,煤焦氣化速率較低,是總反應體系的控速步驟[23]。Keller等[24]研究發現,載氧體對煤焦周圍H2的轉化作用有利于降低煤焦表面H2對其氣化反應平衡的抑制。還原速率增大雖然消耗了部分CO和H2,但氣化速率提升顯著。表5 中過渡區壓力由0.1升至 0.3 MPa,Rg和Rr分別增長2.7倍和2.2倍,對應圖8(a)中過渡區合成氣摩爾分數由72%增長至78%。因此,顆粒體積分數是調控合成氣品質的關鍵參數,其范圍的適當選取,不但可以通過加壓加速煤焦氣化速率,還可以提升合成氣品質。當φp處于1.0%~2.8%時(圖7中過渡區壓力0.1~0.3 MPa的φp值),加壓不僅弱化了氣化產物對煤焦氣化的平衡抑制,還避免了還原反應過程對CO和H2的過度消耗。所以在煤焦加壓化學鏈氣化燃料反應器設計時,可考慮采用氣流床或控制流化床上升管內φp處于1.0%~2.8%區間。
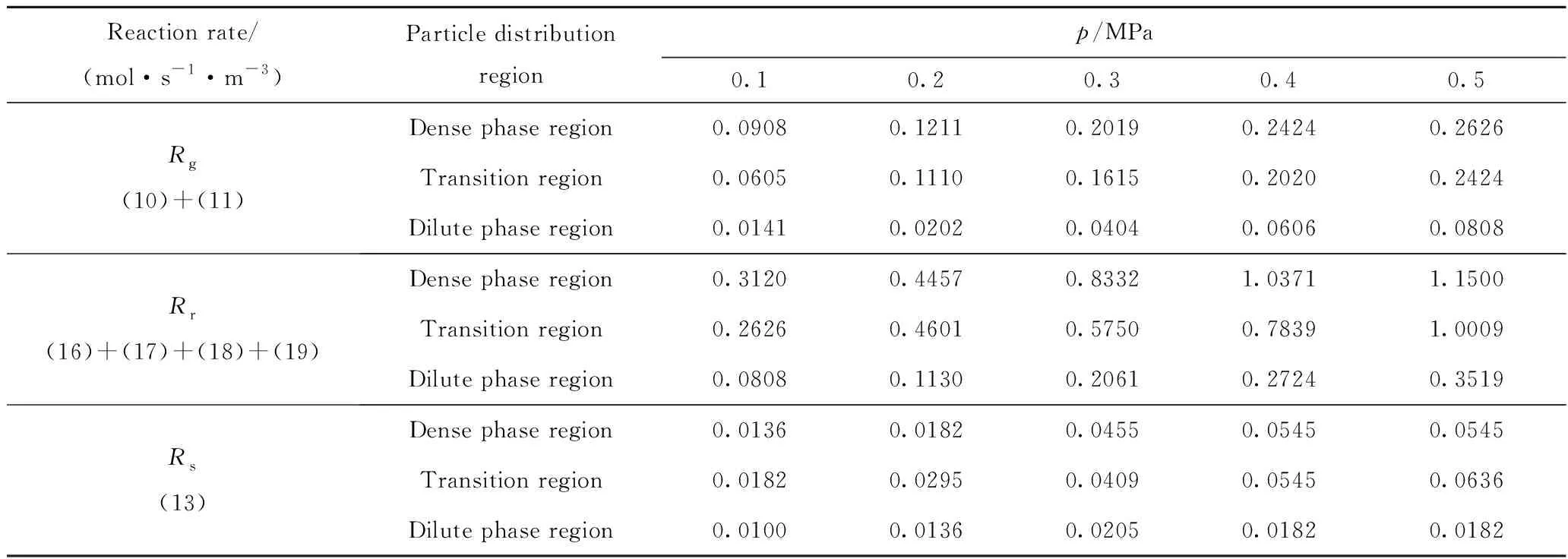
表5 化學鏈氣化(CLG)過程3個顆粒分布區域中氣化、還原和水煤氣變換反應速率模擬結果Table 5 The simulation results of Rg, Rr and Rs in different particle distribution regions during CLG process
將載氧體替換為惰性床料的煤焦氣化速率(Rg)和水煤氣變換反應速率(Rs)模擬結果如表6所示。由表5、6可以看出,與有載氧體化學鏈氣化過程相比,稀相區Rg和Rs數值較為接近,因此,加入載氧體并未對稀相區的煤焦氣化和水煤氣變換反應產生明顯影響。過渡區和密相區的Rg相較于有載氧體的化學鏈氣化過程明顯降低,且隨著壓力的增大降幅更大,最大降幅分別為20%和35%。
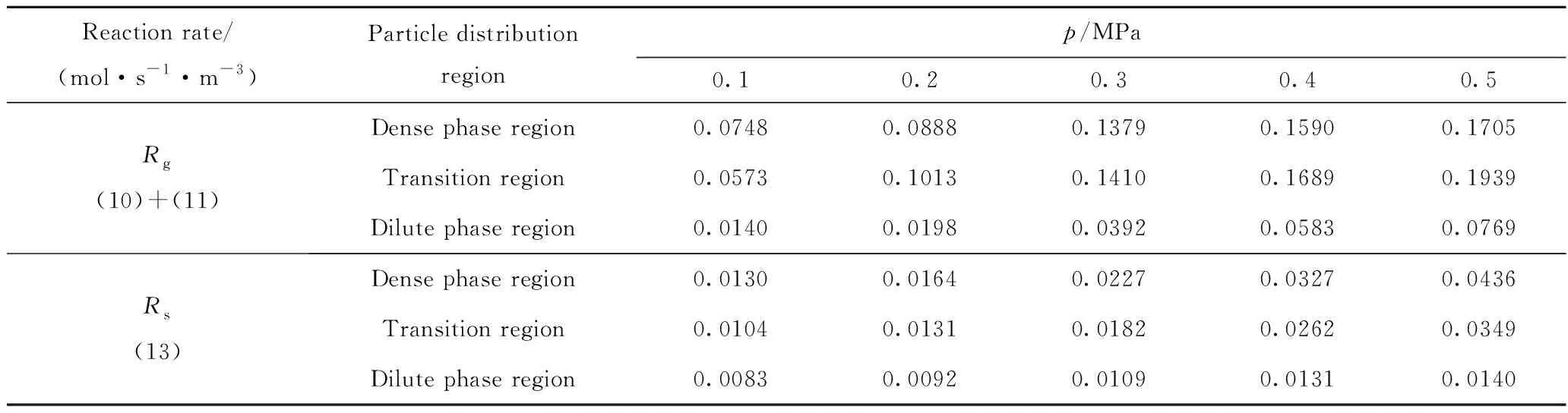
表6 惰性床料氣化過程中各顆粒分布區域中氣化、還原和水煤氣變換反應速率模擬結果Table 6 The simulation results of Rg, Rr and Rs in different particle distribution regions with inert bed materials
2.4 不同價態的還原反應過程分析
Fe2O3分別還原至Fe3O4和FeO的釋氧量和還原反應速率均不同,可通過對二者的調控達到對釋氧量和還原反應速率的要求,載氧體還原反應速率(Rr)為Fe2O3→FeO過程的還原反應速率(Ra)與Fe2O3→Fe3O4過程的還原反應速率(Rb)之和。圖9為0.1~0.5 MPa壓力范圍內過渡區中2種還原態載氧體的還原反應速率(R,mol/(s·m3))及兩還原反應速率比(Ra/Rb)。由圖9可知,在0.1~0.3 MPa升壓階段,Ra/Rb增加,說明此范圍內加壓Ra的增幅更大。但是Ra明顯小于Rb。因此,Ra可減小載氧體還原反應速率的增幅。而在0.3~0.5 MPa升壓階段,Rb顯著增加,說明此范圍內加壓可增大載氧體還原反應速率的增幅。
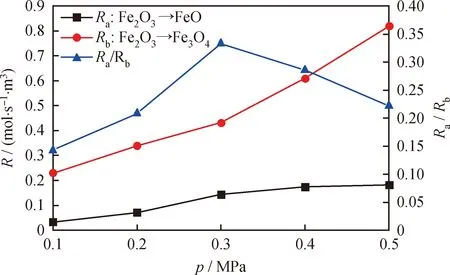
圖9 過渡區中2種還原態載氧體的釋氧速率及釋氧速率比Fig.9 Oxygen release rates and rate ratios of different reduction states in transition zone
晶格氧釋氧量([O])為某一時刻載氧體還原反應質量損失與最大可能質量損失量的比值。當載氧體全部還原轉化為FeO時,達到最大釋氧量,數值為1。圖10 為模擬反應器中載氧體不同價態組分的質量分數(w,%)隨時間的變化關系。由圖10可知,操作壓力從0.1 MPa升至0.3 MPa時,Fe3O4質量分數的最大值由81.6%降至69.2%,Fe2O3更多的轉化為FeO,40 min時晶格氧釋氧量由0.544增大為0.817,增幅達50.18%;壓力從0.3 MPa升至 0.5 MPa 時,Fe3O4質量分數的最大值升至72.3%,40 min時晶格氧釋氧量為0.817,增幅僅為3.92%。
對反應40 min時的Fe2O3/Al2O3載氧體進行XRD分析,如圖11所示。由圖11可知,常壓時Fe2O3/Al2O3載氧體2θ在30.5°、36.0°、63.0°等處出現Fe3O4的明顯特征衍射峰;2θ在31.5°、37.0°、64.0°等處只有微量的FeAl2O4特征衍射峰(FeAl2O4為FeO和Al2O3礦物化產物,視其為Fe2+還原態產物)。壓力為0.3 MPa時的載氧體還原態XRD譜圖積分定量分析顯示FeAl2O3含量超過了Fe3O4,與圖10(b)模擬結果一致,證明了模擬數據可信。
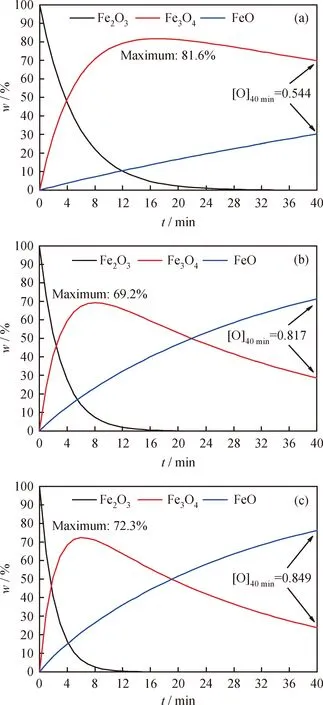
圖10 Fe2O3/Al2O3載氧體不同價態組分的質量分數隨反應時間的變化Fig.10 The variation of mass fraction of components in different valence states of oxygen carriers with time(a) 0.1 MPa; (b) 0.3 MPa; (c) 0.5 MPa
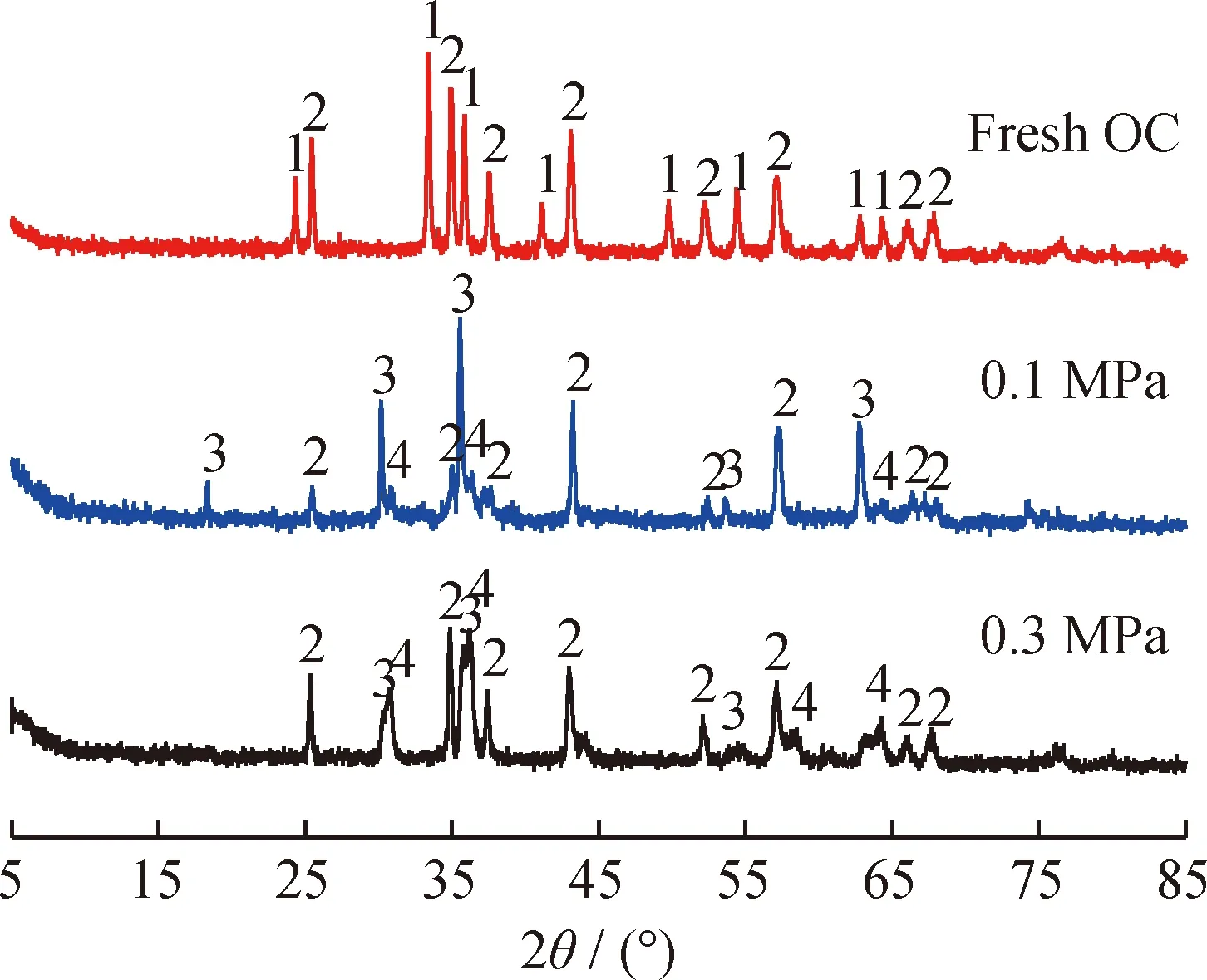
圖11 反應40 min時的Fe2O3/Al2O3載氧體還原態XRD表征Fig.11 XRD patterns of reduced oxygen carriers under different pressures1—Fe2O3; 2—Al2O3; 3—Fe3O4; 4—FeAl2O4
3 結 論
通過實驗和數值模擬相結合的方法,對加壓流化床系統中的煤焦加壓化學鏈氣化過程進行了研究,分析了加壓下煤焦和載氧體的多相流動特征及其對反應的影響規律。
(1)加壓增大了軸向顆粒體積分數,促進了煤焦氣化速率和載氧體還原反應速率的增加。顆粒體積分數是影響加壓下煤氣化速率和合成氣品質的關鍵因素,顆粒體積分數在1.0%~2.8%區間,壓力從0.1 MPa升至0.3 MPa時,煤焦氣化速率增長2.7倍,合成氣摩爾分數由72%增至78%。
(2)壓力從0.1 MPa升至0.5 MPa,以及顆粒流態的改變,對水煤氣變換反應速率無顯著影響,主要通過煤焦氣化反應和載氧體還原反應的耦合作用實現對合成氣組分比例的調控。
(3)實驗驗證了Fe2O3/Al2O3載氧體各還原態組分分布模擬結果的可信。操作壓力從0.1 MPa加至0.3 MPa時,可以減小載氧體還原反應速率的增幅,釋氧量增大50.18%;操作壓力從0.3 MPa加至0.5 MPa時,顯著促進了載氧體還原反應速率的增大,但釋氧量僅增加3.92%。

