黑豆藥材的HPLC指紋圖譜建立及5種異黃酮類成分的含量測定
郭千祥 梁幼玲 史旭華 白俊其 黃娟 黃志海 丘小惠

摘 要 目的:建立黑豆藥材的指紋圖譜和5種異黃酮類成分的含量測定方法,為更好地控制該藥材的質(zhì)量提供參考。方法:采用高效液相色譜法(HPLC)建立指紋圖譜并檢測5種異黃酮類成分的含量。色譜柱為Phenomenex C18,流動相為乙腈-0.12%甲酸水溶液(梯度洗脫),流速為1 mL/min,檢測波長為260 nm,柱溫為30 ℃,進(jìn)樣量為10 ?L。以大豆苷為參照,繪制12批黑豆藥材樣品的HPLC指紋圖譜,采用《中藥特征指紋圖譜相似度評價系統(tǒng)》(2012A版)進(jìn)行相似度評價,確定共有峰;分別采用SPSS 20.0軟件和SIMCA 13.0軟件進(jìn)行聚類分析和主成分分析。結(jié)果:12批黑豆藥材樣品共有19個共有峰,相似度均大于0.94;指認(rèn)了5個成分,分別為大豆苷、黃豆黃苷、染料木苷、大豆苷元、染料木素。聚類分析結(jié)果顯示,12批黑豆藥材樣品可聚為兩類,即S1~ S3聚為一類,S4~S12聚為一類。主成分分析結(jié)果顯示,2個主成分因子的方差貢獻(xiàn)率分別為53.261%、40.715%,累積方差貢獻(xiàn)率為93.976%。上述5種成分的質(zhì)量濃度線性范圍分別為5.97~191.00 ?g/mL(r=0.999 9)、1.05~33.46 ?g/mL(r=0.999 9)、8.93~285.61 ?g/mL(r=0.999 5)、0.82~26.33 ?g/mL(r=0.999 9)、0.93~29.64 ?g/mL(r=0.999 7);定量限分別為0.881 1、0.611 6、0.078 6、0.243 3、0.511 6 ?g/mL,檢測限分別為0.264 3、0.244 7、0.021 4、0.124 8、0.106 7 ?g/mL;精密度、穩(wěn)定性、重復(fù)性、耐用性試驗(yàn)的RSD均小于5%;加樣回收率為95.15%~96.56%(RSD=0.51%,n=6)、98.52%~103.45%(RSD=1.88%,n=6)、95.37%~97.91%(RSD=0.95%,n=6)、99.75%~102.00%(RSD=0.78%,n=6)、100.26%~103.65%(RSD=1.21%,n=6)。12批黑豆藥材中上述5種成分的含量分別為0.178 3~0.265 9、0.021 7~0.096 2、0.288 5~0.597 2、0.014 1~0.058 8、0.012 9~0.082 9 mg/g。結(jié)論:所建指紋圖譜和5種異黃酮類成分的含量測定方法均可用于黑豆藥材的質(zhì)量控制;不同產(chǎn)地黑豆藥材中異黃酮類成分相似,但含量有所差異。
關(guān)鍵詞 黑豆;異黃酮類;高效液相色譜法;指紋圖譜;聚類分析;主成分分析;含量測定
ABSTRACT? ?OBJECTIVE: To establish the fingerprint of Sojae Semen Nigrum and content determination method of 5 kinds of isoflavones, so as to provide reference for controlling its quality better. METHODS: HPLC method was adopted to establish the fingerprint and detect the contents of 5 kinds of isoflavones. The determination was performed on Phenomenex C18 column with mobile phase consisted of acetonitrile-0.12% formic acid solution(gradient elution) at the flow rate of 1 mL/min. The detection wavelength was set at 260 nm; the column temperature was 30 ℃ and sample size was 10 μL. Using daidzin as reference, HPLC fingerprints of 12 batches of samples were determined. The similarity of 12 batches of samples was evaluated by TCM Chromatographic Fingerprint Similarity Evaluation System (2012A) to confirm common peak. Cluster analysis and principal component analysis were performed by using SPSS 20.0 software and SIMCA 13.0 software. RESULTS: There were 19 common peaks in HPLC fingerprints of 12 batches of samples,the similarity of which was higher than 0.94. Totally 5 components were identified, such as daidzin, glycitin, genistin, daidzein, genistein. Cluster analysis showed that 12 batches of Sojae Semen Nigrum were clustered into 2 categories, i.e. S1-S3 clustered into one category, and S4-S12 clustered into the other category. By principal component analysis, the contribution rates of two principle components were 53.261% and 40.715%; accumulative contribution rate was 93.976%. The linear range of above 5 components were 5.97-191.00 ?g/mL(r=0.999 9), 1.05-33.46 ?g/mL(r=0.999 9), 8.93-285.61 ?g/mL(r=0.999 5), 0.82-26.33 ?g/mL(r=0.999 9), 0.93-29.64 ?g/mL (r=0.999 7), respectively. The limits of quantitation were 0.881 1, 0.611 6, 0.078 6, 0.243 3, 0.511 6 μg/mL, respectively. The limits of detection were 0.264 3, 0.244 7, 0.021 4, 0.124 8, 0.106 7 μg/mL, respectively. RSDs of precision, stability, reproducibility and durability tests were all lower than 5%. Recoveries were 95.15%-96.56%(RSD=0.51%,n=6), 98.52%-103.45%(RSD=1.88%,n=6), 95.37%-97.91% (RSD=0.95%, n=6), 99.75%-102.00% (RSD=0.78%, n=6), 100.26%-103.65% (RSD=1.21%, n=6). Among 12 batches of Sojae Semen Nigrum, the contents of above 5 components were 0.178 3-0.265 9,0.021 7-0.096 2, 0.288 5-0.597 2, 0.014 1- 0.058 8,0.012 9-0.082 9 mg/g. CONCLUSIONS: Established HPLC fingerprint and content determination method of 5 kinds of isoflavones can be used for quality control of Sojea Semen Nigrum. The Isoflavone components are similar, but the contents are different among Sojae Semen Nigrum from different producing areas.
KEYWORDS? ?Sojae Semen Nigrum; Isoflavones; HPLC; Fingerprint; Cluster analysis; Principal component analysis; Content determination
黑豆為豆科植物大豆[Glycine max(L.)Merr.]的干燥成熟種子[1]。《本草綱目》中記載,大豆有黑、白、黃、褐、青、斑數(shù)色,黑者入藥[2]。中醫(yī)認(rèn)為,五色入五臟,黑色屬水,水走腎,黑豆專入腎經(jīng),故被認(rèn)定為“補(bǔ)腎”之品[3]。2015年版《中國藥典》(一部)收錄黑豆,載其有益精明目、養(yǎng)血祛風(fēng)、利水、解毒等功效[1]。現(xiàn)代藥理研究表明,黑豆具有抗氧化、調(diào)節(jié)激素水平、預(yù)防動脈血管硬化、延年益智、防癌抗癌等作用[4]。該藥的作用機(jī)制與其所含多種生物活性成分有關(guān),尤以異黃酮最為突出。該類成分除具有緩解更年期綜合征、防治骨質(zhì)疏松及心血管疾病等作用外,還具有顯著的防癌抗癌作用,故備受學(xué)者關(guān)注[5]。
化學(xué)成分是中藥藥效發(fā)揮作用的物質(zhì)基礎(chǔ),中藥質(zhì)量與其復(fù)雜的有效成分密切相關(guān),因此采用指紋圖譜結(jié)合多指標(biāo)成分的含量測定可更好地控制中藥質(zhì)量[6]。黑豆為2010年版《中國藥典》(一部)新收錄的品種,現(xiàn)行標(biāo)準(zhǔn)收載于2015年版《中國藥典》(一部),包括性狀鑒別、顯微鑒別和薄層色譜鑒別等[1],尚無含量測定項。雖然,陸泉[7]采用反相高效液相色譜法測定黑豆中大豆苷的含量;劉洋等[8]研究發(fā)現(xiàn),不同產(chǎn)地黑豆黃酮提取物的抗氧化還原能力不同,其中產(chǎn)地影響較大,因此認(rèn)為不同產(chǎn)地黑豆的藥效也存在一定差異。但這些研究的指標(biāo)單一,存在一定的局限性,且關(guān)于黑豆的指紋圖譜、不同產(chǎn)地質(zhì)量差異的研究較少。本課題組通過前期化學(xué)成分和藥理研究證實(shí),黑豆中含有大豆苷、黃豆黃苷、染料木苷、大豆苷元和染料木素等5種異黃酮成分,這5種成分也是其發(fā)揮藥理作用的活性成分[9]。為更加全面地評價黑豆質(zhì)量,本研究采用高效液相色譜法(HPLC)建立了12批黑豆藥材樣品的HPLC指紋圖譜,測定了上述5種異黃酮類成分的含量,同時結(jié)合聚類分析和主成分分析(PCA)進(jìn)行綜合質(zhì)量評價,旨在為其質(zhì)量標(biāo)準(zhǔn)的完善提供參考。
1 材料
1.1 儀器
1200型HPLC儀,包括G1322A型在線真空脫氣機(jī)、G1311A型四元泵、G1329A型自動進(jìn)樣器、G1316A型柱溫箱、G1315D型二極管陣列檢測器、1200 Series色譜工作站B04.01版(美國Agilent公司);Milli-Q Advantage A10型純水機(jī)(美國Millipore公司);BT-125D型十萬分之一電子天平[賽多利斯科學(xué)儀器(北京)有限公司];LK/CSJ-20型超聲波清洗機(jī)(成都老肯科技股份有限公司)。
1.2 試劑
大豆苷元對照品(批號:JL22382,純度:≥98%)、染料木素對照品(批號:MB2170,純度:≥98%)均購自廣州菲博生物科技有限公司;大豆苷對照品(批號:111738-201603,純度:≥93.3%)、染料木苷對照品(批號:111709-201702,純度:99.9%)均購自中國食品藥品檢定研究院;黃豆黃苷對照品(批號:J04044AS,純度:≥98%)購自大連美侖生物技術(shù)有限公司;甲酸、乙腈為色譜純,甲醇為分析純,水為超純水。
1.3 藥材
12批黑豆藥材樣品(編號:S1~S12)均由康美藥業(yè)股份有限公司提供,經(jīng)廣州中醫(yī)藥大學(xué)第二臨床醫(yī)學(xué)院黃志海主任中藥師鑒定為豆科植物大豆[G. max(L.)Merr.]的干燥成熟種子。黑豆藥材樣品信息來源見表1。
2 方法與結(jié)果
2.1 指紋圖譜的建立
2.1.1 混合對照品溶液的制備 分別取大豆苷、大豆苷元、黃豆黃苷、染料木素、染料木苷對照品各4 mg,精密稱定,置于10 mL棕色量瓶中,加70%甲醇制成質(zhì)量濃度均為0.4 mg/mL的單一對照品溶液。取各單一對照品溶液適量,置于10 mL棕色量瓶中,加70%甲醇定容,搖勻,即得上述5種成分質(zhì)量濃度均為4 μg/mL的混合對照品溶液。
2.1.2 供試品溶液的制備 取黑豆藥材樣品粉末(過80目篩)2 g,精密稱定,置于20 mL棕色量瓶中,加70%甲醇20 mL,超聲(功率:250 W,頻率:40 kHz)提取30 min,經(jīng)0.45 ?m微孔濾膜濾過,取續(xù)濾液,即得供試品溶液。
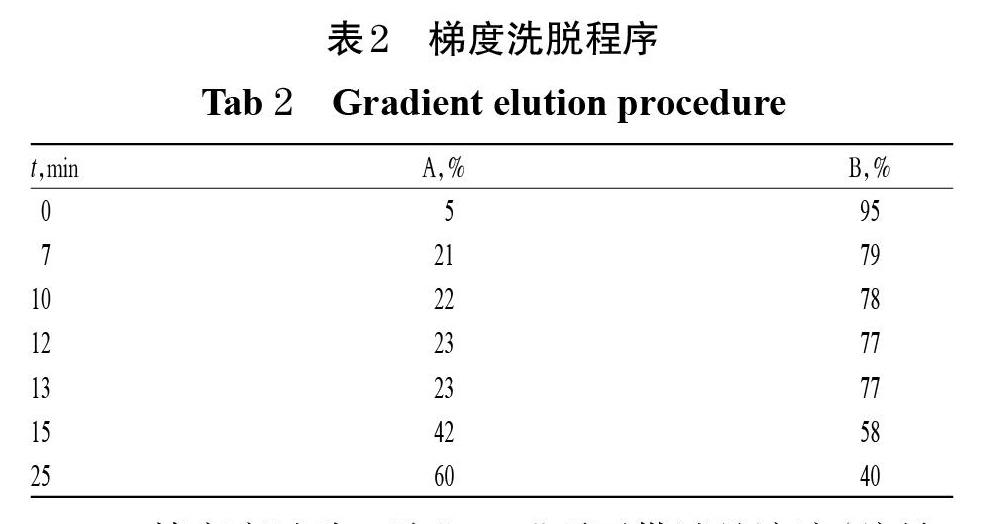
2.1.3 色譜條件 色譜柱:Phenomenex C18(250 mm×4.60 mm,5 μm);流動相:乙腈(A)-0.12%甲酸水溶液(B),梯度洗脫(洗脫程序見表2);流速:1 mL/min;檢測波長:260 nm;柱溫:30 ℃;進(jìn)樣量:10 ?L。
2.1.4 精密度試驗(yàn) 取“2.1.2”項下供試品溶液(編號:S8)適量,按“2.1.3”項下色譜條件連續(xù)進(jìn)樣測定6次,以大豆苷的保留時間和峰面積為參照,記錄各共有峰的相對保留時間和相對峰面積。結(jié)果,19個共有峰相對保留時間的RSD均小于1%(n=6),相對峰面積的RSD均小于5%(n=6),表明本方法精密度良好。
2.1.5 穩(wěn)定性試驗(yàn) 取“2.1.2”項下供試品溶液(編號:S8)適量,分別于室溫避光放置0、2、4、6、8、10、12 h時按“2.1.3”項下色譜條件進(jìn)樣測定,以大豆苷的保留時間和峰面積為參照,記錄各共有峰的相對保留時間和相對峰面積。結(jié)果,19個共有峰相對保留時間的RSD均小于1%(n=7),相對峰面積的RSD均小于5%(n=7),表明供試品溶液于室溫下放置12 h內(nèi)穩(wěn)定性良好。
2.1.6 重復(fù)性試驗(yàn) 取黑豆藥材樣品(編號:S8)粉末2 g,共6份,按“2.1.2”項下方法制備供試品溶液,再按“2.1.3”項下色譜條件進(jìn)樣測定,以大豆苷的保留時間和峰面積為參照,記錄各共有峰的相對保留時間和相對峰面積。結(jié)果,19個共有峰相對保留時間的RSD均小于1%(n=6),相對峰面積的RSD均小于5%(n=6),表明本方法重復(fù)性良好。
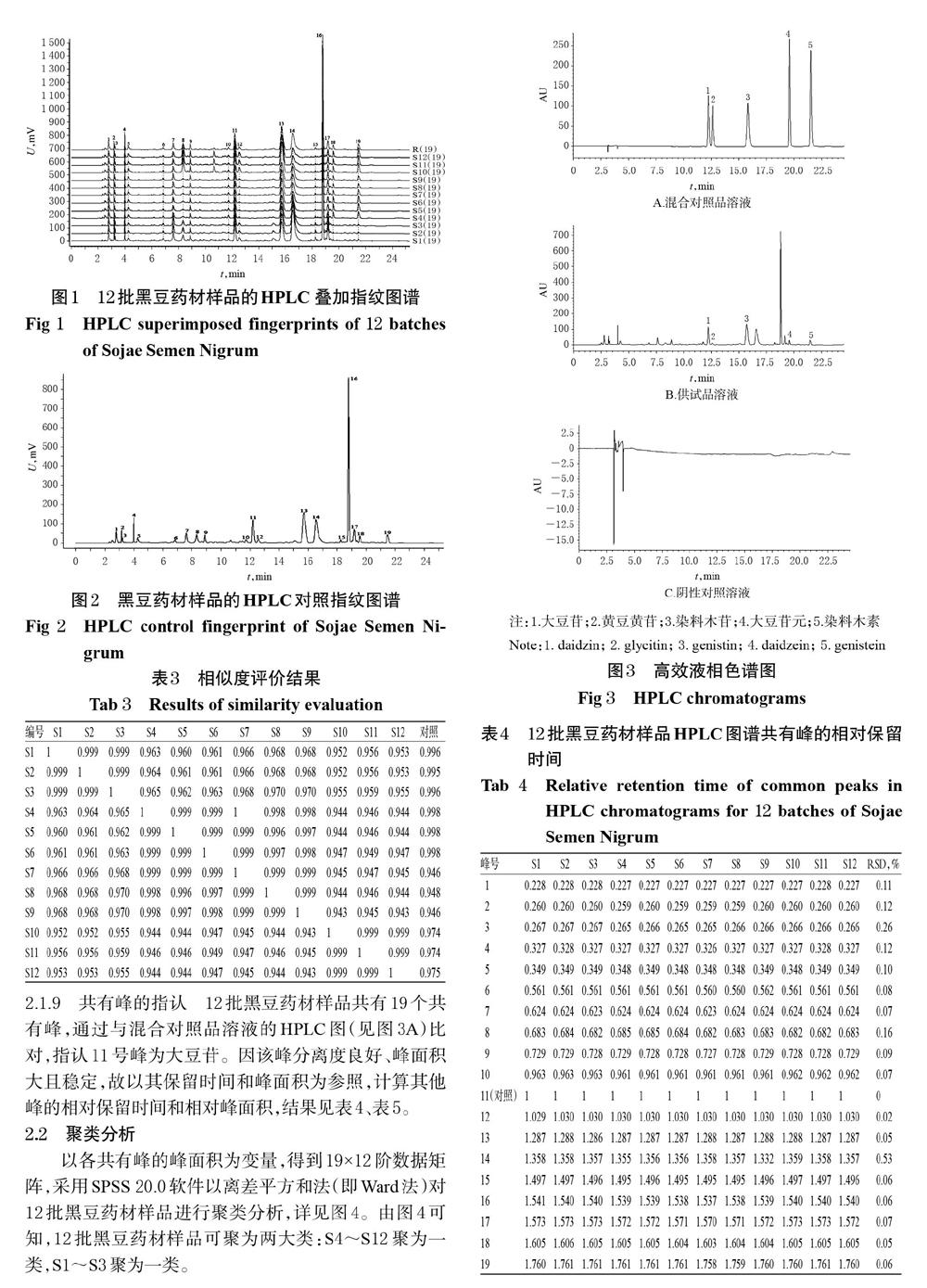
2.1.7 HPLC指紋圖譜的生成 取12批黑豆藥材樣品適量,按“2.1.2”項下方法制備供試品溶液,按“2.1.3”項下色譜條件進(jìn)樣測定,采用《中藥色譜指紋圖譜相似度評價系統(tǒng)》(2012A版)進(jìn)行分析,得HPLC指紋圖譜,詳見圖1、圖2。
2.1.8 相似度評價 采用《中藥色譜指紋圖譜相似度評價系統(tǒng)》(2012A版),以黑豆藥材樣品的HPLC對照指紋圖譜為對照,進(jìn)行整體相似度評價。結(jié)果顯示,12批黑豆藥材樣品的相似度均大于0.94,提示黑豆藥材樣品的化學(xué)成分一致性較好,詳見表3。
2.1.9 共有峰的指認(rèn) 12批黑豆藥材樣品共有19個共有峰,通過與混合對照品溶液的HPLC圖(見圖3A)比對,指認(rèn)11號峰為大豆苷。因該峰分離度良好、峰面積大且穩(wěn)定,故以其保留時間和峰面積為參照,計算其他峰的相對保留時間和相對峰面積,結(jié)果見表4、表5。
2.2 聚類分析
以各共有峰的峰面積為變量,得到19×12階數(shù)據(jù)矩陣,采用SPSS 20.0軟件以離差平方和法(即Ward法)對12批黑豆藥材樣品進(jìn)行聚類分析,詳見圖4。由圖4可知,12批黑豆藥材樣品可聚為兩大類:S4~S12聚為一類,S1~S3聚為一類。
2.3 PCA分析
采用SIMCA 13.0 軟件進(jìn)行PCA分析,結(jié)果見圖5。由圖5可知,S4~S12在PCA得分圖的左側(cè),S1~S3在PCA得分圖的右側(cè),該結(jié)果與聚類分析結(jié)果一致。
對12批黑豆藥材樣品的19個共有峰的峰面積進(jìn)行標(biāo)準(zhǔn)化處理后,采用SPSS 20.0軟件進(jìn)行PCA分析,計算主成分因子的特征值、方差貢獻(xiàn)率等,結(jié)果見表6。由表6可知,共得到2個主成分因子,方差貢獻(xiàn)率分別為53.261%、40.715%,累積方差貢獻(xiàn)率為93.976%,提示主成分因子1、2可作為黑豆藥材的評價指標(biāo),適用于PCA分析。故以主成分因子1、2為指標(biāo)對12批黑豆藥材樣品進(jìn)行整體質(zhì)量評價,結(jié)果見表7。由表7可知,S4~S12藥材樣品質(zhì)量相近,與S1~S3藥材樣品質(zhì)量存在較大差異。
2.4 含量測定
2.4.1 溶液的制備 混合對照品溶液的制備同“2.1.1”項;供試品溶液的制備同“2.1.2”項;以70%甲醇為陰性對照溶液。
2.4.2 色譜條件 同“2.1.3”項。
2.4.3 系統(tǒng)適用性試驗(yàn) 取“2.4.1”項下混合對照品溶液(70%甲醇稀釋)、供試品溶液(編號:S8)、陰性對照溶液適量,按“2.4.2”項下色譜條件進(jìn)樣測定,記錄色譜圖,詳見圖3。由圖3可知,供試品與混合對照品中各待測成分色譜峰的保留時間基本一致,且各成分在對應(yīng)的位置無干擾,均在25 min內(nèi)出峰完畢,分離度均大于1.5,理論板數(shù)以大豆苷峰計大于10 000,陰性對照無干擾。
2.4.4 線性關(guān)系考察 分別精密吸取“2.1.1”項下大豆苷、黃豆黃苷、大豆苷元、染料木素單一對照品溶液955、167.30、131.65、148.20 ?L,置于2 mL棕色量瓶中;另取染料木苷單一對照品溶液1 428.05 ?L,置于2 mL棕色量瓶中;均分別加70%甲醇定容,搖勻,得大豆苷、黃豆黃苷、大豆苷元、染料木素質(zhì)量濃度分別為191.00、33.46、26.33、29.64 ?g/mL的混合對照品溶液以及染料木苷質(zhì)量濃度為285.61 ?g/mL的單一對照品溶液。另取上述4種混合對照品溶液及染料木苷單一對照品溶液,用70%甲醇逐級稀釋2、4、8、16、32倍,得系列線性關(guān)系工作溶液,按“2.4.2”項下色譜條件進(jìn)樣測定,記錄峰面積。以各待測成分質(zhì)量濃度(x,?g/L)為橫坐標(biāo)、峰面積(y)為縱坐標(biāo)進(jìn)行線性回歸,結(jié)果見表8。
2.4.5 定量限與檢測限考察 精密量取“2.4.4”項下大豆苷、黃豆黃苷、大豆苷元、染料木素混合對照品溶液和染料木苷單一對照品溶液適量,用70%甲醇倍比稀釋,按“2.4.2”項下色譜條件進(jìn)樣測定,以信噪比10 ∶ 1、3 ∶ 1分別計算定量限、檢測限,結(jié)果見表8。
2.4.6 精密度試驗(yàn) 精密量取“2.4.4”項下大豆苷、黃豆黃苷、大豆苷元、染料木素混合對照品溶液和染料木苷單一對照品溶液適量,按“2.4.2”項下色譜條件連續(xù)進(jìn)樣測定6 次,記錄峰面積。結(jié)果,大豆苷、黃豆黃苷、染料木苷、大豆苷元、染料木素峰面積的RSD分別為1.33%、1.31%、1.33%、1.36%、1.34%(n=6),表明儀器精密度良好。
2.4.7 穩(wěn)定性試驗(yàn) 取“2.4.1”項下供試品溶液(編號:S8),分別于室溫放置0、2、4、6、8、10、12 h時按“2.4.2”項下色譜條件進(jìn)樣測定,記錄峰面積。結(jié)果,大豆苷、黃豆黃苷、染料木苷、大豆苷元、染料木素峰面積的RSD分別為2.66%、2.47%、2.48%、2.90%、1.20%(n=7),表明供試品在室溫下放置12 h內(nèi)穩(wěn)定性良好。
2.4.8 重復(fù)性試驗(yàn) 取黑豆藥材樣品粉末(編號:S8)共6份,每份約1 g,按“2.4.1”項下方法制備供試品溶液,再按“2.4.2”項下色譜條件進(jìn)樣測定,記錄峰面積并按標(biāo)準(zhǔn)曲線法計算樣品中5種成分的含量。結(jié)果,大豆苷、黃豆黃苷、染料木苷、大豆苷元、染料木素的平均含量分別為0.212 4、0.040 6、0.330 7、0.040 1、0.038 4 mg/g,RSD分別為0.67%、0.87%、0.78%、1.13%、1.82%(n=6),表明方法重復(fù)性良好。
2.4.9? 加樣回收率試驗(yàn)? ?精密稱取已知含量的黑豆藥材樣品粉末(編號:S8),共6份,每份約1 g,精密稱定,加入適量“2.1.1”項下各單一對照品溶液,按“2.4.1”項下方法制備供試品溶液,再按“2.4.2”項下色譜條件進(jìn)樣測定,記錄峰面積并計算加樣回收率,結(jié)果見表9。
2.4.10 耐用性試驗(yàn) 取黑豆藥材樣品粉末(編號:S8)適量,按“2.4.1”項下方法制備供試品溶液,再參照“2.4.2”項下色譜條件[調(diào)整流動相(B)不同含酸量(0.7%、0.12%、0.17%)、不同流速(0.9、1.0、1.1 mL/min)、不同柱溫(20、25、30 ℃)]進(jìn)樣測定,記錄峰面積并按標(biāo)準(zhǔn)曲線法計算樣品中5個成分的含量,結(jié)果見表10。結(jié)果表明,該方法能夠滿足試驗(yàn)要求,耐用性良好。
2.4.11 樣品含量測定 取12批黑豆藥材樣品適量,按“2.4.1”項下方法制備供試品溶液,再按“2.4.2”項下色譜條件進(jìn)樣測定,平行操作3次,記錄峰面積并按標(biāo)準(zhǔn)曲線法計算樣品中5種成分的含量,結(jié)果見表11。
3 討論
在前期預(yù)試驗(yàn)中,筆者分別考察了30%、50%、70%、90%甲醇為提取溶劑時的提取效果,發(fā)現(xiàn)以70%甲醇提取時,各待測成分的色譜峰響應(yīng)相對最高,故選擇70%甲醇為提取溶劑。筆者又比較了不同檢測波長(210、254、260、280、360 nm)下各色譜峰的分離效果,發(fā)現(xiàn)當(dāng)檢測波長為260 nm時,各色譜峰均有較強(qiáng)吸收,且分離度較好,故選擇檢測波長為260 nm。同時,筆者還考察了乙腈-0.10%冰乙酸水溶液、乙腈-0.12%甲酸水溶液不同流動相系統(tǒng)的分離效果,發(fā)現(xiàn)以乙腈-0.12%甲酸水溶液為流動相進(jìn)行梯度洗脫時,各色譜峰分離度較好,故選擇流動相為乙腈-0.12%甲酸水溶液進(jìn)行梯度洗脫。
指紋圖譜能體現(xiàn)中藥成分的整體性,符合中藥質(zhì)量評價的特點(diǎn)[10],但無法確定指紋圖譜中各共有峰所代表的物質(zhì)及其含量,因此在指紋圖譜的基礎(chǔ)上進(jìn)行多成分定量分析,可在一定程度上彌補(bǔ)上述不足[11]。相似度評價結(jié)果顯示,12批黑豆藥材樣品的相似度均大于0.94,表明各批黑豆藥材樣品的化學(xué)成分一致性較好;共獲得19個共有峰,相對保留時間的RSD為0~0.53%,相對峰面積的RSD為0~62.50%,表明不同產(chǎn)地黑豆藥材樣品間雖然具有相同的化學(xué)成分,但含量存在差異。聚類分析、PCA分析結(jié)果均顯示,12批黑豆藥材樣品可聚為兩類:S4~S12聚為一類,S1~S3聚為一類;S4~S12藥材樣品質(zhì)量相近,與S1~S3存在較大差異。含量測定結(jié)果顯示,同一省份產(chǎn)地黑豆藥材樣品中大豆苷、黃豆黃苷、染料木苷、大豆苷元、染料木素含量無顯著差異,但不同省份產(chǎn)地黑豆藥材樣品間含量差異明顯,這可能與其產(chǎn)地的地理位置、氣候、土壤等因素可影響黑豆的次生代謝產(chǎn)物有關(guān)(因黑豆的次生代謝產(chǎn)物中也含有黃酮類成分)[12]。
綜上所述,本文所建指紋圖譜和5種異黃酮類成分的含量測定方法均可用于黑豆藥材的質(zhì)量控制;不同產(chǎn)地黑豆藥材中異黃酮類成分相似,但含量有所差異。
參考文獻(xiàn)
[ 1 ] 國家藥典委員會.中華人民共和國藥典:一部[S].2015年版.北京:中國醫(yī)藥科技出版社,2015:344-345.
[ 2 ] 周三,關(guān)崎春雄,岳旺,等.野生大豆、黑豆和大豆的異黃酮類成分比較[J].大豆科學(xué),2008,27(2):315-319.
[ 3 ] 周莎,宛金,王彥暉,等.基于“黑豆補(bǔ)腎”的科學(xué)內(nèi)涵論中醫(yī)之“道理”觀[J].醫(yī)學(xué)與哲學(xué),2018,39(8):78-81.
[ 4 ] 劉秀玉,王利麗,左瑞庭,等.藥用黑豆的研究進(jìn)展[J].亞太傳統(tǒng)醫(yī)藥,2017,13(20):82-85.
[ 5 ] 張素霞,李紅麗.大豆異黃酮功能特性及其檢測方法的研究進(jìn)展[J].糧油加工,2009,2(19):64-67.
[ 6 ] 黃濤,劉麗,張笑敏,等.夏天無HPLC指紋圖譜及多指標(biāo)含量測定研究[J].中草藥,2019,50(10):2474-2479.
[ 7 ] 陸泉. RP-HPLC法測定藥材黑豆中大豆苷的含量[J].首都醫(yī)藥,2014,21(18):73-74.
[ 8 ] 劉洋,郭曉雨,孫殿奎,等.不同產(chǎn)地黑豆黃酮提取物的抗氧化能力比較研究[J].人參研究,2012,24(1):21-23.
[ 9 ] ZHANG J,GUO Q,WEI M,et al. Metabolite identification and pharmacokinetic profiling of isoflavones from black soybean in rats using ultrahigh-performance liquid chromatography with linear-ion-trap-orbitrap and triple- quadrupole tandem mass spectrometry[J]. J Agric Food Chem,2018,66(49):12941-12952.
[10] 姜華,高原,楊景明,等.源于“整體觀”思想的中藥質(zhì)量評價方法研究概述[J].中國中藥雜志,2015,40(6):1027- 1031.
[11] 何兵,劉艷,李春紅,等.多指標(biāo)定量指紋圖譜在中藥金銀花質(zhì)量評價中的應(yīng)用[J].中國藥學(xué)雜志,2015,50(14):1237-1242.
[12] 屠鵬飛.中藥指紋圖譜制定的方法學(xué)探討[C]//國際色譜指紋圖評價中藥質(zhì)量研討會論文集.廣州:國家中醫(yī)藥管理局,2001:111-114.
(收稿日期:2019-08-19 修回日期:2020-01-03)
(編輯:陳 宏)

