流式微球分析技術在區別活動性結核分枝桿菌與潛伏性結核分枝桿菌感染患者中的應用
陶芃作
(1.中南大學湘雅三醫院 醫學檢驗系,湖南 長沙;2.中南大學湘雅醫學院 醫學檢驗系,湖南 長沙)
0 引言
結核分枝桿菌(Mycobacterium tuberculosis)是結核病的主要致病因子,是最具影響力的人類病原體之一,每年感染大約860萬人,導致130萬人死亡[1,2]。因此,確定潛伏性結核分枝桿菌感染是必要的,以降低疾病發展的風險,而活動性結核病的診斷可以實現快速治療和疾病控制[3]。為此,需要能夠準確指示疾病狀態的診斷生物標志物。結核分枝桿菌感染會引起患者血清中細胞因子水平的變化[4]。然而,不同的研究選擇了不同的細胞因子來檢測活動性結核病,而對于所選細胞因子診斷活動性結核病的可靠性知之甚少[5,6]。因此,細胞因子反應的臨床相關性仍有待闡明。流式微球分析技術(cytometric bead array, CBA)能夠同時測量樣品體積中的多種分析物,包括炎性介質,趨化因子,免疫球蛋白同種型,細胞內信號分子,凋亡介質,粘附分子和抗體[7]。基于此,本研究旨在應用流式微球分析技術區別活動性結核分枝桿菌與潛伏性結核分枝桿菌感染患者。
1 材料與方法
1.1 一般資料
納入2016年3月至2019年3月我院收治的活動性結核分枝桿菌感染患者80例為活動組;其中,男41例,女39例;年齡18~72歲,平均年齡(33.95±14.29)歲。納入2016年3月至2019年3月我院收治的潛伏性結核分枝桿菌感染患者80例為活動組;其中,男33例,女47例;年齡14~71歲,平均年齡(36.17±11.49)歲。80例活動性結核分枝桿菌感染患者與80例潛伏性結核分枝桿菌感染患者均經我院病理科確證。排除標準:①嚴重心、肝、腎功能損害者;②長期使用皮質類固醇激素及免疫抑制劑者;③患有精神疾病者;④患有癌癥者。同時,納入2016年3月至2019年3月至我院體檢的健康體檢者80例為對照組;年齡19~70歲;平均年齡(35.19±12.13)歲。各組一般資料比較差異均無統計學意義(P>0.05),可納入此次分析。受試者均簽署知情同意書。
1.2 流式微球分析技術
采取活動性結核分枝桿菌感染患者80例、潛伏性結核分枝桿菌感染患者80例和健康體檢者80例的肘前靜脈血6mL,使用美國BD公司的商業化流式微球分析技術(cytometric bead array)檢測患者血清中細胞因子EGF, GM-CSF, IL-1α, IL-1β, IL-1RA,IL-2, IL-3, IL-4, IL-7, IL-10, IL-12p40, IL-12p70, IL-13, IL-15, IL-17, MIP-1α, TNF-β, VEGF, IL-5, MIP-1β, Eotaxin, G-CSF,IL-6, IL-8, IP-10, MCP-1, TNF-α的表達水平。
1.3 統計學分析
PRISM 7.0軟件進行統計分析,兩組間比較采用t檢驗,三組間比較采用ANOVA檢驗。應用受試者工作特征(ROC)曲線下面積(AUC)分析Eotaxin, G-CSF, IL-6, IL-8, IP-10, MCP-1,TNF-α檢測活動性結核分枝桿菌與潛伏性結核分枝桿菌感染患者的臨床診斷價值。P<0.05表示差異具有統計學意義。
2 結果
2.1 3組受試人員的一般資料
對照組、潛伏組和活動組在年齡上無顯著差異(P>0.05)。對照組、潛伏組和活動組男女比例分別為35/45、33/47、41/39,分別有41名(51.25%),71名(88.75%)和49名(61.25%)受試者中存在卡介苗。對于QFT-GIT測定,所有非結核桿菌感染對照的結果均為陰性; 在45名(56,25%)潛伏組受試者和80名(100.00%)活動組受試者中觀察到陽性結果。見表1。
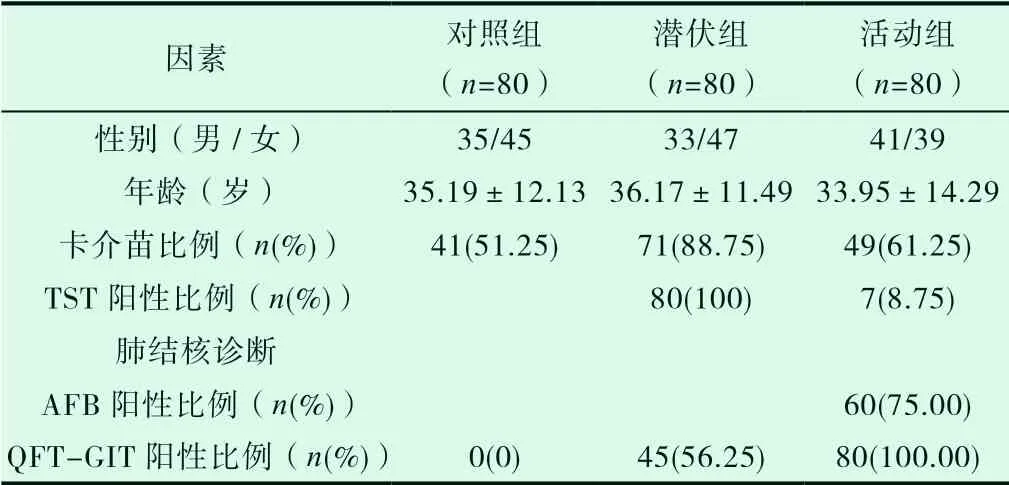
表1 3組受試人員的一般資料
2.2 3組受試人員血清中細胞因子的表達量
在流式微球分析技術檢測的27種細胞因子中,EGF(P=0.0530, F=2.973), GM-CSF(P=0.1136, F=2.195), IL-1α(P=0.0617, F=2.818), IL-1β(P=0.5837, F=0.5397), IL-1RA(P=0.6576, F=0.4199), IL-2(P=0.0948, F=2.38), IL-3(P=0.5414, F=0.6151), IL-4(P=0.2407, F=1.433), IL-7(P=0.0749,F=2.62), IL-10(P=0.8843, F=0.123), IL-12p40(P=0.5781,F=0.5492), IL-12p70(P=0.7985, F=0.2252), IL-13(P=0.1683,F=1.796), IL-15(P=0.6286, F=0.4651), IL-17(P=0.4597,F=0.7798), MIP-1α(P=0.5714, F=0.561), TNF-β(P=0.3029,F=1.2), VEGF(P=0.7584, F=0.2768)在健康體檢者、活動性結核分枝桿菌感染患者與潛伏性結核分枝桿菌感染患者中無明顯差異,IL-5(P<0.0001, t=6.589)和MIP-1β(P=0.0090, t=2.634)在 健 康體檢者與結核桿菌感染患者中有顯著差異,但是IL-5(P=0.1217,t=1.556)和MIP-1β(P=0.7383, t=0.3347)在活動性結核分枝桿菌感染患者與潛伏性結核分枝桿菌感染患者中無明顯差異,Eotaxin(P<0.0001, F=993.4), G-CSF(P<0.0001, F=5397), IL-6(P<0.0001, F=154.2), IL-8(P<0.0001, F=64), IP-10(P<0.0001,F=25.29), MCP-1(P<0.0001, F=12.27), TNF-α(P<0.0001,F=73.33)在健康體檢者、活動性結核分枝桿菌感染患者與潛伏性結核分枝桿菌感染患者中均存在明顯差異,見表2。
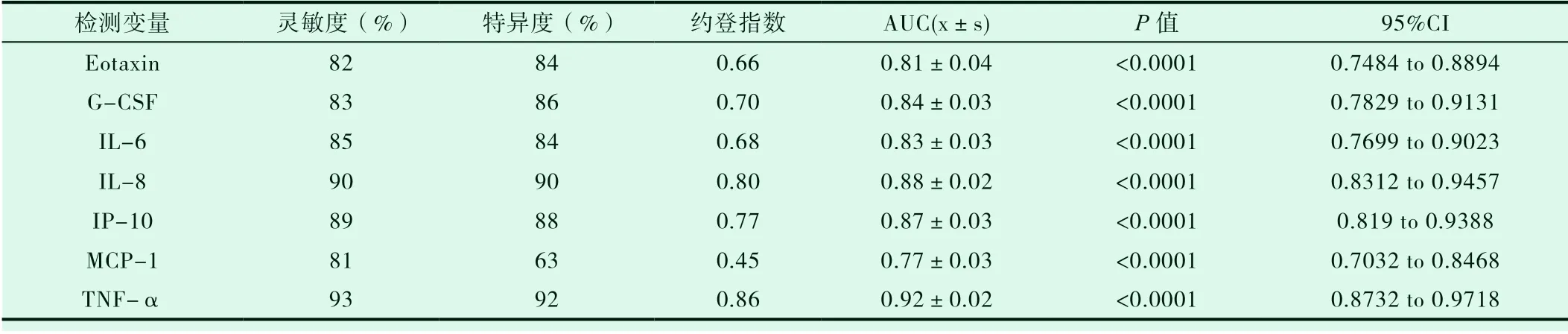
表3 活動性結核分枝桿菌感染患者與潛伏性結核分枝桿菌感染患者血清中Eotaxin, G-CSF, IL-6, IL-8, IP-10, MCP-1, TNF-α的AUC、靈敏度、特異度和約登指數
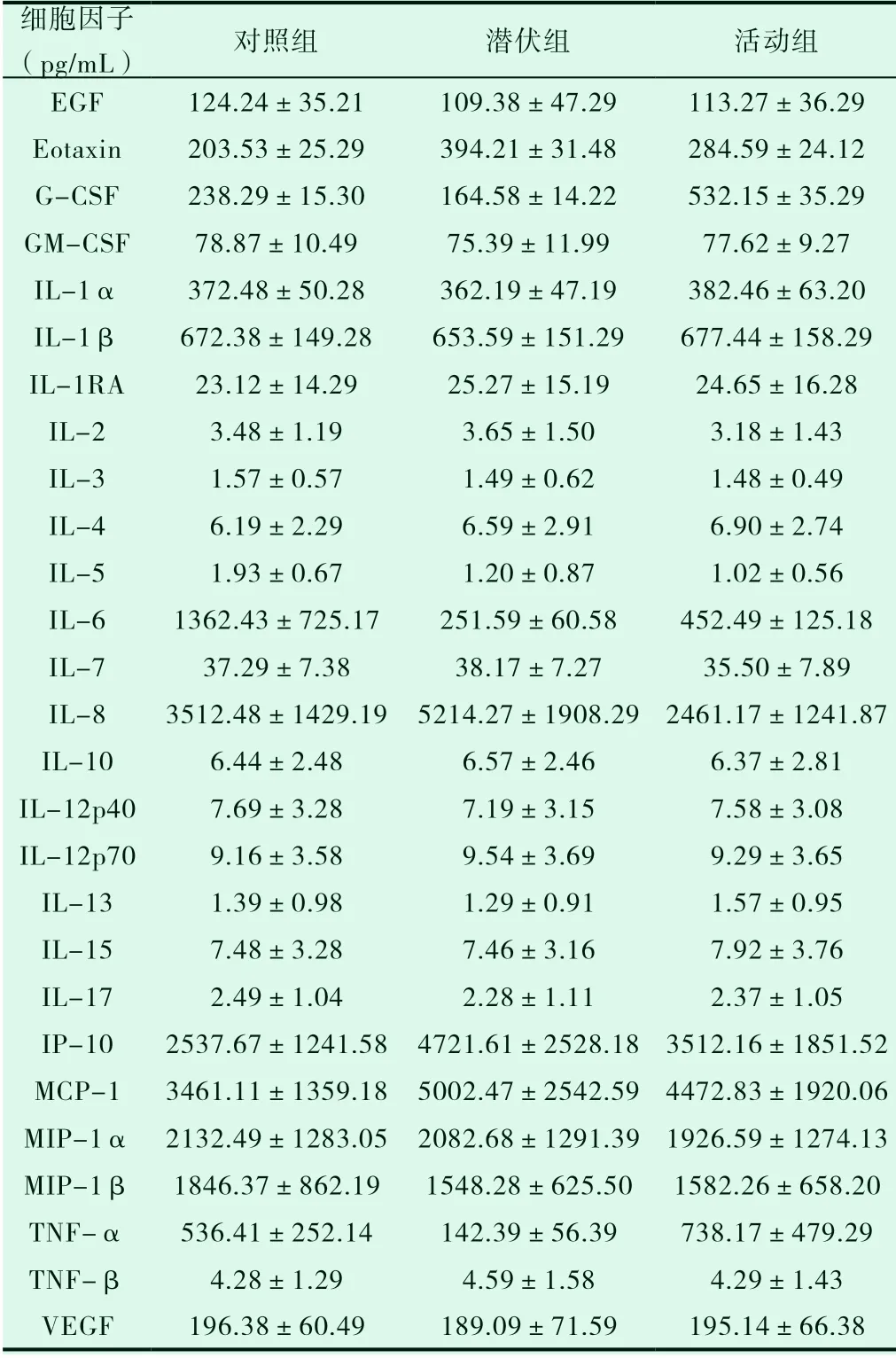
表2 3組受試人員血清中細胞因子的表達量
2.3 流式微球分析技術檢測活動性結核分枝桿菌
感染患者與潛伏性結核分枝桿菌感染患者血清中Eotaxin,G-CSF, IL-6, IL-8, IP-10, MCP-1, TNF-α的ROC曲 線、AUC、靈敏度、特異度和約登指數Eotaxin, G-CSF, IL-6, IL-8, IP-10,MCP-1, TNF-α的ROC曲線下面積分別為0.81±0.04(95%CI 0.7484~0.8894)、0.84±0.03(95%CI 0.7829~0.9131)、0.90±0.02(95%CI 0.7699~0.9023)、0.88±0.02(95%CI 0.8312~0.9457)、0.87±0.03(95%CI 0.819~0.9388)、0.77±0.03(95%CI 0.7032~0.8468)、0.92±0.02(95%CI 0.8732 to 0.9718),其 陽 性 臨界值分別為309.6(pg/mL)、500.8(pg/mL)、279.2(pg/mL)、3490(pg/mL)、4048(pg/mL)、4724 (pg/mL)、159.7(pg/mL),其診斷靈敏度和特異度分別為為82%和84%、83%和86%、83%和86%、85%和84%、90%和90%、89%和88%、81%和63%、93%和92%。見圖1和表3。
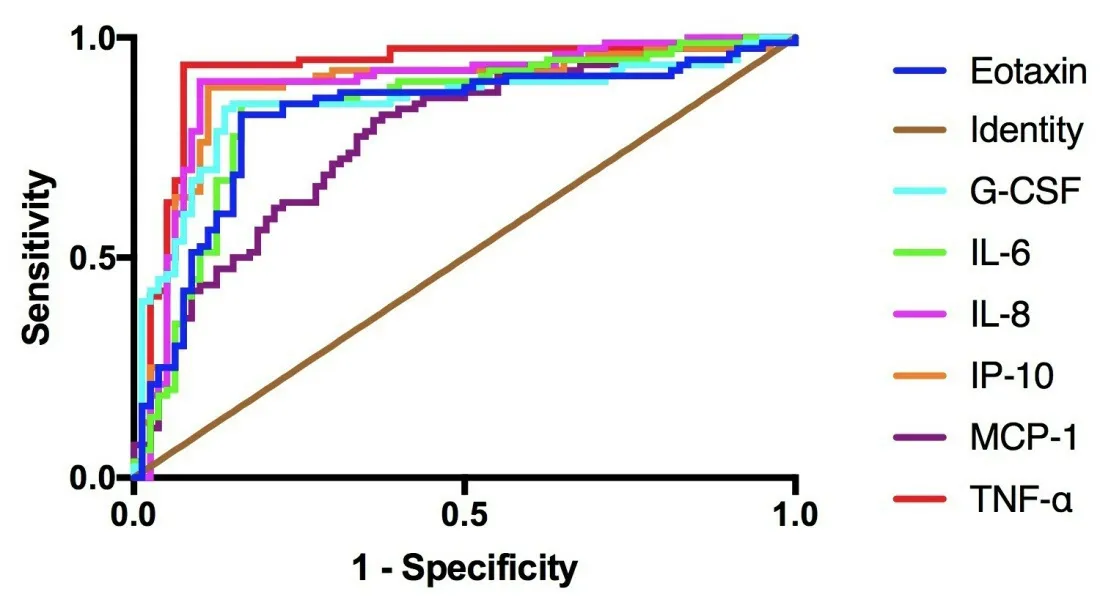
圖1 活動性結核分枝桿菌感染患者與潛伏性結核分枝桿菌感染患者血清中Eotaxin, G-CSF, IL-6, IL-8, IP-10, MCP-1, TNF-α的ROC
3 討論
結核病的發病率和死亡率很高[8,9]。盡管大多數感染結核分枝桿菌的人仍然健康,但這種狀態被稱為潛伏性結核感染。其中約占10%的個體最終會發展為活動性結核病[10-12]。快速診斷檢測的開發,可以區分活動性結核病和潛伏性結核感染或活動性結核病和非活動性結核病對于結核病控制非常重要。結核分枝桿菌感染的診斷沒有金標準,直到最近,結核菌素皮膚試驗(TST)才是檢測潛伏性結核感染的唯一工具[13]。然而,TST本質上無法區分活動性結核分枝桿菌和潛伏性結核分枝桿菌[14]。為了解決這些局限性,本研究引入流式微球分析技術來區別活動性結核分枝桿菌與潛伏性結核分枝桿菌感染患者。
本研究采用美國BD公司的流式微球分析技術檢測患者血清中細胞因子的表達水平,比較其在健康體檢者、活動性結核分枝桿菌感染患者與潛伏性結核分枝桿菌感染患者的差異后,通過ROC曲線分析發現Eotaxin, G-CSF, IL-6, IL-8, IP-10, MCP-1, TNF-α的的ROC曲線下面積(AUC)分別為0.81、0.84、0.83、0.88、0.87、0.77、0.92。相比于傳統的測量患者血清中蛋白質水平的技術,流式微球分析技術有以下優點[15]:(1)允許以定量方式同時測量多種分析物; (2)減少用于測量多種分析物的樣品量; (3)最大限度地減少生成數據所花費的時間。因此,本研究所發現的活動性結核分枝桿菌感染患者與潛伏性結核分枝桿菌感染患者血清中表達差異細胞因子Eotaxin, G-CSF, IL-6, IL-8, IP-10, MCP-1, TNF-α可以通過流式微球分析技術一次同時測定,并且能夠快速得到數據,這為Eotaxin, G-CSF, IL-6, IL-8, IP-10, MCP-1, TNF-α中的一種或多種聯合診斷活動性結核分枝桿菌感染與潛伏性結核分枝桿菌感染提供了技術基礎。

