馬錢子堿誘導人臍靜脈內皮細胞凋亡過程中血管內皮生長因子和上皮細胞激酶A2的表達變化
徐 萌,李 平
馬錢子又稱番木鱉、苦實等,入藥為干燥成熟的種子。始載于《本草綱目》中,臨床上用于跌打損傷、痹癥風濕、瘡毒癰腫等。馬錢子主要活性生物堿單體成分馬錢子堿(brucine),又稱番木鱉堿。近年來有文獻報道,馬錢子堿有一定的抗感染、抗腫瘤功效[1]。在腫瘤發生過程中,血管生成是基礎[2]。人臍靜脈內皮細胞(human umbilical vein endothelial cells,HUVECs)是常用的進行血管內皮細胞功能實驗的細胞模型[3]。馬錢子堿抗腫瘤作用中有無抑制腫瘤血管生成目前已見文獻報道,該實驗通過探索馬錢子堿誘導HUVECs增殖活性和細胞凋亡的影響,并探討血管內皮生長因子(vascular endothelial growth factor,VEGF)和上皮細胞激酶A2(epithelial cell kinase A2,EphA2)的表達變化,從而為臨床使用馬錢子堿抗腫瘤作用提供實驗基礎。
1 材料與方法
1.1 主要材料馬錢子堿(成都普菲德生物技術有限公司);高糖的DMEM培養基(美國Hyclone公司);胰蛋白酶-EDTA消化液、胎牛血清(美國Gibco公司);羊抗人VEGF抗體(美國Proteintech公司);羊抗人EphA2抗體(美國RD Systems公司);Annexin Ⅴ-FITC/碘化丙啶(PI)試劑盒(上海碧云天生物技術有限公司);CCK-8試劑盒(上海玉博生物科技有限公司);HUVECs(上海腫瘤細胞研究所)。
1.2 方法
1.2.1細胞培養實驗 HUVECs的培養與傳代HUVECs細胞用含有10%胎牛血清高糖的DMEM培養基,37 ℃、5% CO2培養箱中常規培養,每2 d換液1次,3~5 d傳代1次,實驗用細胞為3~10代細胞。
1.2.2CCK-8方法檢測馬錢子堿對HUVECs活性的影響 取對數生長期的HUVECs細胞,按照5×103個/孔細胞將接種在96孔板,設未給藥的HUVECs為對照組(僅含培養基)、不同劑量馬錢子堿(1、5、10、 20、40、80、160 μmol/L)處理組,每組設6個復孔5% CO2濃度的培養24 h后,加入20 μl CCK-8試劑,培養2 h后,在450 nm處讀取吸光度值(A450),觀察細胞增殖抑制情況。細胞活力抑制率(%)=[(A對照組-A試驗組)/A對照組]×100%。根據繪制的HUVECs增殖抑制曲線,求得半數抑制濃度(half maximal inhibitory concentration,IC50)值。
1.2.3劃痕實驗檢測馬錢子堿對HUVECs遷移的影響 在6孔板背面中線處,先用Marker筆用直尺均勻劃線,加入5×105個HUVECs細胞,常規培養48 h后,使用槍頭按照劃線,垂直劃痕,PBS充分洗滌細胞5 min×3次,去除劃下細胞,加入含10%胎牛血清的培養基,加入不同濃度馬錢子堿(0、10、20、40 μmol/L),在37 ℃的5% CO2恒溫培養箱中培養。按照0 h、24 h取樣拍照,計算抑制細胞遷徙率,細胞遷徙抑制率(%)=(初始劃痕寬度-24 h劃痕寬度)/初始劃痕寬度×100%。
1.2.4Hoechst 33258染色檢測馬錢子堿對HUVECs凋亡影響 收集不同濃度馬錢子堿(0、10、20、40 μmol/L)處理HUVECs 24 h后,PBS漂洗2次后,離心棄去上清液,加入Hoechst 33258染液(終濃度10 mg/L),避光染色10 min,離心后棄去染液,熒光顯微鏡下觀察照相。
1.2.5Annexin-V/PI雙染法檢測HUVECS細胞凋亡 實驗分組前,在6孔板中接種對數生長期HUVECs的5×105/L細胞懸液,在5% CO2濃度恒溫箱中,培養24 h后,加入不同濃度的馬錢子堿(終濃度0、10、20、40 μmol/L)處理48 h,棄上清液,4 ℃冷PBS沖洗細胞3 min×2次,試管中加入200 μl結合緩沖液重懸細胞,加入10 μl的Annexin V-FITC,暗室反應15 min;再加入10 μl碘化丙啶(PI)染液,流式細胞儀檢測馬錢子堿對HUVECs細胞凋亡率。
1.2.6Western blot檢測 細胞培養、分組和加藥干預同1.2.2項。BCA法測定蛋白濃度,進行SDS-PAGE凝膠電泳以及電轉,血清封閉2 h后,加入相應的一抗(羊抗人VEGF抗體1 ∶2 500、羊抗人EphA2抗體1 ∶2 000)4 ℃孵育過夜。TBST洗滌5 min×3次后,加入二抗,于室溫孵育2 h,TBST再次洗滌5 min×3次,顯影,掃描條帶,以GAPDH作為內參,VEGF、EphA2蛋白表達強度進行灰度比值顯示相對表達量。
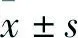
2 結果
2.1 馬錢子堿對HUVECs增殖抑制作用不同濃度的馬錢子堿可抑制HUVECs的生長,隨著馬錢子堿劑量(1、5、10、 20、40、80、160 μmol/L)的升高,對HUVECs的增殖呈明顯抑制作用,以對照組抑制率為0計算,隨著馬錢子堿藥物各處理組的濃度增加,增殖抑制作用逐漸增強(P<0.05,P<0.01),見圖1,90%可信區間的IC50為(28.2±2.6)μmol/L。

圖1 CCK-8 法檢測不同濃度馬錢子堿對HUVECs增殖影響與馬錢子堿濃度0 μmol/L組比較:*P<0.05,**P<0.01
2.2 劃痕實驗示馬錢子堿對HUVECs遷移抑制作用劃痕實驗如圖2所示,馬錢子堿對HUVECs細胞遷移能力的影響,細胞死亡數隨著馬錢子堿濃度增高而增多,遷移能力越來越低,不同濃度馬錢子堿(10、20、40 μmol/L)作用24 h 后,與對照組(0 μmol/L馬錢子堿)比較,馬錢子堿處理組可抑制HUVECs的遷移,10、20、40 μmol/L濃度組馬錢子堿對HUVECs細胞遷移能力下降至(10.7±1.1)%、(21.7±1.9)%、(28.2±2.1)% 。

圖2 不同濃度馬錢子堿對HUVECs細胞24 h遷移能力的影響
2.3 馬錢子堿對HUVECs凋亡的促進作用不同濃度馬錢子堿作用24 h后,光學顯微鏡下觀察各組細胞形態的變化。結果發現,與對照組(0μmol/L馬錢子堿)比較,隨著濃度增加,馬錢子堿(10、20、40 μmol/L)對HUVECs的凋亡影響明顯,細胞數明顯減少,細胞凋亡數明顯增加(圖3)。

圖3 不同濃度馬錢子堿對HUVECs細胞凋亡的影響Hoechst33258×200
2.4 流式細胞術檢測馬錢子堿處理后HUVECS細胞凋亡結果采取流式細胞術,Annexin-V/PI雙染實驗表明,與對照組(0 μmol/L馬錢子堿)(1.76±0.32)%進行比較,不同濃度(10、20、40 μmol/L)馬錢子堿處理組作用24 h后,HUVECs早期的細胞凋亡率顯著增加(圖4),細胞凋亡率分別為(4.01±0.73)%、(8.56±0.87)%、(10.12±1.07)%,差異有統計學意義(F=7.562、8.129、16.318,P=0.045、0.032、0.003)。

圖4 流式細胞術檢測不同濃度馬錢子堿誘導HUVECs的凋亡
2.5 馬錢子堿處理后HUVECS細胞VEGF、EphA2蛋白表達Western blot實驗顯示,與空白對照相比,隨著馬錢子堿(10、20、40 μmol/L)處理組內藥物濃度的增加,VEGF、EphA2蛋白水平呈下降趨勢(圖5A)。圖像分析顯示,與空白對照相比,隨著濃度升高,馬錢子堿(10、20、40μmol/L)處理組VEGF/GAPDH和EphA2/GAPDH蛋白表達明顯下降,差異有統計學意義(P<0.05,P<0.01),見圖5B。

圖5 Western blot法檢測馬錢子堿對HUVECs細胞VEGF和EphA2的蛋白表達A-D:馬錢子堿0、10、20、40μmol/L處理組;與對照組比較:*P<0.05,**P<0.01
3 討論
血管生成是臨床上腫瘤疾病生長、復發和轉移的關鍵環節[1]。抗血管生成是調節腫瘤血管微環境,抑制腫瘤內血管生長,從而誘導腫瘤細胞凋亡,抑制增殖。由于多種細胞和信號通路參與腫瘤生長微環境,臨床上近年來使用的抗腫瘤血管生成藥物療效有限,且有一定的副作用[4-5]。目前,大量臨床研究[6]證實,傳統中藥由于其低毒、多靶點、多個信號通路作用,抗癌療效確切,并可誘導腫瘤細胞凋亡,提高機體免疫功能,從而廣泛使用。該課題組前期研究[1]證實,馬錢子堿具有很好地抗乳腺癌細胞增殖功能。馬錢子堿的生物藥理作用已成為目前抗腫瘤治療作用的研究重題。同時,該研究通過劃痕實驗探討馬錢子堿影響HUVECs的細胞遷移能力,結果表明馬錢子堿可以有效抑制HUVECs的遷移。
馬錢子堿是提取自傳統中藥馬錢子中的吲哚型生物堿,白色結晶性粉末,劇毒,細胞水平抗腫瘤研究表明,馬錢子堿對多種腫瘤具有細胞毒作用,馬錢子堿可顯著抑制多種腫瘤細胞,如乳腺癌[7]、肝癌[8]等細胞增殖。該研究同樣表明,馬錢子堿明顯抑制HUVECs增殖,且隨著馬錢子堿處理組的濃度增加,增殖抑制作用增強。在基因嚴格調控下,細胞可以呈程序性死亡,即細胞凋亡,使得機體細胞增殖生長處于動態平衡;一旦增殖和凋亡失衡,即有可能引起腫瘤。誘導腫瘤細胞凋亡往往是化療藥物抗腫瘤作用的常見機制之一[9]。該研究通過Hoechst 33258檢測馬錢子堿對HUVECs凋亡影響,結果顯示不同濃度馬錢子堿作用24 h后,在光學顯微鏡下,與對照組比較,隨著馬錢子堿濃度增加,HUVECs細胞數明顯減少,核濃縮和碎裂形態的凋亡細胞明顯增加,表明馬錢子堿濃度依賴性增加細胞凋亡。流式細胞儀定量分析凋亡細胞數表明,馬錢子堿處理組明顯增加細胞凋亡,且隨著馬錢子堿濃度的上升,發生細胞凋亡的HUVECs明顯增多。故在一定濃度范圍內,馬錢子堿可能通過誘導HUVECs凋亡,從而抑制HUVECs細胞增殖。但需進一步研究明確馬錢子堿誘導細胞凋亡的分子機制,是通過抑制凋亡信號通路關鍵蛋白Caspase-3,還是升高Bax/Bcl-2蛋白比值,從而更好的為馬錢子堿在臨床上抗腫瘤血管生成提供依據。
腫瘤發生、生長、侵襲和轉移需要新生血管,該過程為一個復雜過程,血管生成是眾多促進和抑制血管生成的細胞因子參與過程,需要許多細胞因子參與信號傳導途徑,VEGF和EphA2是兩種重要的血管內皮細胞標志物,新生血管在腫瘤的發生和轉移中至關重要,在臨床治療中,如果能阻止腫瘤新生血管,就能阻止腫瘤生成[10]。EphA2具有酪氨酸激酶活性,在細胞生長與分化、血管形成、細胞遷徙與粘附中,均有EphA2 介導的信號參與;而VEGF是最為重要血管生成的促進因子,可特異性的促進細胞激活、增殖,通過控制EphA2與VEGF的表達,有可能調控腫瘤的血管生成,進而調控腫瘤行為[11-12]。該研究表明,馬錢子堿可以下調VEGF和EpHA2 的表達,然而是否可以通過激活Caspase-9引起線粒體凋亡途徑,導致細胞凋亡尚需進一步研究。
綜上,馬錢子堿可抑制HUVECs血管生成活性物質VEGF、Eph2的表達,從而抑制HUVECs形成新生血管,有可能成為抗血管生成作用藥物。

