陰離子交換樹脂對碳酸鹽水體中鈾酰離子的吸附研究
摘 要:近些年來,隨著核工業的發展和核能的大規模利用,自然環境面臨放射性污染的風險與日俱增。根據文獻,目前世界上多個國家已經發現采集的地下水水樣中鈾的含量過高[1-4],嚴重超出了各國關于飲用水中鈾含量的相關標準。鈾具備放射性與重金屬毒性,能夠使生物蛋白質發生變質。相關研究表明長期攝入含鈾的地下水,會對人體的腎臟造成不可逆損害,嚴重時致人死亡[5]。世界衛生組織則推薦飲用水中鈾的質量濃度不得超過30 ?g/L[6]。因此有必要關注和探索自然環境水樣中鈾酰離子的存在形態和去除手段。
關鍵詞:鈾酰離子,碳酸鹽,陰離子交換樹脂IRA900,吸附效率
1. 引言
鈾在自然環境中一般呈現正六價,也就是UO22+。然而UO22+容易與水中的CO32-絡合,生成不同形態的碳酸鈾酰絡合物,如UO2(CO3)34-,UO2(CO3)34-和UO2CO3。在某些金屬離子如Ca2+、Mg2+存在條件下,這些碳酸鈾酰絡合物又容易轉化為更復雜的鈾酰絡合物,如Ca2UO2(CO3)3或者MgUO2(CO3)32-等,從而形成一個復雜的含鈾水體系[7, 8]。強堿性陰離子交換樹脂由于其簡單方便并且高效從而被廣泛用于水處理領域,本文探究了陰離子交換樹脂IRA900在碳酸鹽水體系下對鈾酰離子的吸附行為,并且用數學軟件計算了其在實驗條件下的離子形態分布。本研究將為陰離子交換樹脂應用于含鈾污水的處理提供一定的理論指導。
2. 實驗分析
2.1 實驗材料與試劑
本文采用的陰離子交換樹脂為陶氏化學公司生產的IRA900型強堿性陰離子交換樹脂。樹脂使用之前先以1 mol/l的NaOH溶液和1 mol/l 的HCl溶液洗去樹脂中殘留的雜質,然后以大量的超純水將樹脂洗滌至中性為止,此時IRA900轉為氯型。最后將樹脂置于真空干燥箱中于40℃干燥48 h待用。本研究中所用的UO2(NO3)2·6H2O、NaOH和無水NaHCO3等試劑均為分析純。硝酸質量分數為65%~68%。所有的溶液均以超純水制備。
2.2 實驗方法
2.2.1 ?首先配置 1 mg/l的鈾和3 mmol/l 碳酸氫鈉混合溶液。隨后取7個干凈燒杯,每個燒杯內分別倒入35 mL左右該混合溶液。 以1mol/l 的硝酸溶液和 1 mol/l 的氫氧化鈉溶液對燒杯內的溶液進行pH調節,分別調整至4、5、6、7、8、9和10并做好標記。另取多個規格為40 mL的小玻璃瓶,每個玻璃瓶稱取0.05 g樹脂放入。將上述溶液跟玻璃瓶內的樹脂混合并且蓋緊瓶蓋,然后置于空氣震蕩搖床中于室溫震蕩3 小時, 震蕩頻率為120 rpm。待吸附完成后,以0.45 um的針筒過濾器實現固液分離。將過濾后的水樣稀釋后以微量鈾分析儀測定濃度。其中鈾的吸附效率用以下公式計算:
其中A(%)表示IRA900樹脂在實驗條件下對鈾的吸附效率,C0 (μg/l) 和 Ce (μg/l) 分別表示鈾的初始和平衡濃度。
2.2.2 鈾在實驗條件下的離子形態計算鈾的離子形態計算依靠化學計算軟件PHREEQC完成。該軟件由美國地質調查局開發,包含了大量關于鈾的熱力學數據。計算過程中采用的數據庫為wateq4f.dat。
3. 實驗結果
3.1 鈾在不同pH條件下的離子形態分布
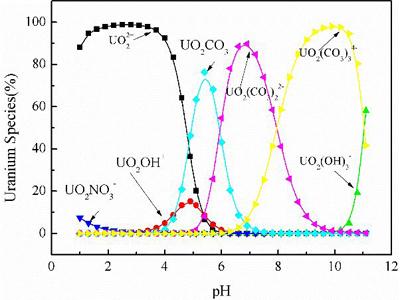
計算過程中輸入的鈾的質量濃度為1 mg/l, 碳酸氫鈉濃度為 3 mmol/l,這些參數與實驗條件一致。計算結果如圖1所示,鈾在碳酸鹽水體系中的離子形態占比會隨著pH值變化。其中在pH<4時,鈾主要是以UO22+存在; 當5
圖1 鈾在不同pH條件下的離子形態分布([U]= 1mg/l,[NaHCO3] = 3 mmol/l)
3.2 pH值對IRA900吸附鈾的影響
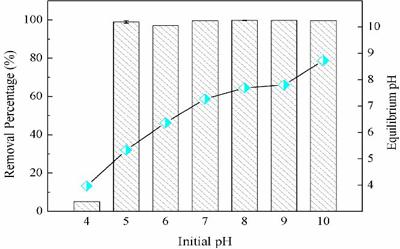
由于pH值對碳酸鹽水體系中鈾的形態分布會產生較大影響,因此研究考察了IRA900在不同pH條件下對鈾的吸附行為,并且測定了吸附前后的pH變化。如圖2所示,在初始pH為4的條件下,IRA900對鈾的吸附效率較低,約為6%左右。這是因為在這種酸性條件下,溶液中存在的碳酸氫根離子已經基本轉化為二氧化碳進入空氣中,導致溶液中沒有足夠的碳酸根離子與鈾酰離子配位進而無法形成碳酸鈾酰絡陰離子。而當pHμ5時,IRA900對鈾的吸附效率接近100%, 并且基本不隨pH值變化。此外,當pHμ8時,平衡pH值均高于初始pH值并且十分接近。然而,后續隨著初始pH值的增加,平衡pH值相對初始pH值均有一定程度下降。
圖2 IRA900在不同pH條件下對鈾的去除效率及前后pH變化([U]= 1mg/l,[NaHCO3] = 3 mmol/l)
4. 總結
本文探究了強堿性陰離子交換樹脂對碳酸鹽水體中U(Ⅵ)的吸附行為。通過理論計算發現,鈾在不同pH條件下的離子形態分布差異較大。其中在pH<4時,鈾主要是以UO22+存在; 當5
參考文獻:
[1] Nriagu J, Nam D H, Ayanwola T A, et al. High levels of uranium in groundwater of Ulaanbaatar, Mongolia[J]. Sci Total Environ, 2012, 414: 722-726.
[2] Katsoyiannis I A, Zouboulis A I. Removal of uranium from contaminated drinking water: a mini review of available treatment methods[J]. Desalination and Water Treatment, 2013, 51(13-15): 2915-2925.
[3] Shin W, Oh J, Choung S, et al. Distribution and potential health risk of groundwater uranium in Korea[J]. Chemosphere, 2016, 163: 108-115.
[4] Daulta R, Singh B, Kataria N, et al. Assessment of uranium concentration in the drinking water and associated health risks in Eastern Haryana, India[J]. Human and Ecological Risk Assessment: An International Journal, 2018, 24(4): 1115-1126.
[5] Domingo J L. Reproductive and developmental toxicity of natural and depleted uranium: a review[J]. Reproductive Toxicology, 2001, 15(6): 603-609.
[6] Organization W H. Uranium in drinking-water: Background document for development of WHO Guidelines for Drinking-water Quality[J]. 2004.
[7] Dong W, Brooks S C. Determination of the Formation Constants of Ternary Complexes of Uranyl and Carbonate with Alkaline Earth Metals (Mg2+, Ca2+, Sr2+, and Ba2+) Using Anion Exchange Method[J]. Environmental Science & Technology, 2006, 40(15): 4689-4695.
[8] Camacho L M, Deng S, Parra R R. Uranium removal from groundwater by natural clinoptilolite zeolite: effects of pH and initial feed concentration[J]. J Hazard Mater, 2010, 175(1-3): 393-398.
作者簡介:
陸玲玉,女,廣西來賓人,本科,廣西壯族自治區輻射環境監督管理站助理工程師,從事放射化學分析測試工作。

