糖耐量異常患者與糖耐量正常人群腸道菌群差異性研究
王智峰 徐心悅 姜玫
【摘要】 目的 探討糖耐量異常(IGT)患者和糖耐量正常人群腸道菌群的差異性。方法 選取20例糖耐量異常患者作為研究組, 另選20例接受健康體檢的健康人群作為常規組。收集所有研究對象的新鮮糞便樣品, 提取其中的細菌總DNA, 采用細菌通用擴增引物分別進行聚合酶鏈式反應(PCR)擴增, 對獲得的PCR產物展開測序分析, 測序完成后, 使用ABI實時熒光定量PCR儀檢驗腸道中常見的細菌種類。比較兩組腸道菌群種類及數量。結果 通過檢測數據發現, 本研究所有樣品中共檢查出三類細菌, 分別為擬桿菌門、厚壁菌門和變形菌門, 而擬桿菌門細菌是人體腸道中的主要優勢細菌。研究組擬桿菌門中普雷沃氏菌屬與擬桿菌屬細菌種類數量分別為(2.3±1.4)、(5.1±1.5)種低于常規組的(5.5±2.0)、(8.1±2.5)種, 差異有統計學意義(P<0.05)。研究組厚壁菌門中毛螺菌屬與乳酸菌屬細菌種類數量分別為(2.2±1.3)、(1.3±0.8)種低于常規組的(6.2±2.1)、(7.0±2.8)種, 差異有統計學意義(P<0.05)。研究組變形菌門中大腸埃希菌與志賀菌屬細菌種類數量分別為(4.3±1.3)、(4.1±1.2)種, 對照組變形菌門中大腸埃希菌與志賀菌屬細菌種類數量分別為(5.1±1.4)、(4.3±1.3)種, 兩組比較差異無統計學意義(P>0.05)。結論 糖耐量異常患者腸道菌群中優勢菌群的含量明顯低于糖耐量正常人群腸道中優勢菌群的含量, 需要針對性地展開治療。
【關鍵詞】 糖耐量異常;腸道菌群;差異性
DOI:10.14163/j.cnki.11-5547/r.2020.07.022
隨著科技進步, 人們的生活質量越來越高, 糖耐量異常患者的腸道菌群情況逐漸成為醫療界的重點研究對象[1]。腸道菌群主要包括人體腸道中的小生物群或基因組。大量實驗表明, 腸道菌群不僅會影響到人體的整體健康, 還是導致肥胖、糖尿病等慢性疾病的主要危險因素[2]。葡萄糖耐量是指人體對攝入葡萄糖的耐受能力, 糖耐量異常(IGT)的判斷標準為人在用餐結束的2 h內, 血糖值大于正常值, 但尚未達到糖尿病的判斷標準, 即稱作糖耐量異常[3]。本課題重點研究了糖耐量異常患者的腸道菌群特點, 以及和健康人群之間的區別, 現報告如下。
1 資料與方法
1. 1 一般資料 選取2018年3~8月本院內分泌科收治的20例糖耐量異常患者作為研究組, 另選取于本院接受健康體檢的20例健康人群作為常規組。研究組中, 男12例, 女8例;年齡31~45歲, 平均年齡(38.5±4.2)歲。
常規組中, 男9例, 女11例;年齡34~43歲, 平均年齡(38.2±4.1)歲。兩組患者一般資料比較, 差異無統計學意義(P>0.05), 具有可比性。本次研究已經大連大學附屬新華醫院倫理委員會認證, 并且所有研究對象均詳細了解整體過程, 同意進行研究并簽訂知情同意書。
1. 1. 1 納入標準 ①與世界衛生組織(WHO)和國際糖尿病聯盟(IDF)糖尿病專家委員會(1999年)指出的糖耐量異常判斷標準完全吻合。②空腹時血糖值<7.0 mmol/L。③接受葡萄糖耐量實驗2 h后, 血糖值<11.1 mmol/L[4]。
1. 1. 2 排除標準 ①患者年齡>25歲且<75歲。②處
于妊娠或者哺乳期的女性。③6個月前伴有嚴重高血壓、心肌梗死或者腦血管意外病史的患者。④患者在研究前3個月內未服用過抗生素, 且在半個月內未服用益生元或益生菌等藥物。⑤研究前3個月內未出現腹瀉、便秘、痢疾等疾病[5]。
1. 2 方法
1. 2. 1 樣本收集 在無菌環境下, 分別收集兩組研究對象的新鮮糞便, 在糞便中心位置收集10~15 g, 置入無菌冷存管后冷藏, 樣品收集的整體過程均和醫院的倫理要求符合[4]。
1. 2. 2 DNA采集 實驗樣品中微生物總DNA的提取工作, 使用購自德國的QIAamp DNA Stool Mini Kit儀器進行, 樣品量為100 mg, 詳細的操作方法參考說明書進行。將收集的DNA使用購自美國的NanoDrop ND-1000分光光度計進行測定, 然后置于-80℃的環境下冷藏備用[6]。
1. 2. 3 聚合酶鏈式反應 參考獲得的總DNA進行擴增工作和產物測序, 16S rRNA PCR引物的主要構成包括:測序接頭引物、Index以及V3區引物。Index是一種主要構成為6bp核苷酸的序列, 主要用途為標記PCR產物的來源。PCR的擴增體系共包括25 μl, 擴增條件為:①在98℃的環境下預變性30 s;②在98℃環境下變性10 s, 在50℃的環境下退火30 s, 在72℃的環境下延伸30s, 持續循環20次;③在72℃的環境下延伸7 min, 并于4℃的環境下儲存。反應完成后, 使用濃度為1.5%的瓊脂糖凝膠電泳檢驗擴增片段的大小, 使用QIAquick Gel Extraction Kit儀器處理目的條帶膠。使用美國的Illumina Miseq高通量測序平臺對獲得16S rRNA-V3區的PCR產物展開測序[7]。
1. 2. 4 生物信息學分析和熒光定量PCR 測序完成后, 對PCR產物的高質量序列展開提取, 然后使用ABI實時熒光定量PCR儀檢驗腸道中常見的細菌種類[8]。
1. 3 統計學方法 采用SPSS23.0統計學軟件對數據進行處理。計量資料以均數±標準差( x-±s)表示, 采用t檢驗;計數資料以率(%)表示, 采用χ2檢驗。P<0.05表示差異有統計學意義。
2 結果
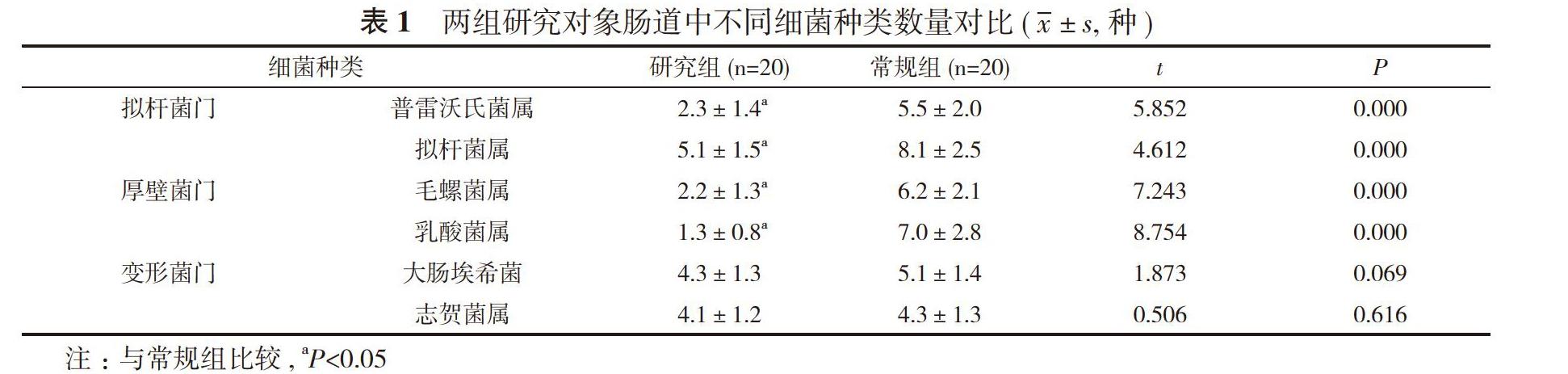
通過檢測數據發現, 本研究所有樣品中共檢查出三類細菌, 分別為擬桿菌門、厚壁菌門和變形菌門, 而擬桿菌門細菌是人體腸道中的主要優勢細菌。研究組擬桿菌門中普雷沃氏菌屬與擬桿菌屬細菌種類數量分別為(2.3±1.4)、(5.1±1.5)種低于常規組的(5.5±2.0)、(8.1±2.5)種,
差異有統計學意義(P<0.05)。研究組厚壁菌門中毛螺菌屬與乳酸菌屬細菌種類數量分別為(2.2±1.3)、(1.3±0.8)種低于常規組的(6.2±2.1)、(7.0±2.8)種, 差異有統計學意義(P<0.05)。研究組變形菌門中大腸埃希菌與志賀菌屬細菌種類數量分別為(4.3±1.3)、(4.1±1.2)種, 對照組變形菌門中大腸埃希菌與志賀菌屬細菌種類數量分別為(5.1±1.4)、(4.3±1.3)種, 兩組比較差異無統計學意義(P>0.05)。見表1。
3 討論
葡萄糖耐量是指機體對體內葡萄糖的耐受能力。若在飯后2 h血糖值超過正常指標, 即7.8 mmol/L, 但沒有超過糖尿病判斷標準(11.1 mmol/L);或者患者在空腹時血糖值雖然上升, 處于6.2~7.0 mmol/L之間, 但未達到糖尿病的判斷標準, 即稱作糖耐量異常[9]。現階段, 醫療界已經將糖耐量異常作為糖尿病初期發病的黃金指標。相關資料[10]表明, 每年約有7%的糖耐量異常患者轉化成2型糖尿病, 并且糖耐量異常患者發生心肌梗死、心絞痛等心血管疾病的幾率也會隨之上升。隨著科技的不斷進步, 關于腸道菌群的研究漸漸增加。腸道菌群屬于腸道中的小生物群或者其他基因組織。大量實驗指出, 腸道菌群不僅能夠保持人體的整體健康, 還和肥胖、2型糖尿病等慢性代謝性疾病的發生、惡化具有緊密聯系。在人類的胃腸道中, 已知的細菌數量超過1000種, 數量約為1014個。菌群的生物學分類從大到小分別為種、屬、科、目、綱、門, 現階段的研究大多集中在“門”與“屬”這兩個范圍, 在此基礎上研究不同菌群和機體代謝之間的聯系[11]。
目前, 國內糖耐量異常的患者基數日益增加, 但是對于該類患者的干預治療措施相對較少, 臨床效果相對較差[12]。通過本研究能夠明確不同糖耐量異常患者的腸道菌群特征, 分析糖耐量異常患者與糖耐量正常人群之間的差別, 通過調控腸道菌群來避免糖耐量異常患者發展成為糖尿病, 從而降低糖尿病的發病率, 以及因糖尿病并發癥導致的社會問題及經濟壓力。
機體腸道中的微生物菌群與機體自身的代謝功能具有緊密聯系, 其含量與種類的改變會直接引起各類慢性代謝類疾病。大量實驗指出, 體內微生物菌群與機體的神經系統、內分泌系統以及免疫系統之間均具有緊密聯系[13]。
綜上所述, 糖耐量異常患者的腸道菌群和健康人群相比存在明顯的差異, 因此需要針對性的實施治療。
參考文獻
[1] Lloyd-Price J, Mahurkar A, Rahnavard G, et al. Strains, functions and dynamics in the expanded Human Microbiome Project. Nature, 2017, 550(7674):61-66.
[2] Medina-Vera I, Sanchez-Tapia M, Noriega-López L, et al. A dietary intervention with functional foods reduces metabolic endotoxaemia and attenuates biochemical abnormalities by modifying faecal microbiota in people with type 2 diabetes. Diabetes Metab, 2018, 45(2):122-131.
[3] Balakumar M, Prabhu D, Sathishkumar C, et al. Improvement in glucose tolerance and insulin sensitivity by probiotic strains of Indian gut origin in high-fat diet-fed C57BL/6J mice. Eur J Nutr, 2018, 57(1):279-295.
[4] 蔣嵐, 陳果, 高陳林, 等. 益生菌對T2DM患者腸道菌群和脂聯素的影響. 中國現代醫學雜志, 2018, 28(11):84-87.
[5] Liu F, Prabhakar M, Ju J, et al. Effect of inulin-type fructans on blood lipid profile and glucose level:a systematic review and meta-analysis of randomized controlled trials. Eur J Clin Nutr, 2017, 71(1):9-20.
[6] 吳琳英, 鄧順有, 王毅飛, 等. 阿托伐他汀對2型糖尿病小鼠腸道菌群的影響. 中國實用醫藥, 2017, 12(22):128-130
[7] 劉丹英, 葉小斌. 阿奇霉素聯合莫沙必利對糖尿病胃輕癱患者腸道菌群的影響. 中國微生態學雜志, 2018, 30(2):185-188.
[8] 胡文斌, 張婷, 張小花, 等. 文化程度和肥胖指標交互作用對糖尿病前期患病影響研究. 中國慢性病預防與控制, 2017, 25(9):658-661.
[9] 徐綺, 薛錦花, 劉連勇, 等. 某社區中年人群糖尿病患者綜合管理現況與分析. 中華全科醫學, 2017, 15(8):1374-1377.
[10] 張景雪. 一體化教育管理模式對糖耐量異常患者治療依從性的影響. 河南醫學研究, 2017, 26(1):160-161.
[11] 陳海燕. 社區綜合干預管理模式在糖耐量異常患者中的應用效果觀察. 中國醫藥科學, 2017, 7(2):113-115.
[12] 王一灑, 袁建軍, 朱好輝, 等. 應用分層應變技術評估Ⅱ型糖尿病及糖耐量異常患者左心室各層心肌收縮功能改變. 中國超聲醫學雜志, 2017, 33(1):27-31.
[13] 賈愛華, 徐少勇, 明潔, 等. 我國不同診斷標準下肥胖流行病學特征分析. 中國糖尿病雜志, 2017, 9(4):221-225.
[收稿日期:2019-07-17]

