基于網絡藥理學及分子對接篩選大血藤防治類風濕性關節炎的關鍵靶點及活性成分
陳平男 楊欣 盧筱瀟
【摘 要】 目的:篩選類風濕性關節炎的關鍵靶點及大血藤的干預研究。方法:基于CTD(Comparative Toxicogenomics Database)篩選類風濕性關節炎靶點,通過KABOX和DAVID對RA靶點進行通路富集分析。借助STRING結合Cytoscape 對RA(Rheumatoid Arthritis)通路中關鍵靶點進行相互作用分析。基于分子對接(SYBYL 2.1.1)研究大血藤活性成分與關鍵靶點的作用特征。結果:類風濕性關節炎靶標175個,DAVID和KOBAX通路中包括RA通路, RA通路包括16個靶點(TNF、IL-6、TLR2、IL1β、IL18、IL23A、CSF2、VEGF2、IFNG、CTLA4、CXCL8、CD28、CXCL6、HLA-DPB1、HLA-DRB1、HLA-DQA2)。通過與10個關鍵靶點分子對接明確:腫瘤壞死因子、血管內皮生長因子A、白介素1β、toll樣受體2為大血藤治療類風濕性關節炎的關鍵靶標蛋白;谷甾醇、毛柳甙、內消旋二氫愈創木酯酸為關鍵活性成分。結論:初步篩選出大血藤發揮抗RA的活性成分及關鍵靶點,為大血藤治療RA活性成分的開發提供理論依據。
【關鍵詞】 大血藤;分子對接;化學成分;類風濕性關節炎;網絡藥理學
【中圖分類號】R284.1 【文獻標志碼】 A 【文章編號】1007-8517(2020)2-0035-05
Abstract:Obstract Screening of key targets for rheumatoid arthritis base on Comparative Toxicogenomics Database; Methods Analysis of pathway enrichment base on KABOX and DAVID; Interaction analysis of key targets in Rheumatoid Arthritis pathway Based on STRING combined with Cytoscape; Study on the action characteristics of active components and key target of Sargentodoxae Caulis; Resuls 175 targets for rheumatoid arthritis, The RA channel has 16 targets: TNF,IL-6,TLR2,IL1β,IL18,IL23A,CSF2,VEGF2,IFNG,CTLA4,CXCL8,CD28, CXCL6, HLA-DPB1, HLA-DRB1, HLA-DQA2. The docking with 10 key target molecules is clear: TNF, VEGF2, IL1β and TLR2 are the key target proteins for treatment of rheumatoid arthritis;The key active components are sitosterol, salidroside and Meso-dihydroguaiaretic acid.Conclusion Sargentodoxae Caulis play the active ingredients and key targets of anti-RA, it provides a theoretical basis for the development of RA active ingredients in A treatment.
Keywords:Sargentodoxae Caulis;Molecular Docking; Chemical Composition; Rheumatoid Arthritis;Network Pharmacology
類風濕性關節炎(Rheumatoid arthritis,RA)為自身免疫疾病,主要表現為多關節炎、關節腫痛、軟骨和骨破壞和關節畸形等。目前,研究者不斷研究與開發防治RA的藥物[1],包括中藥、單體及中藥復方[2]。中藥在防治RA疾病中發揮重要作用,中藥的毒副作用較少,凸顯其在RA中的作用優勢。中藥單體、復方防治RA均有報道。曾光等[3]研究熊果酸對RA及骨質破壞具有一定的作用;黃明進等[4]發現黑骨藤具有防治RA的作用;李健等[5]采用中藥方劑治療類風濕關節炎。中藥化學成分諸多,活性成分與靶標蛋白結合,對疾病的治療中發揮協同作用,但是中藥的活性成分經過提取分離,從分子水平(蛋白、基因)探討其藥理作用的過程比較復雜。隨著科學技術的不斷提高,多學科的交叉,分子對接迅速發展,在中醫藥中廣泛應用[6]。分子對接將中藥、中藥復方、天然產物等小分子與疾病的關鍵靶點(蛋白)進行幾何匹配和能量匹配。查找空間和能量與之最佳契合的生物大分子,是快速的發現藥物作用潛在靶標的新方法[7]。
大血藤為大血藤科藤本植物大血藤(Sargentodoxa cuneata(Oliv) Rehd.et Wils.)的干燥藤莖、根,又稱為“血藤”。用藥歷史悠久,臨床應用廣泛,具有活血散瘀、強筋骨、止痛通經的功效。目前,大血藤主要集中在抗菌、抗炎、抗病毒等藥理作用[8]。但是大血藤抗炎活性成分及靶標蛋白并不清楚,因此對其化學成分進行了進一步的研究,為中藥開發及中藥活性成分應用提供理論依據。以研究大血藤抗RA的活性成分及機制為目的,從整體層面,運用分子對接結合網絡藥理學,闡釋中藥功能描述與現代藥理之間的關系。
1 實驗方法
1.1 類風濕性關節炎靶點篩選 RA的潛在靶標基因通過CTD進行篩選,在線打開CTD,在疾病名稱中輸入“Arthritis, Rheumatoid”為關鍵詞檢索RA的相關靶點,選擇已經有實驗驗證的“M”或“T”為靶標,統計RA靶點的數量。
1.2 通路分析 基于DAVID(https://david. ncifcrf.gov/)和KOBAX3.0(KEGG Orthology Based Annotation System)對RA靶標基因進行通路富集分析,DAVID是基于WEB服務器的富集分析軟件。對RA靶點進行GO功能、通路和疾病分析等;KOBAS軟件的功能模塊中有ID Mapping,將RA基因通過數據庫富集到相應的通路中。分析結果得到RA靶點參與的通路途徑,選擇RA靶點顯著參與的途徑(P≤0.01),基于Rstudio軟件中的ggplot 2繪制氣泡圖,包括通路名稱、富集分析的P值、Rich factor和Q值等。
1.3 相互作用分析 采用STRING結合Cytoscape 3.5.1對RA通路中16個RA靶點進行相互作用分析,STRING是蛋白質相互作用數據庫,可進行是搜索已知蛋白之間和預測蛋白質之間相互作用,通過蛋白質名稱進行檢索16個蛋白質相互作用的相關性。
1.4 大血藤活性成分篩選 大血藤小分子化合物基于中藥系統藥理學數據庫和分析平臺(Traditional Chinese Medicine Systems Pharmacology ,TCMSP)下載[9],通過大血藤名稱查找活性成分。對大血藤關鍵化學成分進行分子量(MW)、氫鍵供體數(Hdon)、氫鍵受體數(Hacc)、生物利用度(OB)、血腦屏障(BBB)、藥物對小腸上皮細胞的穿透性和類藥性等進行分析。基于SYBYL2.1.1對大血藤活性成分進行加氫和加電荷[10],對活性成分進行 Minimize 能量優化,保存為SLN格式。
1.5 分子對接 采用SYBYL2.1 軟件的Surflex-Dock 模塊對大血藤活性成分與RA靶點進行分子對接研究[11]。從蛋白質晶體結構數據庫RCSB (http://www.rcsb.org/pdb ) 下載白細胞介素-6(PDBID∶[KG-*3/5]1ALU)、人白介素1β(PDBID∶[KG-*3/5]1RWN)、腫瘤壞死因子(PDBID∶[KG-*3/5]2AZ5)、toll樣受體2(PDBID∶[KG-*3/5]1FYW)、白細胞介素18(PDBID∶[KG-*3/5]3WO2)、白細胞介素23A(PDBID∶[KG-*3/5]3QWR)、人集落刺激因子2(PDBID∶[KG-*3/5]5C7X)、干擾素-γ(PDBID∶[KG-*3/5]1EKU)、血管內皮生長因子A(PDBID∶[KG-*3/5]3BDY)和細胞毒T淋巴細胞相關抗原4(PDBID∶[KG-*3/5]3OSK)3D 晶體結構。選擇原配體模式產生活性口袋,分子對接結果以Total-Score>5為閾值。
2 實驗結果
2.1 類風濕性關節炎靶點篩選及通路分析 基于CTD 篩選類風濕性關節炎靶標基因,以“Arthritis, Rheumatoid”為關鍵詞檢索類風濕性關節炎的相關靶點,選擇已經有實驗驗證的“M”或“T”為靶標,共篩選出175個RA的靶標基因。
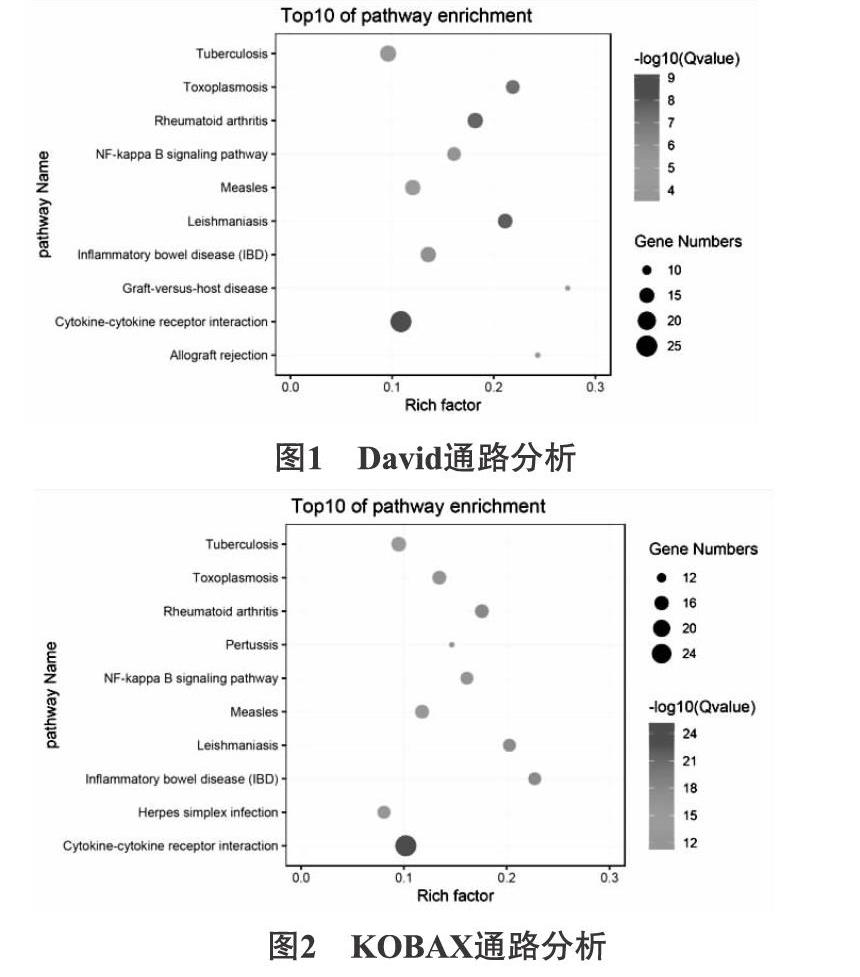
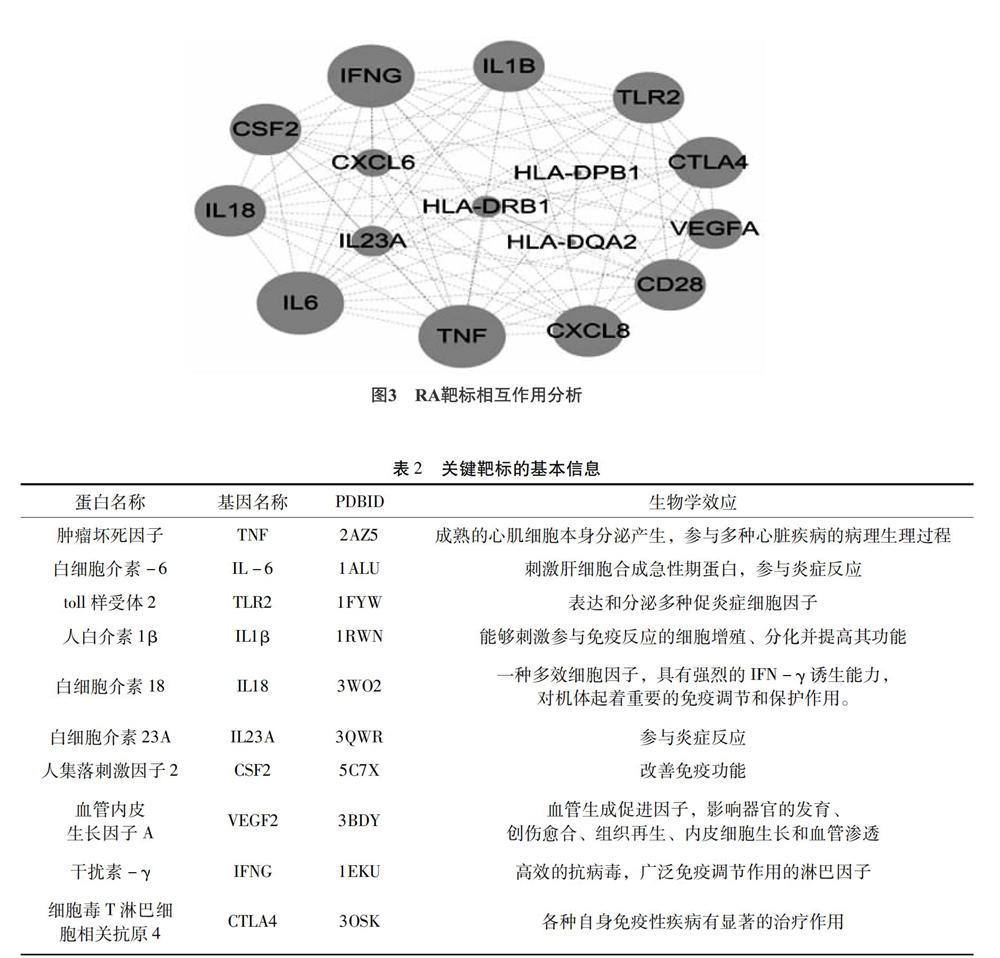
采用DAVID 對RA靶點進行通路分析,得到RA靶點參與的所有途徑,篩選出RA靶點顯著參與的通路途徑(P<0.01),175個RA靶點參與38條代謝途徑,輸出前10條通路(圖1),包括RA通路(P-Value=2.01E-11)。采用KOBAX對RA靶點進行通路分析,175個RA靶點參與85條代謝途徑,輸出前10條通路(圖2),包括RA通路(P-Value=6.04E-20)。
RA通路中包括16個靶標基因(TNF、IL-6、TLR2、IL1β、IL18、IL23A、CSF2、VEGF2、IFNG、CTLA4、CXCL8、CD28、 CXCL6、HLA-DPB1、HLA-DRB1、HLA-DQA2),兩個數據庫RA通路中靶標基因具有一致性。
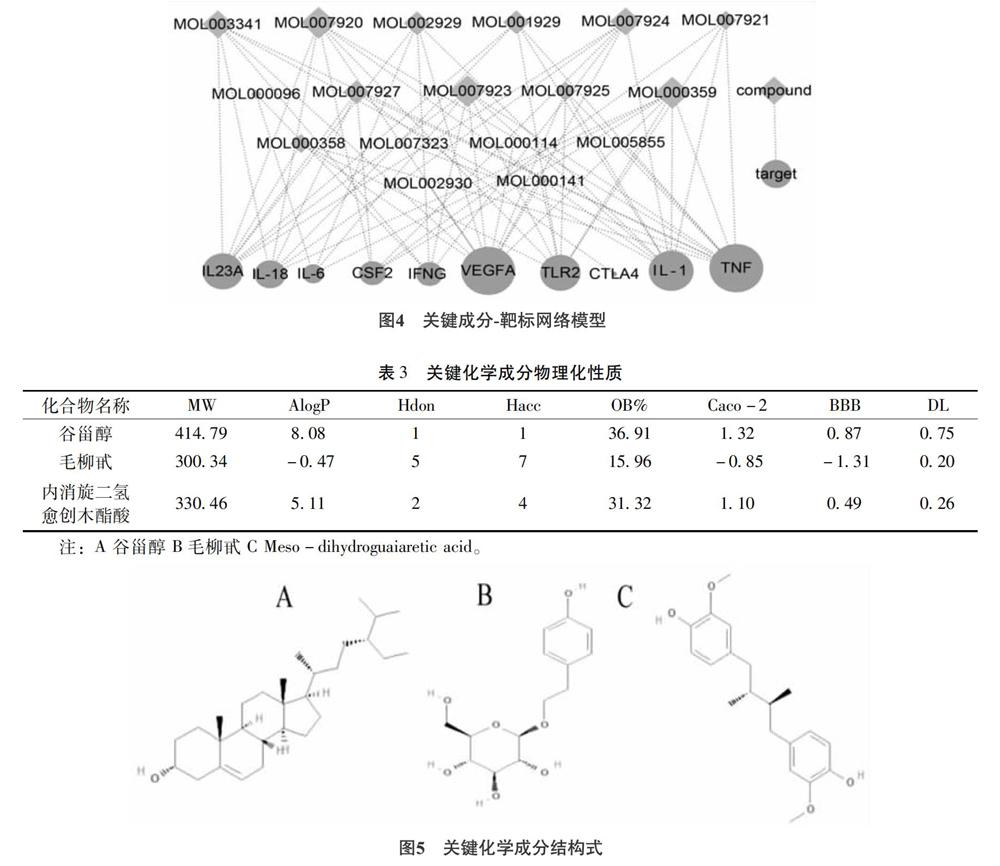
2.2 RA通路靶點相互作用分析 采用STRING結合Cytoscape 3.5.1對RA通路中16個靶標基因進行相互作用分析,結果顯示整個網絡關聯緊密。圖3表明: TNF、VEGFA 、CTLA4和 IFNG等為中心靶點,去掉后,整個網絡渙散。
2.3 類風濕性關節炎的關鍵靶標蛋白 通過蛋白相互作用分析,根據degree(度)的大小,選擇有實驗數據支持的靶點進行分子對接,對關鍵靶標進行生物學效應分析[12-13]。詳見表2。
2.4 分子對接結果 本次研究將處理好的 23個小分子分別與 10個靶標蛋白進行能量匹配,原配體與10個靶標蛋白結合的總分為42.5,選擇總分大于42.5且與靶點結合的數量大于7為抗類風濕性關節炎的活性成分。通過篩選明確大血藤化學成分谷甾醇(MOL000359)與7個靶點(IL-6、TNF、IL1B、IL18、CSF2、VEGFA、TLR2)結合較好,且分子對接總分為43;毛柳甙(MOL003341)與7個靶點(L-6 、TNF、IL1B、IL18、IL23A、VEGFA、IFNG)結合較好,且分子對接總分為49;內消旋二氫愈創木酯酸(MOL007920)與7個靶點(TNF、IL1B、IL18、IL23A、CSF2、VEGFA、TLR2)結合較好,且分子對接總分為48。谷甾醇、毛柳甙、內消旋二氫愈創木酯酸為大血藤發揮抗類風濕性關節炎的關鍵活性成分。
大血藤23個化學成分,其中11個化學成分能調節腫瘤壞死因子(TNF)、血管內皮生長因子A(VEGFA);9個化學成分能調節白介素1β(IL1β);8個化學成分能調節toll樣受體2(TLR2)。腫瘤壞死因子、血管內皮生長因子A、白介素1β、toll樣受體2為大血藤治療類風濕性關節炎的關鍵靶標蛋白。詳見圖4。
2.5 關鍵化學成分的理化性質 大血藤抗RA的關鍵活性成分谷甾醇、毛柳甙、內消旋二氫愈創木酯酸進行ADME/T性質分析。根據Lipinski規則,化合物應該具備氫鍵受體數(Hacc)<10,分子量(MW)<500,氫鍵供體數(Hdon)<10,生物利用度(OB)≥30%,藥物對小腸上皮細胞的穿透性≥-0.4,血腦屏障(BBB)≥-0.3,類藥性≥0.18。如果過多參數不符合,會影響藥物的溶解性及腸吸收能力,谷甾醇、內消旋二氫愈創木酯酸、毛柳甙基本遵循Lipinski規則(表3)。谷甾醇、內消旋二氫愈創木酯酸、毛柳甙的化學結構詳見圖5。
3 討論
本研究從大血藤活性成分、RA靶點、通路、相互作用等幾個方面進行討論。RA是一種慢性自身免疫性疾病,越來越多的證據表明,RA的病理生理機制非常復雜,多種生物學過程和多條信號通路參與了RA損傷進程。本研究篩選出的175個RA靶點主要參與TNF,Toll-like receptor 等通路釋放炎性細胞因子及促炎因子。大血藤可能通過多成分-多靶點或多成分-單靶點干預炎癥、免疫通路減少炎性細胞因子與促炎因子的釋放。本研究通過網絡藥理學結合分子對接技術,系統篩選大血藤治療RA可能的活性成分及分子機制,為治療RA提供新的切入點。本研究僅初步闡釋了其合理性,尚存在一些局限性。
目前,多種生物制劑在RA的治療環節中發揮作用[14]。但是RA疾病反復發作,尚未有根治的方法,臨床上存在治療難點。RA的發病機制非常復雜,并不是單條通路發揮作用,而是多條通路共同作用,需要不斷研究防治RA的靶向藥物。本研究采用分子對接明確大血藤通過多成分-多靶點協同治療類風濕性關節炎,11個活性成分與血管內皮生長因子A(VEGFA)和腫瘤壞死因子(TNF) 有較好的結合;9個活性成分與白介素1β ( IL1β )有較好的結合;8個化學成分能調節toll樣受體2(TLR2)。已經有研究者發現大血藤對佐劑性關節炎大鼠滑膜細胞MMP-9、MMP-2、血清TNF-α和IL-6有調節作用[15-16]。RA的發生、發展與多種細胞因子相關,已經有研究表明:TNF為RA發病的主要促炎因子之一,促進炎癥持續反應,軟骨及骨的破壞,已經開發抗TNF-α藥物[17]。VEGFA為血管生成促進因子之一,主要影響器官的發育、組織再生、血管滲透等[18]。IL是致炎性因子,促進大量炎癥細胞的聚集,開發抑制IL的表達已經成為治療RA的新方法[19]。總之,TNF、VEGFA、IL1β和TLR2可能為大血藤治療類風濕性關節炎的關鍵靶標蛋白,為動物實驗提供理論依據。同時通過本次研究發現:谷甾醇、毛柳甙、內消旋二氫愈創木酯酸為大血藤發揮抗類風濕性關節炎的關鍵活性成分。已經有研究表明:毛柳甙具有抗腫瘤、抗衰老、心血管保護和調節免疫等廣泛的藥理活性[20-21];谷甾醇為植物界最普遍存在的甾醇,在降血膽固醇、抗炎、抗腫瘤等藥理作用中發揮重要作用。本研究初步明確了大血藤抗類風濕性關鍵炎的關鍵靶點及活性成分。
參考文獻
[1]趙光智.黃芪桂枝五物湯加味治療類風濕性關節炎療效觀察[J].山西中醫,2010,26(3):22.
[2]Aletaha D,Ward MM, Machold KP, et al.Remission and active disease in rheumatoid arthritis[J]. Arthritis Rheum, 2005,52(9):2625-2636.
[3]曾光,陳芳,熊新貴,等.熊果酸對 CIA 大鼠關節炎癥及骨質破壞的影響[J]. 湖南中醫藥大學學報,2013,33(7):3-7.
[4]黃明進,羅春麗,郭剛,等.黑骨藤抗類風濕性關節炎作用及其分子機制[J].中國實驗方劑學雜志,2011,17(12):175-177.
[5]李健,郭洪濤,牛旭艷,等.治療類風濕關節炎中藥方劑作用原理的網絡藥理學研究策略[J].中國實驗方劑學雜志,2012,18(6):267-269.
[6]葉德永.計算機輔助藥物設計導論[M].北京:化學工業出版社, 2004.
[7]李翔,吳磊宏,范驍輝,等.復方丹參方主要活性成分網絡藥理學研究[J].中國中藥雜志,2011,36(210)∶2911-2914.
[8]李華, 黃淑鳳, 鄧翀, 等.大血藤鎮痛作用和抗炎作用研究[J].陜西中醫,2013,34(10):1427-1428.
[9]RU J, PENG L, WANG J, et al. TCMSP: a database of systems pharmacology for drug discovery from herbal medicines [J]. J Cheminform, 2014,13(8):1498-1504.
[10]林桂源,姚華聰,鄭細娜,等. 基于分子對接技術的常用降糖中藥有效成分虛擬篩選[J]. 中國實驗方劑學雜志,2015(15):202-206.
[11]Spitzer R, Jain A.N. Surflex-Dock: Docking Benchmarks and Real-World Application[J]. J Comput Aided Mol Des, 2012,26(6): 687-699.
[12]Tanaka Y, Martin Mola E. IL-6 targeting compared to TNF targeting in rheumatoid arthritis: studies of olokizumab,sarilumab and sirukumab[J].Ann Rheum Dis,2014,73(9):1595 -1597.
[13]余建明,劉喜德,曲丕盛,等.祛痹鎮痛方對膠原誘導性關節炎大鼠滑膜 IL-1β、IL-8、VEGF 表達的影響達的影響[J].中國中西醫結合雜志,2013,33(1):105-109.
[14]Smolen J S, Aletaha D, Mcinnes I B. Rheumatoid arthritis[J]. Lancet, 2016,388(10055):2023-2038.
[15]付鈺,王光.中藥大血藤對佐劑性關節炎大鼠滑膜細胞MMP-2、MMP-9的影響[J].貴州醫藥,2009,33(12):1097-1099.
[16]付鈺.中藥大血藤對佐劑性關節炎大鼠血清TNF-α、IL-6的影響[J].現代醫院,2007,7(9):37-39.
[17]Bradley JR.TNF-mediated inflammatory disease[J].J Pathol,2008,214(2) : 149-160.
[18]高俊,丁真奇.細胞因子在類風濕性關節炎中作用的研究現狀[J].醫學綜述, 2006,12(5) : 289-291.
[19]楊涵棋, 劉旭光, 楊馨, 等.不同灸法對類風濕性關節炎家兔腫脹關節及滑膜液中白介素-1、腫瘤壞死因子-α表達的影響[J].針刺研究2013,38(28):134-139.
[20]ZHU Y, SHI YP, WU D, et al. Salidroside protects againsthydrogenperoxide- induced injury in cardiac H9c2 cells via PI3K- Akt dependent pathway[J]. DNA Cell Biol, 2011, 30 (10):809-819.
[21]CHEN X,ZHANG Q,CHENG Q, et al.Protective effect of salidroside against H2O2 induced cell apoptosis in primary culture of rat hippocampal neurons[J]. Mol Cell Biochem,2009,332(1/2):85-93.
(收稿日期:2019-11-26 編輯:程鵬飛)

