持續低效血液透析聯合血液灌流治療 多臟器功能障礙綜合征患者的療效觀察
黃歡 許標 羅瑋

【摘要】 目的 觀察持續低效血液透析(SLED)聯合血液灌流(HP)對多臟器功能障礙綜合征(MODS)患者的炎癥水平及預后的影響, 評價其療效。方法 72例MODS患者, 根據所采用的血液凈化方法不同分為SLED組(給予SLED治療)、SLED+HP組(給予SLED+HP治療)、持續靜脈-靜脈血液濾過(CRRT)組(給予CRRT治療)、CRRT+HP組(給予CRRT+HP治療), 各18例。比較四組患者治療前和治療后的急性生理學及慢性健康狀況評分系統Ⅱ(APACHEⅡ)評分、血清肌酐(Scr)、超敏C反應蛋白
(hs-CRP)、白介素(IL)-6、IL-10、腫瘤壞死因子-α(TNF-α)水平, 治療后28 d存活率。結果 治療后, 四組患者的APACHEⅡ評分、Scr、hs-CRP、IL-6、IL-10、TNF-α水平均顯著降低, 差異有統計學意義(P<0.05)。SLED+HP組的APACHEⅡ評分、Scr、hs-CRP、IL-6、IL-10、TNF-α水平降低大于SLED組, CRRT+HP組的APACHEⅡ評分、Scr、hs-CRP、IL-6、IL-10、TNF-α水平降低大于CRRT組, 差異均有統計學意義(P<0.05)。SLED+HP組和CRRT+HP組、SLED組和CRRT組比較差異無統計學意義(P>0.05)。SLED+HP組的28 d存活率為88.9%, CRRT+HP組的28 d存活率為83.3%, 均高于SLED組的55.6%與CRRT組的50.0%, 差異有統計學意義(P<0.05)。SLED+HP組與CRRT+HP組、SLED組和CRRT組患者的28 d存活率比較, 差異無統計學意義(P>0.05)。結論 四種血液凈化治療方案均能有效降低MODS患者的血清Scr、hs-CRP、IL-6、IL-10、TNF-α水平, 改善患者臨床癥狀和體征。SLED聯合HP具有更強的清除炎癥因子能力和腎功能保護作用, 能改善患者的預后, 其治療效果與CRRT聯合HP相當。
【關鍵詞】 持續低效血液透析;連續腎臟替代治療;血液灌流;多臟器功能障礙綜合征
DOI:10.14163/j.cnki.11-5547/r. 2020.05.001
Efficacy of sustained low-efficiency dialysis combined with hemoperfusion in patients with multiple organ dysfunction syndrome? ?HUANG Huan, XU Biao, LUO Wei. Department of Physician, Guangning Vounty Peoples Hospital, Zhaoqin, 526300
【Abstract】 Objective? ?To observe the effect of sustained low-efficiency dialysis (SLED)combined with hemoperfusion (HP) in patients with multiple organ dysfunction syndrome (MODS), and evaluate its efficacy. Methods? ?A total of 72 MODS patients were divided into sustained low-efficiency dialysis group (SLED), sustained low-efficiency dialysis combined with hemoperfusion group (SLED+HP group), continuous renal replacement therapy group (CRRT group) and continuous renal replacement therapy combined with hemoperfusion group (CRRT+HP group), with 18 cases in each group. The Acute Physiology and Chronic Health Evaluation Ⅱ (APACHEⅡ) score, serum creatinine (Scr), hypersensitive C-reactive protein (hs-CRP), interleukin(IL)-6, IL-10, tumor necrosis factor α(TNF-α) before treatment and after treatment, occurrence of complications and survival rate after 28 d of treatment were compared among the four groups. Results? ?After treatment, the APACHEⅡ score, serum Scr, hs-CRP, IL-6, IL-10 and TNF-α levels in four groups were decreased than those before treatment, and their difference was statistically significant (P<0.05). The degree of reduction of APACHEⅡ score, serum Scr, hs-CRP, IL-6, IL-10 and TNF-α levels in SLED+HP group was greater than those in SLED group, and CRRT+HP group was greater than CRRT group, and the difference was statistically significant (P<0.05). There was no statistically significant difference in APACHEⅡ score, serum Scr, hs-CRP, IL-6, IL-10 and TNF-α levels between SLED+HP group and CRRT+HP group (P>0.05). The 28 d survival rate was 88.9% in SLED+HP group and 83.3% in CRRT+HP group, which were higher than 55.6% in SLED group and 50.0% in CRRT group, and their difference was statistically significant (P<0.05). There was no statistically significant difference in 28 d survival rate between SLED+HP group and CRRT+HP group (P>0.05). Conclusion? ?Four kinds of blood purification therapy can effectively reduce the levels of serum Scr, hs-CRP, IL-6, IL-10, TNF-α, and improve the clinical symptoms and signs of MODS patients. SLED combined with hemoperfusion has a stronger ability to clear inflammatory factors and protect renal function, and can improve the prognosis of patients. Its therapeutic effect is comparable to CRRT combined with hemoperfusion.Its therapeutic effect is similar to CRRT combined with hemoperfusion.
【Key words】 Sustained low-efficiency dialysis; Continuous renal replacement therapy; Hemoperfusion; Multiple organ dysfunction syndrome
全身炎癥反應綜合征(SIRS)是指感染、創傷和休克等等因素引發機體出現嚴重、全身和失控的炎癥免疫反應, 患者機體內的炎性介質或細胞因子產生過多, 進而可以導致機體出現MODS, 而其中急性腎損傷(AKI)是最為常見的臟器功能障礙[1]。目前普遍認為MODS是SIRS惡化進展的結果, 也是導致危重癥患者不良預后和死亡的主要原因。目前研究已經證實, 及時、有效地減輕機體的炎癥反應, 清除過多的炎癥因子和積極的臟器功能保護是成功救治危重病患者的關鍵環節[2]。其中連續腎臟替代治療一方面可以降低炎癥瀑布反應和減輕組織繼發損傷, 另一方面可以調節炎癥/
抗炎和免疫系統的平衡, 已在臨床上廣泛應用于MODS患者的治療[3]。近年來, 研究發現SLED可以使用普通透析機來進行, 且其在血流動力學穩定性方面優于間歇性血液透析(IHD), 而炎癥介質清除能力則與CRRT相當, 也越來越多地被應用于MODS患者的治療[4]。HP則可以更加有效清除超過CRRT和SLED分子量限制的大分子物質, 如各種內毒素和炎癥因子等, 因此, 在理論上HP聯合CRRT或SLED應該具有較高的炎癥介質清除能力, 可以改善MODS患者的臨床療效[5]。本研究對比了SLED、SLED聯合HP、CRRT、CRRT聯合HP 4種不同的血液凈化方案在治療MODS患者中的療效, 現報告如下。
1 資料與方法
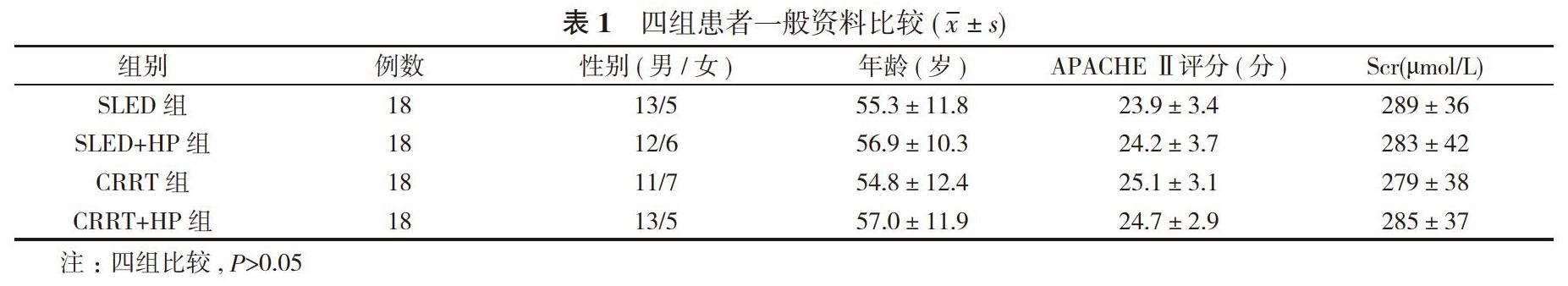
1. 1 一般資料 選擇2017年6月~2019年6月期間在本院住院的危重病患者共72例, 所有患者符合2005年由Goldstein等[6]提出的MODS診斷標準, 患者治療前的APACHEⅡ評分>12分。研究排除合并惡性腫瘤、終末期腎病、腎移植后、妊娠、活動性出血、免疫缺陷性疾病或APACHEⅡ評分>30分的患者。72例患者中男49例, 女23例;年齡36~78歲, 平均年齡(55.4±12.4)歲。其中原發病:重癥肺炎43例, 重癥急性胰腺炎13例, 腹腔感染16例。所有入組患者和(或)家屬同意并簽署研究知情同意書。本研究獲得了本院倫理委員會的批準。將患者按照所采用的血液凈化方法的不同分為SLED組、SLED+HP組、CRRT組、CRRT+HP組, 每組18例。四組患者入院時性別、年齡、APACHEⅡ評分、腎功能等一般資料比較, 差異無統計學意義(P>0.05), 具有可比性。見表1。
1. 2 方法 所有患者首先積極治療原發疾病, 并根據病情給予吸氧、機械通氣、液體復蘇、抗感染、改善微循環、營養支持、糾正酸堿及電解質紊亂等綜合治療。所有入組患者無論是否存在急性腎功能損傷均接受血液凈化治療。血液凈化方法:所有患者采用 Seldingers法將雙腔導管置入股靜脈或頸靜脈建立血管通路。SLED組采用BDD-27血液透析機[威高日機裝(威海)透析機器有限公司]和Hemoflow F6HPS過濾器(德國費森尤斯集團)治療, 透析液流速300 ml/min,
血流量150~180 ml/min, 治療時間12 h/d。SLED+HP 組則先將珠海健帆HA130血液灌流器(健帆生物科技集團股份有限公司)串聯于透析器之前, HP 2 h后取下灌流器, 然后繼續行SLED治療, 總治療時間12 h/d。CRRT組使用多功能血液凈化機Diapact CRRT(B.Braun Medical Inc)和xevonta Hi 18血液過濾器(B.Braun Medical Inc), 血流量150~180 ml/min, 置換液流量30~35 ml/(kg·h), 置換液配制方案:生理鹽水3000 ml+注射用水800 ml+5%葡萄糖注射液150 ml+10%葡萄糖酸鈣注射液30 ml+25%硫酸鎂注射液3.5 ml, 根據患者血鉀情況加入適量的10%氯化鉀注射液, 根據患者有無出血傾向選擇無肝素或低分子量肝素抗凝, 治療時間12 h/d。CRRT+HP組則在此基礎上將珠海健帆HA130血液灌流器串聯于透析器之前, HP 2 h后取下灌流器繼續行CRRT治療, 總治療時間12 h/d。
1. 3 觀察指標 四組患者在治療前和治療后第7天均進行APACHEⅡ評分, 并測定Scr、hs-CRP、IL-6、IL-10、TNF-α水平, 統計四組患者治療后28 d存活率。
1. 4 統計學方法 采用SPSS22.0統計學軟件處理數據。計量資料以均數±標準差( x-±s)表示, 采用t檢驗;計數資料以率(%)表示, 采用χ2檢驗。P<0.05表示差異有統計學意義。
2 結果
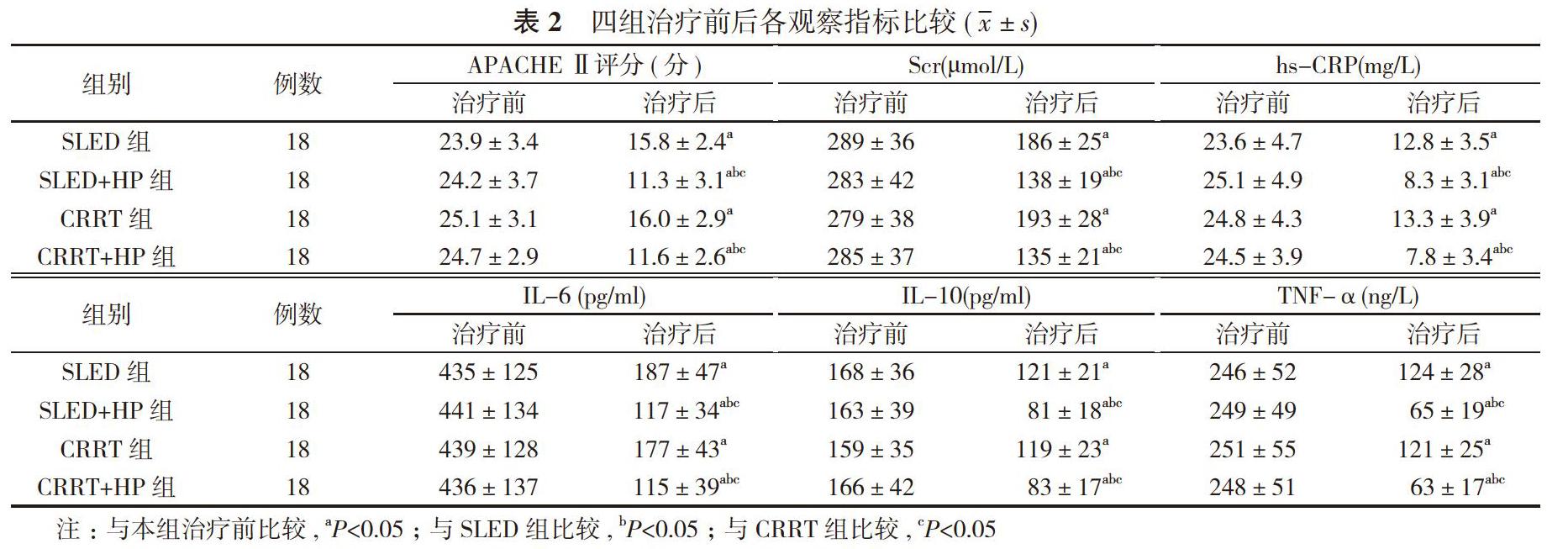
2. 1 四組治療前后各觀察指標比較 治療前, 四組患者APACHEⅡ評分、Scr、hs-CRP、IL-6、IL-10、TNF-α水平比較, 差異無統計學意義(P>0.05)。治療后, 四組患者的APACHEⅡ評分、Scr、hs-CRP、IL-6、IL-10、TNF-α水平均顯著降低, 差異有統計學意義(P<0.05)。SLED+HP組的APACHEⅡ評分、Scr、hs-CRP、IL-6、IL-10、TNF-α水平降低大于SLED組, CRRT+HP組的APACHEⅡ評分、Scr、hs-CRP、IL-6、IL-10、TNF-α水平降低大于CRRT組, 差異均有統計學意義(P<0.05)。SLED+HP組和CRRT+HP組、SLED組和CRRT組比較差異無統計學意義(P>0.05)。見表2。
2. 2 四組患者28 d存活率比較 SLED+HP組的28 d存活率為88.9%, CRRT+HP組的28 d存活率為83.3%, 均高于SLED組的55.6%與CRRT組的50.0%, 差異有統計學意義(P<0.05)。SLED+HP組與CRRT+HP組、SLED組與CRRT組患者的28 d存活率比較, 差異無統計學意義(P>0.05)。見表3。
3 討論
MODS在危重癥患者中很常見, 研究表明其發病率可高達57%。可以導致MODS的疾病和因素有很多, 包括膿毒癥、嚴重外傷、重癥胰腺炎等, 其中各種嚴重感染導致的膿毒癥仍然是其主要原因。在膿毒癥早期, 機體出現廣泛的炎性反應, 伴隨大量炎癥介質和細胞因子的釋放, 最常見的有IL-1、IL-6、IL-10和TNF-α等, 從而可導致血流動力學不穩定、膿毒癥休克和MODS。研究表明, SIRS及MODS發生發展過程中產生的各種促炎及抗炎介質多為水溶性, 且主要是大分子物質, 故血液凈化治療可以清除大多數的炎癥介質, 從而減輕SIRS, 對阻止和減輕MODS的發生發展及改善患者的預后起至關重要的作用[7]。此外, AKI也是MODS患者常見的臟器功能障礙, 而血液凈化治療不僅可以清除炎癥介質, 而且同時可以進行腎臟替代治療, 因此成為了MODS的常規治療方法而被廣泛應用于臨床。
在不同的血液凈化方法中, CRRT因具有血流動力學穩定、患者耐受性好、超濾及清除率高等特點, 應用最為廣泛。但CRRT同時也具有不少的缺點, 包括持續抗凝導致臟器出血風險的增加、需要特殊的機器及專業的護理人員、治療費用高等多方面問題, 較難在基層醫院以及經濟欠發達地區進行推廣應用[3]。SLED是近年來被越來越多采用的一種新的血液凈化方法, 其可以使用普通透析機, 采用低血流速度和低透析液流量, 將透析時間延長到6~12 h/d, 使其可以在血流動力學干擾較小的情況下緩慢逐步清除各種毒素、炎癥介質等。目前的多數研究顯示SLED在血流動力學的穩定性和溶質清除率方面不差于CRRT, 但明顯優于IHD[4, 8]。Abhijat等[4]和 Shakti等[9]的研究均證實SLED用于MODS的治療, 可以達到與CRRT相類似的效果。程駿章等[10]比較了SLED與CRRT在危重癥患者治療中的
療效, 認為SLED具有CRRT相似的血流動力學穩定性, 且兩者在危重癥患者中的治療效果相當。本研究結果也顯示SLED與CRRT在降低MODS患者的炎癥因子水平方面無明顯差異, 兩種方法的28 d的存活率的比較也沒有統計學差異。
CRRT或SLED等血液凈化方法可在一定程度上清除MODS患者體內的補體(如C3a、C5a等)、細胞因子(如TNF-α、IL-1、IL-6、IL-10等)、心肌抑制因子和血小板活化因子等炎癥介質, 從而改善患者的臨床癥狀和體征, 對MODS的治療起到了積極的作用。但這兩種血液凈化方法均對包括多種細胞因子在內的中大分子物質的清除能力有限。HP是一種新型血液凈化技術, 采用樹脂等特殊的吸附材料, 通過吸附作用來清除患者血液中的高分子量內毒素、細胞因子等, 能夠顯著降低血液內各種炎癥介質的水平, 從而大大降低機體內的炎癥級聯反應, 改善患者的預后[11]。因此, SLED聯合HP技術, 通過兩者的互補和疊加作用, 有可能實現對MODS患者體內的各種有害的內毒素和炎癥介質等進行更有效的清除, 調節患者機體內免疫平衡, 有利于阻斷MODS的發生進展, 達到改善患者預后的最終目的。
本次研究中發現, 無論是CRRT還是SLED, 在聯合HP后患者在治療第7 天的各種炎癥介質的水平均較單純的CRRT和SLED治療明顯下降, 差異有統計學意義(P<0.05), 提示聯合HP治療確實能降低細胞因子水平, 而SLED聯合HP和CRRT聯合HP兩種治療方案之間的比較則無明顯差異。同時研究發現, 臨床危重程度評分方面, 治療第7后CRRT+HP組和SLED+HP組患者的APACHEⅡ評分均低于另外兩組, 差異有統計學意義(P<0.05)。同樣, 聯合了HP治療的兩組患者的28 d存活率較高, 差異有統計學意義(P<0.05), 而SLED+HP組和CRRT+HP對比則無明顯差異。
綜上所述, SLED技術同時具備IHD和CRRT兩者的優點, 具有溶質清除率高、血液動力學穩定、無需特殊機器、費用低、易操作、易推廣等特點。SLED聯合HP后具有更強的清除炎癥因子能力和腎功能保護作用, 最終能改善患者的預后, 治療效果與CRRT聯合HP相當, 可以作為一種新的MODS治療方案。但本研究樣本量較少, SLED聯合HP治療MODS的療效仍需更多的多中心、隨機研究來進一步證實。
參考文獻
[1] Mizock BA. The multiple organ dysfunction syndrome. Dis Mon, 2009, 55(8):476-526.
[2] Scott W, Sheri S, Crow MD, et al. Epidemiology and outcomes of pediatric multiple organ dysfunction syndrome (MODS). Pediatr Crit Care Med, 2017, 18(3 Suppl 1):4-16.
[3] Tian H, Zeng R, Wang X, et al. The Effects of Continuous Blood Purification for SIRS/MODS Patients: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. ISRN Hematol, 2012(2012):986795.
[4] Abhijat K, Neill A, Karen E, et al. Outcomes of sustained low efficiency dialysis versus continuous renal replacement therapy in critically ill adults with acute kidney injury: a cohort study. BMC Nephrol, 2015(16):127.
[5] 黃盛玲, 黃德緒, 閆冰, 等. 血液灌流技術臨床應用研究進展. 內科, 2016, 11(5):721, 719-759.
[6] Goldstein B, Giroir B, Randolph A. International pediatric sepsis consensus conference: definitions for sepsis and organ dysfunction in pediatrics. Pediatr Crit Care Med, 2005(6):2-8.
[7] Li L, Pan J, Yu Y. Development of sorbent therapy for multiple organ dysfuntion syndrome (MODS). Biomed Mater, 2007, 2(2):12-16.
[8] Prasad N, Poddar B, Gurjar M, et al. A pilot randomized controlled trial of comparison between extended daily hemodialysis and continuous veno-venous hemodialysis in patients of acute kidney injury with septic shock. Indian Journal of Critical Care Medicine, 2017, 21(5):262-267.
[9] Shakti BM, Ratender KS, Arvind KB, et al. Sustained low-efficiency dialysis in septic shock: Hemodynamic tolerability and efficacy. Indian J Crit Care Med, 2016, 20(12):701-707.
[10] 程駿章, 胡守亮, 盧宏柱, 等. 持續低效血液透析與連續性血液凈化在危重癥患者治療中的效果. 中華急診醫學雜志, 2012, 21(8):874-877.
[11] Lu L, Yong Z, Xiao L, et al. Blood hemoperfusion with resin adsorption combined continuous veno-venous hemofiltration for patients with multiple organ dysfunction syndrome. World J Emerg Med, 2012, 3(1):44-48.
[收稿日期:2019-12-09]

