新補骨脂異黃酮在大鼠體內的藥動學及組織分布研究
張志超,王小康,潘遠安,劉江紅
(深圳市龍華區中心醫院藥學部,廣東 深圳 518110)
新補骨脂異黃酮是補骨脂Psoralea corylifolialL.中常見的黃酮類化合物[1],有著抗氧化[2-3]、抗菌[3]、抗炎[4]、神經保護[5]、抗骨質疏松[6-7]、抗前列腺癌[8]等作用。課題組前期發現,補骨脂對大鼠具有很強的肝毒性和腎毒性,與文獻[9-10]報道一致,故研究該藥材所含新補骨脂異黃酮的體內藥動學及組織分布時,有助于了解其體內代謝途徑、組織蓄積情況、藥理活性、毒性機制。
目前,對新補骨脂異黃酮的研究主要集中在大鼠給予補骨脂后它在血漿中的藥動學和腦組織中的組織分布[11-13],尚無單獨給予該成分后的相關報道。因此,本實驗在前期報道基礎上,建立超高效液相色譜串聯三重四級桿質譜(UPLC-MS/MS)法測定大鼠血清及各組織中新補骨脂異黃酮含有量,并研究該成分體內藥動學和組織分布,為后期相關體內作用機制考察提供依據。
1 材料
1.1 儀器 Waters ACQUITYTMH-class 型超高效液相色譜儀、Waters SYNAPTTMG2 TQD 型三重四極桿串聯質譜儀、MasslynxTM4.1 數據處理系統(美國Waters 公司);Milli-Q 型超純水系統(美國Millipore 公司);QL-861 型微型旋渦混合儀(江蘇省海門市其林貝爾儀器制造有限公司);BP211D 型電子天平(德國賽多利斯公司);KQ3200E 型超聲波清洗器(昆山市超聲儀器有限公司);Anke TGL-16G-A 型高速離心機(上海安亭科學儀器廠);UV-1800 型紫外分光光度計(日本島津公司);DKZ-450B 型電熱恒溫振蕩水槽(上海森信實驗儀器有限公司);MTN-2800D 型氮氣吹干儀(天津奧特賽恩斯儀器有限公司)。
1.2 試劑與藥物 新補骨脂異黃酮對照品(純度≥99%,批號SH-YY0908)購自上海一研生物科技有限公司;芒柄花黃素對照品(純度≥98%,批號JD-65914)購自上海晶都生物技術有限公司。甲醇、乙腈、甲酸、水均為色譜純;其余試劑均為國產分析純。
1.3 動物 SPF 級SD 大鼠,雌雄各半,由廣東省醫學實驗動物中心提供,動物生產許可證號SCXK(粵)-2018-0002,飼養于恒溫[(25±2)℃]、恒濕[相對濕度(55±10)%]動物室,每天12 h亮/暗交替,自由飲水進食。
2 方法
2.1 溶液制備
2.1.1 對照品溶液 精密稱取新補骨脂異黃酮對照品適量,置于10 mL 棕色量瓶中,甲醇溶解并稀釋至刻度,搖勻,配制成25.0 mg/mL 貯備液,甲醇再進一步稀釋,即得(質量濃度分別為5.0、50.0、250.0、500.0 μg/mL),現配現用。
2.1.2 內標溶液 精密稱取芒柄花黃素對照品適量,甲醇配制成50 μg/mL 貯備液,再用甲醇進一步稀釋,即得(質量濃度為500 ng/mL),現配現用。
2.1.3 含藥生理鹽水 取適量新補骨脂異黃酮對照品,加適量生理鹽水超聲處理至溶解,即得(質量濃度為50 mg/mL),現配現用。
2.2 UPLC-MS/MS 分析
2.2.1 色譜條件 Waters ACQUITYTMBEH C18色譜柱(2.1 mm×100 mm,1.7 μm);流動相水(含0.1%甲酸)(A)-乙腈(含0.1%甲酸)(B),梯度洗脫(0~9.0 min,2%~36%B;9.0~10.5 min,36%~48% B;10.5~12.5 min,48%~80% B;12.5~13.5 min,80%~100% B;13.5~14.0 min,100%B;14.0~15.0 min,100%~2% B;15.0~16.0 min,2% B);體積流量0.4 mL/min;柱溫40 ℃;進樣量5 μL。
2.2.2 質譜條件 離子源ESI(正離子),毛細管電壓3.3 kV;離子源溫度150 ℃;脫溶劑氣溫度350 ℃;脫溶劑氣、錐孔反吹氣氮氣,體積流量800、50 L/h;掃描方式多反應監測(MRM);新補骨脂異黃酮檢測離子m/z323.4~267.2,錐孔電壓48 eV,碰撞能量20 eV;內標(芒柄花黃素)檢測離子m/z269.1~253.1,碎裂電壓50 eV,碰撞能量30 eV。
2.3 樣本前處理 取組織樣本1 g,加入3 mL 0.9%NaCl 溶液進行勻漿。取血清或組織勻漿樣品100 μL,加入100 μL 500 ng/mL 內標(芒柄花黃素)溶液,充分混勻后加入300 μL 沉淀劑(乙腈)渦旋1 min,10 000 r/min 離心5 min,取上清液,氮氣吹干,殘渣用60%甲醇復溶,進行UPLCMS/MS 分析。
2.4 大鼠藥動學、組織分布研究 取18 只SD 大鼠,隨機分為3 組,每組6 只,實驗前禁食12 h,并從頸外靜脈抽取空白血液。3 組大鼠分別口服50、100、200 mg/kg 含藥生理鹽水后,于0.5、1、2、4、6、8、10、24、48 h 采集血液,置于EP 管中,室溫下放置2 h 后10 000 r/min 離心10 min,吸取上層血清,于-80 ℃下保存。另取24 只SD 大鼠,隨機分為4 組,每組6 只,隨機選取1 組作為空白組,其余3 組口服100 mg/kg 含藥生理鹽水,分別于0.5、2、8 h 后腹腔注射水合氯醛麻醉,立即處死,取腎臟、肝臟、小腸,0.9%NaCl 溶液洗滌至無血色,濾紙吸干,置于EP 管中,液氮速凍15 min,于-80 ℃下保存。
2.5 數據處理 通過Winnonlin 6.3 軟件進行分析,采用非房室模型計算主要藥動學參數,其中tmax、t1/2、MRT0~t等參數經SPSS 軟件進行組間統計學檢驗。P<0.05 表示差異具有統計學意義。
3 結果
3.1 專屬性考察 取空白血清和組織、空白血清和組織+新補骨脂異黃酮或內標(芒柄花黃素)、給藥0.5 h 后血清和組織,按“2.3”項下方法處理,在“2.2”項條件下進樣測定,結果見圖1~2。由此可知,新補骨脂異黃酮、內標色譜峰的峰形良好,內源性物質不干擾測定。

圖1 大鼠血清和組織中新補骨脂異黃酮MRM 色譜圖Fig.1 MRM chromatograms of neobavaisoflavone in rat serum and tissues
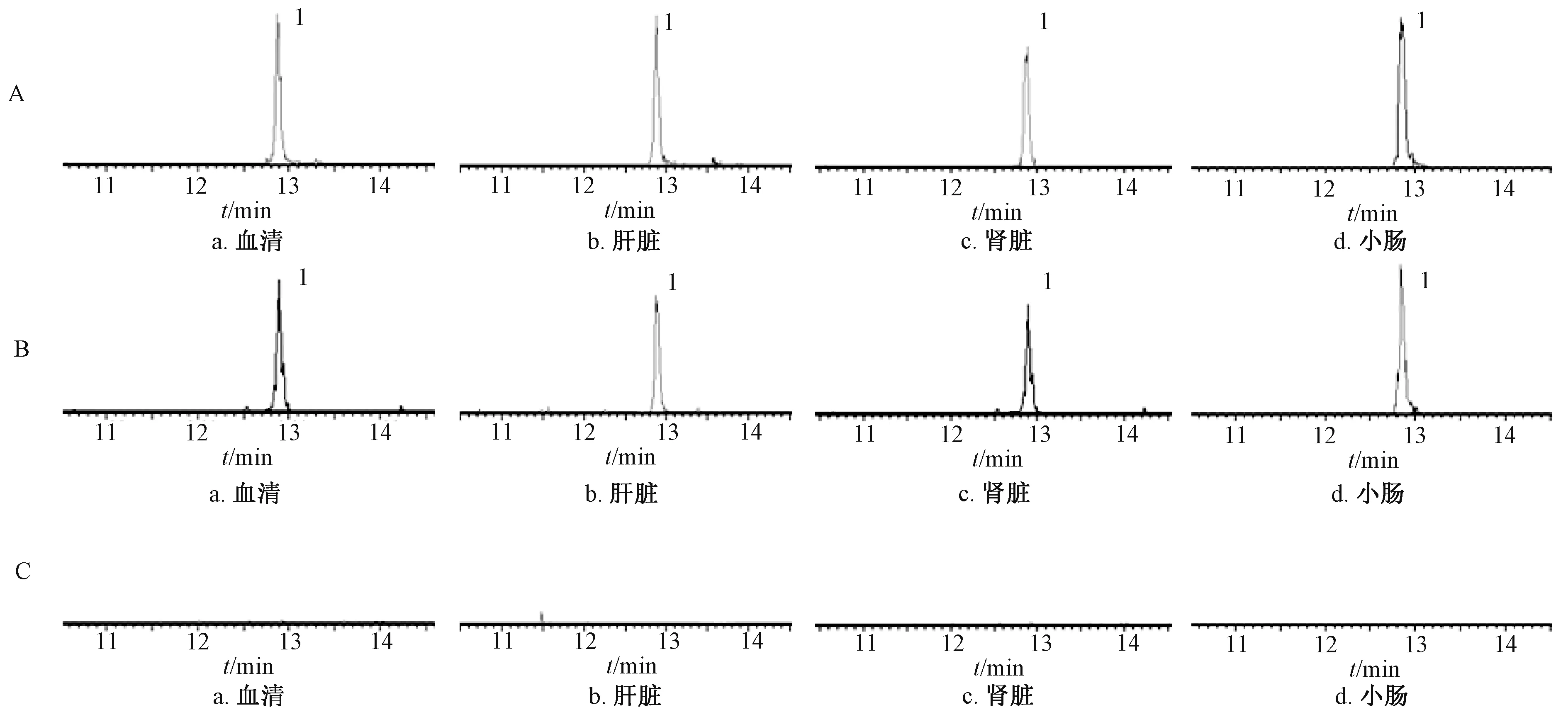
圖2 大鼠血清和組織中內標(芒柄花黃素)MRM 色譜圖Fig.2 MRM chromatograms of internal standard(formononetin)in rat serum and tissues
3.2 線性關系考察 取適量空白血清或空白組織勻漿液,加入“2.1.1”項下對照品溶液,制成含4.0、10.0、20.0、50.0、100.0、300.0、700.0 ng/mL新補骨脂異黃酮的相應樣品溶液,按“2.3”項下方法處理(除了不加60%甲醇外),在“2.2”項條件下進樣測定。以新補骨脂異黃酮質量濃度為橫坐標(X),新補骨脂異黃酮與內標峰面積比值乘以內標溶液質量濃度的響應值為縱坐標(Y)進行回歸,并以信噪比(S/N)=10 為定量限,結果見表1,可知新補骨脂異黃酮在一定范圍內線性關系良好,方法靈敏度較高,可用于微量分析。
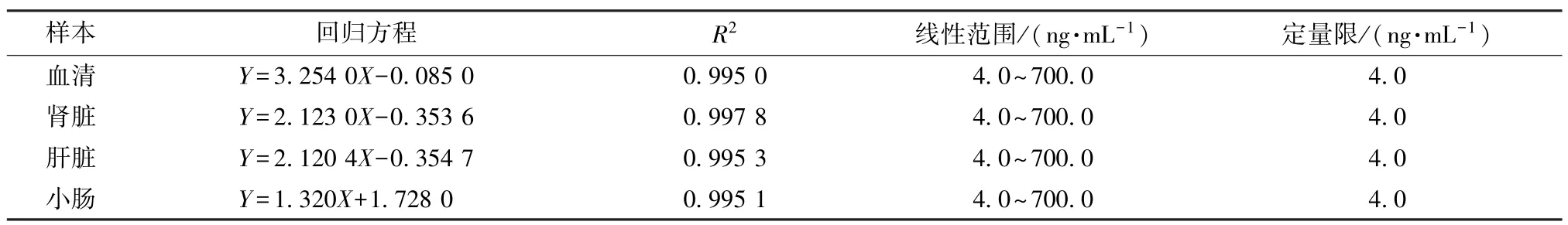
表1 大鼠血清和組織中新補骨脂異黃酮線性關系Tab.1 Linear relationships of neobavaisoflavone in rat serum and tissues
3.3 基質效應、提取回收率試驗 取5 只SD 大鼠空白血清、空白組織勻漿液各100 μL,按“2.3”項下方法處理(除了用甲醇代替內標溶液外),殘渣用“2.1.1”項下12.5、25.0、450 ng/mL 對照品溶液各100 μL 溶解,平行5 份,氮氣吹干后60%甲醇復溶,在“2.2”項條件下進樣測定,得到峰面積A1;取相應質量濃度對照品溶液于EP 管中,加空白血清、空白組織勻漿液混勻,按“2.3”項下方法處理,平行5 份,在“2.2”項條件下進樣測定,得到峰面積A2;取相應質量濃度的對照品溶液于EP 管中,氮氣吹干后殘渣用100 μL 純水復溶,按“2.3”項下方法處理,在“2.2”項條件下進樣測定,得到峰面積A3,以A1與A3的比值為基質效應,A2與A1的比值為提取回收率,結果見表2,可知該方法基質效應、提取回收率良好,符合生物樣品檢測要求。
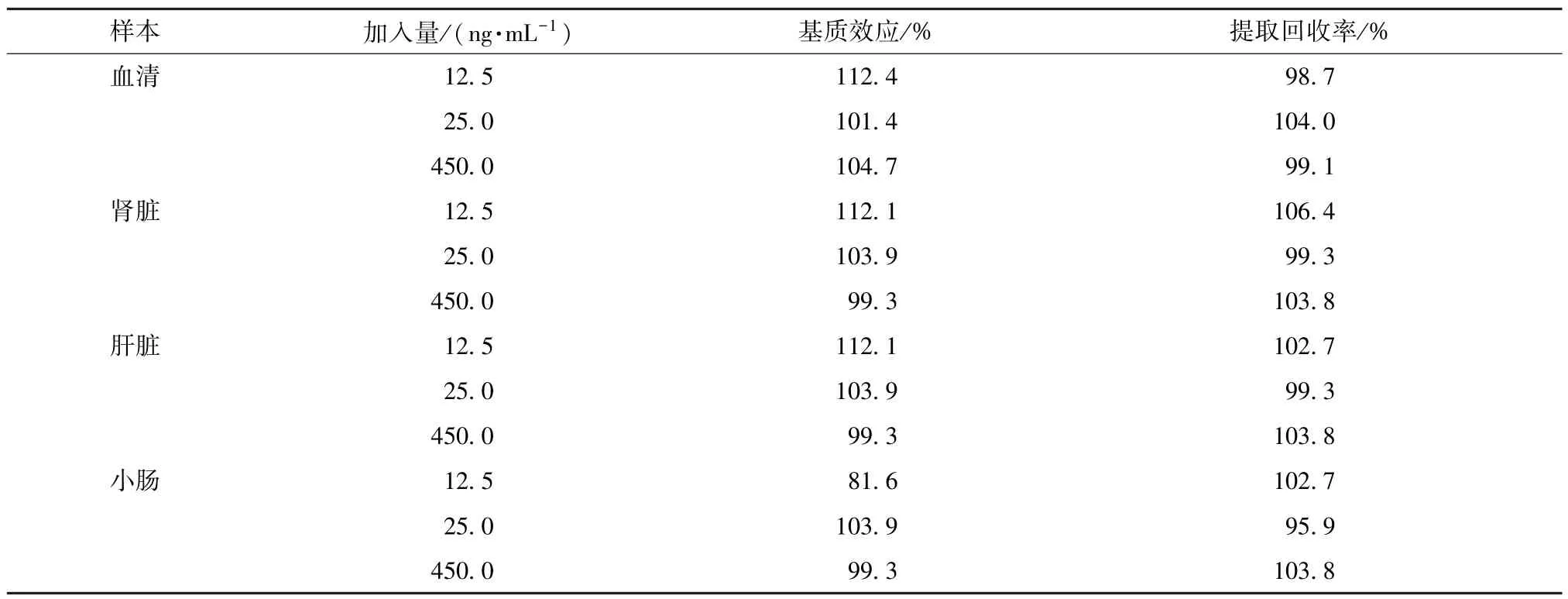
表2 大鼠血清和組織中新補骨脂異黃酮基質效應、提取回收率試驗結果(n=5)Tab.2 Results of matrix effect and extraction recovery tests for neobavaisoflavone in rat serum and tissues(n=5)
3.4 準確度、精密度試驗 空白血清、空白組織勻漿液制成12.5、25.0、450.0 ng/mL 樣品溶液,按“2.3”項下方法處理,平行6 份,在“2.2”項條件下進樣測定5 d,結果見表3,可知該方法準確度、精密度良好,符合生物樣品檢測要求。
3.5 穩定性試驗 空白血清、空白組織勻漿液制成12.5、450.0 ng/mL 樣品溶液,按“2.3”項下方法處理,平行3 份,在“2.2”項條件下進樣測定,分別考察經3 次冷凍-解凍循環、前處理后放置24 h、-80 ℃放置3 個月后的穩定性,結果見表4,可知該方法穩定性良好,符合生物樣品檢測要求。
3.6 藥動學研究 大鼠口服給藥后繪制血藥濃度-時間曲線,再經非室模型統計矩計算主要藥動學參數,見表5、圖3。由此可知,100、200 mg/kg 新補骨脂異黃酮t1/2、tmax、Cmax、AUC0~t、AUC0~∞、MRT0~t、MRT0~∞高于50 mg/kg(P<0.05),以200 mg/kg 更明顯(P<0.05)。
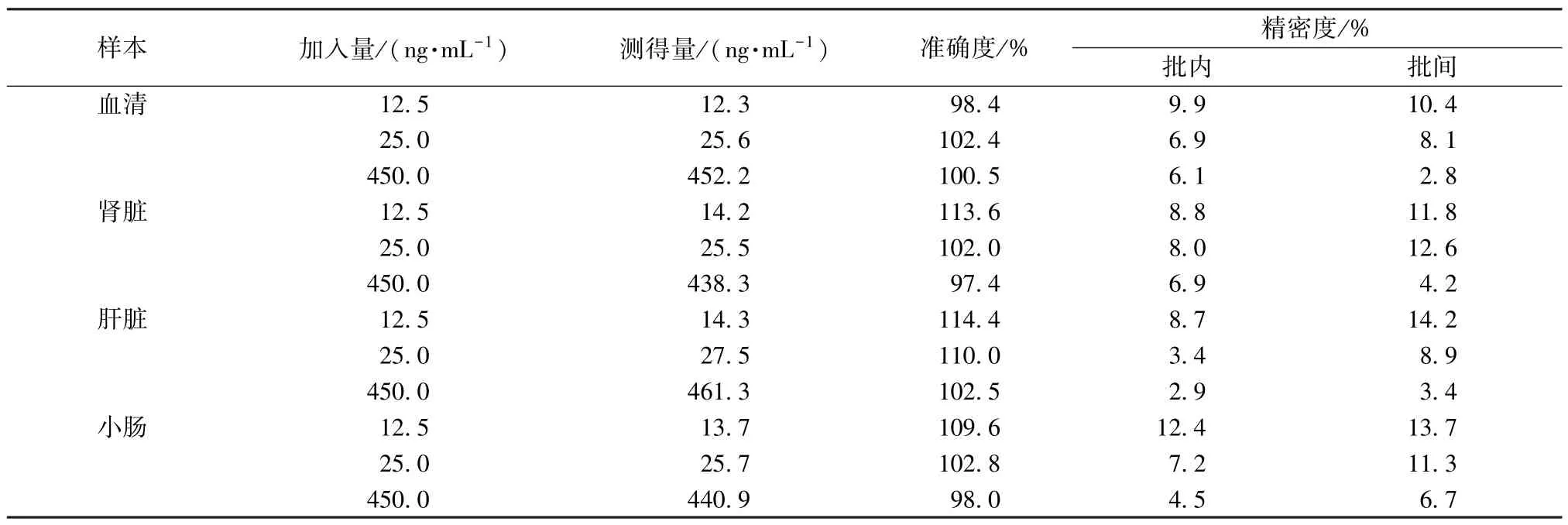
表3 大鼠血清和組織中新補骨脂異黃酮準確度、精密度試驗結果(n=5)Tab.3 Results of accuracy and precision tests for neobavaisoflavone in rat serum and tissues(n=5)
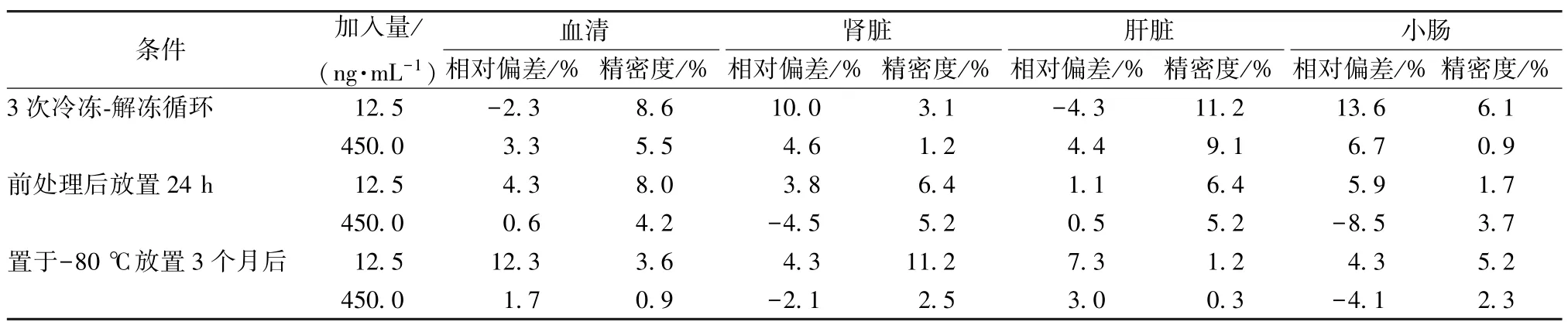
表4 大鼠血清和組織中新補骨脂異黃酮穩定性試驗結果(n=3)Tab.4 Results of stability tests for neobavaisoflavone in rat serum and tissues(n=3)
表5 新補骨脂異黃酮主要藥動學參數(±s,n=6)Tab.5 Main pharmacokinetic parameters for neobavaisoflavone(±s,n=6)
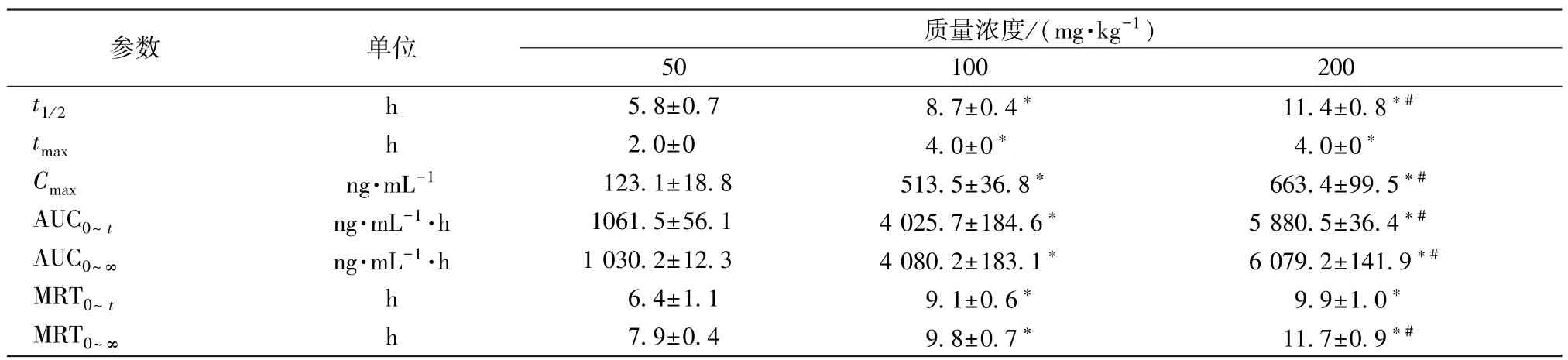
表5 新補骨脂異黃酮主要藥動學參數(±s,n=6)Tab.5 Main pharmacokinetic parameters for neobavaisoflavone(±s,n=6)
注:與50 mg/kg 比較,?P<0.05;與100 mg/kg 比較,#P<0.05。
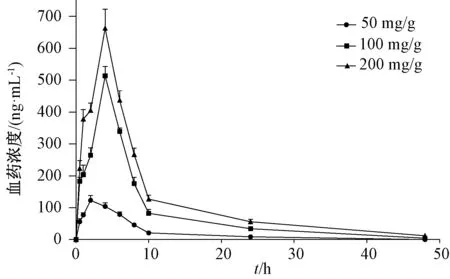
圖3 不同質量濃度新補骨脂異黃酮血藥濃度-時間曲線Fig.3 Plasma concentration-time curves for different concentrations of neobavaisoflavone
3.7 組織分布研究 大鼠口服給予新補骨脂異黃酮后,測定該成分在0.5、2、8 h 的組織分布,結果見圖4。由此可知,不同時間點各組織中新補骨脂異黃酮含有量依次為腎>肝>小腸。
4 討論
本實驗采用UPLC-MS/MS 法,在16 min 內對新補骨脂異黃酮進行定量分析,具有快速靈敏、選擇性好、專屬性強的優點,可為研究該成分藥動學及組織分布提供依據,也有利于闡明其作用機制。課題組前期采用文獻[11]報道的LC-MS/MS 法測定血漿中新補骨脂異黃酮含有量,發現其流動相組成與本實驗基本相同,均為乙腈-水等度洗脫,但該方法在檢測組織樣本時基線高,目標化合物響應低,故又在流動相中加入0.1%甲酸,可顯著改善峰形,降低基線,提高響應值。
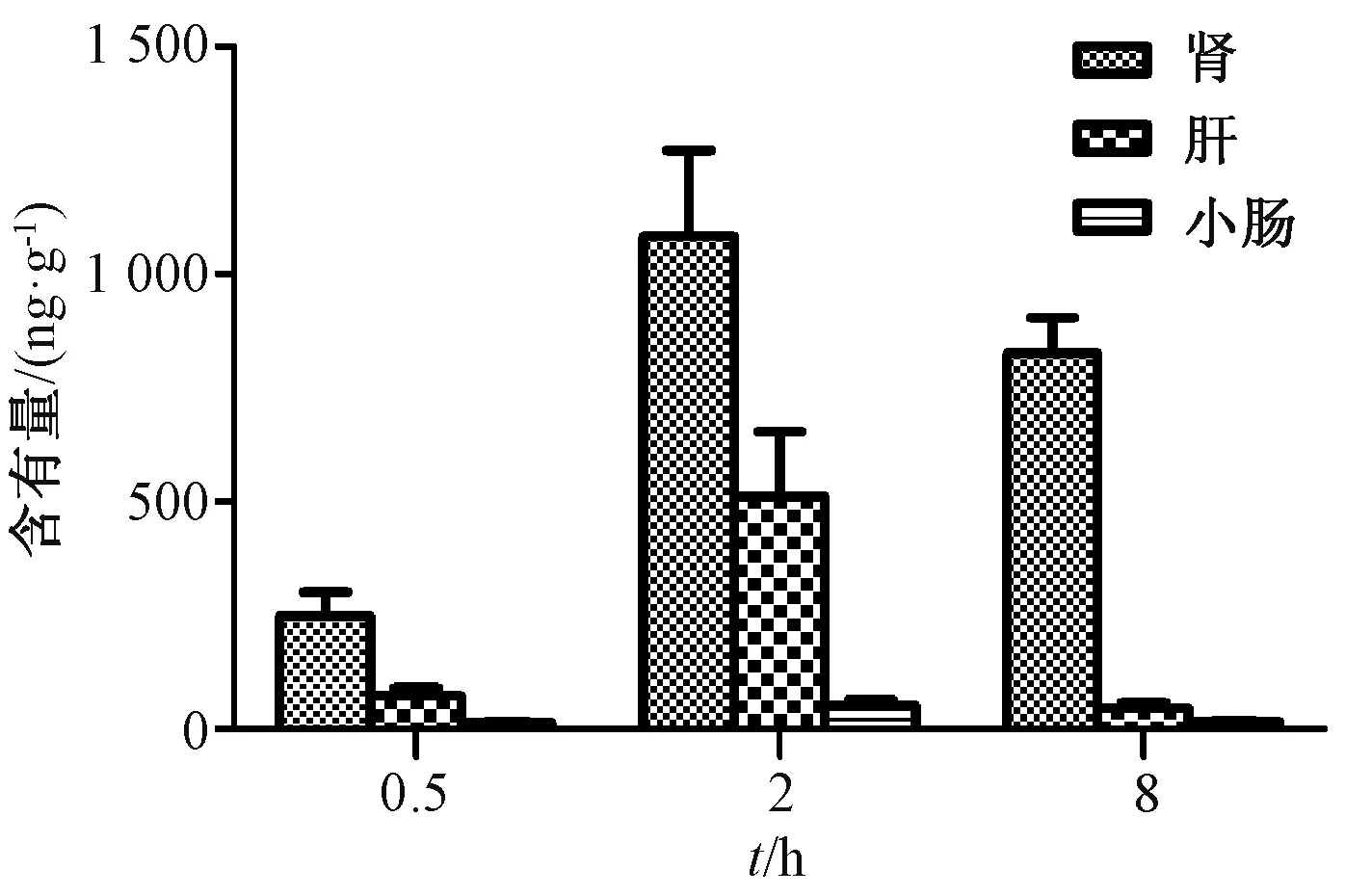
圖4 大鼠組織中新補骨脂異黃酮含有量Fig.4 Neobavaisoflavone contents in rat tissues
結果顯示,大鼠給予50 mg/kg 新補骨脂異黃酮后的藥動學參數與給予100、200 mg/kg 比較具有顯著差異,表明該成分在大鼠體內的吸收、分布、消除存在一定劑量依賴性,但不同劑量之間基本呈非線性關系。本實驗選擇中間劑量100 mg/kg,并以吸收相、分布相、消除相各1 個時間點為組織分布取樣時間點,發現大鼠給藥后新補骨脂異黃酮含有量在腎、肝中較高,維持時間較長,即在這2個部位存在藥物蓄積現象,可能與補骨脂對大鼠具有肝毒性和腎毒性有關[14-15]。前期預實驗發現,在大鼠心、腦、肌肉中未檢測到新補骨脂異黃酮,推測該成分可能對組織分布具有一定的靶向性,需要作進一步研究。

