一種胰蛋白酶親和材料的制備及應用
高柳芳,李晨*
山西大學生命科學學院(太原 030006)
胰蛋白酶是一種絲氨酸蛋白水解酶,分子質量在20~30 kDa范圍內,專一水解堿性氨基酸如精氨酸及賴氨酸羧基形成的肽鍵,不僅能夠消化普通蛋白質,還可以激活胰臟中的其它蛋白酶原,如胰凝乳蛋白酶原、羧肽酶原、彈性蛋白酶原、磷脂酶原等[1]。作為一種非常重要的專一性消化酶,胰蛋白酶被廣泛應用于食品、醫藥、畜牧和現代生物技術等領域[2-4]。食品加工中作為酶制劑主要用于焙烤[5]、肉類嫩化和組織蛋白的水解[6]等。臨床上常用于治療膿胸、血胸、外科炎癥、潰瘍、創傷性損傷、瘺管等產生的局部水腫、血腫及膿腫等,還可用于治療毒蛇咬傷[7]。生物技術領域中主要用于蛋白質的氨基酸序列分析及動物細胞培養前對組織的消化處理等[8]。胰蛋白酶的應用日益廣泛,對其制備方法的研究也成為當前的一個熱點。目前,常用的蛋白酶分離純化方法有硫酸銨沉淀法、有機溶劑分級、離子交換層析、凝膠過濾等。然而這些方法的特異性比較低,通常需要綜合多種方法才能達到純化的目的,存在操作繁瑣、時間較長等一系列問題,而且由于操作時間長,還可能對酶活性造成不同程度的破壞[9-10]。因此,建立一種簡便、快速、高效分離純化胰蛋白酶的方法顯得尤為重要。
親和層析是利用生物大分子的生物學特異性(如酶與酶抑制劑),即生物分子間所具有的專一性親和力而設計的層析技術。與其他純化方法相比,親和層析具有高效、迅速的優點,有時僅一步即可達到純化的目的。將酶抑制劑固定化做成親和層析材料特異吸附純化對應的酶是一種有效可行的方法[11]。然而,親和層析配體需滿足非特異性吸附低、純度高、親和作用力強、穩定性好等特點,尋找合適的抑制劑是制備酶親和材料的首要關鍵問題。蕎麥胰蛋白酶抑制劑(Buckwheat trypsin inhibitor,BTI)是從蕎麥種子中提取出的一種胰蛋白酶的競爭型抑制劑。課題組通過基因工程技術獲得了重組BTI,對其活性位點、空間結構及理化性質已進行了詳盡研究。BTI由69個氨基酸組成,分子質量為7.9 kDa,具有很高的耐熱性及酸堿穩定性,100℃處理60 min對胰蛋白酶的抑制作用仍可保留在80%以上[12-14]。BTI良好的穩定性及對胰蛋白酶較強的抑制作用適于固定化反應,能夠用于制備親和層析介質。
試驗選用溴化氰活化的瓊脂糖凝膠作為載體,將其與配基BTI偶聯制備成親和層析吸附劑,并進一步研究BTI親和層析介質用于純化胰蛋白酶的作用條件,實現一步層析得到高純度胰蛋白酶的目的,為今后大規模制備胰蛋白酶及開發新型胰蛋白酶提供重要的理論依據。
1 材料與方法
1.1 材料、儀器與設備
胰蛋白酶、C N B r 活化瓊脂糖凝膠(C N B r- Sepharose CL-4B)購于生工生物工程(上海)股份有限公司;牛血清白蛋白、考馬斯亮藍R-250購于北京索萊寶科技有限公司;苯甲酰-DL-精氨酰-對硝基苯氨(BApNA)為美國Sigma產品,其余試劑為分析純。
恒溫水浴鍋,北京市長風儀器儀表公司;蛋白質純化系統,美國BIO-RAD公司;TU-1810紫外分光光度計,上海美鋪達儀器有限公司;HC-2518R高速冷凍離心機,安徽中科中佳科學儀器有限公司;BSA224S精密電子天平,德國Sartorius公司;PB-10精密pH計,德國Sartorius公司;恒溫振蕩培養箱,上海博訊實業有限公司;電泳儀,北京六一生物科技有限公司。
1.2 試驗方法
1.2.1 重組蛋白BTI的制備
向液體LB培養基(含50 μg/mL Kan和100 μg/mL Kan)中接入含有pQE30-BTI的E.coliBL21(DE3)菌種,于37℃,180 r/min振蕩培養至對數生長期,加入誘導劑IPTG(終濃度為0.5 mmol/L),繼續振蕩培養4 h,以8 000 r/min離心收集菌體。用Tris-HCl緩沖液(20 mmol/L,pH 7.3)將菌體洗滌三次,用相同Tris-HCl緩沖液將菌體重懸,在冰浴條件下超聲破碎,直至菌體懸浮液由黏稠變為透亮。將破碎的菌液在80℃加熱30 min,然后以12 000 r/min離心10 min,取上清,即得BTI粗蛋白。
重組蛋白BTI帶有6×His標簽,采用親和層析法純化,在蛋白純化系統(美國BIO-RAD)上進行,檢測280 nm處吸光度,流速控制為1 mL/min。用緩沖液(20 mmol/L Tris-HCl,500 mmol/L NaCl,20 mmol/L咪唑,pH 7.5)平衡Ni2+-NTA親和層析柱,將表達的菌體粗蛋白用0.22 μm濾膜過濾后上樣于親和層析柱,用平衡緩沖液充分洗去未結合蛋白后,分別用咪唑濃度為80和300 mmol/L的緩沖液(均含20 mmol/L Tris-HCl,500 mmol/L NaCl,pH 7.5)洗脫親和柱。收集洗脫峰,進行胰蛋白酶抑制活性的測定。收集活性峰,進行SDS-PAGE分析,用Superdex G-25脫鹽柱將BTI的緩沖液置換為NaHCO3溶液(20 mmol/L,pH 8.0)后,進一步用真空冷凍干燥機凍干得到BTI干粉。
1.2.2 BTI-Sepharose親和材料的制備
用碳酸鈉緩沖液(250 mmol/L,pH 9.0)溶解BTI,并調整BTI濃度為5 mg/mL。用去離子水清洗CNBr活化瓊脂糖凝膠表面的溶劑后,繼續用碳酸鈉緩沖液浸泡并洗滌。將凝膠與BTI溶液混合,在搖床上振蕩,于25℃偶聯6 h。然后加入Tris-HCl緩沖液(250 mmol/L,pH 8.3),繼續反應6 h封閉剩余的活性基團。將偶聯了BTI的凝膠填料裝于柱中,分別用1 mol/L NaCl溶液和蒸餾水清洗10個柱床體積,置于4℃保存備用。
1.2.3 BTI-Sepharose柱對胰蛋白酶的親和作用
用緩沖液(pH 7.2,20 mmol/L Tris-HCl,50 mmol/L NaCl)平衡制備好的BTI-瓊脂糖親和層析柱。用相同的緩沖液配制胰蛋白酶溶液(濃度為30 mg/mL),過0.22 μm濾膜后,取1 mL上樣于親和層析柱,流速控制為1 mL/min,然后用HAc-NaAc緩沖液(pH 3.5,100 mmol/L)洗脫。檢測280 nm處吸光度,收集蛋白峰,測定胰蛋白酶活性。
1.2.3.1 pH對BTI-Sepharose吸附胰蛋白酶的影響
用pH 7.2的20 mmol/L Tris-HCl,50 mmol/L NaCl緩沖液平衡BTI-瓊脂糖親和層析柱,取100 μL胰蛋白酶(30 mg/mL),與250 μL牛血清白蛋白(5 mg/mL)溶液混合后,上樣于層析柱,流速控制為1 mL/min,用pH 3.5的HAc-NaAc緩沖液(100 mmol/L)洗脫。收集穿透峰與洗脫峰,測定胰蛋白酶的活性,并進行SDS-PAGE鑒定。
改變緩沖液pH,用pH 5.0的20 mmol/L HAc-NaAc,50 mmol/L NaCl緩沖液平衡BTI-瓊脂糖親和層析柱,其它操作同上,研究不同pH對BTI-瓊脂糖凝膠吸附胰蛋白酶的影響。
1.2.3.2 pH對BTI-Sepharose解吸附胰蛋白酶的影響
取100 μL 30 mg/mL胰蛋白酶,與250 μL 5 mg/mL牛血清白蛋白溶液混合后上樣于親和層析柱,平衡緩沖液為Tris-HCl 20 mmol/L,NaCl 50 mmol/L,pH 7.2,流速控制為1 mL/min。上樣后,用pH 4.5的HAc-NaAc緩沖液(100 mmol/L)洗脫層析柱。分別收集穿透峰與pH 4.5緩沖液洗脫峰,測定各蛋白峰胰蛋白酶活性,并進行SDS-PAGE鑒定。
1.2.4 胰蛋白酶活性測定
胰蛋白酶活性測定按照文獻[15-16]的方法進行,并稍加改動。以BApNA(Na-苯甲酰-DL-精氨酸-對硝基酰胺鹽酸鹽)為底物,在3.2 mL活性測定體系(100 mmol/L Tris-HCl,pH 8.0,含10 mmol/L CaCl2)中加入0.5 mL待測樣品,37℃預熱5 min后,加入17 μL底物BApNA(150 mmol/L,溶劑為二甲基亞砜),繼續保溫10 min后,加入0.5 mL 33%醋酸溶液終止反應,在410 nm的波長下測定反應體系中由產物對硝基苯胺(PNA)所產生的吸光度。空白體系加樣順序為先加入反應終止液33%醋酸,再加入相同體積的樣品溶液。
1.2.5 胰蛋白酶抑制劑活性測定
按Sappasith等[17]的方法進行,并略作修改。在2.5 mL活性測定體系(100 mmol/L Tris-HCl,pH 8.0,含10 mmol/L CaCl2)中加入0.5 mL胰蛋白酶(20 mg/mL)和100 μL待測樣品,37℃預熱5 min后,加入17 μL底物BApNA(150 mmol/L,溶劑為DMSO),持續保溫10 min后,加入0.5 mL 33%的醋酸溶液終止反應,測定410 nm處吸光度。對照組以100 μL待測樣品的溶劑代替待測樣品。按照公式(1)計算抑制率。

1.2.6 SDS-PAGE電泳
采用SDS-PAGE法鑒定蛋白純度,以低分子質量蛋白質Marker(14.4~97.4 kDa)為對照,采用4%濃縮膠和15%濃縮膠,濃縮膠電壓為80 V,分離膠電壓為120 V。采用考馬斯亮藍R-250染色液,脫色液為50 mL甲醇、75 mL冰醋酸與875 mL重蒸水的混合液。
1.2.7 蛋白質濃度測定
采用福林酚法測定蛋白濃度,以牛血清白蛋白為標準品,按照福林酚蛋白濃度測定試劑盒說明書進行。
2 結果與分析
2.1 SDS-PAGE鑒定BTI
BTI具有很好的耐熱性,破碎菌體后在80℃下加熱30 min,大量熱不穩定的雜蛋白變性沉淀。離心后進行Ni2+-NTA親和層析,結果見圖1。通過對各蛋白峰抑制活性測定發現蛋白峰1和2無抑制活性,而蛋白峰3(含300 mmol/L咪唑的洗脫液)抑制胰蛋白酶活性很強,為目的蛋白。以低分子質量蛋白質Marker(14.4~97.4 kDa)為參照,將經Superdex G-25脫鹽后的BTI進行SDS-PAGE鑒定,結果見圖2。BTI(泳道1)在電泳圖譜上顯示單一條帶,表明所得BTI純度較高,達到電泳純。同時也表明親和層析是一種很高效的純化方法,僅需一次層析便得到了高純度的目的蛋白。
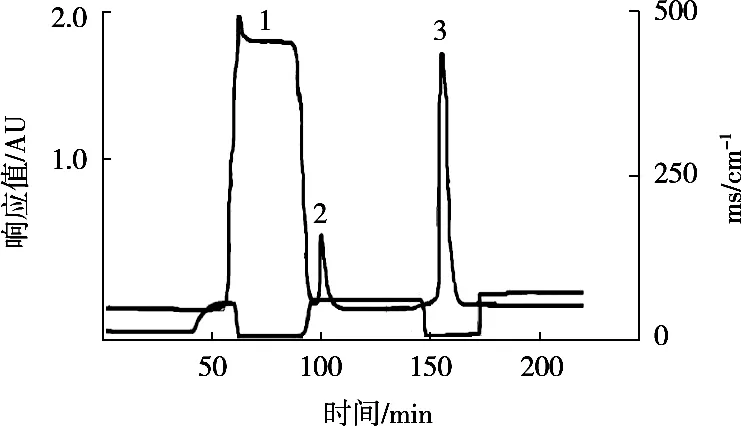
圖1 BTI的親和層析分離
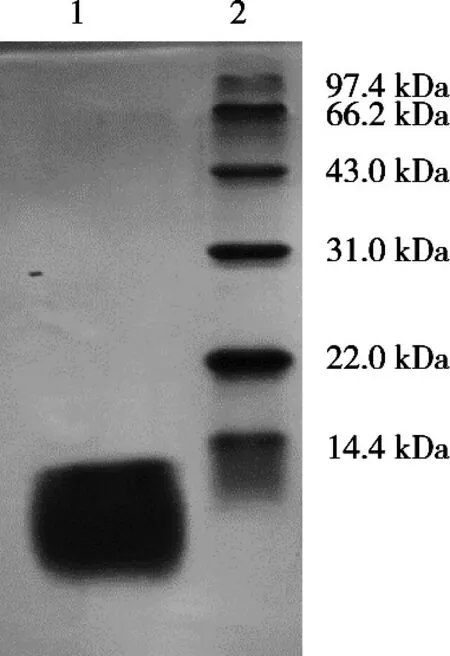
圖2 BTI的SDS-PAGE電泳圖譜
2.2 BTI-瓊脂糖凝膠對胰蛋白酶的吸附作用
BTI-瓊脂糖凝膠與胰蛋白酶的結合見圖3。如圖3所示,在上樣時出現了穿透峰1。當用pH 3.5的醋酸-醋酸緩沖液洗脫時,出現了蛋白峰2。以BApNA為底物鑒定胰蛋白酶活性,發現穿透峰1與洗脫峰2均能催化底物反應,產生明顯黃色產物,具有胰蛋白酶活性。洗脫峰2的出現表明在pH 7.2的平衡緩沖液條件下上樣時,胰蛋白酶結合到了BTI-瓊脂糖凝膠上,抑制劑與胰蛋白酶的活性部位以非共價鍵相互作用形成類似酶-底物的米氏復合物[18],在pH 3.5緩沖液條件下這種作用力減弱,胰蛋白酶從柱上洗脫下來。洗脫下來的胰蛋白酶在pH 3.5時催化活性不受影響。穿透峰1的出現可能是因為胰蛋白酶上樣量過大,超過了親和柱的吸附容量。
2.3 pH對BTI-Sepharose柱吸附胰蛋白酶的影響
降低胰蛋白酶上樣量為3 mg,將胰蛋白酶與牛血清白蛋白混合樣品上樣于BTI親和層析柱,在pH 7.2的平衡緩沖液條件下上樣,pH 3.5的緩沖液洗脫,純化層析結果見圖4。上樣與洗脫時均出現了蛋白峰,表明有一種蛋白在pH 7.2緩沖液的條件下未與親和柱結合,另一種蛋白在此條件與親和柱結合,但在pH 3.5緩沖液條件下與柱解離,被洗脫出來。對兩個蛋白峰進行胰蛋白酶活性鑒定,發現穿透峰沒有胰蛋白酶活性,而洗脫峰有活性,表明穿透峰為牛血清白蛋白,沒有胰蛋白酶,胰蛋白酶全部結合到親和柱上。SDS-PAGE結果(圖5)顯示洗脫樣品胰蛋白酶為單一條帶,穿透峰中只有牛血清白蛋白,進一步說明BTI-Sepharose柱可以特異結合胰蛋白酶。

圖3 胰蛋白酶的親和層析分離圖譜
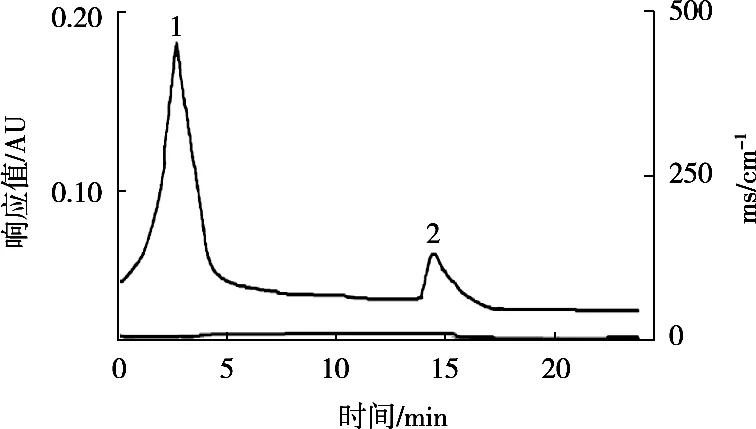
圖4 胰蛋白酶與BSA在pH 7.2平衡條件下的層析圖

圖5 親和層析蛋白峰的SDS-PAGE圖譜
將胰蛋白酶(3 mg)與牛血清白蛋白混合樣品在pH 5.0的平衡緩沖液條件下上樣,收集穿透峰,經鑒定穿透峰有胰蛋白酶活性。SDS-PAGE結果(圖6)顯示穿透峰樣品顯示兩條帶,分別是牛血清白蛋白(BSA)和胰蛋白酶(Trypsin)。胰蛋白酶活性測定與SDS-PAGE結果均說明在pH 5.0的平衡緩沖液條件下,部分胰蛋白酶未能與BTI-Sepharose柱結合,吸附效果不好。由于BTI具有很好的pH穩定性,胰蛋白酶的最適作用條件為堿性環境,推測在pH 5.0時親和柱吸附胰蛋白酶效率下降是由于胰蛋白酶空間構象發生了變化。圖6 胰蛋白酶與BSA在pH 5.0平衡液下穿透峰的SDS-PAGE圖譜
2.4 pH對BTI-Sepharose柱解吸附胰蛋白酶的影響
將胰蛋白酶與牛血清白蛋白混合樣品在pH 7.2的平衡緩沖液條件下上樣,用pH 4.5的醋酸緩沖液(0.2 mol/L)洗脫,純化層析圖譜見圖7。經活性檢測發現穿透峰樣品沒有胰蛋白酶活性,洗脫峰樣品有一定活性(A410為0.075),但活性顯著低于pH 3.5緩沖液的洗脫峰(A410為0.845)。SDS-PAGE(圖8)結果顯示穿透峰只有牛血清白蛋白條帶,與活性測定結果一致。洗脫峰有一定胰蛋白酶活性,但SDS-PAGE結果并未出現酶的條帶,表明洗脫峰中胰蛋白酶含量甚微,因此,洗脫效果不如pH 3.5的緩沖液。在pH 4.5條件下,胰蛋白酶與BTI-Sepharose柱仍有一定的親和力,不能完全從柱上解吸,pH 4.5的緩沖液只能將一小部分與BTI結合不牢固的胰蛋白酶洗脫下來。
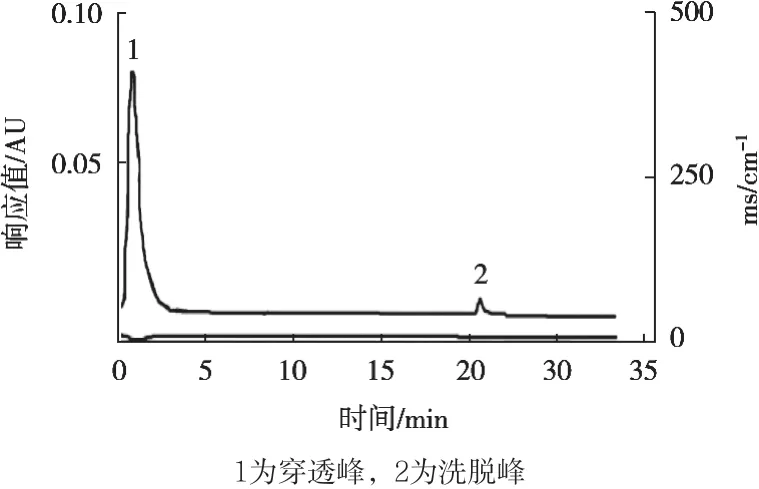
圖7 在pH 4.5洗脫條件下胰蛋白酶與BSA的層析分離圖譜
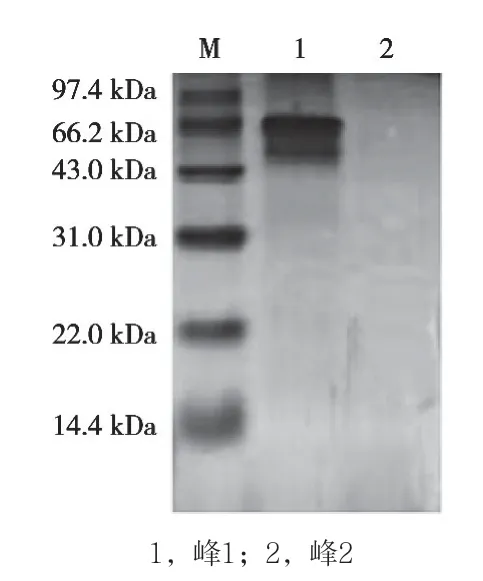
圖8 在pH 4.5洗脫條件下樣品的SDS-PAGE圖譜
3 結果與討論
通過原核表達、Ni2+親和柱層析和Superdex G-25凝膠過濾層析技術分離純化得到電泳純的BTI,與CNBr-Sepharose載體偶聯制備出親和吸附劑BTI- Sepharose,可用于純化胰蛋白酶。結果表明,所制備的BTI-Sepharose對胰蛋白酶具有良好的特異吸附性能,BTI-Sepharose與胰蛋白酶的吸附及解吸附作用受到緩沖液pH的影響。二者吸附的最適pH為7.2,緩沖液pH為3.5時能有效將柱上吸附的胰蛋白酶洗脫。試驗制備的BTI-Sepharose親和柱能夠將胰蛋白酶與牛血清白蛋白的混合物分離且不降低原有酶的生物活性,實現了簡單、快速、高效一步純化胰蛋白酶的目的。
目前制備胰蛋白酶的方法常以動物胰臟為原材料,采用傳統的鹽析、沉淀結合超濾、分子篩層析、離子交換層析、疏水層析等技術。胰臟中大多數酶以酶原非活性的形式存在,經胰蛋白酶激活后形成具有活性的酶,然而動物胰臟中大部分的酶為絲氨酸蛋白酶家族,其中糜蛋白酶與胰蛋白酶的理化性質相近,難以將二者分離。傳統方法純化效率低、往往需要多種介質與多個步驟組合才能達到產品質量要求,難以形成產業化。親和層析利用蛋白質等生物大分子間的相互作用力,與配體特異、可逆地結合在一起,從復雜的生物樣品中分離得到目標產物,與其他方法相比較,特異性高,純化效率高,適合含量少、雜質多的物質的分離純化,具備產業化生產的條件[19]。目前雖然有牛和豬來源的胰蛋白酶已經商業化,然而胰蛋白酶在自然界很多物種中普遍存在,其性質不盡相同,可用于不同領域。如哺乳動物來源的胰蛋白酶最適作用溫度多為50℃左右,在低溫(如低于20℃)時活性較低,而某些深海生物來源的胰酶最適作用溫度為20℃左右。在某些技術領域,如食品或藥品加工制造領域,需要低溫催化,可減少熱能消耗、更多地保留熱敏營養成分或減少副產物的生成等[20]。此次試驗制備了胰蛋白酶親和材料,有望分離得到更多未知胰蛋白酶類,開拓新型酶的研究與應用,具有巨大的科研意義和市場前景。

