超聲引導下凝血酶注射術治療股動脈假性動脈瘤3例并文獻復習
張 坤,王曉冬,王 偉,李玉明
(天津醫科大學心血管病臨床學院泰達國際心血管病醫院 心內五科,天津 300457)
股動脈是心血管介入手術最重要的入路之一,股動脈假性動脈瘤(PSA)是較為常見的血管并發癥,既往常用治療方法包括人工壓迫、手術修補等,近年來超聲引導下凝血酶注射術(UGTI)亦有良好效果[1],因其安全有效,成為廣泛使用的方法。現報道3例假性動脈瘤的治療并進行文獻復習。
1 病例資料
病例1,男性,66歲,體質指數(BMI)32.28 kg/m2,2017年7月16日經右股動脈入路行右冠狀動脈支架術治療。術后即刻拔管并使用血管縫合器(Angio-seal VIP)閉合股動脈穿刺點,術后臥床制動12 h,常規阿司匹林、氯吡格雷抗血小板,低分子肝素(4 000 IU皮下注射,1次/12 h)抗凝治療。術后12 h查體,右股動脈穿刺點局部可及搏動性包塊,可聞及雜音,超聲明確假性動脈瘤,股動脈前壁見約1.7 mm破口,瘤體約4.3 cm×1.6 cm×1.5 cm大小;采用人工壓迫30 min后局部加壓包扎并臥床12 h,復查超聲無改善;遂決定行UGTI,使用生理鹽水將凝血酶(凝血酶凍干粉,規格500 IU,北京第一生物化學藥業有限公司)稀釋至5 ml,即100 IU/ml濃度,使用5 ml注射器于超聲引導下瘤體內遠離破口處緩慢注射約300 IU,即刻復查超聲瘤體內血栓形成,動脈破口血液分流消失,24 h后復查超聲無復發。見圖1。
病例2,男性,62歲,BMI 24.44 kg/m2,2017年9月10日經右股動脈入路處理左主干病變,使用7F股動脈鞘管,術中順利于前降支至左主干病變處置入2枚支架,術后即刻拔除鞘管并使用血管縫合器(Angio-seal VIP)縫合穿刺點,術后臥床制動12 h,常規阿司匹林、氯吡格雷抗血小板,低分子肝素(4 000 IU皮下注射,1次/12 h)抗凝治療。術后12 h下地后出現右下肢傷口處疼痛,右腹股溝局部可及搏動性包塊,并可聞及雜音,超聲明確假性動脈瘤形成,右側股動脈近分叉處前壁可見1.9 mm破口,瘤體4.0 cm×2.0 cm×1.8 cm大小,可見多個分隔;同例1方法注射凝血酶約500 IU,即刻查超聲動脈瘤已封閉,24 h復查超聲無復發。
病例3,女性,27歲,BMI 29.5 kg/m2,2019年9月28日經右股動脈行動脈導管未閉(PDA)封堵術,術后即刻拔除鞘管,徒手壓迫止血后,加壓包扎并臥床制動,術后7 h右下肢活動后出現穿刺局部腫脹疼痛,超聲提示假性動脈瘤形成,瘤體大小2.7 cm×2.1 cm×0.9 cm,動脈破口約2 mm,同例1方法注射凝血酶約約300 IU,即刻查超聲動脈瘤封閉,24 h復查超聲無復發。
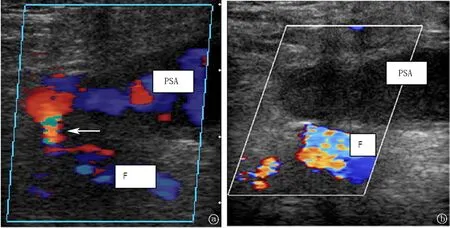
圖1 超聲引導下凝血酶注射術治療股動脈假性動脈瘤前后對比a.示注射凝血酶前,白色箭頭提示瘤頸部位,瘤體內可見血流信號;b.示注射凝血酶后PSA瘤體內血栓形成,瘤頸及瘤體內血流信號消失。F:股動脈,PSA:假性動脈瘤
2 討 論
假性動脈瘤(PSA)是股動脈穿刺后較常見的并發癥之一,又被稱為稱醫源性股動脈假性動脈瘤(IFAP),是附著于動脈壁的搏動性的囊性血腫,瘤體經動脈穿刺點與動脈腔相通,但瘤腔無動脈壁的全層結構。患者常有局部疼痛不適癥狀,聽診可及收縮期雜音,多普勒超聲可見特征性的血流往復征。形成原因主要有:穿刺點位置過低、反復穿刺、壓迫位置錯誤、穿刺點位于動脈側壁、鞘管直徑過大、術后未能嚴格制動以及肥胖、高血壓、嚴重動脈硬化等[2]。
PSA的治療方法,最常用的主要有外科手術、超聲引導下人工壓迫(UGMC)、UGTI三種方式[3]。外科手術是治療其他方法無效的、感染性的、體積快速擴大的、伴有皮膚壞死、壓迫神經、血管等情況的首選方法[4]。
UGMC文獻報道有較高的成功率,但是操作時間普遍較長,壓迫時間12~85 min不等,平均35.6分鐘[5],患者痛苦高,對操作者亦有較高的體力損耗,抗凝治療的患者成功率下降[1]。UGTI的原理是利用凝血酶加速瘤腔內血栓形成,從而使得動脈破口處封閉。大量的研究證實這種方法具有良好的安全性和有效性[6-7],UGTI目前成為臨床上治療PSA的一線手段。
Dzijan-Horn等[6]的回顧了29 091名股動脈入路的患者,有432例(1.49%)PSA患者,根據超聲下的瘤體形態特點,選擇干預方法,145名患者瘤體<20 mm,沒有明確的瘤頸,直接與血管臨近或合并動靜脈瘺,首選人工壓迫;余287名患者使用UGTI處理,部分患者采用了兩種處理方法,最終總成功率達97.2%。值得注意的是,有10名患者最終進行外科手術,3例出現了并發癥,包括出血、感染、神經損傷。另一項研究[8]納入了121例PSA患者,繼發于心血管診斷、介入、導管消融治療手術,平均年齡70.7歲,均以UGTI為首選治療方案,平均直徑26.7 mm,111名(92%)患者即刻成功,7名患者復發,其中3名需要外科修補術,未出現如血栓栓塞、動脈瘤破裂、膿腫等嚴重并發癥,而且發現抗凝、抗血小板治療及瘤體大小對手術結果無明顯影響。Jargiello等[9]報道成功率達98.5%(133/135),其中5例通過2次UGTI治療。Ehieli等[10]亦回顧性總結了326例注射凝血酶治療的患者,總成功率達98.2%(320/326),進行超聲隨訪的145例患者中,108例成功,21例進行二次注射治療成功。統計分析瘤體直徑、體積及分葉數量并不影響操作成功率,而抗凝治療則與瘤體內未能完全血栓化相關。而另一項包含46例患者的研究證實瘤體的大小、頸部的大小及其復雜度不影響療效,且抗凝治療亦不影響治療成功率[11]。總體來說,目前的證據顯示對于常規PSA,UGTI有良好的效果,對于復雜多葉的、使用抗凝劑的患者可能需要二次操作。本文中3例PSA,瘤體最大長度4.3 cm,且雖有1例有多葉,但破口直徑較小,在超聲引導下,可以準確的定位注射部位,均實現1次注射成功封閉。
對于特殊的患者,亦有相關研究。對于重度肥胖的患者(BMI≥35 kg/m2)該方法同樣有效,但對于超聲成像具有一定的挑戰性[12]。有報道在兒童患者中亦有良好效果[13],8例9個股骨PSA患者接受了13次UGTI治療,患者平均年齡為3.3歲,平均凝血酶劑量為119 IU,成功治療了8個PSA,其中1個由于動脈壁疾病而未能閉合,沒有發現并發癥。
在合并有動靜脈瘺(AVF)的PSA患者中,有研究[14]嘗試該治療方法,在成功的患者中發現瘺管舒張期動脈血流速度≤ 25 cm/s,且同時口服抗凝治療是安全有效的,但是在大的AVF中,不主張使用UGTI,警惕發生靜脈栓塞。有研究顯示UGTI方法失敗與動脈瘤直徑增加、終末期腎臟疾病和股淺動脈瘤起源相關[15]。
在并發癥方面,在一項納入353例患者的研究中[16],動脈微栓塞發生53例(15%),肺栓塞1例(0.3%),未發生外周動脈栓塞。栓塞風險與動脈腔與PSA之間的連通通道的長度呈負相關,通道長度小于2 mm和反復注射凝血酶增加栓塞的風險。
我們在臨床中使用UGTI方法成功處理的3例PSA,均發生于內科經股動脈入路的介入治療后,鞘管直徑6F和7F,也是臨床上內科介入治療中最常用的,回顧病例,發生PSA的原因可能與肥胖、圍術期抗凝及術后術肢制動不足相關,值得注意的是有2例使用的血管縫合器(Angio-seal VIP),但仍有PSA的發生,文獻亦有報道,這可能與圍術期的抗凝相關[17]。UGTI主要的操作要點是利用超聲定位,注射時的進針點盡量遠離動脈破口處,緩慢注射,即刻復查超聲確認,術后臥床數小時即可。
由于UGTI方法在操作時間、成功率及并發癥等方面明顯的優勢,目前已經成為IFAP的一線治療手段。我們成功使用這種方法處理了3例患者,與單純壓迫相比較,患者痛苦小,省時省力,值得推廣使用。

