氣相色譜質譜法測定魚油膠囊殼中22種鄰苯二甲酸酯類含量及遷移量
鄧 龍,周 思,張瑞瑞,劉 苗
(1.廣東食品藥品職業學院,廣東廣州 510520;2.廣州市疾病預防控制中心,廣東廣州 510440;3.廣州檢驗檢測認證集團有限公司,廣東廣州 511447)
鄰苯二甲酸酯類(PAEs)是一種常見的高分子材料助劑,可用于改善材料的可塑性和柔韌性,在食品包裝材料、醫療用品等方面使用廣泛。PAEs與塑料單體間相互作用為氫鍵和范德華力,鍵合強度弱,容易造成PAEs遷移,隨著PAEs的大量生產和廣泛應用,PAEs逐漸遍布每一個角落,研究表明,在大氣、水體、生物乃至人體等各類環境中均有PAEs存在[1-3]。PAEs作為一種環境激素,可通過多種途徑影響機體內分泌系統的正常功能,危害人體健康[4-6]。早在1995年,世界衛生組織就將PAEs列為必須控制的一類擾亂內分泌的化學物質。我國衛生部公告2011年第16號將鄰苯二甲酸二(2-乙基)己酯等17種PAEs列為可能違法添加的非食用物質[7]。2017年實施的食品安全國家標準GB 9685-2016將食品接觸材料中允許使用的PAEs減少至鄰苯二甲酸二丁酯、鄰苯二甲酸二(2-乙基)己酯、鄰苯二甲酸二異壬酯、鄰苯二甲酸二烯丙酯4種,且明確不得用于接觸脂肪性食品[8]。魚油作為大眾接受度極高的一類營養補充劑,是較為特殊的脂肪性食品,受原料、提取、精煉、包裝工藝等因素的影響,PAEs富集、遷移、溶入風險較高,魚油膠囊殼不論是直接食用或僅作為包裝材料,都將直接影響魚油保健品中PAEs的含量水平,魚油膠囊殼中PAEs殘留水平和遷移量的檢測未見相關報道。
目前,報道的PAEs檢測方法包括氣相色譜法(GC)[9-10]、液相色譜法(LC)[11]、氣相色譜-質譜法(GC-MS)[12-13]、氣相色譜-串聯質譜法(GC-MS/MS)[14-15]、液相色譜-串聯質譜法(LC-MS/MS)[16-17]等。其中,質譜法因靈敏度高、抗干擾能力強等優勢,在PAEs的檢測中應用廣泛。本文選取22種常見PAEs為目標物,結合GC-MS在易揮發化合物定性定量方面的優良性能,通過優化樣品前處理方法、色譜條件,建立魚油膠囊殼及食品模擬物中22種PAEs的GC-MS檢測方法,研究市售魚油膠囊殼中PAEs的殘留現狀及正常儲存條件下的遷移水平,可為魚油膠囊類保健食品的質量監控提供技術支撐和數據支持。
1 材料與方法
1.1 材料與儀器
魚油膠囊15款 購自采芝林和大叁林藥房;脂肪性食品模擬物、精制玉米油 購自家樂福超市,氣相色譜測試滿足GB 5009.156要求[18];22種鄰苯二甲酸酯類標準品 Dr Ehrenstorfer GmbH公司,純度均大于98%;乙腈、正己烷等試劑 德國Merck公司,均為色譜純。
7890A-5975C氣相色譜-質譜聯用儀 美國安捷倫公司;Milli-Q去離子水發生器 美國Millipore公司;MS3漩渦混合器 德國IKA公司;SIGMA 3-18K離心機 德國Sigma公司;固相萃取裝置 美國Waters公司。
1.2 實驗方法
1.2.1 標準溶液的配制 目標物用乙腈配制成濃度為500 mg/L的單標儲備液,于-20 ℃冰箱保存。分別吸取適量的單標儲備液,用乙腈稀釋成濃度為5.00 mg/L混合標準溶液,于-20 ℃冰箱保存。使用時,用乙腈逐級稀釋成濃度為5、10、20、50、100、200、500 μg/L的系列標準工作溶液。
1.2.2 魚油膠囊殼中PAEs的提取 準確稱取碎膠囊殼1.0 g(精確至0.01 g)于50 mL具塞離心管中,加入60 ℃熱水5 mL,渦旋至溶解,待冷卻,加入10 mL正己烷,渦旋2 min,超聲20 min,經4000 r/min離心2 min,吸取上清液至25 mL氮吹管中,殘渣加入10 mL正己烷重復萃取,合并清液,40 ℃氮吹至1 mL供測試。
1.2.3 氣相色譜條件 色譜柱:Agilent Select PAH(30 m×0.25 mm×0.15 μm);載氣:高純氦氣,流速1.0 mL/min;升溫程序:初始溫度60 ℃,20 ℃/min升至160 ℃,保持1 min,15 ℃/min升至220 ℃,4 ℃/min升至280 ℃,保持4 min,20 ℃/min升至320 ℃,保持1 min,進樣口溫度:280 ℃;進樣量:1 μL,不分流進樣;溶劑延遲6 min。
1.2.4 質譜條件 離子源:EI,70 eV;離子源溫度250 ℃;四極桿溫度150 ℃;傳輸線溫度:300 ℃;選擇離子監測(SIM)模式;保留時間和特征離子見表1。
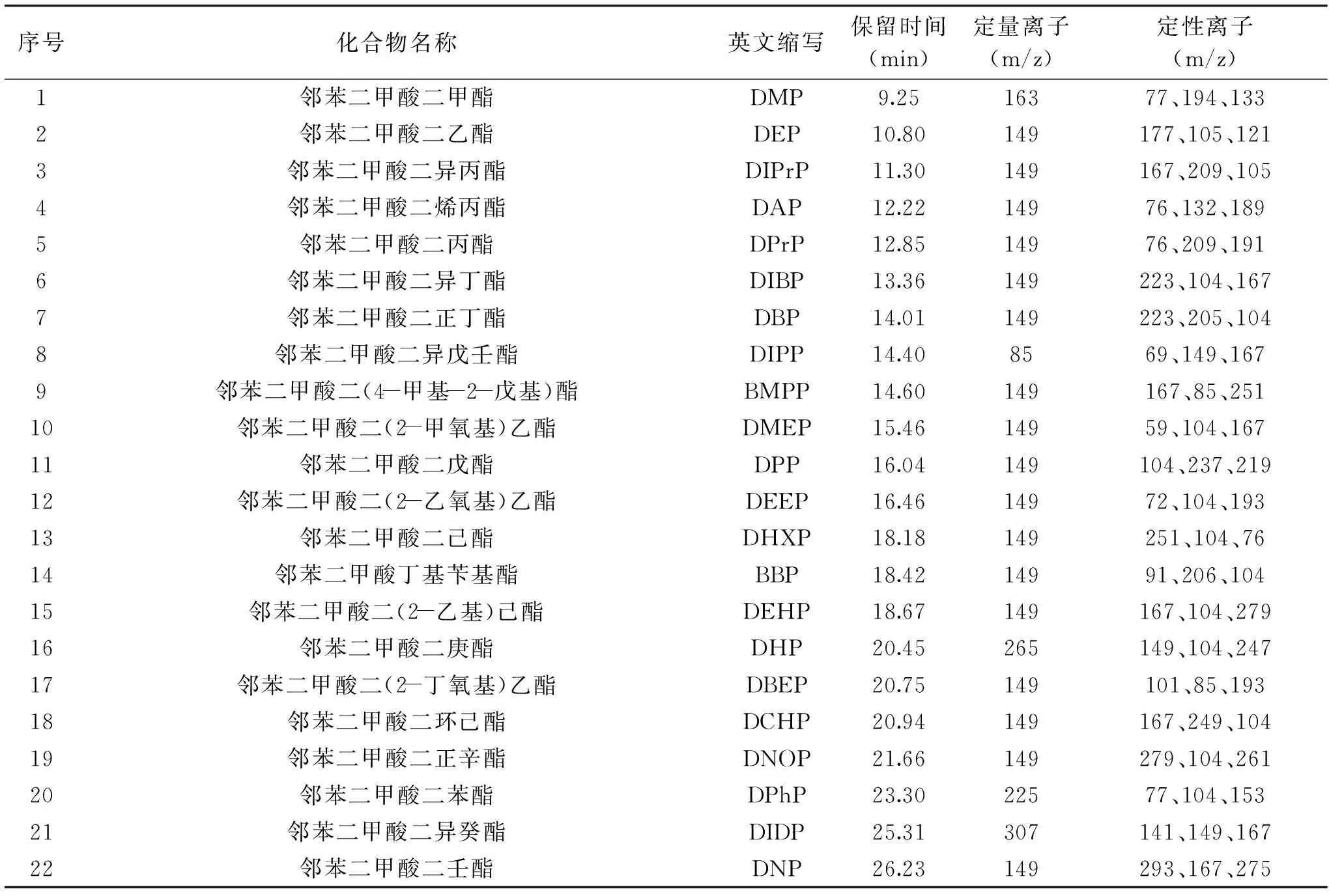
表1 鄰苯二甲酸酯類化合物的質譜參數Table 1 MS parameters of PAEs
1.2.5 魚油膠囊殼中PAEs遷移量的測定 剪取1.2 cm2膠囊殼,浸入4 mL玉米油中,25 ℃測定各時間的遷移量。食品模擬物中PAEs的測定參照GB 5009.271中植物油的前處理方法[19],準確稱取1.0 g食品模擬物于具塞離心管中,加入0.2 mL正己烷和10 mL乙腈,渦旋2 min,超聲20 min,吸取上清液至25 mL氮吹管中,殘渣加入10 mL乙腈重復萃取1次,合并上清液,40 ℃氮吹至1 mL供測試。
1.3 數據處理
采用外標法進行定量,通過標準加入法和控制變量法優化實驗條件。應用儀器配套工作站Data Analysis進行數據處理,使用Origin 8.5進行作圖和分析。
2 結果與分析
2.1 樣品前處理條件的優化
市售魚油膠囊殼多以明膠為基質,加入甘油、著色劑、遮光劑等輔料制成。基于明膠的親水性,選擇以溫水進行溶解以充分釋放出樣品中的目標物,水溫過低膠囊殼溶解不充分,水溫過高容易導致目標物損失,且增加后續處理時間,故選擇以60 ℃熱水進行溶解。目標物鄰苯二甲酸酯為親脂性化合物,根據相似相溶的原理結合文獻報道[20],本實驗對比了乙腈、正己烷、石油醚3種萃取溶劑的提取效果。實驗發現,石油醚中DBP和DEHP的本底值較高,其中DBP的本底值高于方法的定量限。相比之下,乙腈和正己烷的試劑空白較低,兩者作為萃取溶劑目標物回收率在80%~120%之間,符合GB/T 27404標準要求[21]。使用乙腈萃取樣品的同時萃取了較多的水溶性雜質,部分樣品的檢測產生干擾待測物的雜質峰,增加后續凈化處理的難度,而正己烷對于水溶性雜質的溶解性較差,樣品基質干擾少,因此,選擇正己烷作為萃取溶劑。
魚油是從鯖魚、鯡魚等多脂魚類中提取的油脂,按照食品安全國家標準GB 31604。選擇精制玉米油作為食品模擬物[22]。根據GB 5009.156標準要求遷移實驗食品接觸材料的面積(S)與食品模擬物的體積(V)應反映實際的使用情形[18],由于不同品牌的魚油膠囊規格、形狀各異,接觸面積值難以估算,加之膠囊殼體積小、材質均一,統一按每6 dm2食品接觸材料對應1 L食品模擬物的比例采用全浸沒法進行遷移實驗。查看15款魚油膠囊的產品信息,保質期為9~24個月不等,產品儲藏方法多描述為置陰涼干燥處、常溫保存,按特定遷移實驗條件的選擇原則,可選擇60 ℃,10 d條件開展加速實驗[22]。實驗發現,明膠在此條件下會發生變黑、軟化等理化性質的改變。考慮魚油膠囊殼可直接食用或僅作為包裝材料,是一類特殊的食品接觸材料,且本文側重考察正常儲存情況下魚油膠囊殼中的PAEs的遷移情況。最終確定實驗條件為:剪取1.2 cm2的膠囊殼,浸入4 mL玉米油中,25 ℃下測定各個時間的遷移量。
2.3 儀器條件的優化
2.3.1 質譜條件的優化 將配制好的濃度為50.0 μg/L的PAEs單標溶液進行全掃描采集,通過NIST譜庫查詢功能結合文獻報道,確定22種目標物的定性定量離子,并采用選擇離子(SIM)掃描方式分段檢測不同保留時間的待測物,以提高樣品檢測的靈敏度并消除部分雜質干擾。參照歐盟2002/657/EC決議中有關質譜分析方法不少于4分的規定,每個待測物選取4個離子為質譜采集參數[23]。22種待測化合物的監測條件如表1所示。
2.3.2 色譜柱的選擇 本次測定的鄰苯類化合物共22種,存在多種結構相似物和同分異構體,碎片離子相似度高,采用鄰苯類化合物測定中常用的DB-5MS色譜柱進行測試[24],DIPP和BMPP、DHP和DEHP等化合物分離效果不佳,且離子碎片相似,不易實現單獨定量。為了實現各目標物的分離,需要精細程序升溫條件,導致分析時間過長,不利于檢測工作的開展。實際工作中發現,PAH專用柱通過修飾固定相,優化膜厚,可提高柱效,改善色譜峰型,有效地增大了目標物的分離度。選擇Agilent Select PAH色譜柱對22種PAEs進行分析,在27 min內所有目標物全部出峰,達到基線分離,目標物峰型尖銳,半峰寬窄,檢測靈敏度和分離度得到大幅提高。本方法檢出限與國家標準GB 31604.30-2016相比[25]低2~3個數量級。22種PAEs的總離子流色譜圖如圖1所示。
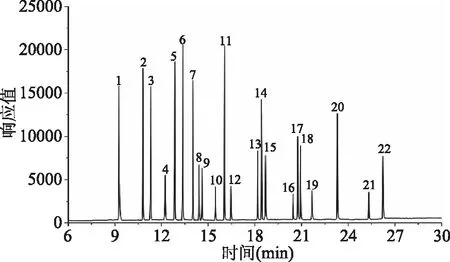
圖1 PAEs混標溶液總離子流色譜圖Fig.1 Total ion chromatogram of mixed standard solution注:序號對應表1相應化合物。
在優化條件下,測試1.2.1節的混合標準溶液,以目標物的質量濃度(x,μg/L)為橫坐標,定量離子的峰面積(y)為縱坐標作圖,得到22種PAEs的線性方程如表2所示。由表可知,22種目標物在一定濃度范圍內線性關系良好,相關系數均大于0.9987。以3倍信噪比(S/N=3)計算檢出限,以10倍信噪比(S/N=10)計算定量限,結合樣品前處理過程得到方法檢出限為3.1~9.8 μg/kg,定量限為10~29 μg/kg,表明本方法具有較高的靈敏度。
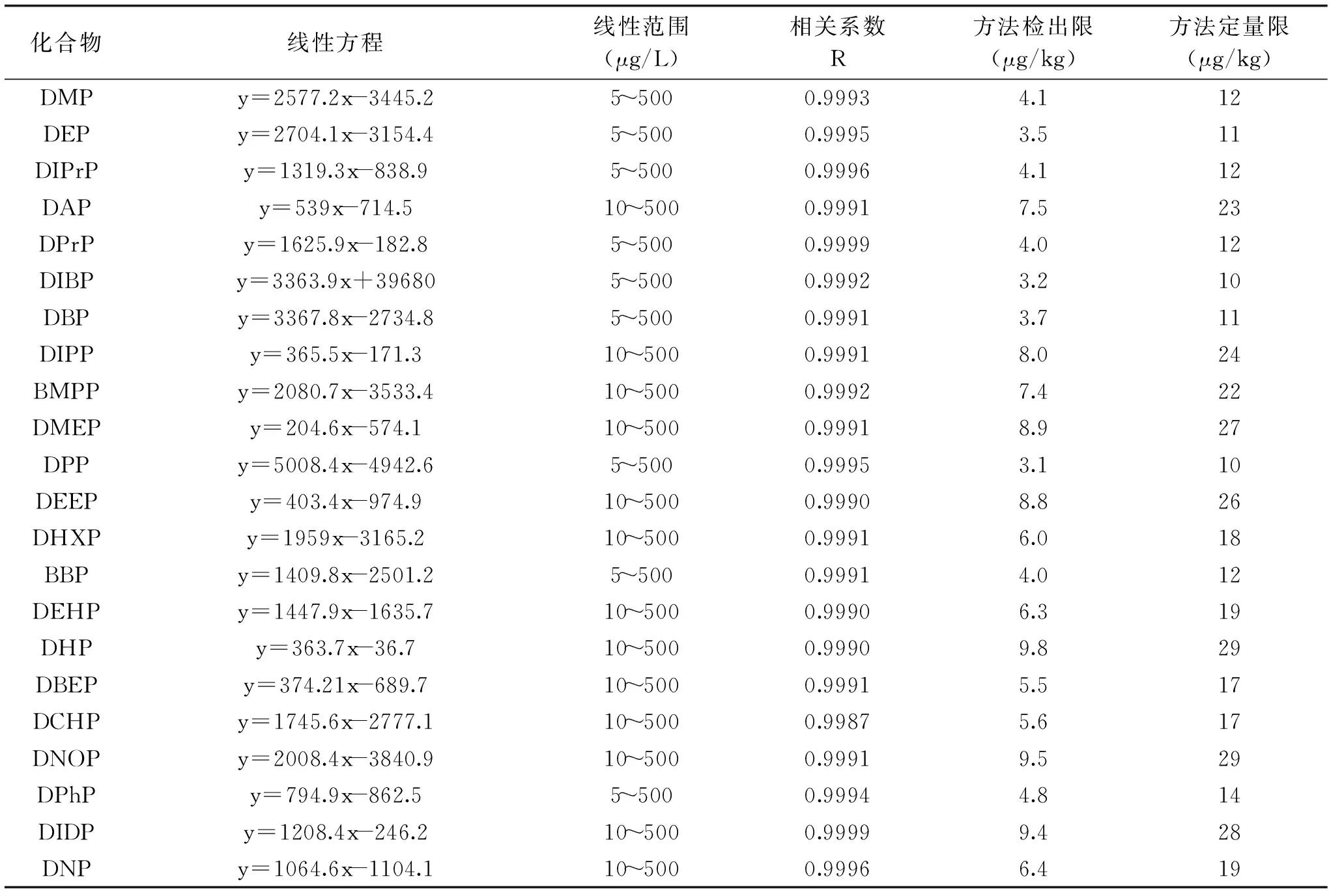
表2 化合物的線性方程、相關系數、線性范圍、方法檢出限和方法定量限Table 2 Linear equations,linear ranges,correlation coefficients,detection limits and quantification limits of PAEs
2.5 回收率與精密度
為考察樣品處理的可靠性,進行加標回收率試驗。選取陰性樣品參照GB/T 27404[21]選取1倍、2倍和10倍方法測定低限進行3水平加標回收實驗,每個水平平行測試6次,實驗結果見表3。由表可知,在加標濃度范圍內,22種待測物的平均回收率為82.1%~112.1%,相對標準偏差(RSD,n=6)為2.1%~7.7%,說明方法具有良好的回收率與精密度。
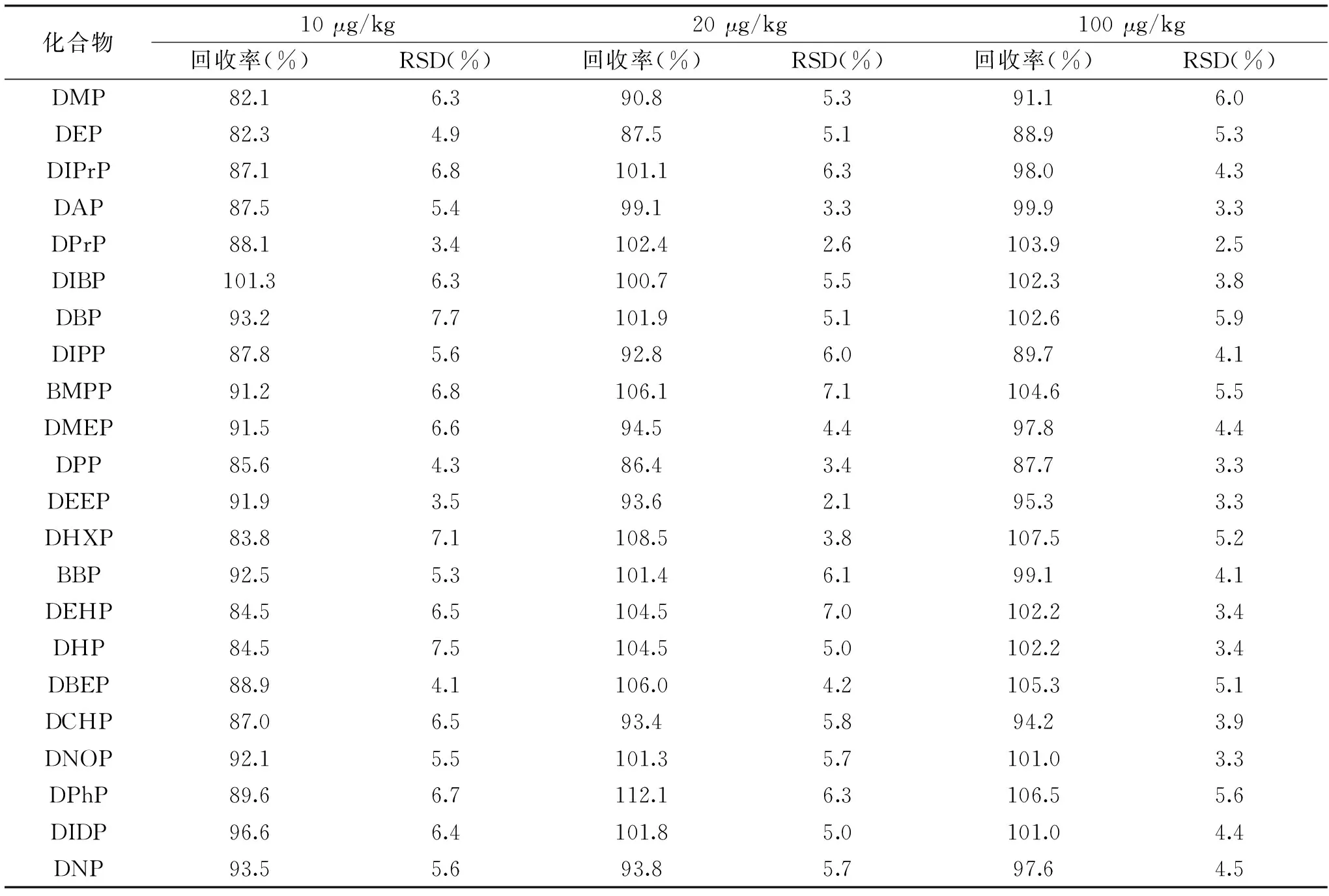
表3 加標回收和精密度實際測定結果(n=6)Table 3 Determination results of recovery and precision(n=6)
2.6 實際樣品的檢測
利用建立的分析方法檢測15個市售魚油樣品膠囊殼。結果表明,有5個膠囊殼檢出少量PAEs,檢出種類包括DEP、DBP、DIBP、DEHP,含量水平在0.14~0.78 mg/kg之間。鑒于含量較低,排除在生產過程中故意添加的可能性;此外,有1個膠囊殼檢出較高水平的PAEs,DEHP含量為4.51 mg/kg,DBP含量為1.13 mg/kg。GB 9685規定DEHP、DBP作為食品接觸材料及制品用添加劑不得用于接觸脂肪性食品,最大殘留限量分別是1.5、0.3 mg/kg,此樣品中的膠囊殼作為包裝材料,最大殘留限量不符合GB 9685標準要求[8]。需進行溯源,排查含量過高的原因。陽性樣品稀釋25倍后測定的總離子流色譜圖見圖2。
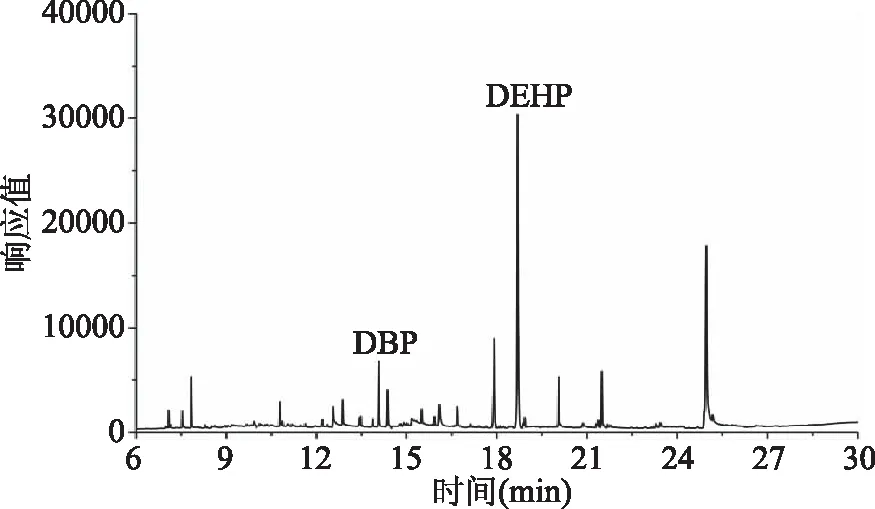
圖2 陽性樣品總離子流色譜圖Fig.2 Total ion chromatogram of positive sample
2.7 魚油膠囊殼中PAEs的遷移量
以精制玉米油為食品模擬物,考察25 ℃下魚油膠囊殼中PAEs的遷移情況。鑒于DEHP是報道污染較為嚴重的化合物,且市售魚油膠囊樣品檢出較高水平的DEHP,故選擇DEHP作為遷移實驗的研究對象,考察浸泡時間為1、2、5、10、20、30、40 d遷移量的變化,DEHP遷移量隨時間的變化趨勢如圖3所示。由圖3可知,膠囊殼中的PAEs存在明顯的遷移現象,隨著時間增加,DEHP的遷移量不斷增加,增加幅度逐漸減小,20 d后遷移量增加值逐漸變緩。衛辦監督函[2011]551號規定嚴禁在食品、食品添加劑中人為添加增塑劑,DEHP在食品和食品添加劑中的最大殘留量1.5 mg/kg[26]。該樣品在40 d時食品模擬中DEHP的含量為0.49 mg/kg,未超過最大限量要求。實際樣品中魚油與膠囊殼的接觸面積之比(S/V)遠小于1∶6,遷移量水平更高,存在潛在風險。因此,魚油膠囊殼不論是直接食用還是僅作為包裝材料,都將直接影響魚油產品中PAEs的含量水平,生產過程除考慮魚油的品質外,還應關注膠囊殼的質量安全。
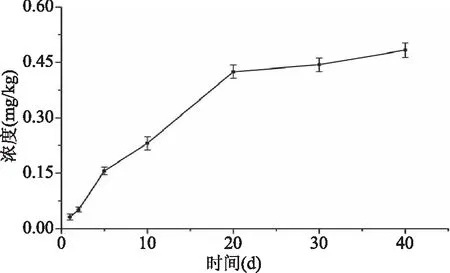
圖3 DEHP遷移量隨著時間的變化趨勢圖Fig.3 Migration of DEHP from fishoilcapsule shells for different time
3 結論
本文建立了氣相色譜-質譜同時檢測魚油膠囊殼及食品模擬物中22種鄰苯二甲酸酯類化合物的檢測方法。通過優化樣品前處理方法,選擇PAH專用柱進行分析,通過優化色譜條件和質譜參數,實現了22種目標物的有效分離,22種鄰苯二甲酸酯類化合物在10~500 μg/L濃度范圍內線性關系良好,定量限在10~29 μg/kg之間。本方法具有操作簡便、檢出限低,選擇性好、精密度高等特點,方法學結果符合GB/T 27404中理化檢測質量控制相關技術要求,適用于魚油膠囊殼及食品模擬物中鄰苯二甲酸酯類的測定。

