胃癌中CXCR1的表達及其臨床意義
王娜娜,王岳君,馮天一,黃偉超,章俊生,孟 剛,3
胃癌是全球第二大腫瘤相關性致死因素[1]。根治性手術是治療胃癌的主要方法,但胃癌患者初期癥狀隱匿,超過半數(shù)患者在疾病進展期時被確診。侵襲和轉(zhuǎn)移是導致胃癌患者復發(fā)和死亡的主要原因。長期以來腫瘤微環(huán)境一直被認為在腫瘤的發(fā)生和發(fā)展中起重要作用[2];在腫瘤微環(huán)境的眾多因素中,炎癥介質(zhì)與腫瘤的進展關系密切[3]。由于IL-8是腫瘤微環(huán)境的重要組分,也是維持癌細胞干性的關鍵細胞因子,趨化因子與其受體相互作用與腫瘤的進展密切相關[4]。目前,關于IL-8的受體CXCR1在胃癌組織中表達的報道較少。本實驗收集141例胃癌患者的臨床病理資料,初步探討CXCR1在胃癌中的表達及其與臨床病理特征的關系,旨在提高臨床和病理醫(yī)師的認識水平。
1 材料與方法
1.1 臨床資料收集2015~2019年安徽醫(yī)科大學第四附屬醫(yī)院存檔的行胃癌根治性切除標本141例,所有病例均為首發(fā),并經(jīng)病理學證實為胃癌,術前均未行放、化療等抗腫瘤治療。另收集癌組織及其對應癌旁>5 cm正常胃黏膜標本作為對照。患者年齡26~85歲,中位年齡67歲,男性102例,女性39例。所有組織標本均經(jīng)石蠟包埋,每張切片厚3 μm,備用。臨床分期(TNM):T1/2,N0:26例;T1/2,N+:5例;T3/T4a,N0:22例;T3/T4a,N+:82例;T4b,M+:6例。本實驗經(jīng)安徽醫(yī)科大學第四附屬醫(yī)院倫理委員會批準,所有患者均知情同意。
1.2 方法選取胃癌組織和癌旁正常胃黏膜組織的存檔蠟塊,3 μm厚連續(xù)切片。免疫組化采用MaxVision兩步法染色,一抗IL-8RA(CXCR1)(鼠單克隆抗體B-1,1 ∶300)購自Santa Cruz公司,CK(鼠單克隆抗體,AE1/AE3)及其余相關試劑均購自福州邁新公司。以PBS代替一抗作為陰性對照,組織內(nèi)中性粒細胞、單核細胞、內(nèi)皮細胞等作為陽性內(nèi)對照。
1.3 結果判斷所有切片均采用數(shù)字掃描儀轉(zhuǎn)換成數(shù)字切片,免疫組化染色由兩位病理醫(yī)師采用雙盲法進行半定量評分[5],每個標本隨機選取10個高倍視野,對陽性細胞著色強度和所占百分比進行評分。CXCR1陽性著色定位于細胞膜和細胞質(zhì),以中性粒細胞、單核細胞等作為陽性內(nèi)對照。(1)按腫瘤細胞陽性染色強度計分:未著色為0分,淡黃色為1分,中等棕黃色2分,深棕褐色為3分;(2)按腫瘤細胞著色的百分比計分:無陽性細胞為0分,≤10%為1分,11%~50%為2分,51%~80%為3分,>80%為4分;將上述兩項評分結果相乘:<3分為陰性,≥3分為陽性。
1.4 統(tǒng)計學分析采用SPSS 21.0軟件進行統(tǒng)計學分析。對CXCR1蛋白在胃癌組織中的表達特點和與各臨床病理參數(shù)的關系采用χ2檢驗,分類變量采用頻率描述。以P<0.05為差異有統(tǒng)計學意義。
2 結果
2.1 癌旁正常胃黏膜及胃癌組織中CXCR1的表達本實驗結果顯示,CXCR1在癌旁正常胃黏膜組織表達較弱或不表達,表達于嗜中性粒細胞、單核細胞、內(nèi)皮細胞表面和部分胃癌細胞表面,其陽性率與腫瘤的分化程度有關。胃癌組織高+中分化組陽性率為36.5%,明顯低于低分化組(64.1%)(P=0.001 1,圖1)。
2.2 胃癌組織中CXCR1的表達141例胃癌有脈管侵犯組織中,CXCR1陽性者63例(61.8%);明顯高于無脈管內(nèi)侵犯的胃癌組(25.6%),差異有統(tǒng)計學意義(P=0.000 1)。本組采用免疫組化MaxVision兩步法和HE染色,鏡下可見CXCR1、CK在胃癌脈管內(nèi)癌栓或胃癌組織中表達時常伴中性粒細胞簇的存在,且中性粒細胞的形態(tài)有差異(圖2)。
2.3 胃癌中CXCR1表達與臨床病理特征的關系141例胃癌組織中,CXCR1陽性73例(51.78%),CXCR1陰性68例(48.22%);CXCR1表達與患者性別、年齡、腫瘤大小無關;與胃癌分化(P=0.001 1)、腫瘤浸潤深度(P=0.017 0)、脈管侵犯(P=0.000 1)、神經(jīng)侵犯(P=0.000 1)和淋巴結轉(zhuǎn)移(P=0.000 1)、TNM分期(P=0.004 1)均有關(表1)。
3 討論
CXCR1基因組首先由Holmes等[6]成功克隆。人類CXCR1基因定位于染色體2q35,包含2個外顯子與1個長約1.7 kb的內(nèi)含子,包含1個糖基化N-端和1個具有7次跨膜域的G蛋白偶聯(lián)受體[7]。CXCR1在機體內(nèi)主要表達于中性粒細胞表面,當有外來病原體入侵時,炎癥組織釋放IL-8等趨化因子,經(jīng)血液循環(huán)與中性粒細胞表面的CXCR1/2結合,從而趨化中性粒細胞遷移至炎癥發(fā)生部位吞噬和殺滅病原體[8]。IL-8與其受體的結合可導致多個主要下游信號傳導途徑的激活,其中包括:磷脂酰肌醇-3激酶(PI3K)/AKT,磷脂酶C(PLC)/蛋白激酶C(PKC)和促分裂原活化蛋白激酶(MAPK),Rho家族GTP酶和Janus激酶(JAK)等,從而在多方面促進了腫瘤的進展[9]。有研究表明[10],CXCL8/CXCR1除具有免疫調(diào)節(jié)作用外,還能影響腫瘤的微環(huán)境、調(diào)節(jié)腫瘤血管形成。腫瘤的生長和轉(zhuǎn)移,關鍵在于腫瘤細胞的增殖、黏附、遷移、血管生成和免疫逃避的能力[11]。CXCR1/2受體在卵巢癌、肝細胞癌、前列腺癌、腎細胞癌、鼻咽癌、乳腺癌等腫瘤中均高表達,且與腫瘤的增殖、轉(zhuǎn)移和血管生成有關[12-15],分析表明腫瘤細胞可分泌大量IL-8,與自身或其他腫瘤細胞表面的CXCR1/2受體結合,從而促進腫瘤組織的血管生成、腫瘤細胞增殖和轉(zhuǎn)移。腫瘤細胞可以受到某些趨化因子的趨化作用而發(fā)生遷移,該性質(zhì)類似于某些炎細胞的特性,如中性粒細胞;Bi等[16]研究表明,腎癌組織細胞分泌的IL-8,可促進腫瘤間質(zhì)干細胞的遷移,人類多種腫瘤的發(fā)生涉及到上皮細胞-間質(zhì)轉(zhuǎn)化(epithelial to mesenchy-mal transition, EMT)[17],目前其具體的機制尚不清楚。
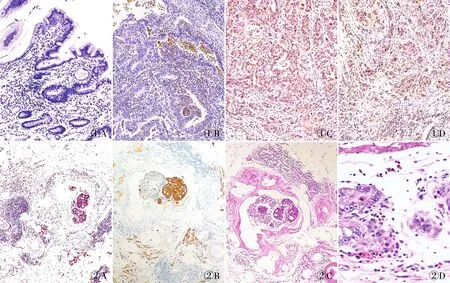
圖1 A.CXCR1在癌旁正常胃黏膜組織中呈陰性,MaxVision兩步法;B.CXCR1在部分高分化胃癌組織中呈陰性,MaxVision兩步法;C.CXCR1在部分中分化胃癌組織中呈陽性,MaxVision兩步法;D.CXCR1在部分低分化胃癌組織中呈陽性,MaxVision兩步法 圖2 A.胃癌脈管內(nèi)癌栓及周圍散在的腫瘤細胞中CXCR1呈細胞膜/細胞質(zhì)陽性,MaxVision兩步法;B.胃癌脈管內(nèi)癌栓及脈管周圍大量散在的腫瘤細胞中CK呈陽性,MaxVision兩步法;C.胃癌脈管內(nèi)癌栓旁伴大量中性粒細胞浸潤;D.腫瘤周圍中心粒細胞核形態(tài)多樣,呈分葉狀、圓形或不規(guī)則
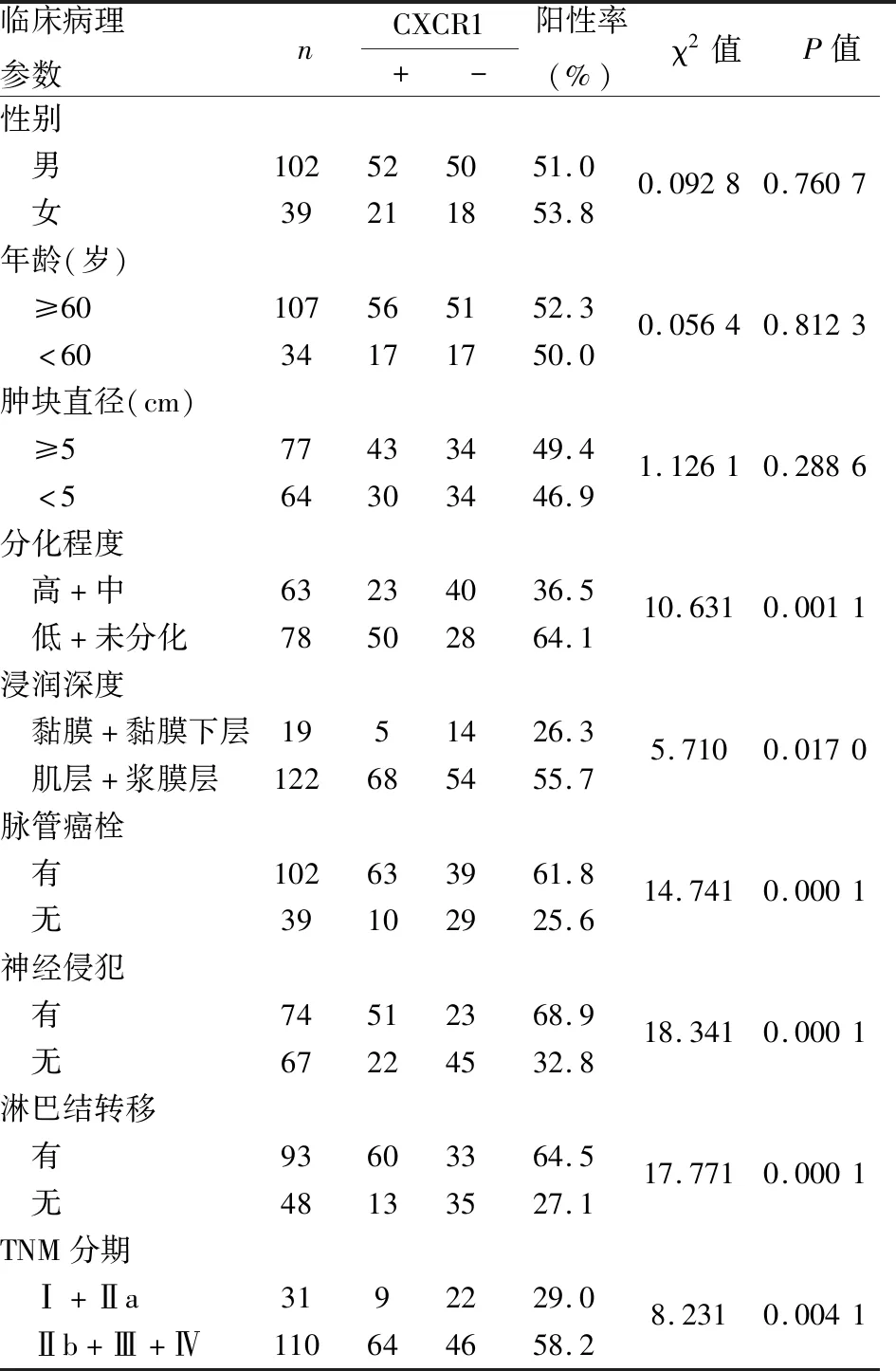
表1 胃癌組織中CXCR1表達與臨床病理特征的關系
本組141例胃癌組織中,CXCR1在正常胃黏膜組織中不表達,其表達于嗜中性粒細胞、單核細胞、內(nèi)皮細胞和部分胃癌組織及腫瘤相關間質(zhì)細胞表面;CXCR1陽性者占51.78%(73/141),CXCR1陰性患者占48.22%(68/141);CXCR1表達與患者性別、年齡、腫瘤大小無關,與胃癌分化(P=0.001 1)、腫瘤的浸潤深度(P=0.017 0)、脈管侵犯(P=0.000 1)、神經(jīng)侵犯(P=0.000 1)和淋巴結轉(zhuǎn)移(P=0.000 1)、TNM分期(P=0.004 1)有關,均提示CXCR1在胃癌的浸潤和轉(zhuǎn)移中起一定作用,與在其他腫瘤[11-14]中的表達和作用的研究結果一致。
本組實驗還發(fā)現(xiàn),CXCR1在胃癌脈管內(nèi)癌栓或胃癌組織中表達,常伴中性粒細胞簇的存在,且中性粒細胞的形態(tài)有差異。有研究報道[18],中性粒細胞在腫瘤微環(huán)境中可被誘導分化為N1和N2兩種亞型,其中N1型核在形態(tài)上呈分葉核,細胞毒性作用強,表達和分泌更多的促炎因子,能夠趨化和誘導更多CD8+T細胞到達腫瘤部位,而抑制腫瘤的進展;而N2型在形態(tài)上細胞核分葉少,呈圓形或不規(guī)則,細胞毒性相對較弱,表達和分泌促炎因子較少,而VEGF等促進血管新生的因子增多,具有明顯的促腫瘤作用。巴賽爾大學等[19]機構科學家研究表明腫瘤細胞會利用中性粒細胞來增強癌癥的轉(zhuǎn)移能力。因此,作者推測腫瘤組織或中性粒細胞、單核細胞表面表達CXCR1,與腫瘤微環(huán)境的主要成分IL-8相互作用,引起主要下游相關信號傳導途徑的激活,從而促進腫瘤的發(fā)展。
綜上所述,胃癌組織中CXCR1表達與腫瘤浸潤、轉(zhuǎn)移有關,對胃癌組織中CXCR1表達與炎癥因子的相互作用分析,為開發(fā)抑制胃癌轉(zhuǎn)移的新型藥物提供參考。

