混合澄清槽萃取過程的瞬態行為及瞬態數學模型
于 婷,何 輝,劉占元,張 嵐,李 崢,趙皓貴,葉國安,*
1.中國原子能科學研究院 放射化學研究所,北京 102413 2.中國科學院 上海應用物理研究所 放射化學與工程技術部,上海 201800
萃取過程瞬態模型可反映萃取設備從啟動到最終動態平衡,設備內兩相液體流速、組成、組分濃度等的變化及分布。穩態模型則為設備達到動態平衡時組成、組分濃度的分布,穩態模型實質上是一種特殊情況的瞬態模型。混合澄清槽是核化工領域普遍采用的一類級式萃取設備,對其瞬態行為進行研究,建立瞬態數學模型,對混合澄清槽啟動至萃取平衡以及停車過程等進行過程透視,可對實際操作過程進行優化,對于工藝運行過程有指導意義[1-2]。
混合澄清槽瞬態模型主要對設備內流體流動行為(物理模型)和萃取行為(化學模型)進行模擬[3]。模型按照模擬對象不同可以分為三類:流體力學行為模擬,萃取行為模擬,同時對流體力學行為和萃取行為進行模擬。兼顧流體力學行為和萃取行為的瞬態模擬因數學模型復雜、難以求解的問題,模擬效果并不理想。流體力學行為瞬態模型多借助商用流體力學軟件,對設備內兩相流體在物理攪動下的混合、分散、聚合以及分相等行為進行模擬,對此過程建模無需考慮傳質行為,流體力學行為最終會體現在對級效率、傳質系數等傳質過程參數的影響上[4]。傳質行為瞬態模擬出于模型簡化、降低計算復雜度的目的,多會忽略流體力學行為影響[5-6]。
國外研究人員針對混合澄清槽的流體力學瞬態模型,開展了一系列研究工作,如Gomes針對澄清室提出的“淺層澄清室模型”(shallow-layer settler),該模型主要針對澄清室中分散帶行為進行模擬,后期Gomes又對模型算法進行了優化[3]。
后處理混合澄清槽萃取過程的數學模擬軟件鮮見詳細報道。可對后處理混合澄清槽萃取行為進行瞬態模擬的模擬軟件僅有SEPHIS系列[7-8]、SOLVEX[9]、PUBG[10]和MIXSET系列[11]。SEPHIS是20世紀80年代美國橡樹嶺國家實驗室開發的系列軟件,所建立的混合澄清槽瞬態模型對同一級的混合室和澄清室分別計算,假設傳質僅在混合室發生,對于混合室中與時間相關的微分方程使用龍格-庫塔數值算法求解,澄清室與時間相關的微分方程簡化成為有限差分形式迭代求解。國際原子能機構(IAEA)開發的模擬軟件PUBG,該軟件中瞬態模型對混合室和澄清室分開計算,其中澄清室的數學模型中與時間相關的微分方程使用龍格-庫塔數值方法求解,混合室瞬態模型則簡化成為穩態形式進行求解。SOLVEX是薩凡納河實驗室開發的一款可以對萃取過程穩態和瞬態計算的流程模擬軟件,建立的瞬態模型與SEPHIS相似。
化工行業也有進行混合澄清槽瞬態行為模擬研究的,建立的瞬態模型對于組分在兩相間分配比恒定的萃取體系,對各級聯立線性方程組進行求解;分配比變化時則使用數值方法求得數值解。后者的瞬態模型中使用傳質速率方程(雙膜模型)求解分配比,但實際上各種組分的傳質速率難以確定且計算耗時,模型求解困難[6]。化工行業現在針對蒸餾、吸收等過程已經開發了大量的穩態和瞬態模擬軟件,如ASPEN、PROII、CHEMCAD等,但這些軟件目前針對級式逆流萃取只能進行穩態模擬,不能進行瞬態模擬計算[2,4]。
掌握混合澄清槽從啟動到穩態運行各級濃度變化以及運行穩態的實現,甚至包括料液流速的變動、組成、濃度變化,以及其他參數變化時混合澄清槽的動態響應,均離不開混合澄清槽瞬態行為的研究和瞬態模型的建立。因此有必要開展混合澄清槽瞬態行為及模型研究,為后續工藝模擬提供技術支持。
1 混合澄清槽瞬態模擬數學模型
1.1 單級模型
混合澄清槽是一種物理界限劃分非常明顯的級式萃取設備,其最小的萃取單元為一級,因此首先對萃取單元進行分析。對混合澄清槽、離心萃取器等級式設備進行穩態模擬時,不需要考慮時間的因素,因此兩相液體在槽子中的停留時間、混合室以及澄清室體積等均不需要考慮;而在瞬態模擬中,這些參數均是預測混合澄清槽性能所需要的參數[4]。
一般認為在混合室發生傳質反應、氧化還原反應等,澄清室一般只發生兩相的分離,則兩相液體在一級中的平均停留時間為:
(1)
其中:t′表示一級的停留時間,Vm為混合室體積,Vs為澄清室體積,L為有機相流速,V表示水相流速。
在實際操作中,料液在混合室中的平均停留時間一般為1~2 min[2],在一級中停留時間為4~8 min,在本模型中選擇一級的停留時間作為最小的時間計算單元,則對于單元時間而言,萃取單元內符合物料守恒,具體濃度表達式如下式:
xj+1,t-1V+yj-1,t-1L+R=xj,tV+yj,tL
(2)
(3)
(4)
式中:x表示水相組分濃度,y表示有機相組分濃度,V為水相流速,L為有機相流速,R表示化學反應項,D為組分在兩相中的分配比,E表示級效率,下標j表示第j級,t表示停留時間單元數。在此需要說明,若是傳質速率控制或者存在化學反應的萃取體系(如硝酸羥胺(HAN)還原反萃Pu(Ⅳ)),其對化學反應項或傳質反應項計算所采用的時長應為實際平均停留時間。第j級萃取模型概念圖示于圖1。
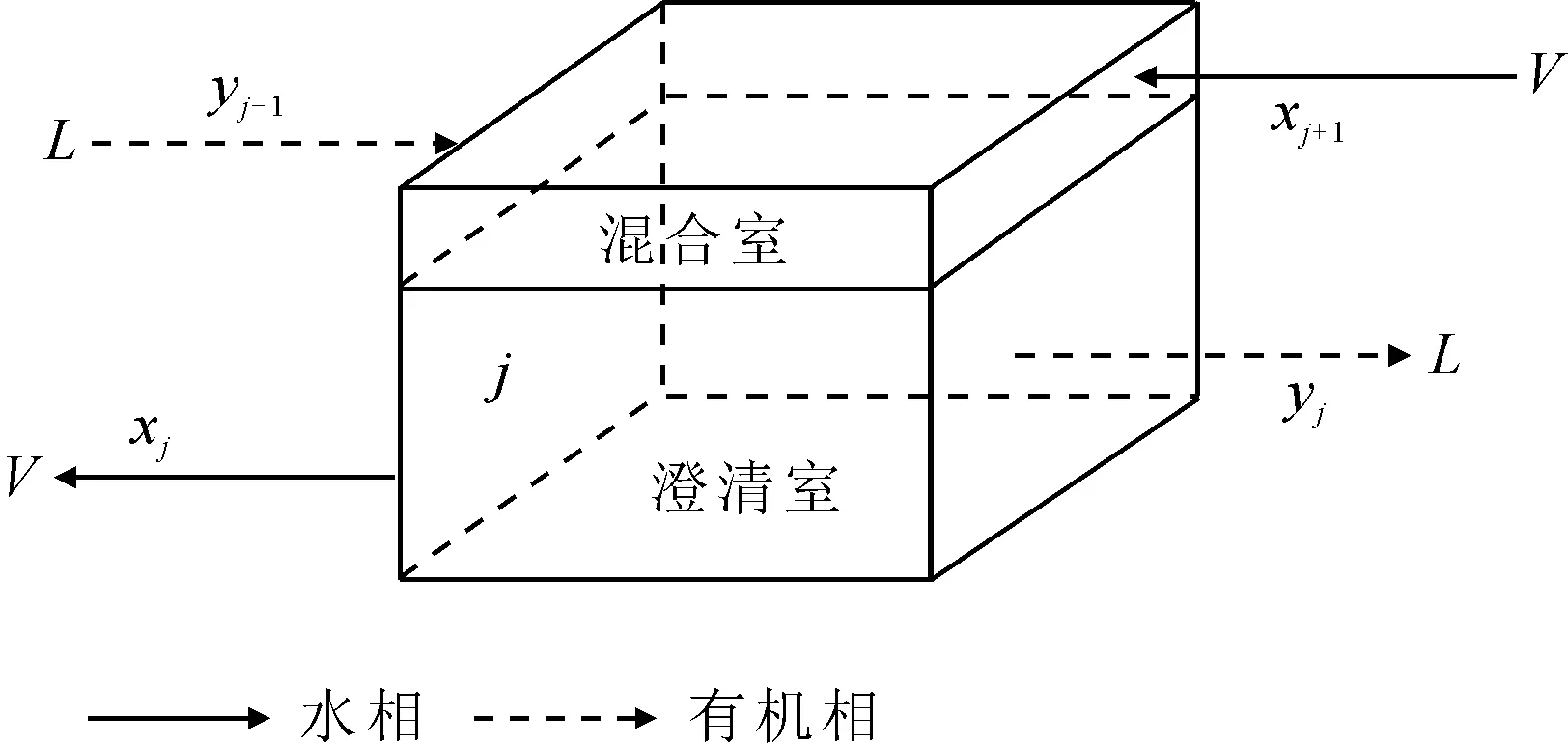
圖1 第j級萃取模型概念圖Fig.1 Conceptual graph of stage j
1.2 級聯瞬態模型
混合澄清槽瞬態模型所需要的參數有:級數、進料口和出料口、混合室體積、澄清室體積(確定停留時間)、級效率(計算得到或者由用戶輸入)等。如圖2所示,一個N級的混合澄清槽,有機相料液AX從第一級進料,水相AF從第N級進料,有機相AP從第N級出料,水相料液AW從第一級出料。
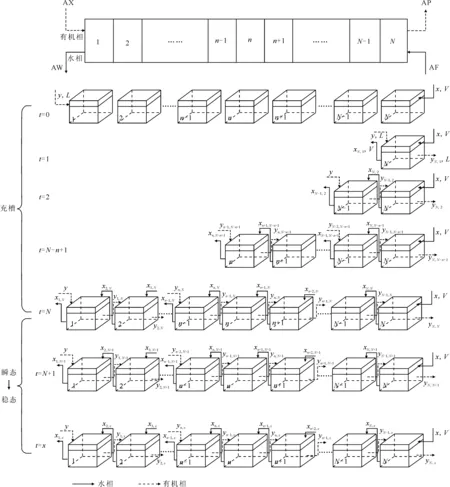
圖2 逆流萃取混合澄清槽瞬態模型概念圖Fig.2 Conceptual graph of counter-current mixer-settler transient model
經過對混合澄清槽運行過程分析,模型假設:啟動時使用不含組分的空白料液充槽,即混合澄清槽中每一級均按照運行相比填充水相和有機相料液;不存在氧化還原反應的萃取過程,每一級的停留時間按照式(1)計算,存在氧化還原反應的萃取過程,在進行反應動力學模型計算時,反應時間按照式(1)計算;以每個停留時間t′作為一個時間間隔進行計算,每個時間間隔結束后,第n級的有機相和水相作為下一時間間隔第n+1級和第n-1級的有機相輸入和水相輸出;假設各級水相和有機相體積在傳質前后無變化。
對于每一級則按物料守恒計算方程求解得到水相和有機相中物料組成。
1.3 瞬態模型算法
以圖2所示的萃取流程,即先使用有機相充槽,之后進含有待萃取組分的水相,瞬態模型的算法具體如下,其中t表示一個停留時間,t=0~N為混合澄清槽充槽階段的瞬態模擬,N+1~∞即為從瞬態到穩態運行的計算過程:
(1)t=0時刻:水相和有機相空白料液按照正常運行時流比充滿混合澄清槽,此時是混合澄清槽開始傳質的臨界時間;
(2)t=1:第N級進行傳質反應,并完成兩相間的傳質,該時間段第N級的水相和有機相輸入組分濃度分別為x和y,流入速率分別為V和L,水相和有機相輸出組分濃度分別為xN,1和yN,1,流出速率不變仍為V和L,下同;
(3)t=2:第N級和第N-1級進行傳質反應,其中第N-1級的水相和有機相輸入組分濃度分別為xN,1和y,輸出組分濃度分別為xN-1,2和yN-1,2,第N級的水相和有機相輸入組分濃度分別為x和y,輸出組分濃度分別為xN,2和yN,2;
(4)t=N:除第N級外,各級的水相輸入均是水相流入方向上一級t=N-1的輸出,第N級的水相輸入組分濃度是x,水相輸出組分濃度為xN,N,除第1級外的各級有機相輸入均是有機相流入方向上一級t=N-1的輸出,第1級的有機相輸入組分濃度為y,有機相輸出組分濃度為yN,N;
(5)t=∞:對于混合澄清槽相鄰兩個停留時間的兩相出口組分濃度進行比較,當濃度差小于設定的某個極小值ε時,則認為混合澄清槽達到穩態運行(或判斷混合澄清槽內是否達到物料守恒,即進入混合澄清槽的物質的量等于流出混合澄清槽的物質的量,則認為混合澄清槽的運行達到動態平衡),輸出不同停留時間的各級濃度。
2 混合澄清槽瞬態行為研究及模型驗證
實驗所用硝酸鈾酰由中國原子能科學研究院提供,其他試劑均為市售分析純。
2.1 HNO3萃取瞬態行為研究
2.1.1HNO3萃取臺架試驗 采用4級5 mL混合澄清槽開展HNO3萃取實驗。有機相為30%(體積分數,下同)TBP/正十二烷,水相為3.20 mol/L HNO3溶液。有機相∶水相(O∶A)體積比為1∶1。采用酸堿滴定法分析HNO3。具體實驗步驟如下:
(1) 使用HNO3濃度為3.20 mol/L的水溶液充槽,水相從水相出口(第1級)流出的時間設為t=0(運行槽體積為0);
(2) 初始時刻為空白有機相進料時刻,有機相從混合澄清槽第4級流出時記為一個槽體積運行時間,分別對各級水相和有機相取樣;
(3) 此后每隔2個停留時間(0.5個槽體積)對4級取水相以及有機相平行樣,直至混合澄清槽穩態運行為止(酸萃取一般3~4個槽體積即可平衡,故需要運行4個槽體積以上),要求水相和有機相取樣量要足夠小,盡量減少對混合澄清槽運行的影響。
(4) 停車后取得各級穩態樣品。
2.1.2結果與討論 混合澄清槽瞬態→穩態實驗結果及同等條件模擬結果列于表1和2。由表1可知,不同運行槽體積下水相酸度計算值與實驗值相對誤差均低于|5%|,有機相酸度計算值與實驗值相對誤差低于|15%|,計算值與實驗值符合良好,從而證明提出的瞬態→穩態算法的可靠性。圖3為4級混合澄清槽萃取實驗濃度剖面圖。由圖3可知,混合澄清槽中30%TBP/正十二烷萃取HNO3達到穩態速度較快,以水相充槽,運行3.0個槽體積即可達到萃取平衡,此時混合澄清槽內各級有機相和水相中HNO3濃度不再發生變化。圖4是混合澄清槽運行不同槽體積時出口水相和出口有機相中HNO3濃度的計算值與實驗值的比對,由圖4可知,實測值和計算值符合良好。
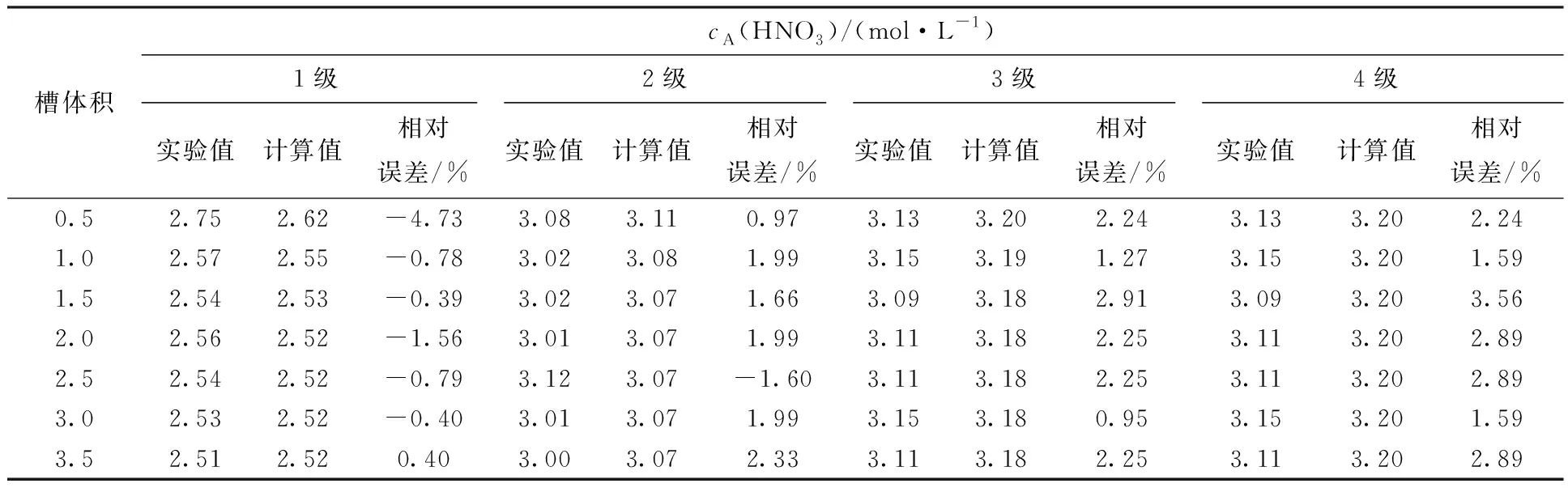
表1 4級混合澄清槽臺架試驗各級水相HNO3濃度(cA(HNO3))計算值與實驗值比對Table 1 Concentration profiles of aqueous HNO3 (cA(HNO3)) in 4-stage mixer-settler contactor
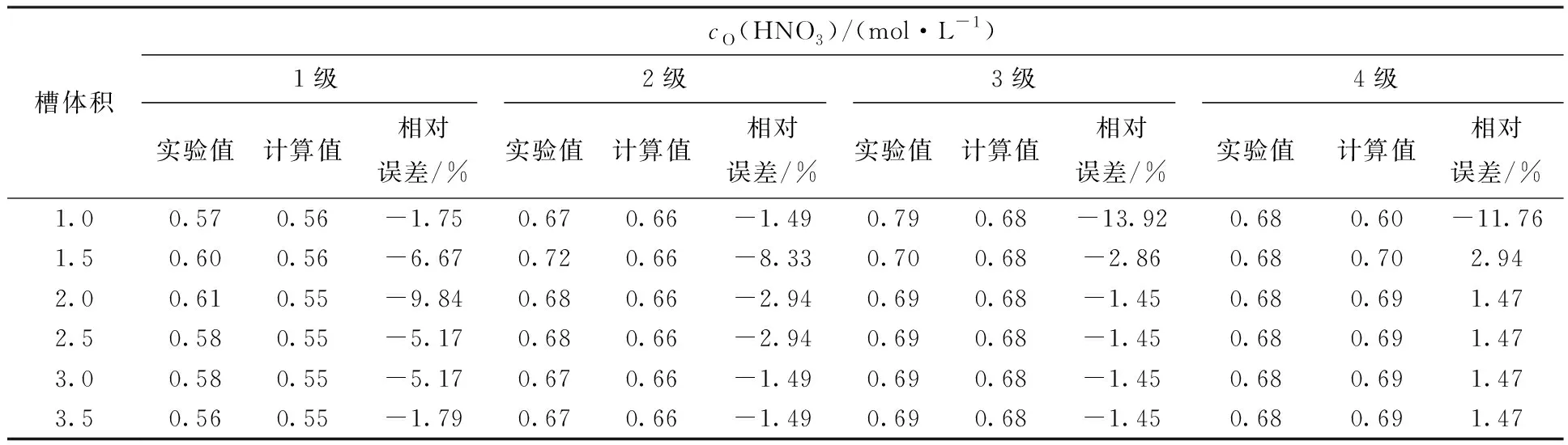
表2 4級混合澄清槽臺架試驗各級有機相HNO3濃度(cO(HNO3))計算值與實驗值比對Table 2 Concentration profiles of organic HNO3 (cO(HNO3)) in 4-stage mixer-settler contactor
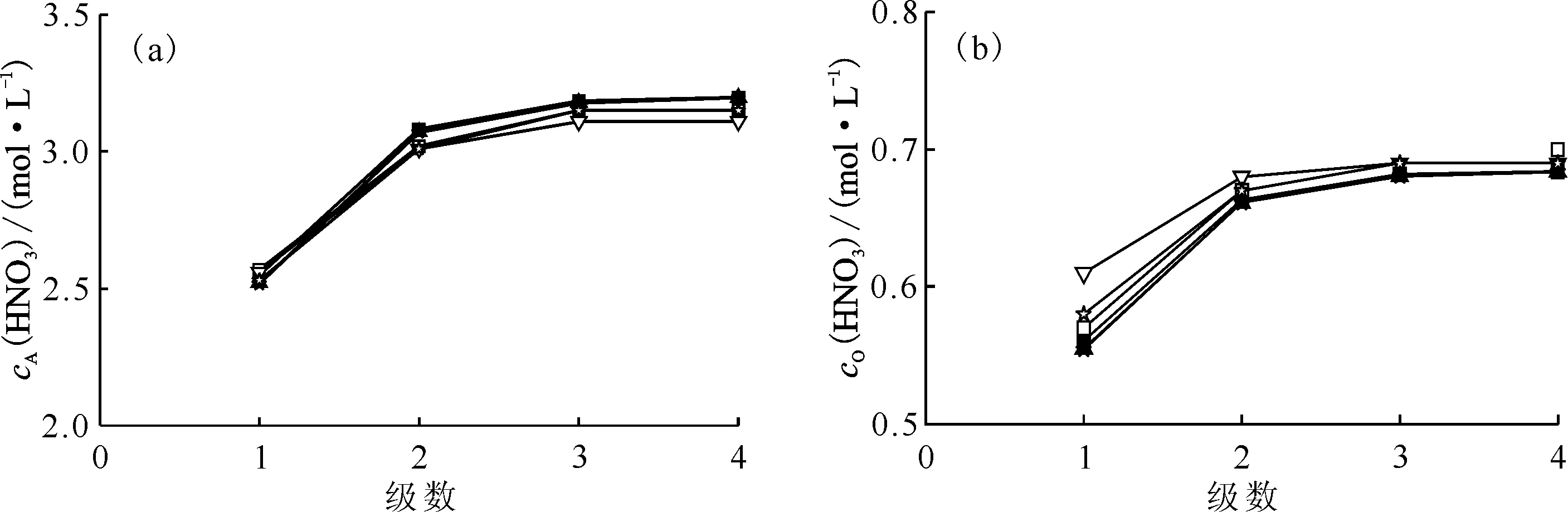
■、▲、★分別表示運行1.0、2.0、3.0個槽體積時的濃度計算值;□、▽、☆分別表示運行1.0、2.0、3.0個槽體積時的濃度實驗值(a)——水相,(b)——有機相圖3 4級混合澄清槽萃取實驗HNO3濃度剖面Fig.3 Concentration profiles of HNO3 in 4-stage mixer-settler contactor
2.2 HNO3-U(Ⅵ)萃取瞬態行為研究
2.2.1HNO3-U(Ⅵ)萃取臺架試驗 采用8級9 mL混合澄清槽(混合室體積為9 mL,澄清室體積為22.5 mL)進行HNO3萃取實驗。有機相為30%TBP/正十二烷,水相為3.03 mol/L HNO3、44.6 g/L U(Ⅵ)溶液;O∶A體積比為1∶1。采用酸堿滴定法分析HNO3濃度。常量U的水相樣品使用METTLER TOLEDO T70電位滴定儀,利用硫酸亞鐵還原-重鉻酸鉀氧化滴定法(GB 11841-89)進行分析;微量U的水相樣品用w=2% HNO3稀釋適當倍數后,使用電感耦合等離子體發射光譜儀(ICP-OES)分析。有機相U濃度分析,先使用0.5 mol/L(NH4)2CO3溶液反萃有機相U(反萃相比A∶O體積比10∶1),后按水相U濃度分析方法進行分析。具體實驗步驟如下:
(1) 使用3.03 mol/L HNO3、44.6 g/L U(Ⅵ)溶液充槽,水相從水相出口(第1級)流出的時間設為t=0(運行槽體積為0);
(2) 初始時刻為空白有機相進料時刻,有機相從混合澄清槽第8級流出時記為一個槽體積運行時間,分別對各級水相和有機相取樣;
(3) 此后每隔4個停留時間(0.5個槽體積),對8級取水相以及有機相平行樣,直至混合澄清槽穩態運行為止(共運行6個槽體積),要求水相和有機相取樣量要足夠小,盡量減少對混合澄清槽運行的影響;
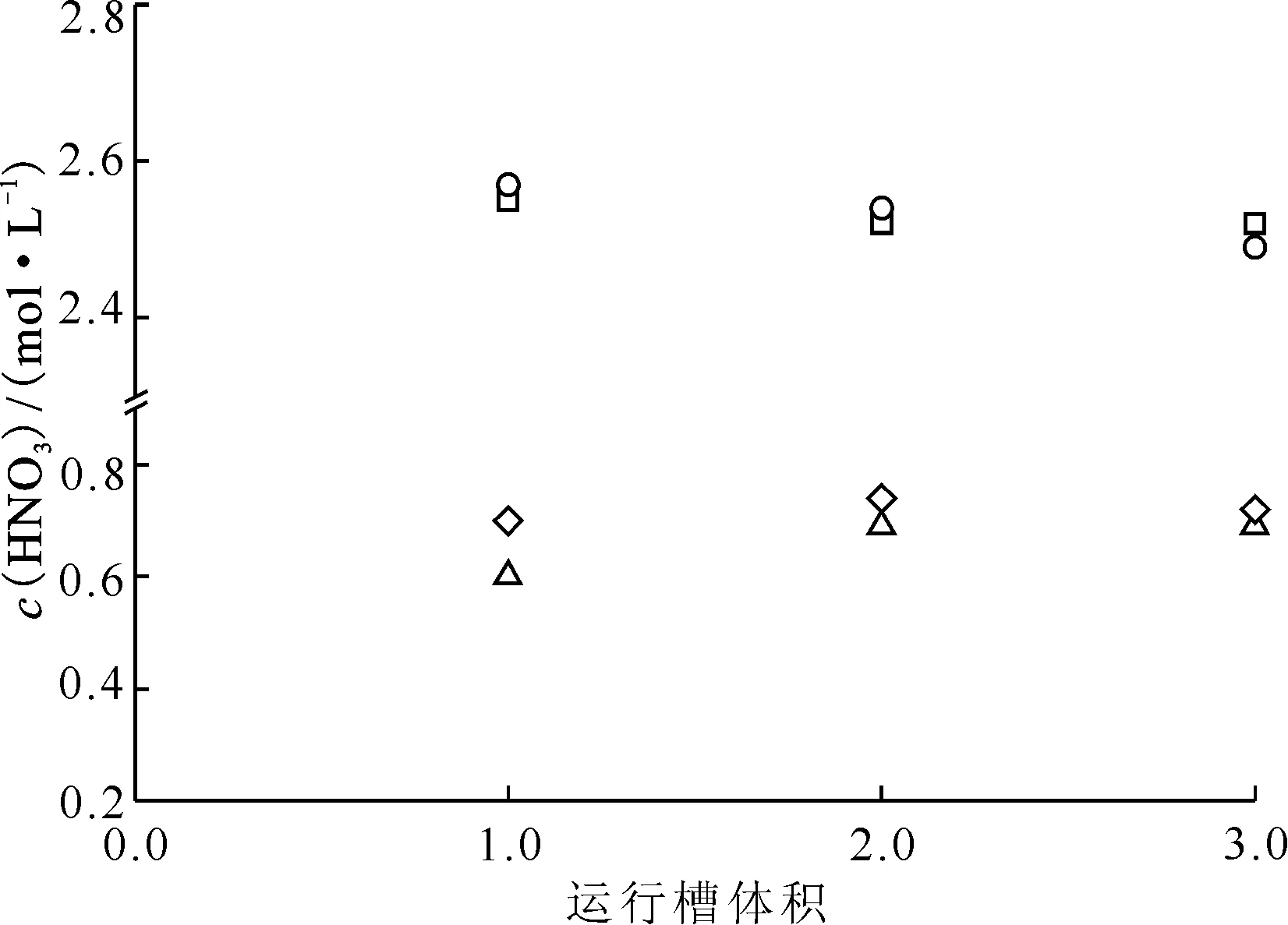
○——水相出口料液HNO3濃度的實驗值,□——水相出口料液HNO3濃度的計算值,◇——有機相出口料液HNO3濃度的實驗值,△——有機相出口料液HNO3濃度的計算值圖4 4級混合澄清槽兩相出口HNO3濃度計算值與實驗值比對Fig.4 HNO3 concentrations in outlet of 4-stage mixer-settler contactor
(4) 臺架試驗結束后取各級平衡態樣品,分析其中的U濃度及酸濃度。
2.2.2結果與討論 HNO3-U(Ⅵ)萃取混合澄清槽瞬態→穩態實驗運行不同槽體積的實驗結果及同等條件模擬計算結果列于表3—6。由表3和表5可知,在不同運行槽體積時,各級水相酸度計算值和實驗值相對誤差低于|6%|,各級有機相酸度計算值和實驗值相對誤差基本低于|10%|,計算值與實測值符合良好。由表4和表6可知,水相及有機相中U濃度的計算值和實驗值相對誤差隨混合澄清槽運行槽體積的增大逐漸降低,最終穩態時有機相出口端水相及有機相U濃度計算值和實驗值基本符合,通過計算發現模型計算比混合澄清槽實際運行更快達到穩態,分析原因是在實際實驗過程中混合澄清槽每一級級效率低于100%導致實際結果偏離理論計算值所致。圖5是萃取實驗運行不同槽體積時水相及有機相出口HNO3、U濃度值。由圖5可知,兩相出口HNO3濃度基本不隨槽體積的變化而變化,U濃度受運行槽體積的變化影響較大,這說明在HNO3-U(Ⅵ)萃取體系中,酸較U更快達到萃取平衡,HNO3-U(Ⅵ)萃取體系基本在運行2~3個槽體積即可達到穩態運行。實驗值和計算值基本符合良好,證明了所提出的瞬態→穩態模型算法的正確性。圖6為8級混合澄清槽運行達到穩態時,各級水相和有機相中HNO3、U濃度剖面。由圖6可知,計算軟件的穩態計算值和實驗值符合良好。
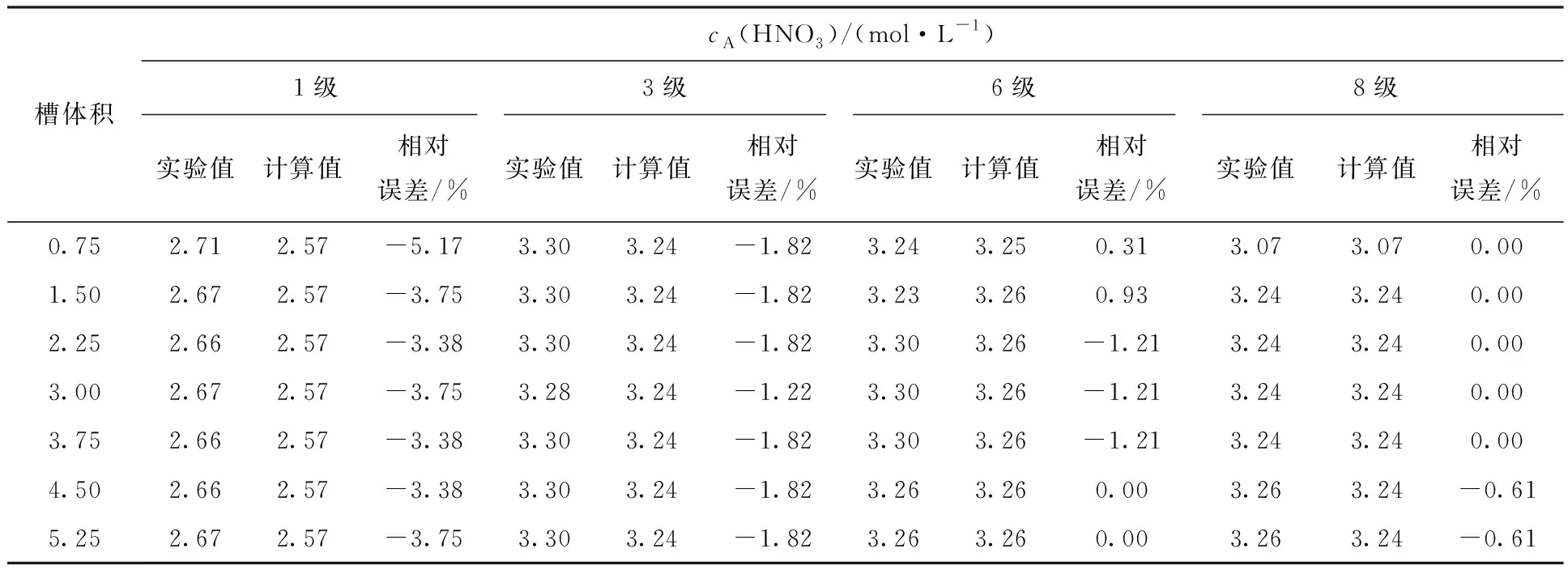
表3 8級混合澄清槽臺架試驗各級水相HNO3濃度計算值與實驗值比對Table 3 Concentration profiles of aqueous HNO3 in 8-stage mixer-settler contactor
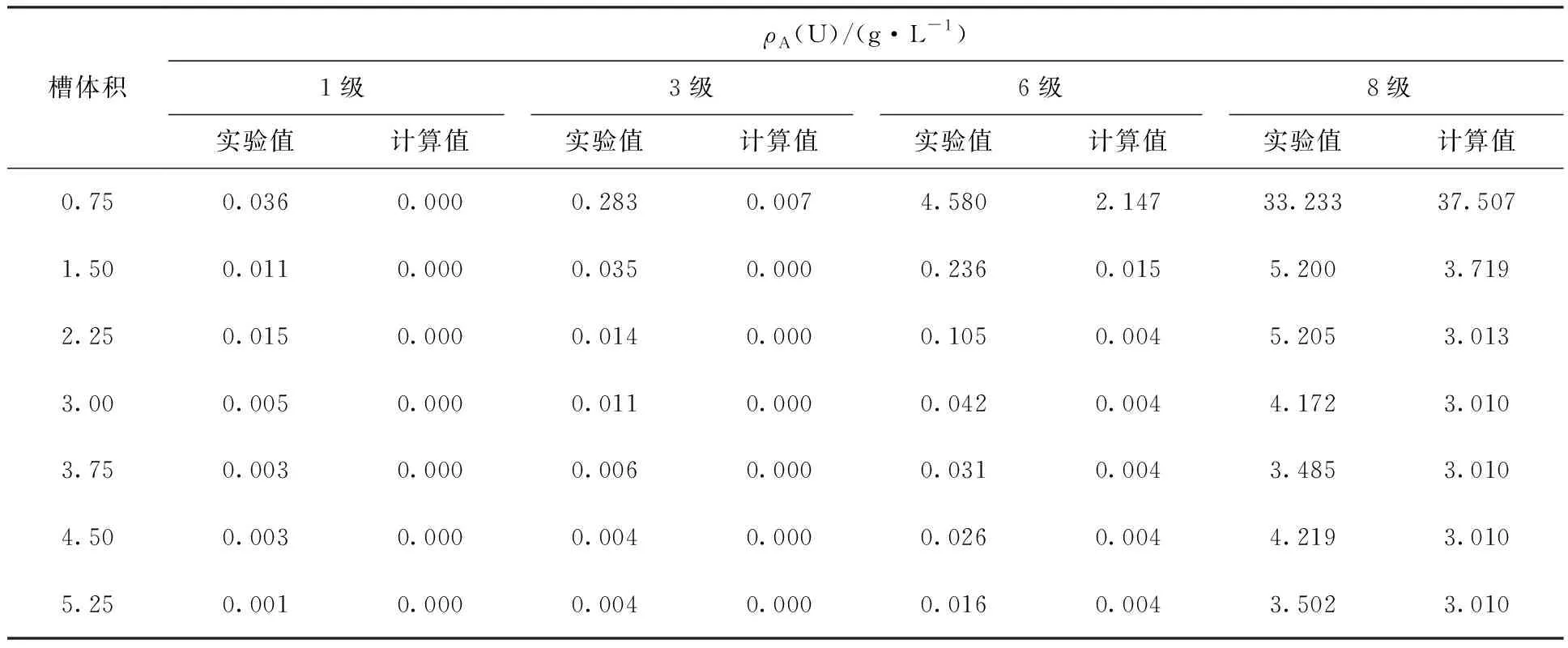
表4 8級混合澄清槽臺架試驗各級水相U濃度計算值與實驗值比對Table 4 Concentration profiles of aqueous U in 8-stage mixer-settler contactor
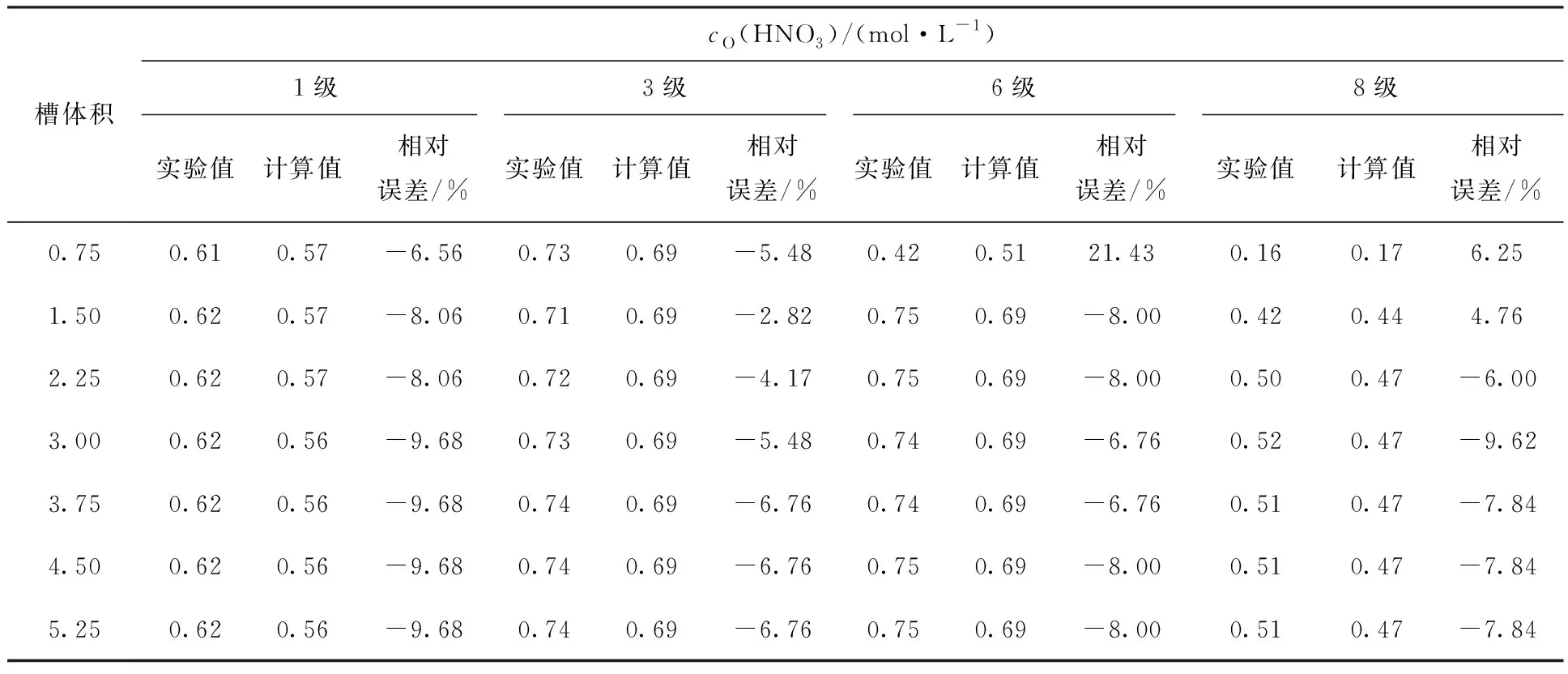
表5 8級混合澄清槽臺架試驗各級有機相HNO3濃度計算值與實驗值比對Table 5 Concentration profiles of organic HNO3 in 8-stage mixer-settler contactor

表6 8級混合澄清槽臺架試驗各級有機相U濃度計算值與實驗值比對Table 6 Concentration profiles of organic U in 8-stage mixer-settler contactor
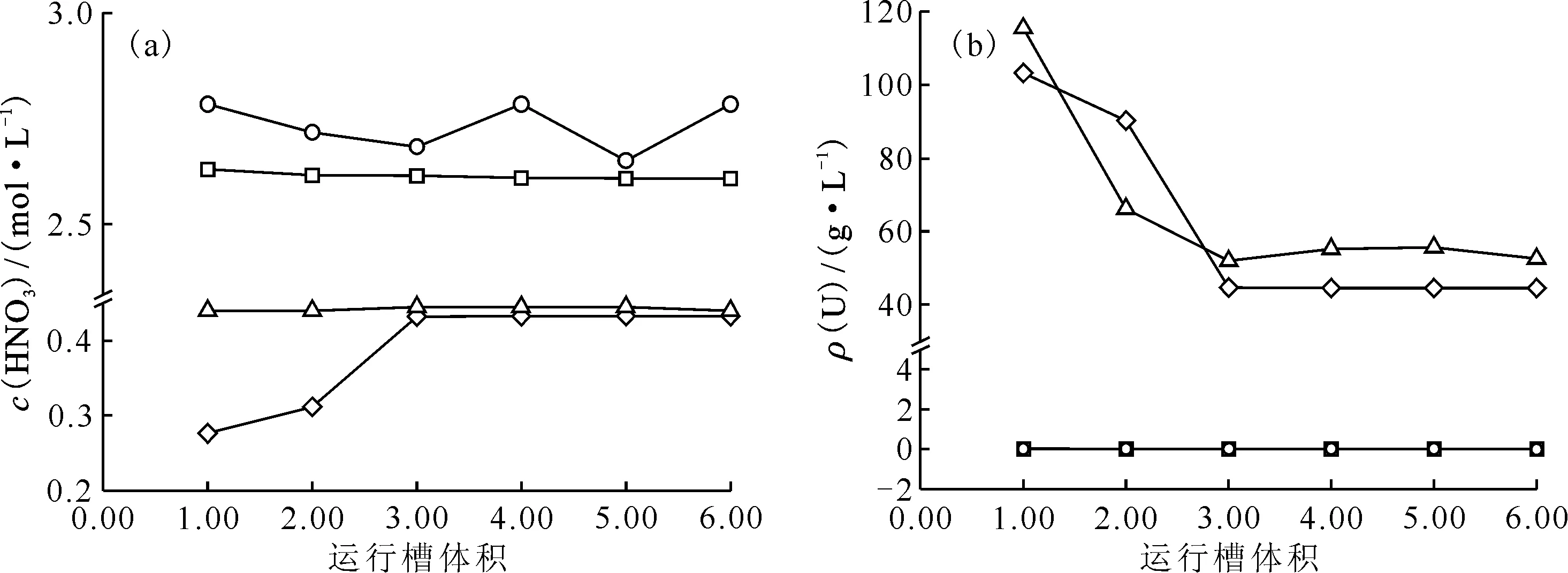
(a)——HNO3,(b)——U○——水相出口濃度實驗值,□——水相出口濃度計算值,◇——有機相出口濃度計算值,Δ——有機相出口濃度實驗值圖5 8級混合澄清槽萃取實驗運行不同槽體積時出口組分濃度Fig5 Concentrations in outlet of 8-stage mixer-settler contactor in different flow volumn
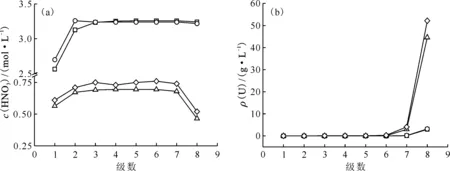
(a)——HNO3,(b)——U○——水相出口濃度實驗值,□——水相出口濃度計算值,Δ——有機相出口濃度計算值,◇——有機相出口濃度實驗值圖6 8級混合澄清槽萃取實驗穩態時各物質濃度剖面Fig.6 Equilibrium concentration profile of 8-stage mixer-settler contactor
3 計算研究
3.1 酸萃取計算研究
使用編寫的混合澄清槽瞬態模擬計算程序對混合澄清槽運行瞬態→穩態的影響因素進行了研究,首先進行了HNO3萃取的計算,在8級混合澄清槽、操作溫度為25 ℃條件下,分別對使用水相充槽和有機相充槽所需要的平衡槽體積進行研究,計算初始條件以及計算結果列于表7。由表7結果可知,對于單HNO3萃取而言,使用含有萃取組分的水相或使用空白萃取相充槽,混合澄清槽達到穩態所需要的運行槽體積是不同的,有機相充槽所需要的槽體積要比水相充槽所需的槽體積要多,即萃取過程中使用萃取相(有機相)充槽,所需要的槽體積要比使用水相充槽的槽體積要多。圖7(a)—(e)分別表示表7編號為1、2、3、4、5萃取條件時的混合澄清槽運行達到穩態后的各級水相和有機相中HNO3的濃度分布。由圖7可知,使用有機相充槽和水相充槽,混合澄清槽運行達到穩態(動態平衡)后各級有機相和水相中HNO3濃度值相同。使用水相和有機相充槽到達混合澄清槽穩態運行時所需要的時間不同,但最終穩態結果相同。
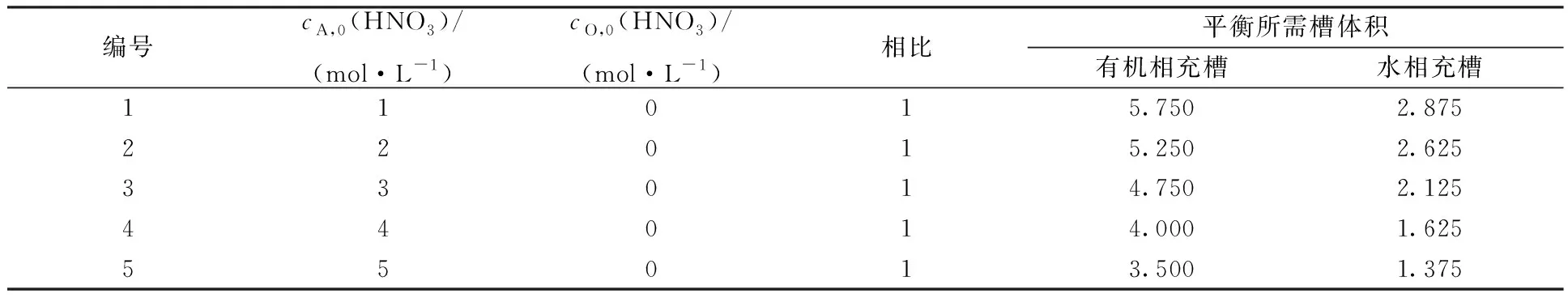
表7 HNO3萃取混合澄清槽瞬態→穩態運行所需槽體積Table 7 Flow volumn needed to achieve mass-transfer equilibrium
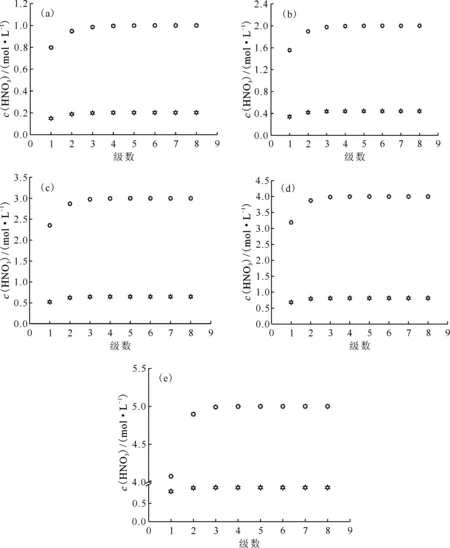
◇——有機相充槽時平衡水相濃度,□——水相充槽時平衡水相濃度,Δ——有機相充槽時平衡有機相濃度, ▽——水相充槽時平衡有機相濃度萃取條件:(a)——表7編號1,(b)——表7編號2,(c)——表7編號3,(d)——表7編號4,(e)——表7編號5圖7 不同萃取條件下8級混合澄清槽穩態運行時HNO3濃度剖面Fig.7 Equilibrium concentration profile of HNO3 in 8-stage mixer-settler contactor at different extraction conditions
3.2 鈾、钚萃取計算研究
使用編寫的混合澄清槽萃取瞬態模擬計算程序對混合澄清槽運行瞬態→穩態的影響因素進行了研究(表8),使用有機相充槽,混合澄清槽為8級,操作溫度為25 ℃,計算對象為HNO3、U(Ⅵ)-HNO3、Pu(Ⅳ)-HNO3。
將一個槽體積運行時間作為一個計算時間單元,由計算得到不同運行槽體積的HNO3濃度,以及U(Ⅵ)、HNO3、Pu(Ⅳ)的濃度剖面,具體示于圖8—12。
由圖8可知,表8中編號7的萃取條件下,30%TBP/正十二烷對HNO3的萃取運行3.00個槽體積時即達到穩態,即運行3.00個槽體積后,各級有機相中HNO3濃度不再隨時間變化而變化,整個混合澄清槽達到動態平衡(進入混合澄清槽的HNO3的量等于流出槽體的HNO3的量)。
HNO3和U(Ⅵ)混合體系的萃取(萃取條件如表8中編號21)模擬計算結果示于圖9和圖10。從圖9、10可以看出,各級有機相中酸濃度隨著萃取時間變長而增大,萃取運行4.00個槽體積時,整個混合澄清槽達到穩態,實現動態平衡,各級有機相中HNO3濃度剖面和U(Ⅵ)濃度剖面不再改變。且對比圖9和圖10可知,HNO3和U(Ⅵ)共萃時,各級有機相中HNO3達到萃取平衡所需要的時間要比U(Ⅵ)達到萃取平衡所需要的時間更長。由圖9、10可知,不同槽體積時各級有機相中HNO3濃度變化較大,而U(Ⅵ)濃度對運行槽體積并不敏感,運行槽體積為2.00、3.00、4.00時,各級濃度無太大差異。分析原因是HNO3濃度是U(Ⅵ)萃取的主要影響因素,不同運行槽體積時,水相入口端(第8級)的HNO3濃度并無明顯變化,則對于U(Ⅵ)萃取影響有限,雖然從第8級到第1級HNO3濃度變化范圍較大,然而理想萃取條件下(級效率為100%),第5級至第1級的水相中U(Ⅵ)濃度已經很低,此時酸度對于U(Ⅵ)的萃取影響程度有限。
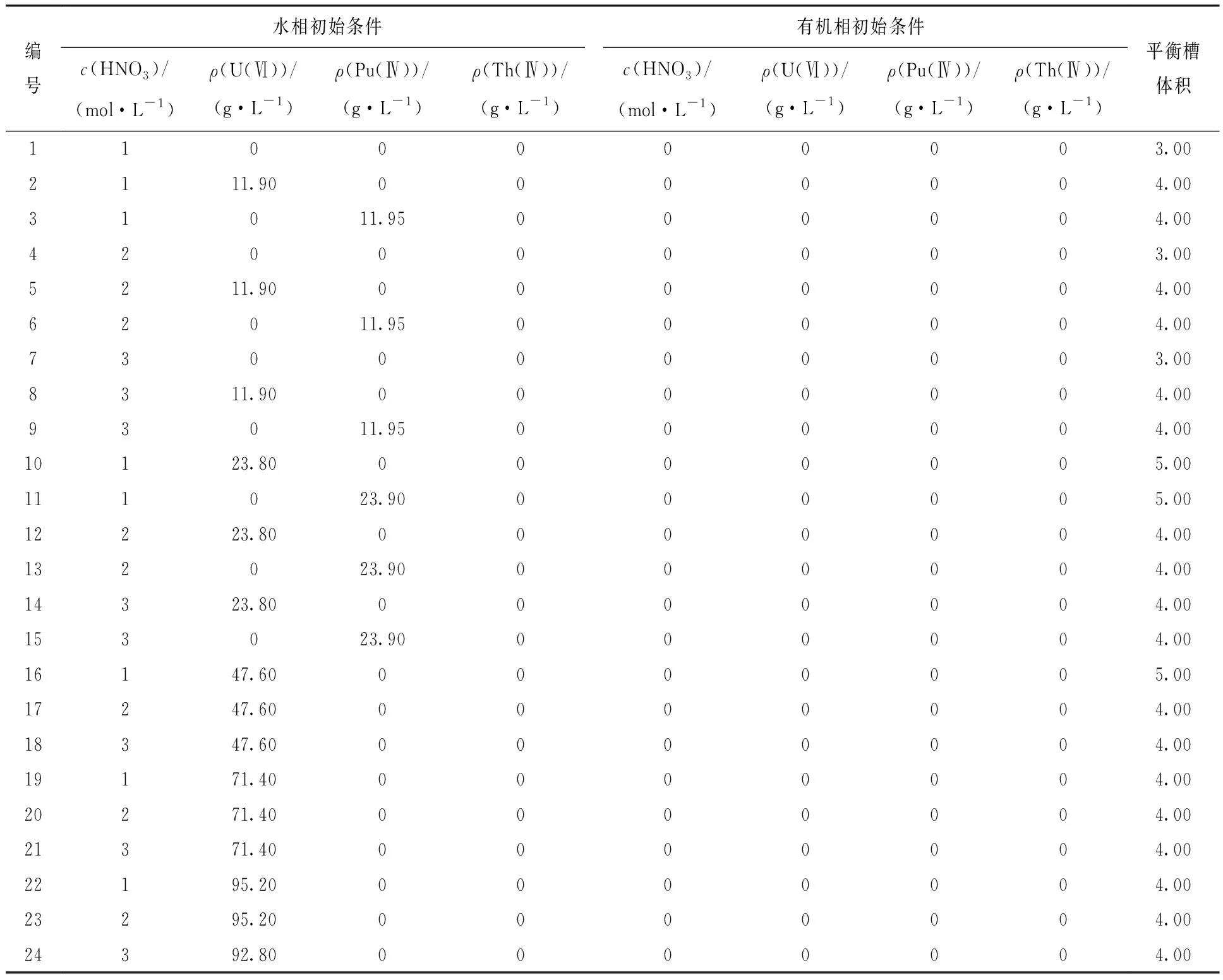
表8 金屬M(U(Ⅵ)、Pu(Ⅳ))萃取混合澄清槽瞬態→穩態運行所需槽體積Table 8 Flow volumn needed to achieve mass-transfer equilibrium in extractions of metal ions(U(Ⅵ), Pu(Ⅳ))
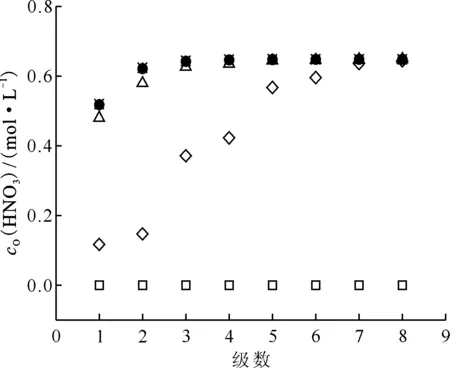
運行槽體積:□——0,◇——1.00,Δ——2.00,●——3.00,×——4.00,*——4.50圖8 表8編號7萃取條件下運行不同槽體積時有機相HNO3濃度剖面Fig.8 Concentration profiles of organic HNO3in mixer-settler contactor at different flow volumn at No.7 of table 8
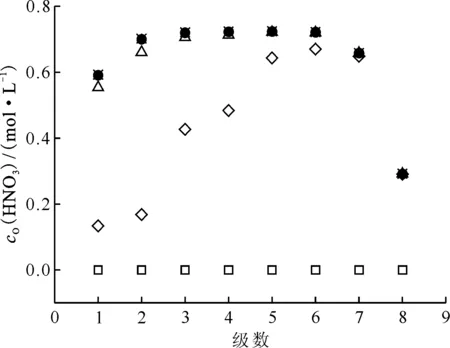
運行槽體積:□——0,◇——1.00,Δ——2.00,●——3.00,×——4.00,*——4.50圖9 表8編號21萃取條件下運行不同槽體積時各級有機相HNO3濃度剖面Fig.9 Concentration profiles of organic HNO3 in mixer-settler contactor at different flow volumn at No.21 of table 8
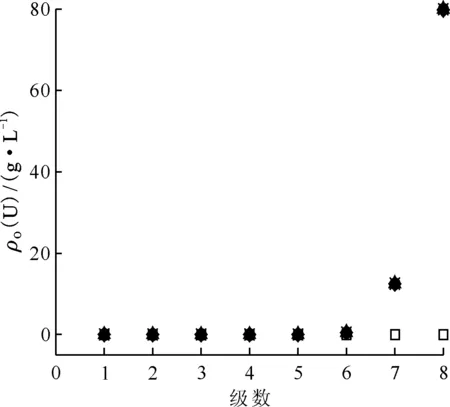
運行槽體積:□——0,◇——1.00,Δ——2.00,●——3.00,×——4.00,*——4.50圖10 表8編號21萃取條件下運行不同槽體積時各級有機相U(Ⅵ)濃度剖面Fig.10 Concentration profiles of organic U(Ⅵ) in mixer-settler contactor at different flow volumn at No.21 of table 8
HNO3和Pu(Ⅳ)混合體系的萃取(萃取條件如表8編號15)模擬計算結果示于圖11、12。從圖11、12可以看出,各級有機相中酸濃度隨著時間增長而增大,運行4.00個槽體積時,整個混合澄清槽達到穩態,實現動態平衡,各級HNO3濃度剖面和Pu(Ⅳ)濃度剖面不再改變。與HNO3-U(Ⅵ)萃取過程相似,各級有機相中HNO3達到萃取平衡所需要的時間要比Pu(Ⅳ)達到萃取平衡所需要的時間更長,運行不同槽體積時,有機相中HNO3濃度變化較大,如在運行1.00個槽體積時,第1級中有機相HNO3濃度為0.1 mol/L,運行2.00個和3.00個槽體積時,第1級HNO3濃度為0.55 mol/L和0.6 mol/L,而第1級有機相中Pu(Ⅳ)濃度基本無變化,第5級至第1級的Pu(Ⅳ)濃度無明顯變化,原因與前文U(Ⅵ)萃取過程濃度變化原因相似。
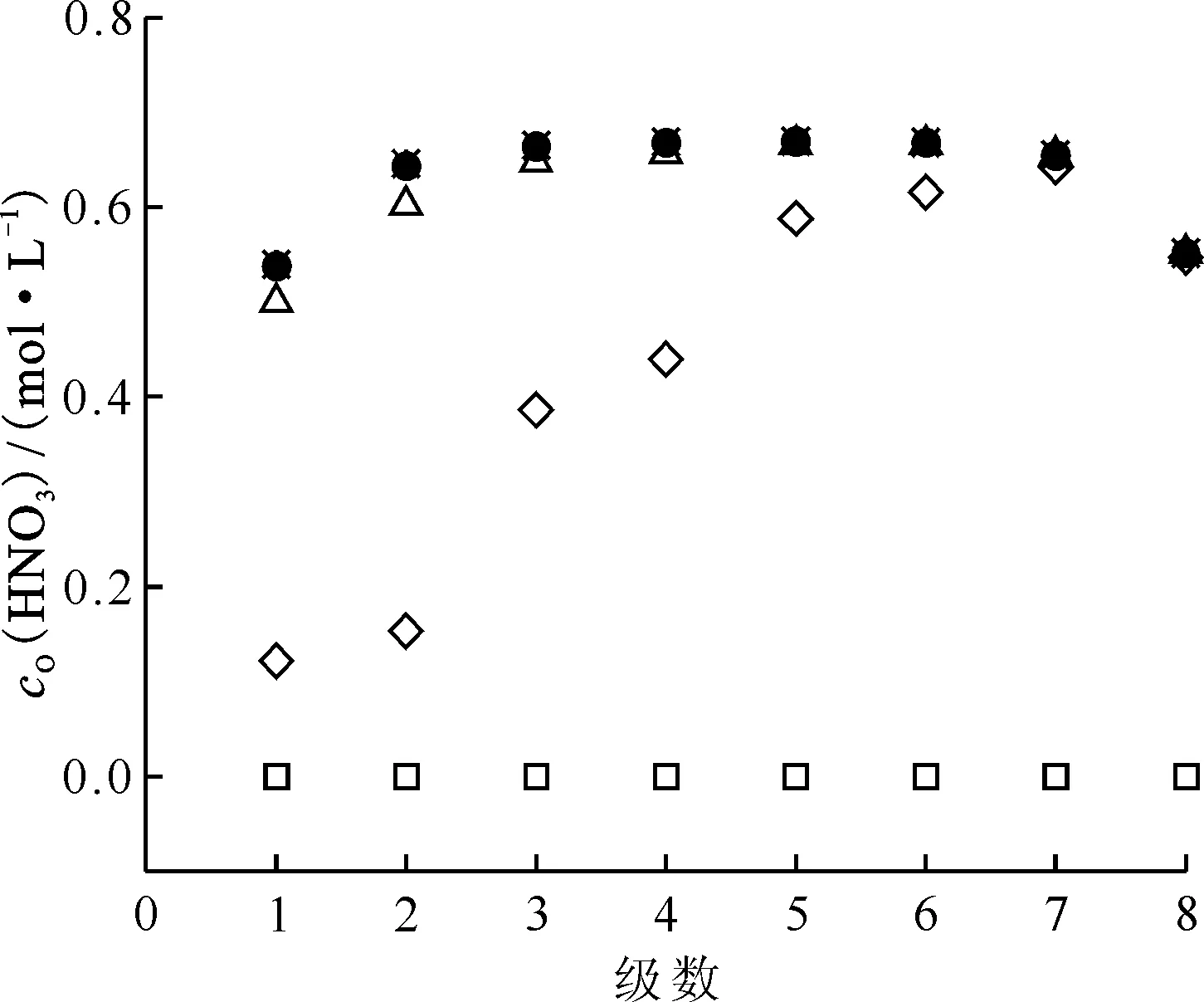
運行槽體積:□——0,◇——1.00,Δ——2.00,●——3.00,×——4.00,*——4.50圖11 表8編號15萃取條件下運行不同槽體積時各級有機相HNO3濃度剖面Fig.11 Concentration profiles of organic HNO3 in mixer-settler contactor at different flow volumn at No.15 of table 8
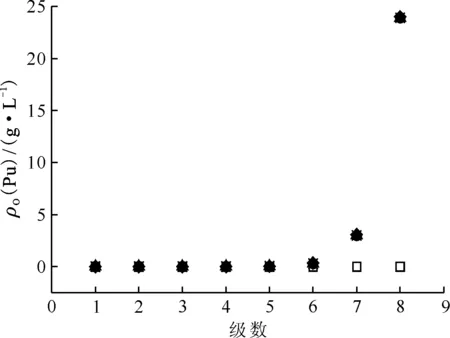
運行槽體積:□——0,◇——1.00,Δ——2.00,●——3.00,×——4.00,*——4.50圖12 表8中編號15萃取條件下運行不同槽體積時各級有機相Pu(Ⅳ)濃度剖面Fig.12 Concentration profiles of organic Pu(Ⅳ) in mixer-settler contactor at different flow volumn at No.15 of table 8
由圖8—12、表8可知,以8級混合澄清槽為萃取設備,各級級效率為100%理想情況下,瞬態→穩態的過渡主要受酸度影響,HNO3濃度為3 mol/L時,不同萃取體系達到穩態運行所需要的運行槽體積基本為4個,分析原因是酸度是金屬M兩相分配比的主要影響因素。
4 結 論
(1) 使用4級及8級小型混合澄清槽臺架試驗數據對混合澄清槽瞬態→穩態過程數學模型進行驗證,模型計算結果與實驗結果吻合良好,證明提出的瞬態模型及算法可靠;
(2) 使用模型計算研究發現,萃取過程使用水相和有機相充槽達到穩態(動態平衡)所需要的運行槽體積不同,水相充槽所需要的槽體積要小于有機相充槽所需要的槽體積;
(3) 模型計算發現,30%TBP/正十二烷萃取HNO3-U(Ⅵ)、HNO3-Pu(Ⅳ)過程,HNO3是萃取平衡主要的影響因素。

