內皮抑素和血管抑素融合基因在桿狀病毒中的表達及抗肝癌效果評價
王志昇 李夢婷 姬勇敢 楊萌萌
寧夏醫科大學1實驗動物中心,2藥學院(銀川750004)
原發性肝癌是我國常見的惡性腫瘤之一,全世界每年約有85.4 萬例新發患者,其中約50%發生在我國,并呈逐年上升趨勢,現有的治療手段如手術、放療、化療等都有不同的弊端,無法徹底根除[1-2]。隨著分子生物學的發展,基因治療已成為治療腫瘤最具潛力的方法之一。基因治療要想成功實施,靶基因的選擇至關重要。眾所周知,原發腫瘤的發展以及轉移關鍵依靠新生血管的生成來提供氧氣和營養。因此,內皮抑素、血管抑素基因等抗血管生成基因治療作為一種抗癌策略廣受關注[3]。內皮抑素是膠原ⅩⅧ的C 末端水解片段,是研究最廣泛的內源性血管生成抑制劑之一。血管抑素是纖溶酶原內部蛋白水解片段的四個Kringle結構域中的第一個,被認為是一種有效的內源性血管生成抑制劑。目前血管抑素和內皮抑素已在不同的表達系統如慢病毒[4]、腺相關病毒[5]以及減毒鼠傷寒沙門氏菌[6]等獲得了表達,并在不同的腫瘤模型中表現出了一定的抗腫瘤潛力。然而,這些病毒或細菌載體在人體內的生物安全性有待進一步驗證。與這些病原體相比,桿狀病毒是一種昆蟲病毒,對哺乳動物和人類無致病性,但能有效進入多種哺乳動物細胞這一特點使其成為良好基因傳遞潛能的載體。因此,本研究為了提高抗血管生成基因治療的效果和安全性,擬以桿狀病毒為載體,表達由人內皮抑素和血管抑素組成的融合蛋白(human endostatin and angiostatin,hEA),以此來評價桿狀病毒介導的hEA 的抗血管生成功能和抗肝癌效果。
1 材料與方法
1.1 材料
1.1.1 質粒、菌株和細胞pFastBac DUAL 質粒購自美國Thermo 公司;pUNO1-hEndo18Angio 質粒購自美國InvivoGen 公司;pEGFP-C1 質粒、大腸埃希菌DH10Bac 感受態細胞、昆蟲Sf-9 細胞、人肝癌細胞HepG2 和人臍靜脈內皮細胞HUVEC 由寧夏醫科大學實驗動物中心保存。Sf-9 細胞在含有10 %胎牛血清(FBS)的Grace 昆蟲培養基(含3.3 g/L 水解乳蛋白和3.3 g/L 酵母提取物)于27 ℃生化培養箱中培養;HepG2 和HUVEC 細胞用含有10 % FBS的DMEM 培養基于37 ℃、5%CO2培養箱中培養。
1.1.2 實驗動物4~6 周齡,體質量為18~22 g,SPF 級雄性BALB/c 裸小鼠由寧夏醫科大學實驗動物中心提供。實驗動物飼養在寧夏醫科大學實驗動物中心標準化的SPF 級動物屏障環境中,動物實驗方案經由寧夏醫科大學實驗動物福利倫理審查委員會審核并獲得批準。
1.1.3 主要試劑各種內切酶、T4 DNA 連接酶、Taq DNA 聚合酶和dNTP 購自美國Thermo 公司;DNA Marker 購自南京諾唯贊生物公司;質粒回收試劑盒、DNA 凝膠回收試劑盒購自北京天根生化科技公司;MTT 試劑盒、BCA 試劑盒購自江蘇凱基生物;丁酸鈉購自Sigma 公司;FBS、Grace 昆蟲細胞培養基、DMEM 培養基及Lipofectamine 2000 購自Gibco 公司;Angiostatin ELISA 試劑盒購自南京云克隆公司;Matrigel 基質膠購自美國康寧公司;其他試劑均為國產分析純。
1.1.4 主要儀器PCR 儀(T100,美國BIORAD 公司);全波長酶標儀(Multiskan FC,美國Thermo 公司);倒置顯微鏡(Axio Vert.A1,德國蔡司公司);高速冷凍離心機(Centrifuge 5430R,美國Eppendorf 公司);CO2培養箱(Forma 311,美國Thermo 公司)。
1.2 方法
1.2.1 pBac-ChEA 質粒的構建以質粒pFastBac DUAL 為骨架,將pPh 啟動子替換為CMV 啟動子,CMV 啟動子從pEGFP-C1 質粒通過引物CMV-F:5′-CGCGGTATACTAGTTATT AATAGTAATCAA-3′和CMV-R:5′-GCGGGATCCGGATCTGACGGTTCACTAAAC-3′擴增獲得(下劃線為分別引入的BST Z17I和Bam HI 酶切位點),獲得的重組質粒命名為pBac-CMV。以質粒pUNO1-hEndo18Angio 為模板,設計引物hEA-F:5′-TCAGGATCCCGCCACCA-TGTAC AGGATGCAACTC-3′和hEA-R:5′-GCGAAGCTTTCATACAACACTCGCTTCTGT-3′(下劃線為分別引入的Bam HI 和Hind III 酶切位點),用于擴增hEndo18Angio(hEA)基因,將hEA PCR 產物雙酶切回收后插入同樣位點酶切后的pBac-CMV 質粒中,獲得的重組質粒命名為pBac-ChEA。
1.2.2 重組病毒粒子的獲得重組病毒的獲得按照Bac-to-Bac(Invitrogen)表達系統說明書操作。將pBac-ChEA 轉化DH10Bac 感受態細胞,經三抗(卡那霉素、慶大霉素和四環素)篩選,提取桿狀病毒DNA,經由Lipofectamine 2000 轉染Sf-9 細胞,27 ℃培養,待細胞大部分從瓶底脫落時,收集細胞培養液,離心取上清液,作為原毒種P1 代毒,再以1 MOI 的重組病毒量繼續感染Sf-9 細胞,完成重組病毒的增殖,直至P3 代毒,分裝,-80 ℃凍存備用。對照質粒pBac-CMV 按照同樣方法處理。經PCR 鑒定正確的重組病毒分別命名為Bac-ChEA和Bac-CMV,病毒的滴度通過噬斑實驗測定。
1.2.3 在HUVEC 細胞中的表達將Bac-ChEA 和Bac-CMV 以MOI 400 轉導HUVEC 細胞,所加入的病毒先用昆蟲培養基稀釋,然后與不含NaHCO3的DMEM 培養基配成1∶4 的比例,然后將混合培養液加入細胞中,使其完全覆蓋細胞,于27 ℃,搖床上孵育5~6 h,吸出培養液,加入含有3 mmol/L 丁酸鈉的DMEM 完全培養基,于37 ℃,5% CO2培養箱中培養24 h,第2 天更換為不含丁酸鈉的DMEM完全培養基繼續培養,直到第3 天收集細胞,按照Angiostatin ELISA 試劑盒說明書的方法進行操作,最后用酶標儀在450 nm 處檢測各孔的吸光度值,然后根據標準曲線計算出各組hEA 蛋白的濃度。
1.2.4 對HUVEC 細胞增殖能力的影響將HUVEC 細胞接種于96 孔板中(4 × 103個/孔),待細胞貼壁后,將Bac-ChEA 和Bac-CMV 以MOI 400 轉導HUVEC 細胞,對照組為不含病毒的空轉導組。直到第3 天,每孔加入50 μL 1×MTT 試劑繼續培養4 h,然后吸出上清液,加入150 μL DMSO,立即通過酶標儀在490 nm 波長下測定其吸光度值。細胞存活率(%)=OD實驗組/OD對照組×100%
1.2.5 對HUVEC細胞遷移能力的影響將HUVEC細胞接種于6 孔板中(7 × 105個/孔),待細胞貼壁 后,將Bac-ChEA 和Bac-CMV 以MOI 400 轉 導HUVEC 細胞,對照組為不含病毒的空轉導組,過夜培養后棄去細胞培養液,用槍頭在每孔中筆直劃一條線,使其成為無細胞區域,用PBS 清洗后加入含有1 % FBS 的DMEM 培養基于37 ℃,5 % CO2培養箱中繼續培養24 h,分別于培養開始時和培養24 h 時在倒置顯微鏡下拍照,最后用Image J 軟件統計劃痕縮小的面積。
1.2.6 對HUVEC 細胞血管形成能力的影響將Bac-ChEA 和Bac-CMV 以MOI 400 轉 導HUVEC 細胞,對照組為不含病毒的空轉導組,72 h 后消化并收集細胞。用Matrigel 基質膠包被96 孔培養板,37 ℃孵育30 min,然后將重組病毒轉導的HUVEC細胞制成懸液(5×105cell/mL),每孔加入100 μL,置于37 ℃,5%CO2培養箱中繼續培養6 h,然后用倒置顯微鏡觀察血管網絡形成并拍照,每孔任意選取5 個視野,實驗重復3 次,通過Image J 軟件統計分析血管網絡總主段長度。
1.2.7 體內抗腫瘤效果評價取200 μL 生長狀態良好的HepG2 細胞懸液(1 × 107cell/mL)接種在BALB/c 裸小鼠背部左側皮下,當腫瘤體積長至100 mm3時,隨機分為3組,每組5只,分別在瘤內注射200 μL Bac-ChEA 和Bac-CMV(1 × 108pfu/mL)以及等體積的PBS,每隔5 d 注射1 次,共注射3 次。每2 d 測量小鼠腫瘤體積,當腫瘤體積達到1 500 mm3時,認定小鼠死亡,記錄小鼠的死亡情況。
1.2.8 統計學方法采用SPSS 26.0 軟件進行統計分析,通過Kaplan-Meier 和Log-rank 檢驗分析小鼠的存活率;計量資料兩組對比采用t檢驗,數據結果以()表示,P<0.05 為差異有統計學意義。
2 結果
2.1 重組桿狀病毒Bac-ChEA 的PCR 鑒定將重組質粒pBac-ChEA 轉化DH10Bac 細胞,提取重組病毒Bac-ChEA DNA,轉染Sf-9 細胞3 d 后,細胞大量從瓶底脫落,倒置顯微鏡下觀察可見細胞核膨大,胞內顆粒增多,部分細胞裂解、死亡。此時收集細胞培養上清液,經堿裂解法提取病毒DNA,經PCR 和核酸瓊脂糖凝膠電泳鑒定,在預期位置處出現了特異性條帶,結果見圖1,證明hEA 基因已成功整合入病毒基因組中。
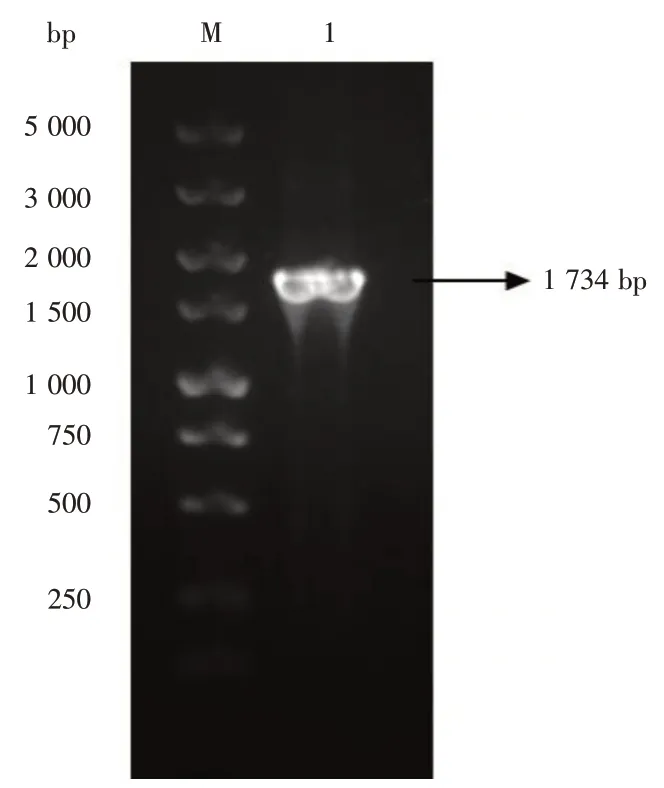
圖1 重組桿狀病毒Bac-ChEA PCR 鑒定Fig.1 PCR identification of recombinant baculovirus Bac-ChEA
2.2 在HUVEC細胞中的表達經Angiostatin ELISA試劑盒檢測,Bac-ChEA 在HUVEC 細胞中能有效表達hEA 蛋白,其平均濃度達到了(223±20)pg/mL,而在轉導Bac-CMV 的細胞中基本檢測不到hEA 蛋白(圖2)。結果表明桿狀病毒介導的hEA 蛋白在哺乳動物細胞中獲得了表達。
2.3 對HUVEC 細胞增殖能力的影響MTT 結果表明(圖3),Bac-CMV 組和空白對照組對細胞的增殖基本無影響,而Bac-ChEA 組能有效抑制HUVEC細胞的增殖,細胞平均存活率下降到了65%左右,與Bac-CMV組相比,差異有統計學意義(P<0.001),證明重組桿狀病毒介導的hEA 蛋白能有效抑制HUVEC 細胞的增殖,而桿狀病毒本身對細胞的增殖無影響。

圖2 桿狀病毒介導的hEA 蛋白在HUVEC 細胞中的表達Fig.2 Baculovirus mediated hEA protein expression in HUVEC cells
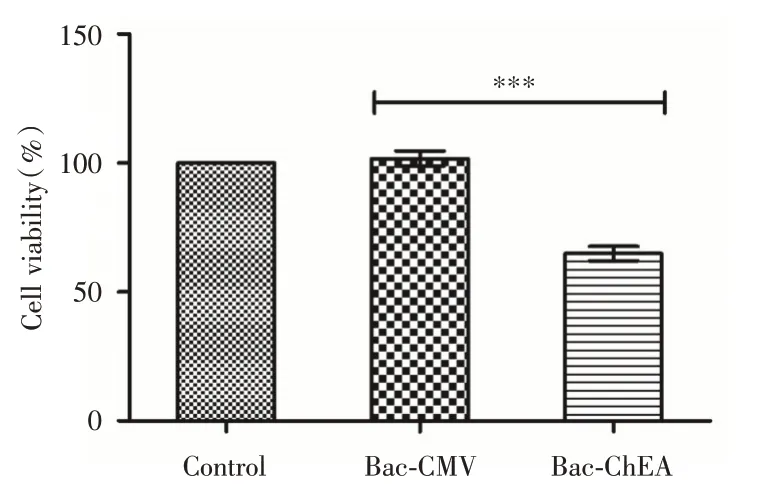
圖3 桿狀病毒介導的hEA 蛋白對HUVEC 細胞增殖能力的影響(n=3)Fig.3 Effects of baculovirus-mediated hEA protein on the proliferation of HUVEC cells(n=3)
2.4 對HUVEC 細胞遷移能力的影響通過劃痕實驗評估其對細胞遷移能力的影響。結果見圖4,Bac-ChEA 組與Bac-CMV 和空白對照組相比,細胞遷移速度減慢,進一步通過計算劃痕傷口面積,發現Bac-ChEA 組與Bac-CMV 組相比能顯著抑制HUVEC細胞傷口愈合(P<0.05),而Bac-CMV組與空白組相比,差異無統計學意義(P>0.05)。說明桿狀病毒介導的hEA 蛋白能夠有效地抑制HUVEC 細胞的遷移。
2.5 對HUVEC 細胞血管形成能力的影響通過體外成管實驗驗證桿狀病毒介導的hEA 蛋白是否具備抑制HUVEC 細胞血管形成的能力。結果如圖5所示,空白對照組和Bac-CMV 組中HUVEC 細胞相互聚集,形成清晰可見的小管網絡,而Bac-ChEA 組的細胞較分散,抑制了小管形成。進一步統計血管網絡主段長度發現,與Bac-CMV 組相比,Bac-ChEA組的成管抑制能力更為顯著(P<0.001)。說明重組桿狀病毒介導的hEA 蛋白能有效抑制HUVEC 細胞血管的形成。
2.6 體內抗腫瘤效果評價為了進一步評價桿狀病毒介導的hEA 蛋白體內抗腫瘤效果,建立裸鼠皮下HepG2 腫瘤模型。結果表明(圖6a),PBS 組和Bac-CMV 組的平均腫瘤體積分別在給藥后24 d迅速增長至1 500 mm3,而Bac-ChEA 組明顯抑制了腫瘤體積的增長,直至第38 天才達到1 500 mm3。小鼠存活率結果(圖6b)證實,小鼠的壽命(中位生存期)從Bac-CMV 組的24 d 顯著延長(P<0.05)至Bac-ChEA 組的36 d。這些結果共同證實桿狀病毒介導的hEA 蛋白能夠在體內有效地抑制腫瘤的生長,延長了其生存期。
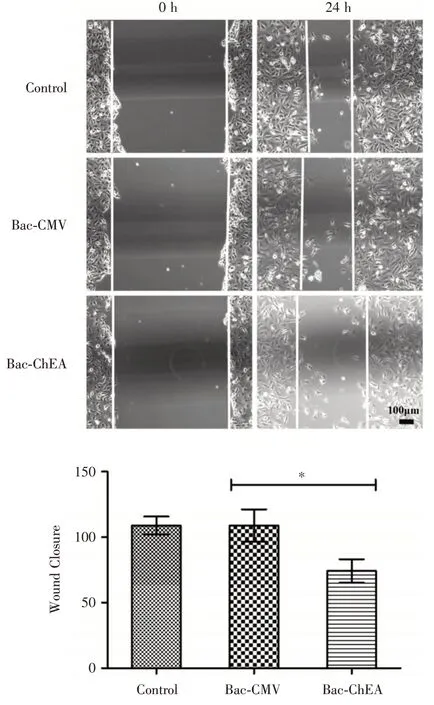
圖4 桿狀病毒介導的hEA 蛋白對HUVEC 細胞遷移能力的影響(n=3)Fig.4 Effect of baculovirus-mediated hEA protein on the migration of HUVEC cells(n=3)
3 討論
桿狀病毒-昆蟲細胞表達系統較其他病毒載體如腺病毒、腺相關病毒、慢病毒等具有獨特的優點:如對人類和哺乳動物不引起致病,能在I 級生物安全實驗室進行操作;在哺乳動物細胞中復制缺陷,沒有預先存在的抗體;能容納大片段外源基因插入;重組病毒的構建及純化操作簡單等[7]。這些優點使得桿狀病毒在疫苗生產[8]、表面展示真核蛋白[9]等方面得到了廣泛的應用。進一步研究發現當桿狀病毒攜帶含有目標細胞功能啟動子時,能有效地將基因轉移到目標細胞中,使得桿狀病毒作為基因傳遞載體在基因治療方面表現出了很大的潛力[10-11]。
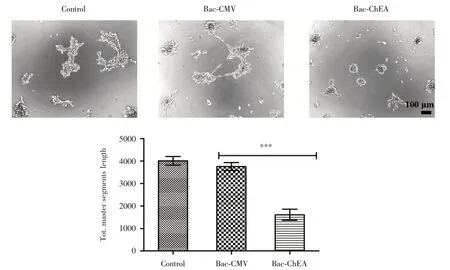
圖5 桿狀病毒介導的hEA 蛋白對HUVEC 細胞血管形成能力的影響Fig.5 Effect of baculovirus-mediated hEA protein on the angiogenesis of HUVEC cells
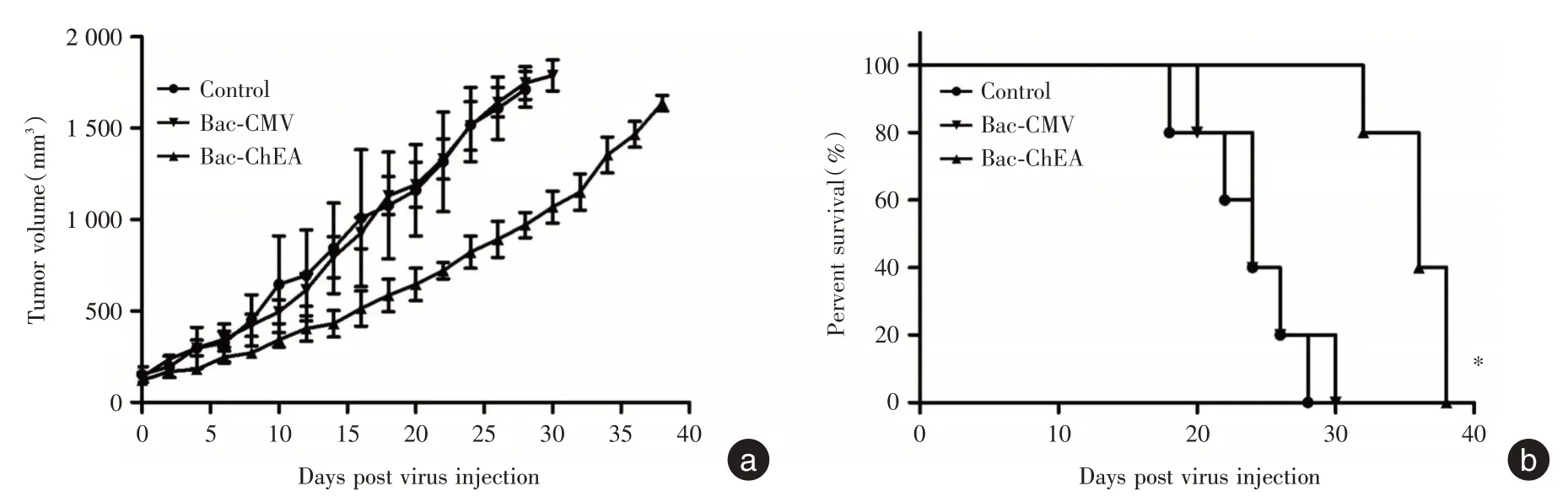
圖6 桿狀病毒介導的hEA 蛋白體內抗腫瘤效果評價Fig.6 Evaluation of antitumor effect of baculovirus-mediated hEA protein in vivo
本研究以桿狀病毒載體pFastBac DUAL 為骨架,將桿狀病毒pPh 啟動子替換為哺乳動物CMV啟動子,然后在其作用下表達hEA 基因。通過PCR 和ELISA 檢測hEA 基因成功插入桿狀病毒基因組中,并成功在HUVEC 細胞中獲得表達。盡管CMV 是廣譜型哺乳動物啟動子,但SINN 等[12]研究發現,CMV 在胚胎干細胞(ESCs)中的表達活性很低,因此應根據靶細胞的類型選擇合適的啟動子。由于血管生成涉及到內皮細胞的增殖、遷移以及隨后血管的形成,因此為了證實hEA 蛋白的抗血管生成活性,本研究以HUVEC 細胞為模型,驗證hEA 蛋白的功能活性。結果表明,Bac-ChEA能有效抑制HUVEC 細胞的增殖、遷移以及血管網絡的形成,裸鼠肝癌腫瘤模型結果進一步表明,Bac-ChEA 能有效抑制肝癌腫瘤體積的增長,小鼠壽命(中位生存期)從Bac-CMV 組的24 d 顯著延長至Bac-ChEA 組的36 d。盡管抗血管生成蛋白表現出了一定的抑制腫瘤生長的潛力,但其主要是通過抑制腫瘤血管生成而非直接針對腫瘤細胞達到抗腫瘤目的。有學者將內皮抑素與促凋亡蛋白TRAIL 或與化療藥吉西他濱或與放射療法聯合應用,都表現出了增強的協同作用[13-15]。因此,為了提高抗血管生成治療效果,聯合化療或放療以及在桿狀病毒載體中插入多種抗血管生成基因、免疫刺激和腫瘤靶向自殺基因等的雞尾酒療法,成為腫瘤基因治療今后的發展方向。盡管桿狀病毒作為基因傳遞載體表現出了一定的潛力,但桿狀病毒介導的外源蛋白在宿主細胞中瞬時表達以及在體內應用時載體易被補體系統滅活,極大地影響了蛋白的表達效率。為此,研究者們開發了一系列的桿狀病毒嵌合系統,如AAV ITR[16],Sleeping Beauty[17]系統等,這些系統都可不同程度的延長外源基因的表達。為了抵抗血清補體系統滅活,通過在桿狀病毒表面展示補體調節因子,如DAF[18]、CD46-DAF-CD59 融合蛋白[19]等手段可以有效地抑制補體系統的攻擊。在筆者最近的研究中,借助SB 轉座子系統和表面展示技術,成功構建了既能在哺乳動物細胞中長效穩定表達外源蛋白又能有效抵抗補體系統攻擊的重組桿狀病毒載體[20]。
總之,盡管桿狀病毒作為基因傳遞載體仍有不足,但桿狀病毒的安全性以及操作的簡便性使得其作為基因傳遞載體擁有獨特的優勢,通過對桿狀病毒改造,可以極大地改善其轉導效率。

